Новые кодирующие нуклеотидные последовательности гена zwal
Иллюстрации
Показать всеИзобретение относится к биотехнологии. Предложен полинуклеотид, кодирующий продукт гена Zwal, содержащий полинуклеотидную последовательность, выбранную из группы, включающей: а) полинуклеотид, кодирующий полипептид, который содержит аминокислотную последовательность, идентичную по крайней мере на 90% аминокислотной последовательности, представленной в SEQ ID NO:2, б) полинуклеотид, комплементарный полинуклеотидам, указанным в подпункте а), а также праймер, представляющий собой полинуклеотид, содержащий по крайней мере 15 последовательных пар оснований указанного выше полинуклеотида. Данное изобретение позволяет получить новый ген zwal, кодирующий генный продукт Zwal, 2 н. и 4 з.п. ф-лы, 1 ил., 1 табл.
Реферат
Настоящее изобретение относится к кодирующим нуклеотидным последовательностям гена zwa1 и к способу ферментативного получения аминокислот, прежде всего L-лизина, с использованием коринебактерий, в 10 которых усиливают ген zwa1.
Предпосылки создания изобретения
Аминокислоты, прежде всего L-лизин, находят применение в медицине и в фармацевтической промышленности, но прежде всего в кормах для животных.
Известно, что аминокислоты получают ферментативным путем с использованием штаммов коринебактерий, прежде всего с использованием Corynebacterium glutamicum. Поскольку эти продукты имеют большое значение, постоянно ведется работа по совершенствованию способа их получения. Усовершенствования способа могут касаться технологических сторон процесса ферментации, таких как перемешивание и обеспечение кислородом, или состава питательных сред, например концентрации сахара в процессе ферментации, или переработки продукта, например с помощью ионообменной хроматографии, или присущей самому микроорганизму продуктивности.
Для улучшения продуктивности этих микроорганизмов применяют методы мутагенеза, селекции и отбора мутантов. Таким путем получают штаммы, которые обладают устойчивостью к антиметаболитам, таким как аналог лизина S-(2-аминоэтил)цистеин, или которые являются ауксотрофами в отношении обладающих регуляторной функцией метаболитов и продуцируют L-аминокислоты.
В течение ряда лет для улучшения продуцирующих аминокислоты штаммов Corynebacterium также применяют методы рекомбинантной ДНК, с помощью которых амплифицируют отдельные гены биосинтеза аминокислот и исследуют влияние на продуцирование аминокислот. Обзор работ в этой области можно найти среди прочего у Kinoshita ("Glutamic Acid Bacteria", Biology of Industrial Microorganisms, под ред. Demain и Solomon, изд-во Benjamin Cummings, London, Великобритания, 115-142 (1985)), у Hilliger (BioTec 2, 40-44 (1991)), у Eggeling (Amino Acids 6, 261-272 (1994)), у Jetten и Sinskey (Critical Reviews in Biotechnology 15, 73-103 (1995)) и у Sahm и др. (Annuals of the New York Academy of Sciences 782, 25-39 (1996)).
Задача изобретения
Задачей изобретения является разработка новых подходов по усовершенствованию способа ферментативного получения аминокислот, прежде всего L-лизина.
Описание изобретения
Аминокислоты, прежде всего L-лизин, находят применение в медицине, в фармацевтической промышленности и прежде всего в кормах для животных. Поэтому представляет большой интерес разработка нового более эффективного способа получения аминокислот, прежде всего L-лизина.
Если в дальнейшем упоминается L-лизин или лизин, то при этом подразумеваются не только сами эти основания, но и их соли, такие как моногидрохлорид лизина или сульфат лизина.
Объектом изобретения является выделенный из коринебактерий полинуклеотид, содержащий полинуклеотидную последовательность, выбранную из группы, включающей
а) полинуклеотид, идентичный по крайней мере на 70% полину клеотиду, кодирующему полипептид, который содержит аминокислотную последовательность, представленную в SEQ ID NO:2,
б) полинуклеотид, кодирующий полипептид, который содержит аминокислотную последовательность, идентичную по крайней мере на 70% аминокислотной последовательности, представленной в SEQ ID NO:2,
в) полинуклеотид, комплементарный полинуклеотидам, указанным в подпункте а) или б), и
г) полинуклеотид, содержащий по крайней мере 15 последовательных пар оснований полинуклеотидной последовательности, указанной в подпункте а), б) или в).
Объектом изобретения является также полинуклеотид, который предпочтительно представляет собой реплицируемую ДНК и который содержит:
(I) нуклеотидную последовательность, представленную в SEQ ID NO:1, или
(II) по меньшей мере одну последовательность, которая соответствует последовательности, указанной в подпункте (I), в пределах вырожденности генетического кода, или
(III) по меньшей мере одну последовательность, которая гибридизуется с последовательностями, комплементарными последовательностям, указанным в подпункте (I) или (II), и при необходимости
(IV) функционально нейтральные смысловые мутации в последовательности, указанной в подпункте (I).
Другими объектами изобретения являются следующие:
полинуклеотид, содержащий нуклеотидную последовательность, представленную в SEQ ID NO:1, и представляющий собой реплицируемую в коринебактериях, предпочтительно рекомбинантную, ДНК,
полинуклеотид, кодирующий полипептид, который содержит аминокислотную последовательность, представленную в SEQ ID NO:2,
вектор, включающий кодирующую последовательность ДНК гена zwa1 С.glutamicum, которая содержится в векторе (плазмиде) pCR2.1zwa1exp, депонированном в штамме Е.coli Top10F' под регистрационным номером DSM 13115, и
служащие в качестве клеток-хозяев коринебактерии, которые содержат указанный вектор или в которых усиливают ген zwa1.
Объектом изобретения являются также полинуклеотиды, которые практически представляют собой полинуклеотидную последовательность и которые могут быть получены путем скрининга с использованием гибридизации соответствующего банка генов, содержащего полный ген, который имеет полинуклеотидную последовательность, соответствующую SEQ ID NO:1, или ее части, с зондом, который имеет указанную полинуклеотидную последовательность, представленную в SEQ ID NO:1, или ее фрагмент, и путем выделения указанной последовательности ДНК.
Полинуклеотидные последовательности по изобретению пригодны в качестве гибридизационных зондов для РНК, кДНК и ДНК для выделения полноразмерной кДНК, кодирующей генный продукт Zwal, и для выделения тех кДНК или генов, которые имеют высокую степень сходства с последовательностью гена zwa1.
Кроме того, полинуклеотидные последовательности по изобретению пригодны в качестве праймеров для получения с помощью полимеразной цепной реакции (ПНР) ДНК генов, кодирующих генный продукт Zwal.
Такие олигонуклеотиды, которые служат в качестве зондов или праймеров, включают по крайней мере 30, предпочтительно по крайней мере 20, наиболее предпочтительно по крайней мере 15 последовательных пар оснований. Также могут использоваться олигонуклеотиды, имеющие длину по крайней мере 40 или 50 пар оснований.
Понятие "выделенный" в контексте настоящего изобретения относится к какому-либо элементу, выделенному из его естественного окружения.
Понятие "полинуклеотид" в целом относится к полирибонуклеотидам и полидезоксирибонуклеотидам, которые могут представлять собой как немодифицированную РНК или ДНК, так и модифицированную РНК или ДНК.
Понятие "полипептиды" означает пептиды или протеины, содержащие две или более аминокислот, которые связаны пептидными связями.
Полипептиды по изобретению включают полипептид, последовательность которого представлена в SEQ ID NO:2, прежде всего полипептиды, обладающие биологической активностью продукта гена zwa1, а также полипептиды, идентичные полипептиду, последовательность которого представлена в SEQ ID NO:2, по крайней мере на 70%, предпочтительно по крайней мере на 80% и наиболее предпочтительно по крайней мере на 90-95%, и обладающие указанной активностью.
Объектом изобретения является также способ ферментативного получения аминокислот, прежде всего L-лизина, с использованием коринебактерий, прежде всего таких, которые уже обладают способностью продуцировать аминокислоты и в которых усиливают, прежде всего сверхэкспрессируют, кодирующие нуклеотидные последовательности гена zwa1.
В контексте настоящего описания понятие "усиление" означает повышение в микроорганизме внутриклеточной активности одного или нескольких ферментов, кодируемых соответствующей ДНК, за счет, например, увеличения количества копий гена или генов, использования более сильного промотора или гена, кодирующего соответствующий фермент с высокой активностью, и при необходимости за счет сочетания этих мер.
Микроорганизмы, являющиеся объектом настоящего изобретения, могут продуцировать L-лизин из глюкозы, сахарозы, лактозы, фруктозы, мальтозы, мелассы, крахмала, целлюлозы или из глицерина и этанола. Они могут включать представителей коринебактерий, прежде всего из рода Corynebacterium. В роде Corynebacterium следует прежде всего отметить вид Corynebacterium glutamicum, который, как известно специалистам, обладает способностью продуцировать L-аминокислоты.
Пригодными штаммами бактерий р. Corynebacterium, прежде всего вида Corynebacterium glutamicum, являются, например, следующие известные штаммы дикого типа:
Corynebacterium glutamicum ATCC 13032,
Corynebacterium acetoglutamicum ATCC 15806,
Corynebacterium acetoacidophilum ATCC 13870,
Corynebacterium melassecola ATCC 17965,
Corynebacterium thermoaminogenes FERM BP-1539,
Brevibacterium flavum ATCC 14067,
Brevibacterium lactofermentum ATCC 13869 и
Brevibacterium divaricatum ATCC 14020,
а также полученные из них мутанты, соответственно штаммы, продуцирующие L-лизин, такие как:
Corynebacterium glutamicum FERM-P 1709,
Brevibacterium flavum FERM-P 1708,
Brevibacterium lactofermentum FERM-P1712,
Corynebacterium glutamicum FERM-P 6463,
Corynebacterium glutamicum FERM-P 6464 и
Corynebacterium glutamicum DSM 5715.
Авторам изобретения удалось выделить новый ген zwa1 С.glutamicum, кодирующий генный продукт Zwal.
Для выделения гена zwa1, а также других генов С.glutamicum сначала создают банк генов этого микроорганизма в Е. coli. Создание банка генов описано в широко известных учебниках и справочниках. В качестве примера можно назвать учебник Winnacker: Gene und Klone, Eine Einführung in die Gentechnologie (изд-во Chemie, Weinheim, Германия, 1990) или справочник Sambrook и др.: Molecular Cloning, A Laboratory Manual (изд-во Cold Spring Harbor Laboratory Press, 1989). Одним из широко известных банков генов является банк генов штамма Е.coli K-12 W3110, созданный Kohara и др. (Cell 50, 495-508 (1987)) в λ-векторах. У Bathe и др. (Molecular and General Genetics, 252: 255-265 (1996)) описан банк генов штамма С.glutamicum ATCC 13032, полученный с помощью космидного вектора SuperCos I (Wahl и др., Proceedings of the National Academy of Sciences USA, 84: 2160-2164 (1987)) в штамме Е.coli K-12 NM554 (Raleigh и др., Nucleic Acids Research 16, 1563-1575 (1988)). В свою очередь у Börmann и др. (Molecular Microbiology 6(3), 317-326 (1992)) описан банк генов штамма С.glutamicum ATCC 13032, полученный с использованием космиды рНС79 (Hohn и Collins, Gene 11, 291-298 (1980)). Для создания банка генов С.glutamicum в Е. coli могут быть использованы также такие плазмиды, как pBR322 (Bolivar, Life Sciences, 25, 807-818 (1979)) или pUC9 (Vieira и др., Gene, 19: 259-268, (1982)). В качестве хозяев могут быть использованы прежде всего такие штаммы Е.coli, которые имеют дефекты, полученные в результате рестрикции и рекомбинации. Примером такого штамма является штамм DH5αmcr, описанный у Grant и др. (Proceedings of the National Academy of Sciences USA, 87: 4645-4649 (1990)). Затем клонированные с помощью космид длинные фрагменты ДНК могут быть снова субклонированы в обычных пригодных для секвенирования векторах и после этого секвенированы, например, согласно методу, описанному у Sanger и др. (Proceedings of the National Academy of Sciences USA, 74: 5463-5467, (1977)).
Таким способом была получена новая кодирующая последовательность ДНК гена zwa1 С.glutamicum, которая в виде SEQ ID NO:1 является составной частью настоящего изобретения. Кроме того, из данной последовательности ДНК была выведена аминокислотная последовательность соответствующего продукта гена zwa1. Выведенная аминокислотная последовательность продукта гена zwa1 представлена в SEQ ID NO:2.
Кодирующие последовательности ДНК, которые получают из SEQ ID NO:I на основе вырожденности генетического кода, также являются составной частью изобретения. Аналогично этому составной частью изобретения являются последовательности ДНК, которые гибридизуются с SEQ ID NO:1 или с частями SEQ ID NO:1.
Кроме того, в данной области известны консервативные замены аминокислот в протеинах, такие как замена глицина на аланин или аспарагиновой кислоты на глутаминовую кислоту, так называемые "смысловые мутации", которые не приводят к существенному изменению активности протеина, т.е. являются функционально нейтральными. Кроме того, известно, что изменения на N- и/или на С-конце протеина не оказывают существенного влияния на его функциональную активность или даже могут стабилизировать ее. Соответствующую информацию можно найти среди прочего у Ben-Bassat и др. (Journal of Bacteriology 169, 751-757 (1987)), у O'Regan и др. (Gene 77: 237-251 (1989)), у Sahin-Toth и др. (Protein Sciences 3: 240-247 (1994)), у Hochuli и др. (Bio/Technology 6: 1321-1325 (1988)), а также в известных учебниках по генетике и молекулярной биологии. Аминокислотные последовательности, которые могут быть получены соответствующим образом из SEQ ID NO:2, также являются составной частью изобретения.
Равным образом составной частью изобретения являются последовательности ДНК, которые гибридизуются с последовательностью, представленной в SEQ ID NO:1, или с частями последовательности, представленной в SEQ ID NO:1. Помимо этого, составной частью изобретения являются последовательности ДНК, которые могут быть созданы путем полимеразной цепной реакции (ПЦР) с использованием праймеров, полученных из SEQ ID NO:1. Такие олигонуклеотиды, как правило, имеют длину по крайней мере 15 пар оснований.
Соответствующие рекомендации по идентификации последовательностей ДНК с помощью гибридизации можно найти, в частности, в справочнике "The DIG System Users Guide for Filter Hybridization" фирмы Boehringer Mannheim GmbH (Маннгейм, Германия, 1993) и у Liebl и др. (International Journal of Systematic Bacteriology, 41: 255-260 (1991)). Рекомендации касательно амплификации последовательностей ДНК с помощью полимеразной цепной реакции (ПЦР) можно найти среди прочего в справочнике Gait: Oligonucleotide synthesis: a practical approach (изд-во IRL Press, Oxford, Великобритания, 1984) и у Newton и Graham: PCR (изд-во Spektrum Akademischer Veriag, Heidelberg, Германия,1994).
При создании изобретения было установлено, что в результате сверхэкспрессии гена zwa1 может быть повышена эффективность синтеза коринебактериями аминокислот, прежде всего L-лизина.
Для достижения сверхэкспрессии может быть увеличено количество копий соответствующего гена или могут быть вызваны мутации в промоторной и регуляторной областях или сайте связывания рибосом, расположенном против хода транскрипции относительно структурного гена. Равным образом действуют кассеты экспрессии, встраиваемые против хода транскрипции относительно структурного гена. Кроме того, экспрессию можно дополнительно повышать в процессе ферментативного получения аминокислот с помощью индуцибельных промоторов. Экспрессия также может быть усилена за счет увеличения продолжительности жизни мРНК. Кроме того, ферментативная активность также может быть усилена путем ингибирования разложения протеинов ферментов. При этом гены или генные конструкции либо могут находиться в различном количестве копий в плазмидах, либо их интегрируют в хромосомы и амплифицируют. В альтернативном варианте сверхэкспрессия рассматриваемых генов также может быть достигнута путем изменения состава среды и условий культивирования.
Соответствующие рекомендации можно найти у Martin и др. (Bio/Technology 5, 137-146 (1987)), у Guerrero и др. (Gene 138, 35-41 (1994)), Tsuchiya и Morinaga (Bio/Technology 6, 428-430 (1988)), у Eikmanns и др. (Gene 102, 93-98 (1991)), в ЕР 0472869, в патенте US 4601893, у Schwarzer и Pühler (Bio/Technology 9, 84-87 (1991)), у Reinscheid и др. (Applied and Environmental Microbiology 60, 126-132 (1994)), у LaBarre и др. (Journal of Bacteriology 175, 1001-1007 (1993), в заявке WO 96/15246, у Malumbres и др. (Gene 134, 15-24 (1993)), в заявке JP-А 10-229891, у Jensen и Hammer (Biotechnology and Bioengineering 58, 191-195 (1998)), у Makrides (Microbiological Reviews 60: 512-538 (1996)) и в известных учебниках по генетике и молекулярной биологии.
Ген zwa1 по изобретению можно, например, дуплицировать, соответственно сверхэкспрессировать с помощью интеграционного метода, как это описано, например, у Reinscheid и др. (Applied and Environmental Microbiology 60, 126-132 (1994)). С помощью этого метода полноразмерный ген клонируют в плазмидном векторе, который может реплицироваться в определенном хозяине (обычно в Е.coli), но не в С.glutamicum. В качестве векторов могут рассматриваться, например, pSUP301 (Simon и др., Bio/Technology 1, 784-791 (1983)), pK18mob или pK19mob (Schäfer и др., Gene 145, 69-73 (1994)), pGEM-T (фирма Promega corporation, Мадисон, шт.Висконсин, США), pCR2.1-TOPO (Shuman, Journal of Biological Chemistry, 269: 32678-32684 (1994); US 5487993), pCR®Blunt (фирма Invitrogen, Groningen, Нидерланды; Bernard и др., Journal of Molecular Biology, 234: 534-541 (1993)) или pEMl (Schrumpf и др., Journal of Bacteriology 173: 4510-4516 (1991)). Затем плазмидный вектор, содержащий подлежащий амплификации ген, переносят путем конъюгации или трансформации в пригодный штамм С.glutamicum. Метод конъюгации описан, например, у Schäfer и др. (Applied and Environmental Microbiology 60, 756-759 (1994)). Методы трансформации описаны, например, у Thierbach и др. (Applied Microbiology and Biotechnology 29, 356-362 (1988)), у Dunican и Shivnan (Bio/Technology 7, 1067-1070 (1989)) и у Tauch и др. (FEMS Microbiological Letters 123, 343-347 (1994)). В результате гомологичной рекомбинации с помощью одного кроссинговера образовавшийся штамм содержит по крайней мере две копии рассматриваемого гена. Таким путем с помощью интеграционной плазмиды pCR2.1zwa1exp конструировали штамм DSM 5715::pCR2.1zwa1exp, несущий две копии гена zwa1.
Кроме того, для повышения эффективности синтеза аминокислот, прежде всего L-лизина, может оказаться предпочтительным наряду с генным продуктом Zwal дополнительно усиливать, прежде всего сверхэкспрессировать, один или несколько ферментов, участвующих в соответствующем пути биосинтеза, в гликолизе, анаплеротическом обмене веществ, цикле лимонной кислоты или экспорте аминокислот.
Так, например, для получения L-лизина можно одновременно сверхэкспрессировать один или несколько генов, выбранных из группы, включающей
- ген dapA, кодирующий дигидродипиколинат-синтазу (ЕР-В 0197335),
- ген lysC, кодирующий устойчивую в отношении обратной связи аспартаткиназу,
- ген dapD, кодирующий тетрадигидродипиколинат-сукцинилазу (Wehrmann и др., Journal of Bacteriology 180, 3159-3165 (1998),
- ген dapE, кодирующий сукцинилдиаминопимелат-десукцинилазу (Wehrmann и др., Journal of Bacteriology 177, 5991-5993 (1995),
- ген gap, кодирующий глицеральдегид-3-фосфатдегидрогеназу (Eikmanns и др., Journal of Bacteriology 174: 6076-6086 (1992)),
- ген рус, кодирующий пируваткарбоксилазу (Eikmanns, Journal of Bacteriology 174: 6076-6086 (1992)),
- ген mqo, кодирующий малат-хинон-оксид оредуктазу (Molenaar и др., European Journal of Biochemistry 254, 395-403 (1998)),
- ген lysE, кодирующий экспорт лизина (DE-A 19548222).
Кроме того, для продуцирования аминокислот, прежде всего L-лизина, может оказаться целесообразным наряду с усилением гена zwa1 одновременно ослаблять
- ген pck, кодирующий фосфоенолпируват-карбоксикиназу (DE 19950409.1 DSM 13047), и/или
- ген pgi, кодирующий глюкозо-6-фосфатизомеразу (US 09/396478, DSM 12969).
Кроме того, для получения аминокислот, прежде всего L-лизина, может оказаться целесообразным наряду со сверхэкспрессией гена zwa1 исключить нежелательные побочные реакции (Nakayama: "Breeding of Ammo Acid Producing Microorganisms", Overproduction of Microbial Products, под ред. Krumphanzl, Sikyta, Vanek, изд-во Academic Press, London, Великобритания, 1982).
Помимо усиления гена zwa1 может оказаться целесообразным дополнительно ослаблять ген zwa2 или действие соответствующего продукта гена zwa2. Этот ген и соответствующие методы описаны в одновременно поданной заявке DE 19959327.2.
Пригодный для инсерционного мутагенеза интеграционный вектор pCR2.1zwa2int депонирован в штамме Е.coli TOP10F' под регистрационным номером DSM 13113.
Плазмида pCR2.1zwa2int состоит из описанной у Mead и др. (Bio/Technology 9: 657-663 (1991)) плазмиды pCR2.1-TOPO, в которую встроен внутренний фрагмент гена zwa2, представленный в SEQ ID NO:1 заявки DE 19959327.2. Указанная плазмида в результате трансформации и гомологичной рекомбинации в хромосомном гене zwa2 (инсерция) приводит к полной потере функции гена. Таким путем, например, создают штамм DSM 5715::pCR2.1zwa2int, у которого отсутствует генный продукт Zwa2.
Для получения аминокислот, прежде всего L-лизина, созданные согласно изобретению микроорганизмы можно культивировать непрерывно или периодически с использованием периодического процесса (культивирование партий) или периодического процесса с подпиткой либо периодического процесса с повторяющейся подпиткой. Обзор известных способов культивирования представлен в учебнике Chmiel (Bioprozesstechnik 1. Einführung in die Bioverfahrenstechnik (изд-во Gustav Fischer, Stuttgart, 1991)) или в учебнике Storhas (Bioreaktoren und periphere Einrichtungen (изд-во Vieweg, Braunschweig/Wiesbaden, 1994)).
Используемая культуральная среда должна быть соответствующим образом адаптирована к требованиям конкретного штамма. Описания культуральных сред для различных микроорганизмов содержатся в справочнике "Manual of Methods for General Bacteriology" Американского общества бактериологии (Вашингтон, округ Колумбия, США, 1981). В качестве источника углерода могут быть использованы сахара и углеводы, такие как глюкоза, сахароза, лактоза, фруктоза, мальтоза, меласса, крахмал и целлюлоза, масла и жиры, такие как соевое масло, подсолнечное масло, арахисовое масло и кокосовое масло, жирные кислоты, такие как пальмитиновая кислота, стеариновая кислота и линолевая кислота, спирты, такие как глицерин и этанол, и органические кислоты, такие как уксусная кислота. Эти вещества могут применяться по отдельности или в виде смеси. В качестве источника азота могут применяться органические азотсодержащие соединения, такие как пептоны, дрожжевой экстракт, мясной экстракт, солодовый экстракт, жидкость, образующаяся после замачивания зерен кукурузы до разбухания, соевая мука и мочевина, или неорганические соединения, такие как сульфат аммония, хлорид аммония, фосфат аммония, карбонат аммония и нитрат аммония. Источники азота могут применяться по отдельности или в виде смеси. В качестве источника фосфора могут применяться фосфорная кислота, кислый фосфат калия или дикалийгидрофосфат либо соответствующие натриевые соли. Кроме того, культуральная среда должна содержать соли металлов, такие как сульфат магния или сульфат железа, которые необходимы для роста. И, наконец, в дополнение к вышеназванным соединениям могут использоваться такие важные для роста вещества, как аминокислоты и витамины. Помимо этого, в культуральную среду могут быть добавлены соответствующие предшественники. Вышеуказанные добавки могут быть введены в культуральную среду в виде одноразовой добавки или добавляться соответствующим образом в процессе культивирования.
Для контроля значения рН культуральной среды используют соответственно либо основания, такие как гидроксид натрия, гидроксид калия, аммиак, соответственно аммиачную воду, либо кислоты, такие как фосфорная кислота или серная кислота. Для контроля пенообразования добавляют антивспениватели, такие как полигликолевые эфиры жирных кислот. Для поддержания стабильности плазмид могут быть добавлены соответствующие конкретной среде вещества, обладающие избирательным действием, например антибиотики. Для поддержания аэробных условий в культуру вводят кислород или содержащие кислород газовые смеси, например воздух. Температура культуральной среды в норме составляет от 20°С до 45°С, предпочтительно от 25°С до 40°С. Культивирование продолжают до тех пор, пока не образуется максимальное количество лизина. Как правило, эта цель достигается за 10-160 ч.
Анализ L-лизина можно проводить с помощью анионообменной хроматографии с последующей дериватизацией с обнаружением нингидрином согласно методу, описанному у Spackman и др. (Analytical Chemistry, 30, 1190 (1958)).
В соответствии с Будапештским договором в Немецкой коллекции микроорганизмов и клеточных культур (DSMZ, Брауншвейг, Германия) был депонирован следующий микроорганизм:
- штамм Escherichia coli Top10F'/pCR2.1zwa1exp под регистрационным номером DSM 13115.
Способ по изобретению предназначен для ферментативного получения аминокислот, прежде всего L-лизина.
Может оказаться целесообразным наряду с усилением гена zwa1 дополнительно ослаблять ген zwa2. Соответствующий ген, соответственно пригодный для инсерционного мутагенеза вектор pCR2.1zwa2int, депонирован в штамме Е.coli TOP10F' под регистрационным номером DSM 13113.
Примеры
Ниже настоящее изобретение проиллюстрировано на примерах его осуществления.
Пример 1
Создание геномного космидного банка генов штамма Corynebacterium glutamicum ATCC 13032
Хромосомную ДНК выделяли из штамма Corynebacterium glutamicum ATCC 13032 по методу, описанному у Tauch и др. (Plasmid 33: 168-179 (1995)), и частично расщепляли рестриктазой Sau3AI (фирма Amersham Pharmacia, Фрейбург, Германия, описание продукта Sau3AI: продукт №27-0913-02). Фрагменты ДНК дефосфорилировали щелочной фосфатазой креветки (ЩФК) (фирма Roche Molecular Biochemicals, Маннгейм, Германия, описание продукта ЩФК: продукт №1758250). ДНК космидного вектора SuperCos I (Wahl и др., Proceedings of the National Academy of Sciences USA 84: 2160-2164 (1987)), полученного от компании Stratagene (Ла Джолла, США, описание продукта, представляющего собой набор SuperCos I Cosmid Vector Kit: продукт №251301) расщепляли рестриктазой Xbal (фирма Amersham Pharmacia, Фрейбург, Германия, описание продукта Xbal: продукт №27-0948-02) и также дефосфорилировали щелочной фосфатазой креветки. Затем космидную ДНК расщепляли рестриктазой BamHI (фирма Amersham Pharmacia, Фрейбург, Германия, описание продукта BamHI: продукт №27-0868-04). Обработанную таким образом космидную ДНК смешивали с обработанной ДНК штамма ATCC 13032 и смесь обрабатывали ДНК-лигазой фага Т4 (фирма Amersham Pharmacia, Фрейбург, Германия, описание продукта ДНК-лигазы фага Т4: продукт №27-0870-04). Полученный в результате лигирования продукт встраивали затем в фаги с помощью наборов Gigapack II XL Packing Extract (фирма Stratagene, Ла Джолла, США, описание продукта, представляющего собой набор Gigapack II XL Packing Extract: продукт №200217). Для инфицирования штамма Е.coli NM554 (Raleigh и др., Nucleic Acid Research 16: 1563-1575 (1988)) клетки переносили в 10 мМ MgSO4 и смешивали с аликвотным количеством суспензии фага. Инфицирование и титрование космидного банка осуществляли в соответствии с методом, описанным у Sambrook и др. (Molecular Cloning: A Laboratory Manual, Cold Spring Harbor (1989)), при этом клетки высевали на LB-arap (Lennox, Virology, 1: 190 (1955)), содержащий 100 мкг/мл ампициллина.
После инкубации в течение ночи при 37°С отбирали отдельные рекомбинантные клоны.
Пример 2
Выделение и секвенирование гена zwa1
Космидную ДНК из отдельной колонии выделяли с помощью набора Qiaprep Spin Miniprep Kit (продукт №27106, фирма Qiagen, Гильден, Германия) согласно инструкциям производителя и частично расщепляли рестриктазой Sau3AI (фирма Amersham Pharmacia, Фрейбург, Германия, описание продукта Sau3AI: продукт №27-0913-02). Фрагменты ДНК дефосфорилировали щелочной фосфатазой креветки (фирма Roche Molecular Biochemicals, Маннгейм, Германия, описание продукта ЩФК: продукт №1758250). После разделения с помощью гель-электрофореза выделяли фрагменты космиды, имеющие размеры в интервале от 1500 до 2000 пар оснований, с использованием набора QiaExII Gel Extraction Kit (продукт №20021, фирма Qiagen, Гильден, Германия). ДНК секвенирующего вектора pZero-1, полученного от компании Invitrogen (Гронинген, Нидерланды, описание продукта, представляющего собой набор Zero Background Cloning Kit: продукт №K2500-01), расщепляли рестриктазой BamHI (фирма Amersham Pharmacia, Фрейбург, Германия, описание продукта BamHI: продукт №27-0868-04). Встраивание фрагментов космиды в секвенирующий вектор pZero-1 путем лигирования осуществляли по методу, описанному у Sambrook и др. (Molecular Cloning: A Laboratory Manual, Cold Spring Harbor (1989)), при этом смесь ДНК инкубировали в течение ночи с лигазой фага Т4 (фирма Pharmacia Biotech, Фрейбург, Германия). Затем этот полученный в результате лигирования продукт встраивали путем электропорации (Tauch и др., FEMS Microbiol. Letters, 123: 343-347 (1994)) в штамм Е.coli DH5αmcr (Grant, Proceedings of the National Academy of Sciences USA, 87: 4645-4649 (1990)) и высевали на LB-arap (Lennox, Virology, 1: 190 (1955)), содержащий 50 мкг/мл зеоцина. Плазмиду выделяли из рекомбинантных клонов с помощью устройства Biorobot 9600 (продукт №900200, фирма Qiagen, Гильден, Германия). Секвенирование проводили с помощью дидезоксиметода на основе разрыва цепи, описанного у Sanger и др. (Proceedings of the National Academy of Sciences USA 74: 5463-5467 (1977)), с модификациями согласно Zimmermaim и др. (Nucleic Acids Research, 18: 1067 (1990)). Использовали набор "RR dRhodamin Terminator Cycle Sequencing Kit" фирмы РЕ Applied Biosystems (продукт №403044, Вейтерштадт, Германия). Разделение с помощью гель-электрофореза и анализ результатов реакции секвенирования проводили в геле "Rotiphorese NF Akrylamid/Bisakrylamid" (29:1) (продукт №А124.1, фирма Roth, Карлсруэ, Германия) с использованием секвенатора типа "ABI Prism 377" фирмы РЕ Applied Biosystems (Вейтерштадт, Германия).
Полученные первичные данные о последовательностях затем обрабатывали с использованием пакета программ Staden (Nucleic Acids Research, 14: 217-231 (1986)), версия 97-0. Отдельные последовательности производных pZero-1 объединяли в непрерывную группу последовательностей. Компьютерный анализ кодирующей области проводили с использованием программы XNIP (Staden, Nucleic Acids Research, 14: 217-231 (1986)). Дальнейшие анализы проводили с помощью программы "BLAST search programs" (Altschul и др. Nucleic Acids Research, 25: 3389-3402 (1997)) на основе неизбыточного банка данных Национального центра биотехнологической информации (NCBI, Бетезда, шт.Мэриленд, США).
Полученная нуклеотидная последовательность гена zwa1 представлена в SEQ ID NO:1. Анализ нуклеотидной последовательности позволил выявить открытую рамку считывания длиной 597 пар оснований, которую обозначили как ген zwa1. Ген zwa1 кодирует состоящий из 199 аминокислот полипептид, который представлен в SEQ ID NO:2.
Пример 3
Создание вектора для сверхэкспрессии гена zwa1
Из штамма АТСС 13032 выделяли хромосомную ДНК по методу, описанному у Eikmanns и др. (Microbiology 140, 1817-1828 (1994)). На основе известной последовательности гена zwa1 из С.glutamicum, полученной согласно примеру 2, выбирали следующие олигонуклеотиды для полимеразной цепной реакции:
zwa1-dl:
5'-ТСА САС CCG ATG АТТ CAG GC-3';
zwa1-d2:
5'-AGA TTT AGC CGA CGA AAG CG-3'.
Указанные праймеры были синтезированы фирмой MWG Biotech (Эберсберг, Германия), а ПЦР проводили согласно стандартному методу, описанному у Innis и др. (PCR protocols. A guide to methods and applications, изд-во Academic Press (1990)), с использованием полимеразы Pwo фирмы Boehringer. С помощью полимеразной цепной реакции выделяли фрагмент ДНК длиной приблизительно 1,0 т.п.н., несущий ген zwa1.
Амплифицированный фрагмент ДНК с помощью набора ТОРО ТА Cloning Kit фирмы Invitrogen Corporation (Карлсбад, шт.Калифорния, США; каталожный номер К4500-01) встраивали путем лигирования в вектор pCR2.1-ТОРО (Mead и др., Bio/Technology 9: 657-663 (1991)). Затем полученный в результате лигирования продукт встраивали путем электропорации в штамм Е.coli Top10F' (Hanahan, DNA cloning. A practical approach, т.1, изд-во IRL Press, Oxford, Washington D.C., США). Отбор несущих плазмиду клеток осуществляли путем посева полученного в результате трансформации продукта на LB-агар (Sambrook и др., Molecular Cloning: A Laboratory Manual, 2-е изд., изд-во Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., 1989), дополненный 25 мг/л канамицина. Из одного трансформанта выделяли плазмидную ДНК с помощью набора QIAprep Spin Miniprep Kit фирмы Qiagen и проверяли путем рестрикции с помощью рестриктазы EcoRI и последующего электрофореза на агарозном геле (0,8%-ном). Плазмиду обозначили как pCR2.1zwa1exp.
Пример 4
Удвоение гена zwa1 в продуцирующем лизин штамме DSM 5715
Описанный в примере 3 вектор pCR2.1zwa1exp встраивали путем электропорации в штамм Corynebacterium glutamicum DSM 5715 по методу, описанному у Tauch и др. (FEMS Microbiol. Letters, 123: 343-347 (1994)). Штамм DSM 5715 представляет собой продуцирующий лизин штамм, устойчивый к АЭЦ (аминоэтилцистеин). Вектор pCR2.1zwa1exp не может самостоятельно реплицироваться в DSM 5715 и сохраняется в клетке только тогда, когда он интегрирован в хромосому штамма DSM 5715. Отбор клонов, несущих интегрированный в хромосому вектор pCR2.1zwa1exp, осуществляли путем посева полученного в результате электропорации продукта на LB-агар (Sambrook и др., Molecular Cloning: A Laboratory Manual, 2-е изд., изд-во Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., 1989), дополненный 15 мг/л канамицина. Для подтверждения успешной интеграции проводили контрольную ПЦР с использованием полимеразы Pwo фирмы Boehringer согласно стандартному методу, описанному у Innis и др. (PCR protocols. A guide to methods and applications, изд-во Academic Press (1990)). С использованием комбинации праймеров zwa1-dl и zwa1-d2 (см. пример 3) с универсальным прямым праймером М13 (5'-gttttcccagtcacgac-3') (фирма Invitrogen Corporation, каталожный номер N540-02) и универсальным обратным праймером М13 (5'-caggaaacagctatgac-3') (фирма Invitrogen Corporation, каталожный номер N530-02), которые могут связываться только в пределах последовательности вектора pCR2.1zwa1exp, удалось установить, что плазмида pCR2.1zwa1exp встроена в хромосому продуцирующего лизин штамма DSM 5715. Штамм обозначили как DSM 5715::pCR2.1zwa1exp.
Пример 5
Получение лизина
Созданный согласно примеру 4 штамм С.glutamicum DSM 5715::pCR2.1zwa1exp культивировали в среде, пригодной для получения лизина, и определяли содержание лизина в надосадочной жидкости культуры.
Для этого штамм сначала инкубировали в течение 24 ч при 33°С на агаровой пластине, содержащей соответствующий антибиотик (агар со средой, используемой для инфузии в мозг и сердце и дополненной канамицином (25 мг/л)). Этой культурой, выращенной на агаровой пластине, инфицировали предварительную культуру (10 мл среды в колбе Эрленмейера объемом 100 мл). В качестве среды для предварительной культуры использовали полную среду CgIII, в которую добавляли канамицин (25 мг/л). Предварительную культуру инкубировали в течение 48 ч при 33°С на шейкере при 240 об/мин. Этой предварительной культурой инфицировали основную культуру таким образом, чтобы начальная оптическая плотность ОП (660 нм) основной культуры составляла 0,1. В качестве среды для основной культуры использовали среду ММ.
Состав среды MM:
| жидкость, образующаяся при замачивании зерен кукурузы | до 5 г/л |
| разбухания (ЖЗК) | |
| морфолинпропансульфоновая кислота (МОПС) | 20 г/л |
| глюкоза (автоклавированная отдельно) | 50 г/л |
| соли | |
| (NH4)2SO4 | 25 г/л |
| КН2PO4 | 0,1 г/л |
| MgSO4•7H2O | 1,0 г/л |
| CaCl2•2H2O | 10 мг/л |
| FeSO4•7H2O | 10 мг/л |
| MnSO4•H2O | 5,0 мг/л |
| биотин (стерилизованный фильтрацией) | 0,3 мг/л |
| тиамин•HCl (стерилизованный фильтрацией) | 0,2 мг/л |
| лейцин (стерилизованный фильтрацией) | 0,1 г/л |
| СаСО3 | 25 г/л |
Значения рН ЖЗК, МОПС и раствора солей доводили до 7 с помощью аммиачной воды, и эти растворы автоклавировали. Затем добавляли стерильные растворы субстрата и витаминов, а также безводный автоклавированный CaCO3.
Культивирование осуществляли в колбе Эрленмейера объемом 100 мл с дефлекторами, в которую помещали 10 мл среды. В среду добавляли канамицин (25 мг/л). Культивирование осуществляли при 33°С и 80%-ной относительной влажности воздуха.
Через 48 ч с помощью прибора типа Biomek 1000 (фирма Beckmann Instruments GmbH, Мюнхен) определяли ОП при длине волны 660 нм. Концентрацию образовавшегося лизина определяли с помощью анализатора аминокислот фирмы Eppendorf-BioTronik (Гамбург, Германия) с использованием ионообменной хроматографии и последующей дериватизации на колонках с обнаружением нингидрином.
В таблице 1 представлены результаты опыта.
| Таблица 1 | ||
| Штамм | ОП (660 нм) | Лизин•HCl, г/л |
| DSM 5715::pCR2.1zwa1exp | 12,1 | 11,93 |
| DSM 5715 | 13,1 | 9,54 |
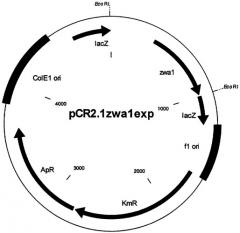
На прилагаемом к описанию чертеже показана карта плазмиды pCR2.1zwa1exp.
Данные о длинах представляют собой приблизительные величины. Использованные сокращения и обозначения имеют следующие значения:
| ColE1 ori: | начало репликации плазмиды ColE1, |
| lacZ: | 5'-конец гена β-галактозидазы, |
| f1 ori: | начало репликации фага f1, |
| KmR: | ген устойчивости к канамицину, |
| ApR: | ген устойчивости к ампициллину, |
| EcoRI: | сайт рестрикции рестриктазы EcoRI, |
| zwa1: | ген zwa1. |
1. Полинуклеотид, кодирующий продукт гена Zwal и содержащий полинуклеотидную последовательность, выбранную из группы, включающей
а) полинуклеотид, кодирующий полипептид, который содержит аминокислотную последовательность, идентичную по крайней мере на 90% аминокислотной последовательности, представленной в SEQ ID NO:2,
б) полинуклеотид, комплементарный полинуклеотидам, указанным в подпункте а).
2. Полинуклеотид по п.1, который представляет собой реплицируемую в коринебактериях, предпочтительно рекомбинантную, ДНК.
3. Полинуклеотид по п.1, который представляет собой РНК.
4. Полинуклеотид по п.2, содержащий нуклеотидную последовательность, представленную в SEQ ID NO:1.
5. Полинуклеотид по п.2, который представляет собой реплицируемую ДНК, включающую
(I) нуклеотидную последовательность, представленную в SEQ ID NO:1, или
(II) по крайней мере одну последовательность, которая соответствует последовательности, указанной в подпункте (I), в пределах вырожденности генетического кода, или
(III) по крайней мере одну последовательность, которая гибридизуется с последовательностями, комплементарными последовательностям, указанным в подпункте (I) или (II), и при необходимости
(IV) функционально нейтральные смысловые мутации в последовательности, указанной в подпункте (I).
6. Праймер, представляющий собой полинуклеотид, содержащий по крайней мере 15 последовательных пар оснований полинуклеотидной последовательности, указанной в подпунктах а) и б) п.1.