Производное пирролидинацетамида или его комбинация для лечения расстройств цнс
Иллюстрации
Показать всеПредложено: применение леветирацетама и соответствующая фармацевтическая композиция для лечения биполярных расстройств, мании, мигрени на основе леветирацетама; фармацевтическая композиция для лечения эпилепсии, синдрома отмены алкоголя, тремора, биполярных расстройств, мании, обсессивно-компульсивного расстройства, панического состояния, беспокойства, депрессии, мигрени, головной боли, боли, ишемии и травмы головы на основе леветирацетама и по меньшей мере одного ингибитора нейрональных рецепторов ГАМК типа А; соответствущие способы лечения; способ селективного усиления терапевтического действия ингибитора нейрональных рецепторов ГАМК типа А; способ лечения пациента ингибитором нейрональных рецепторов ГАМК типа А, включающий совместное введение указанного ингибитора нейрональных рецепторов ГАМК типа А с левератирацета. Изобретение отличается тем, что выявлена возможность использовать леветирацетам для лечения хронической и невропатической боли в дозах гораздо ниже тех, что вызывают вторичные эффекты, также выявлено его свойство повышать активность ингибитора нейрональных рецепторов ГАМК типа А. 7 н. и 11 з.п.ф., 20 табл.
Реферат
Данное изобретение относится к применению (S)-(-)-α-этил-2-оксо-1-пирролидинапетамида для приготовления лекарств для лечения и/или профилактики биполярных расстройств, мигрени, хронической или невропатической боли и к фармацевтической композиции, включающей (S)-(-)-α-этил-2-оксо-1-пирролидинацетамид и по меньшей мере одно соединение, индуцирующее невральное ингибирование, опосредованное GABA рецепторами.
(S)-(-)-α-этил-2-оксо-1-пирролидинацетамид формулы
является известным и далее называется леветирацетамом (Международное наименование).
Применение леветирацетама в качестве защитного агента для лечения и предотвращения поражений центральной нервной системы (ЦНС) гипоксического и ишемического типа описано в патенте ЕР-В-0162036. Это соединение можно также применять при лечении эпилепсии, терапевтическое его применение показало, что его правовращающий энантиомер (R)-(-)-α-этил-2-оксо-1-пирролидинацетамид, полностью лишен активности (А.J. GOWER et al., Eur. I Pharmacol., 222, (1992), 193-203). Последнее соединение описано также в патенте ЕР-В-0645139 в качестве агента для лечения тревожных состояний.
В ЕР-В-0162036, указанном выше, описаны также способы получения леветирацетама, которые требуют синтеза исходного реагента, получаемого разрешением соответствующего рацемата. В патенте GB 2225322 описан способ получения леветирацетама с использованием природной аминокислоты, которая уже имеет желательную стереохимическую конфигурацию, в качестве исходного продукта.
Теперь неожиданно было установлено, что леветирацетам обладает терапевтическими свойствами, которые делают его особенно пригодным при лечении и профилактике биполярных расстройств, мании, мигрени и хронической или невропатической боли. Эти виды активности не наблюдались у правовращающего энантиомера (R)-(+)-α-этил-2-оксо-1-пирролидинацетамида.
Настоящее изобретение касается, таким образом, применения леветирацетама для приготовления лекарств для лечения биполярных расстройств, мании, мигрени и хронической или невропатической боли.
Настоящее изобретение касается также способа лечения мигрени, биполярных расстройств, мании, хронической или невропатической боли, включающего введение терапевтической дозы леветирацетама пациенту, нуждающемуся в таком лечении.
Термин "лечение", используемый в данной заявке, означает целебное лечение и профилактическое лечение.
Термин "целебное" означает здесь эффективность лечения осложнений (например, маниакальных периодов или депрессивных периодов в случае биполярных расстройств).
Термин "профилактическое" означает предотвращение возникновения или повторения маниакальных/депрессивных периодов, приступов мигрени или невропатической боли.
Термин "мигрень" означает расстройство, характеризующееся повторяющимися приступами головной боли, которые сильно отличаются друг от друга по интенсивности, частоте и продолжительности. Головная боль обычно бывает односторонней и часто связана с анорексией, тошнотой, рвотой, фонофобией и/или фотофобией. В некоторых случаях приступам головной боли предшествуют неврологические расстройства и ухудшение настроения или же эти приступы связаны с указанными нарушениями. Приступы мигрени могут длиться от 4 до примерно 72 часов. Международное общество изучения головных болей (IHS, 1988) классифицирует мигрень на следующие основные типы: мигрень с аурой (классическая мигрень) и мигрень без ауры (обычная мигрень). Мигрень с аурой состоит из периода головной боли и предшествующих ему характерных визуальных, сенсорных, речевых или моторных симптомов. В отсутствие таких симптомов головная боль называется мигренью без ауры.
Цифры о распространенности этого заболевания за 1 год зависят в основном от возраста и пола (Ferrari М. D. "Migraine" The Lancet (1998); 351:1043-1051 - SheffieldR. E. "Migraine prevalence: a literature review" Headache (1998); 38:595-601).
Десять процентов всего населения (6% мужчин и 15% женщин) страдают от приступов мигрени. Пики распространенности заболевания приходятся на возраст 35-50 лет у женщин и 25-35 лет у мужчин. У возрастной группы от 10 до 19 лет распространенность заболевания сильно зависит от возраста: пик приходится на возраст около 14-16 лет. До наступления полового созревания распространенность заболевания у юношей и девушек одинакова. Среди взрослых отношение числа женщин к числу мужчин составляет примерно 2,5:1. Данные о распространенности заболевания за год свидетельствуют, что мигрень без ауры встречается в 1,5-7 раз чаще, чем мигрень с аурой.
Методы лечения мигрени можно разделить на четыре типа: общие меры, абортивная терапия, методы облегчения боли и профилактические (Silberstein S. D. "Preventive treatment of migraine: an overview" Cephalalgia (1997); vol. 17, p. 67-72 -Diamond M. L. "Contemporary diagnosis and management ofheadache and migraine" (1998); First Edition. Handbooks in Health Care Co., Newtown, Pennsylvania, USA. Diener H.., Kaube H., Limmroth V. "A practical guide to the management and prevention of migraine", Drugs (1998); vol.56(5): p.811-824).
Общие меры могут включать регулярный сон, регулярный прием пищи, соблюдение диеты и т.д. Существует целый ряд агентов, используемых при абортивном лечении, от простых анальгетиков, таких как ацетилсалициловая кислота, не стероидные противовоспалительные средства (NSAID), эрготические соединения, антиемстики, до появившихся недавно агонистов серотонина (5-НТ) (триптановых соединений).
Средства для облегчения боли могут включать NSAIDs, наркотические анальгетики или терапевтические методы. Для хронических случаев используют целый ряд препаратов, применяемых для профилактики мигрени. Профилактическое лечение обычно предусматривает прием лекарств каждый день в течение ряда месяцев или лет. Его следует назначать пациентам, у которых бывает два или более приступов мигрени в месяц. Бета-адриноцепторные блокаторы - в основном пропранол, считаются эффективными для профилактики мигрени. Таким же эффективным является лекарство для лечения эпилепсии - дивальпрекс натрия. Другие соединения включают трицикпические антидепрессанты (амитриптилин), блокаторы кальциевых каналов (нифедипин, флунаризин, верапамил), NSAIDs (кетопрофен, напроксен), рибофлавин (витамин В2) и 5-НТ антагонисты.
Традиционными теориями патогенеза мигрени являются вазогенная теория и нейрогенная теория. Ни одна из них не объясняет полностью все клинические явления, наблюдаемые во время приступа мигрени.
Современные взгляды на патофизиологию мигрени принимают во внимание как неврологические, так и сосудистые явления в начале приступа. Эндогенные нейрофизиологическис явления активируют тригеминоваскулярные волокна в стволе мозга с последующим периваскулярым высвобождением вазактивных нейропептидов. При проведении опытов на животных было установлено, что эти нейропептиды промотируют нейрогенный воспалительный ответ, состоящий из вазодилатапии и длительной плазменной транссудации. Кортикально распространяющаяся депрессия (CSD) описана как медленно распространяющиеся волны ингибирования кортикальных нейронов, что связано с клиническими симптомами ауры. Экспериментальная CSD может активировать тригемино-сосудистую систему в стволе мозга, создавая возможную связь между механизмами ауры и головной боли. Существуют некоторые данные о том, что 5-НТ действует как нейротрансмиттер и гуморальный медиатор в невральных и сосудистых компонентах мигрени.
Пациенты, страдающие мигренью, имеют системное нарушение 5-НТ-метаболизма.
Существует теория, что люди, склонные к мигрени, характеризуются пониженным порогом нейронной возбудимости, возможно, благодаря пониженной активности ингибирующего нейротранемиттера гамма-амино-масляной кислоты (GABA). GABA обычно снижает клеточное действие нейротрансмиттера серотонина (5-НТ) и глютамата, которые оба принимают участие в приступах мигрени.
Дивальпрекс натрия представляет собой стабильное координационное соединение, содержащее вальпроат натрия и вальпроевую кислоту в мольном отношении 1:1. Нарушенный GABA метаболизм наблюдается у пациентов, страдающих от мигрени, во время приступов мигрени были обнаружены изменения в уровнях цереброспинальной GABA. Полагают, что дивальпрекс натрия увеличивает содержание в мозгу гамма-аминомасляной кислоты (GABA), снижая ее разложение. Повышенная активность GABA систем может влиять на возникновение мигрени прямо или косвенно по целому ряду механизмов. Возможные косвенные механизмы включают снижение скорости серотонергических нейронов в дорсальной линии ядрышка.
Термин "вальпроат" означает вальпроевую кислоту и ее производные, такие как вальпромид, вальпроат пивоксил, вальпроат магния, дивальпрекс натрия, вальпроат натрия и полувальпроат натрия.
Известно, что вальпроат повышает эндогенные уровни энкефалина в мозгу, что играет решающую роль в процессе обезболивания.
Было установлено, что вальпроат снижает уровень возбудительных аминокислот в мозгу, затрагивая CSD Mathew NT and col., "Migraine prophylaxis with divalproex" Arch. Neurol. (1995); vol.52: p.281-286 - Welch KM, D'Andrea G., Tepley N., Barkley G., Ramadan N.M., "The concept of migraine as a state of central neuronal hyperexcitability" Neurol. Clin. (1990); vol.8: p.817-828).
Наиболее часто встречающиеся побочные эффекты, связанные с вальпроатом, представляют собой тошноту, рвоту, несварение, астению, сонливость, головокружение, тремор, потерю веса и алопецию. Поскольку большинство побочных эффектов связано с дозировкой, пациент и больной должны стремиться к самой низкой из возможных терапевтических доз.
Известно, что вальпроат связан с риском развития печеночной недостаточности, особенно у маленьких детей. Необходимо осуществлять исследование работы печени с регулярными интервалами. Сообщалось, что вальпроат имеет тератогенное действие, например, вызывая повреждение нервной трубки.
Тем не менее, предотвращение приступа мигрени предпочтительнее, чем ослабление приступа, так как профилактическое лечение легче переносится больными. Это особенно справедливо в более тяжелых случаях, когда пациенты страдают от частых приступов. Конечной целью в любом случае является полное избавление от приступов при продолжительном профилактическом лечении. До сих пор эта цепь достигалась только при применении вальпроата, но ценой проявления побочных эффектов, упомянутых выше, при наличии противопоказаний (например, взаимодействие с другими лекарствами, возможный порок развития).
Существует действительная необходимость в создании альтернативных средств и получении соединения с терапевтическим действием, более походящим для лечения и особенно для профилактического лечения этой патологии.
Для демонстрации особенной пригодности леветирацетама для лечения мигрени с хорошим терапевтическим действием проводились клинические испытания по методике, известной специалистам.
Такая активность является неожиданной вследствие того, что леветирацетам не оказывает прямого действия на GABA систему (Н. Klitgaard and col., "Evidence for a unique profile of levetiracetam in rodent models of seizures and epilepsy" European Journal of Pharmacology (1998); vol.353, p.191-206). Полагали, что имеет место GABA ингибирование, но обширные in vitro исследования не показали никакого значительного вытеснения лигандов, специфического для 55 различных сайтов связывания, включая различные системы рецепторов, сайты повторного поглощения, системы вторичных мессенджеров и канальные протеины (М. Noyer and col. "The novel antiepileptic drug levetiracetam (ucb L059) appears to act via a specific binding site in CNS membranes" European Journal of Pharmacology (1995), vol.286, p.137-146). Кроме того, леветирацетам не модулирует потоки хлоридов, индуцированных мусцимолом. Наконец, отсутствие действия на содержание GABA и ферментативные активности GABA трансаминазы и глутаминовой декарбоксилазы было установлено при нейрохимическом исследовании мозга мыши (G.J.Sills and col. "Neurochemical studies with the novel anticonvulsant levetiracetam in mouse brain" European Journal of Pharmacology (1997), vol.325, p.35-40). Вальпроат является единственным лекарством против эпилепсии, которое было одобрено из-за его эффективности при профилактическом лечении головной боли при мигрени, следовательно, не было оснований ожидать, что лекарство против эпилепсии, леветирацетам, с другим, до сих пор неизвестным видом активности, будет особенно пригодно для лечения мигрени.
По этим причинам полагают, что лечение или профилактическое лечение при помощи леветирацетама будет приводить к хорошим результатам, проявляющимся в уменьшении приступов и улучшении состояния и способности работать.
Термин "биполярные расстройства" поясняется ниже.
Биполярные расстройства классифицируются как нарушения настроения в соответствии с Diagnostic and Statistical Manual of Mental Disorders, 4th edition (Diagnostic and Statistical Manual of Mental Disorders (DSM-IV TM), American Psychiatry Association, Washington, DC, 1994). Биполярные расстройства характеризуются, в общем, спонтанно возникающими повторяющимися (а именно, по меньшей мере, двумя) приступами, во время которых сверхвозбудимость, активность и настроение больного значительно изменяются, в некоторых случаях это изменение заключается в улучшении настроения, увеличении энергии и активности (мания или гипомания), а в других случаях - в ухудшении настроения и снижении энергии и активности (депрессия).
Биполярные расстройства подразделяются на четыре основных категории DSM-IV (биполярное расстройство I, биполярное расстройство II, циклотимия и другие биполярные расстройства).
Характерный признак биполярного расстройства I состоит в клиническом течении болезни, характеризующейся одним или несколькими маниакальными приступами, чередующимися с одним или несколькими приступами депрессии.
Существенный признак биполярного расстройства II состоит в клиническом течении болезни, характеризующейся одним или несколькими приступами депрессии, сопровождающимися, по меньшей мере, одним приступом гипомании. При этом приступы мании или смешанные приступы не наблюдаются.
Циклотимия характеризуется многочисленными периодами гипоманиакальных симптомов, не характерными для маниакальных приступов, и периодами симптомов депрессии, не характерных для приступов депрессии.
Другие виды биполярных расстройств могут дополнять шизофрению, бред или другие психические расстройства. Если происходит очень быстрое изменение (в течение дней) маниакальных и депрессивных симптомов (например, несколько дней ярко выраженных маниакальных симптомов с последующими несколькими днями ярко выраженных депрессивных симптомов), которое не соответствует по минимальной длительности приступу мании или приступу депрессии, диагнозом являются биполярные расстройства, не названные выше.
Под приступом мании подразумевается четко выраженный период, в течение которого наблюдается ненормально и устойчиво повышенное экспансивное или раздраженное настроение с признаками ускоренной речи и психомоторного возбуждения.
Под гипоманией подразумевают менее выраженный приступ мании, являющийся не таким серьезным.
Смешанный приступ характеризуется периодом времени (по меньшей мере одна неделя), в течение которого почти каждый день наблюдаются как маниакальные, так и основные приступы депрессии.
В течение десятилетий лечение мании и маниакальных приступов биполярных расстройств, в основном, было направлено на применение солей лития. В последние годы неполное излечение и непереносимость, обусловленные длительным применением лития (Li+) при лечении биполярных расстройств, привело к необходимости создания альтернативных методов лечения. Клинические испытания показывают, что во время острой фазы биполярного расстройства до 40% пациентов не поддавались лечению при помощи лития (Gustavo et al., Anticonvulsant for treatment of manic depression; Current Drug Therapy, vol.56, N 8, 1989).
Во время испытаний наблюдался ряд проблем, связанных с длительным применением лития. Так, в 25% случаев во время лечения в течение более 2 лет наблюдались хроническая интерстипиальная нефропатия, полиурия, несахарный диабет или нефрогенный несахарный диабет. Далее, использование лития часто вызывает дизартрию, дрожание, атаксию, гипотиреоз (30% субъектов в первые 2 года) и импотенцию.
Один из альтернативных методов состоит в применении антиконвульсанта, вальпроата, который, как это было установлено, обладает антиманиакальной активностью, а также стабилизирует настроение. Однако полученные результаты не являются удовлетворительными и, более того, вальпроат приводит к появлению различных побочных эффектов. Обычные побочные эффекты вальпроата относятся к желудочно-кишечному тракту, проявляясь в возникновении тошноты, рвоты, анорексии и диареи, как указано в предыдущем параграфе.
Фармакологические испытания показали, что в терапевтически активных дозах вальпроат вызывает значительную гиперактивность при введении здоровым контрольным грызунам. Профилактическое применение вальпроата, таким образом, может вызвать у больных эффект, обратный желательному, и/или вызвать легкую гиперактивность после каждого приема таблетки. Точно также во время активного лечения вальпроат способен поддерживать состояние гиперактивности после того, как маниакальная фаза закончится. Наконец, это исследование показало трудности в подборе нужной дозы лития или вальпроата субъекту. Таким образом, в случае этих двух соединений небольшая передозировка имеет тенденцию снижать активность грызунов по сравнению с контрольными грызунами.
Поэтому действительно существует необходимость создания альтернатив литию или вальпроату для того, чтобы избежать многочисленных побочных эффектов и создать соединение с более подходящим для лечения вышеописанной патологии терапевтическим действием.
Неожиданно было установлено, что леветирацетам, в добавление к его активности вызывает только небольшую гиперактивность у контрольных крыс без всяких маниакальных симптомов. Следовательно, леветирапетам будет особенно пригоден для лечения мании.
Еще одним неожиданным преимуществом леветирацетама является нормализация уровня активности контрольных субъектов в отличие от лития и вальпроата.
Таким образом, в случае вальпроата и лития слишком высокая доза этих соединений может привести к пониженной активности по сравнению с нормальным состоянием пациента, чего необходимо избегать. Следовательно, леветирапетам обладает определенными преимуществами, так как он позволяет практикующему врачу более легко подобрать дозы пациенту, не рискуя вызвать побочные эффекты, заключающиеся в пониженной активности, из-за передозировки. Кроме того, сводятся к минимуму последствия ошибочного приема таблеток.
Наконец, с учетом вводимых терапевтических доз леветирапетам также имеет преимущество, так как эти дозы гораздо меньше доз, вызывающих побочные эффекты, а такие соединения, как вальпроат или карбамазепин имеют гораздо меньший интервал безопасности (А.J. Gower et al., Eur. J. Pharmacol., 22, p.193-203 (1992) - W. Loscher and D. Honack, Eur. J. Pharmacol., 232, p.147-158 (1993) - H. Klitgaard, A. Matagne, J. Gobert, E. Wulfert, Eur. J. Pharmacol., 353, р.191-206 (1998).
Этот неожиданный спектр свойств означает, что леветирацетам представляет особый интерес для производства лекарства для лечения биполярных расстройств. Это соединение имеет предел безопасности, недостижимый ранее для подобных терапевтических средств.
Термин "хроническая боль", используемый в данной заявке, означает болезнь, отличающуюся от острой боли. Обычно определяемая как боль, которая продолжается и после окончания обычного периода выздоровления, боль также считается хронической, когда больной осознает, что боль становится неотъемлемой частью его жизни в обозримом будущем. По всей видимости, большинство синдромов хронической боли включает невропатический компонент, который обычно поддается лечению труднее, чем острая соматическая боль.
Самыми яркими примерами синдрома невропатической боли являются диабетическая периферическая невропатия и невралгия при опоясывающем лишае. Первичный синдром соматической хронической боли характерен для пациентов с ревматоидным артритом или другими ревматическими заболеваниями. С другой стороны, самый распространенный синдром хронической боли, включающий боль, связанную с полученной травмой, часто связан с системами различных органов. Основной причиной хронической боли является рак, который способен проникать в ткани различных органов и повреждать ряд систем. Следовательно, большинство посттравматических и раковых больных страдают от боли, развивающейся как по соматическому, так и по невропатическому механизмам (Н. С. Hansen, MD "Treatment of chronic Pain With Antiepileptic Drugs: A New Era" South Medical Journal - Southern Medical Association (1999), 92(7), p.642-649).
Термин "невропатическая боль" означает боль, вызванную патологическим изменением в нерве, которая сигнализирует о наличии вредного раздражителя, когда нет такого узнаваемого раздражителя, давая начало ложному ощущению боли. Другими словами, оказывается, что включилась и не может отключиться болевая система. Это может относиться к периферическим или центральным (спинальным или мозговым) патологическим нервным поражениям или дисфункции нервной системы.
Невропатическая боль может проявляться как результат таких состояний, как повреждение нерва (например, хирургическая операция, несчастный случай, ампутация), травма, задевшая конечность (с очевидным повреждением нерва или без него), болезни, поражающие нервную систему, инфаркт, связанный с нервной системой, анормальная функция нерва, спинальные и корешковые болезненные ощущения.
Под повреждением нерва подразумевают такие состояния, как фантомная боль (боль в ампутированной конечности), боль в культе (боль в месте ампутации), фантомные безболезненные ощущения в ампутированной конечности, послеоперационные боли, таламический болевой синдром (боль после инсульта). Под травмой, затронувшей конечности, подразумеваются состояния, такие как рефлекторная симптоматическая дистрофия, каузалгия. Под болезнями, поражающими нервную систему, подразумеваются такие состояния, как диабетическая невропатия, другие виды невропатии, невралгия тройничного нерва (TN), невралгия при опоясывающем лишае (PHN), множественный склероз, невропатия, связанная со СПИД, невропатия, вызванная раком (после химиотерапии) (S.Troel, М.D.Jensen "Mechanisms of Neuropathic Pain" Pain 1996-An updated review, IASP Press, Seattle (1996), p.77-86).
Хроническая и/или невропатическая боль остаются синдромами боли, которые наиболее трудно поддаются лечению, поэтому существует необходимость в создании новых активных веществ.
В течение почти тридцати лет в лекарственном лечении хронической и невропатической боли был достигнут очень небольшой прогресс, поэтому оно остается ограниченным применением антидепрессантов, нестероидных противовоспалительных лекарственных средств, местных анестетиков и антиконвульсантов.
Ряд антиконвульсантов, таких как вальпроат или карбамизепин, проявляют активность при лечении этих болезненных состояний, но другие, такие как пентобарбитал, не эффективны (H.L.Fields et al., Excitability Blockers, p.93-116 - H.С.Hansen MD ""Treatment of chronic Pain With Anticpileptic Drugs: A New Era" South Medical Journal - Southern Medical Association (1999), 92(7), p.642-649).
При применении карбамазепина следует применять меры предосторожности, так как разница между терапевтической дозой и дозой, вызывающей побочные эффекты, чрезвычайно мала. Кроме того, дозировка, вызывающая эти эффекты, зависит от пациента. Таким образом, практикующий врач должен быть чрезвычайно осторожным при подборе этих доз каждому индивидуальному больному. Побочные эффекты могут включать седативный эффект, атаксию, головокружение, затуманенное зрение, а также тошноту и рвоту. Кроме того, почти у 10% пациентов наблюдается легкая лейкопения (H.L.Fields et al., Excitability Blockers, p.93-116).
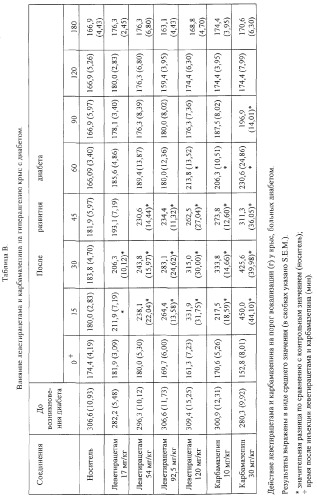
Карбамазепин, который относится к антиэпилептикам, является эталоном для фармакологических исследований в области лечения хронической и невропатической боли, обладает выраженной активностью в процессе ингибирования искусственновызванной боли или гипералгизии. Однако фармакологические исследования подтвердили, что кривая доза - активность не только возвращает болевое ощущение к контрольному пороговому значению (изменение гипералгезии), но и вызывает частичную десенсибилизацию у подвергаемых лечению субъектов (изменение нормального порогового ощущения). Поэтому при терапевтических дозах наблюдается антинопицептивный эффект, и животное больше не чувствует боли, ощущаемой в нормальном состоянии. Такая десенсибилизация может быть особенно нежелательной для пациента, Таким образом, если пациент, желающий уменьшить хроническую и невропатическую боль, примет слишком большую дозу карбамазепина, он будет ощущать частичную десенсибилизацию из-за более высокого порога чувствительности, он будет гораздо менее чувствителен к любому внешнему неблагоприятному воздействию, такому как тепло, раздражение или т.п. и рискует получить травмы или ожог.
Фармакологические исследования показали, что леветирацетам ведет себя неожиданно при лечении хронической или невропатической боли. В противоположность карбамазепину это вещество нормализует кривую доза/активность до контрольного порогового значения (то есть ответ до развития диабета). Таким образом, применение леветирацетама позволяет гораздо меньше рисковать в случае передозировки.
Кроме того, при использовании терапевтических доз леветирацетам можно использовать в дозах, гораздо меньших, чем те, которые вызывают вторичные эффекты, в то время как такие соединения, как карбамазепин, имеют гораздо более узкий интервал безопасных доз. Такое неожиданное сочетание свойств означает, что применение леветирацетама имеет большое значение для приготовления лекарства для лечения хронической и/или невропатической боли.
Настоящее изобретение предусматривает введение эффективной дозы леветирацетама при лечении биполярных расстройств, мигрени и хронической или невропатической боли. Доза, требующаяся согласно данному изобретению, должна быть довольно высокой для того, чтобы привести к облегчению биполярных расстройств, мигрени и хронической или невропатической боли. Фармкомпозипии, содержащие леветирацетам, могут вводиться, например, перорально или парентерально, например, внутривенно, внутримышечно или подкожно или внутриоболочечно.
Таким образом, настоящее изобретение касается также фармацевтической композиции для лечения биполярных расстройств, мании, мигрени и хронической или невропатической боли, включающей терапевтически эффективное количество леветирацетама и фармацевтически приемлемый носитель.
Фармацевтические композиции, используемые для перорального введения могут быть твердыми или жидкими и могут быть, например, в виде таблеток, пилюль, драже, желатиновых капсул, растворов, сиропов и т.д.
Для этой цели леветирацетам можно применять в смеси с инертным разбавителем или нетоксичным фармацевтически приемлемым носителем, например, крахмалом или лактозой. Эти фармацевтические композиции могут также содержать связующее, такое как микрокристаллическая целлюлоза, трагакантовая смола или желатин, дезинтегрант, такой как альгиновая кислота, смазывающий агент, такой как стеарат магния, агент, улучшающий скольжение, такой как коллоидная двуокись кремния, подсластитель, такой как сахароза или сахарин, красящие вещества или ароматизатор, такой как перечная мята или метилсалипилат. Они также включают композиции с регулируемым выделением активного ингредиента.
Фармацевтические композиции, которые могут быть использованы для парентерального введения, представляют собой фармацевтические формы, известные для этого метода введения, и могут быть в виде водных или масляных растворов или суспензий, обычно содержащихся в ампулах, шприцах, стеклянных или пластиковых флаконах или контейнерах для инфузии. Кроме активного ингредиента эти растворы или суспензии могут также содержать стерильный разбавитель, такой как вода для инъекции, физиологический раствор, масла, полиэтиленгликоли, глицерин, пропиленгликоль или другие синтетические растворители, антибактериальные агенты, такие как бензиловый спирт, антиоксиданты, такие как аскорбиновая кислота или бисульфит натрия, хелатирующие агенты, такие как этилендиаминтетрауксусная кислота, буферные агенты, такие как ацетаты, цитраты или фосфаты, и агенты для регулирования осмомолярности, такие как хлорид натрия или декстроза.
Эти фармацевтические формы получают, применяя методы, используемые в фармацевтике.
Дневная доза активного ингредиента, вводимая пациенту, находится в широком интервале и зависит от различных факторов, таких как пол пациента, возраст, вес, состояние здоровья, а также метода введения. Так, количество активного ингредиента в композиции для перорального введения составляет, по меньшей мере, 5 вес.% и может быть до 80% от веса композиции.
Клинические исследования, проведенные с участием добровольцев, показали, что леветирацетам хорошо переносится при введении единичной дозы (до 5,000 г) и повторяющихся доз (1500 мг/день в течение 14 дней). Предварительные данные, полученные при исследовании переносимости, показывают, что больные эпилепсией хорошо переносят дозы до 4000 мг/день).
Перорально вводимые композиции предпочтительно содержат 50-300 мг, более предпочтительно 250-1500 мг леветирацетама на дозу.
В композициях для парентерального введения количество леветирацетама составляет 0,5 вес.% и может быть до 33% от веса композиции. Единица дозы предпочтительных парентеральных композиций содержит 1-400 мг леветирацетама.
Дневная доза леветирацетама может меняться в широких пределах и обычно составляет 5-70 мг/кг. Однако следует иметь в виду, что в конкретных случаях в зависимости от индивидуальных особенностей врач может подобрать особые дозировки.
Леветирацетам может применяться в отдельности или в сочетании с, по меньшей мере, еще одним фармацевтически активным ингредиентом для лечения указанных патологических состояний. Не ограничивающие объем изобретения примеры таких соединений, которые можно применять в сочетании с леветирацетамом, включают антивирусные агенты, антиспастические агенты (а именно, баклофен), противорвотные агенты, агенты, стабилизирующие настроение, анальгетики (а именно, аспирин, ибупрофен, парацетамол), наркотические анальгетики, местные анестетики, ориоидные анальгетики, соли лития, антидепрессанты (а именно, миансерин, флуоксетин, тразодон), трициклические антидепрессанты (а именно, имипрамин, дезипрамин), противосудорожные средства (а именно, вальпроат, карбамазепин, фенитоин...), антипсихотические средства (а именно, рисперидон, галоперидол), нейролептики, бензодиазепины (а именно, диазепам, клоназепам), фенотиазины (а именно, хлорпромазин), блокаторы кальциевых каналов, амфетамин, кпонидин, лидокаин, мексилетин, капсайцин, каффеин, кветиапин, антагонисты серотонина, β-блокаторы, антиаритмические средства, триптаны, производные спорыньи.
В частности, было обнаружено, что леветирацетам повышает активность соединений, индуцирующих невральное ингибирование, опосредованное рецепторами GABAA, без обострения побочных эффектов. В результате этой неожиданной фармакологической селективности пациенты, подвергающиеся монотерапии с применением этих соединений и страдающие от побочных эффектов, могут получить более эффективное лечение при комбинированном введении этих соединений с небольшим количеством леветирацетама.
Таким образом, данное изобретение также относится к тому неожиданному факту, что леветирацетам, известный как антиэпилептик, является эффективным стимулятором противосудорожных средств и противоманиакальной активности вальпроата, клоназепама, хлордиозэпоксида, фенобарбитала и их фармацевтически приемлемых солей.
Примерами соединений, индуцирующих невральное ингибирование, опосредованное GABAA рецепторами, являются следующие вещества: бензодиазепины, барбитураты, стероиды и противосудорожные агенты, такие как вальпроат, виагабатрин, тиагабин или их фармацевтически приемлемые соли.
Бензодиазепины включают 1,4-бензодиазепины, такие как диазепам и клоназепам, и 1,5-бензодиазепины, такие как клобазам. Предпочтительным соединением является клоназепам.
Барбитураты включают фенобарбитал и пентобарбитал. Предпочтительным соединением является фенобарбитал.
Предпочтительные противосудорожные средства включают вальпроевую кислоту, вальпромид, вальпроат пивоксил, вальпроат натрия, полувальпроат натрия, дивальпрекс, клоназепам, фенобарбитал, вигабатрин, тиагабин.
Предпочтительными соединениями являются вальпроевая кислота, вальпромид, вальпроат пивоксил, дивальпрекс, вальпроат натрия и полувальпроат натрия, еще более предпочтительным соединением является вальпроат натрия. Для лечения эпилепсии рекомендуемая начальная доза вальпроата для взрослого в Европе составляет 600 мг/день, эту дозу увеличивают на 200 мг с интервалом в 3 дня, пока не будет достигнут контроль над припадками или же дальнейшее увеличение дозы не приведет к проявлению побочных эффектов. Обычная доза равна 1-2 г/день (20-30 мг на кг веса пациента в день) при максимальной дневной дозе 2,5 г.
Дневная доза, рекомендуемая для детей весом более 20 кг, составляет 20-30 мг/кг/день. Для детей весом менее 20 кг рекомендуется доза 20 мг/кг/день; в случае когда требуется доза более 40 мг/кг/день, следует контролировать параметры клинической химии и гематологические показатели. Для пожилых людей дозы вальпроата должны быть меньше вследствие изменений фармакокинетических параметров. Для большинства пациентов терапевтическая концентрация вальпроата в плазме составляет 40-100 мкг/мл.
Количество активных ингредиентов (леветирацетам и соединение, индуцирующее невральное ингибирование, опосредованное GABAA рецепторами) в соответствии с этим аспектом изобретения будет меняться в зависимости от млекопитающего, которому вводят композицию, вида подвергаемой лечению болезни, наличия других активных ингредиентов и т.д. Обычно количество соединения, индуцирующего невральное ингибирование, опосредованное GABAA рецепторами, и количество леветирацетама для данной композиции и данной дозированной формы можно легко определить рутинными методами.
Соответственно данное изобретение касается фармацевтической композиции, содержащей леветирацетам и, по меньшей мере, одно соединение, индуцирующее невральное ингибирование, опосредованное GABAA рецепторами.
Фармацевтическая композиция по данному изобретению содержит терапевтически эффективное количество соединения, индуцирующего невральное ингибирование, опосредованное GABAA рецепторами, и терапевтически эффективное количество леветирацетама, предпочтительно в отношении 2-15.
Фармацевтические композиции согласно изобретению могут вводиться перорально или парентерально, как указано выше.
Композиции, содержащие уменьшенную дозу вальпроата, также представляют интерес.
Композиции по изобретению можно использовать для лечения эпилепсии и борьбы с припадками, для лечения депрессии, биполярных расстройств, хронической или невропатической боли и для лечения мигрени и других заболеваний, контролируемых при помощи соединения, индуцирующего невральное ингибирование, опосредованное GABAA рецепторами. Требуемая эффективная доза зависит от состояния больного и его индивидуальных характеристик.
В фармацевтических композициях по изобретению количество леветирацетама является, по меньшей мере, достаточным для возбуждения активности соединения, индуцирующего невральное ингибирование, опосредованное GABAA рецепторами.
Предпочтительная композиция содержит леветирацетам в количестве, по меньшей мере, достаточном для уменьшения количества соединения, индуцирующего невральное ингибирование, опосредованное GABAA рецепторами при сохранении нужного терапевтического эффекта.
Другая предпочтительная композиция содержит соединение, индуцирующее невральное ингибирование, опосредованное GABAA рецепторами, в таком количестве, которое при введении отдельно не будет терапевтически эффективным, и леветирацетам в количестве, по меньшей мере, достаточном для получения необходимого терапевтического эффекта.
Как указано ниже в примере 4, повышение активности леветирацетама означает, что обычное эффективное количество соединения, индуцирующего невральное ингибирование, опосредованное GABAA рецепторами, может быть уменьшено в 3-15 раз при сохранении желательного терапевтического эффекта. Например, обычное количес