Способ получения микросферического сорбента для очистки жидких отходов от радионуклидов, ионов цветных и тяжелых металлов
Иллюстрации
Показать всеИзобретение относится к сорбентам, полученным из микросферических компонентов летучих зол тепловых электростанций. Для синтеза микросферического сорбента используют ценосферы, выделенные из летучих зол от сжигания каменного угля и стабилизированные по составу методами гранулометрической классификации, гравитационной и магнитной сепарации. Предварительно ценосферы перфорируют обработкой раствором травления на основе минеральной кислоты, после чего проводят осаждение активного компонента во внутреннем объеме микросферического носителя. В качестве активного компонента вводят неорганические ионообменные материалы (молибдофосфат аммония, ферроцианиды и сульфиды переходных металлов, фосфат магния, карбонат магния и др.) или органические экстрагенты (триоктилфосфиноксид, триизобутилфосфинсульфид и др.). Осаждение активного компонента ведут из его пересыщенных органических растворов или путем синтеза непосредственно во внутреннем объеме микросферического полого носителя. Полученный сорбент эффективен для извлечения радионуклидов, цветных и тяжелых металлов и металлов платиновой группы. 5 з.п. ф-лы, 1 табл., 2 ил.
Реферат
Изобретение относится к сорбентам, полученным из техногенного сырья, в частности из микросферических компонентов летучих зол тепловых электростанций, и может быть использовано в ядерной энергетике и химико-металлургической промышленности для очистки жидких радиоактивных отходов и сточных вод гидрометаллургических производств от радионуклидов, ионов цветных и тяжелых металлов, а также для доизвлечения металлов платиновой группы, преимущественно палладия, из сбросных растворов и пульп.
Сорбционная технология, в том числе с использованием твердых экстрагентов (ТВЭКСов), считается более эффективной по сравнению с жидкостной экстракцией в случае выделения металлов из очень разбавленных растворов (менее 1 мг/л). Известны неорганические ионообменные материалы (сульфиды, оксиды, гидроксиды, фосфаты, ферроцианиды, гетерополисоединения и др.) [Вольхин В.В. Селективные неорганические сорбенты и их применение // Химия и технология неорганических сорбентов. Межвузовский сборник научных трудов. Пермский политехнический институт, 1980, с.3-19] и органические экстрагенты, специфичные в отношении катионов металлов определенного типа [Мазуренко Е.А. Справочник по экстракции. Киев: Техника, 1972, 448 с.], которые применяются для очистки жидких отходов радиохимических и гидрометаллургических производств от радионуклидов, катионов цветных и тяжелых металлов, металлов платиновой группы. Механически прочные формы твердых сорбентов на основе неорганических ионообменников (композитные сорбенты) и органических экстрагентов (ТВЭКСы) могут быть получены нанесением активного компонента на пористые неорганические или органические полимерные носители.
Так, твердые экстрагенты для извлечения из растворов палладия, серебра и ртути в режиме экстракционной хроматографии получают нанесением триизобутилфосфинсульфида и экстрагентов близкой природы на органический носитель на основе сополимеров стирола и дивинилбензола [Dakshinamoorthy А., Kumar Т., Nandy К.К., et al. Separation of palladium by extraction chromatographic technique using Cyanex 471X (tri isobutyl phosphine sulphide) on Chromosorb-102 // Journal of Radioanal and Nucl. Chemistry, 2000, Vol.245, No.3, p.595-598], кизильгур, пористые стеклянные шарики [Пат. США №4623522, 1986 г.] или силикагель [Singh R., Khwaja A.R., Gupta В., et al. Uptake and extraction chromatographic separation of mercury (II) by triisobutylphosphine sulfide (TIBPS) sorbed on silica gel and decontamination of mercury containing effluent // Talanta, 1999, V.48, p.527-535}. Такие ТВЭКСы эффективно извлекают серебро и палладий из водных растворов, однако, не могут быть использованы для извлечения указанных компонентов из гетерогенных сред, содержащих взвешенные твердые частицы.
Композитные сорбенты на основе неорганических ионообменников для извлечения из жидких радиоактивных отходов (ЖРО) радионуклида 137Cs получают нанесением гексацианоферратов (II) переходных металлов на волокнистый или гранулированный целлюлозный носитель {Пат. РФ №2111050, 1998 г.], а также на силикагель [Пат. США №6046131, 2000 г.]. За рубежом разработан композитный селективный сорбент 137Cs на основе аммонийной соли молибдофосфорной гетерополикислоты, введенной в полимерную матрицу из полиакрилонитрила (АМФ-ПАН) [Tranter Т.J., Herbsta R.S., Todd Т.A., et al. Evaluation of ammonium molybdophosphate-polyacrylonitrile (AMP-PAN) as a cesium selective sorbent for the removal of 137Cs from acidic nuclear waste solutions // Advances in Environmental Research, 2002, V.6, p.107-121]. Однако несмотря на высокую эффективность органоминеральных сорбентов на стадии сорбции, на конечной стадии кондиционирования радиоактивных отходов возникает проблема перевода насыщенного радионуклидами сорбента в минералоподобную устойчивую форму, пригодную для долговременного захоронения. При использовании традиционных неорганических носителей (силикагель, алюмогель) высока вероятность уноса с поверхности сорбента высокодисперсной фазы неорганического активного компонента в процессе контактирования с растворами радиоактивных и других токсичных элементов.
Наиболее близким к заявляемому изобретению является микросферический цеолитный сорбент для очистки жидких отходов от радионуклидов, ионов цветных и тяжелых металлов (Пат. РФ №2214858, 2003 г.), который содержит один или несколько цеолитов типа NaX, NaA или NaP1, локализованных в матрице микросферического полого носителя диаметром до 400 мкм. Сорбент получают путем гидротермальной обработки полых алюмосиликатных микросфер энергетических зол (ценосфер) в присутствии активирующего раствора, при этом синтез цеолитов протекает как на внешней, так и на внутренней поверхности полых микросфер. Обменная емкость сорбента в отношении цезия и стронция составляет 2 мг-экв/г сорбента, а по катионам Ni, Cu, Cr, Co, Cd, Hg, Zn - около 1 мг-экв/г. Несмотря на широкий спектр извлекаемых катионов, цеолитный сорбент обеспечивает высокие степени очистки лишь в узкой области кислотности (рН 3-7) и при низком содержании солевого фона (не более 0,1 г-экв Na+/л). Сорбент выбран за прототип.
Целью изобретения являются сорбенты в форме полых сферических гранул размером до 400 мкм с пористой стеклокристаллической оболочкой и локализованным во внутреннем свободном объеме активным компонентом. Другой целью изобретения является получение микросферических сорбентов на основе ценосфер энергетических зол, активными компонентами которых являются неорганические ионообменники и органические экстрагенты.
Указанная цель достигается тем, что ценосферы предварительно перфорируют обработкой реагентом травления на основе минеральной кислоты, а введение активного компонента во внутренний объем осуществляют путем его синтеза непосредственно в полости ценосфер или осаждения из пересыщенных органических растворов.
Сущность заявленного изобретения заключается в следующем. Ценосферы летучих зол являются доступным и относительно дешевым алюмосиликатным материалом, получаемым в качестве побочного продукта при сжигании угля на тепловых электростанциях. Ценосферы летучих зол кузнецких углей характеризуются следующим химическим составом (мас.%): SiO2 - 63,1-65,2; Al3O3 - 20-26,4; Fe2O3 - 4,2-5,1; Са - 0,9-2,1; MgO - 1,0-2,6; К2О - 2,3-4,0; Na2O - 0,5-1,2. Дальнейшая стабилизация состава ценосфер может быть проведена путем разделения ценосфер по размеру, плотности и магнитным свойствам [Пат. РФ №2212276, 2003 г.].
Особенности морфологии и минерально-фазового состава ценосфер делают этот материал перспективным сырьем для получения микросферических носителей и сорбентов. За счет наличия внутренней полости, высокой прочности стеклокристаллической оболочки, термостабильности и кислотостойкости ценосферы можно рассматривать как механически прочные и устойчивые в агрессивных средах микроконтейнеры для капсулирования активного компонента во внутреннем объеме носителя. Такой дизайн микросферического сорбента наиболее соответствует требованиям процессов очистки особо опасных отходов, поскольку алюмосиликатная оболочка носителя с заданной сквозной пористостью препятствует неконтролируемому выносу дисперсного активного компонента и может служить матрицей для захоронения радионуклидов в составе устойчивых минералоподобных соединений.
Наряду с этим по своему минерально-фазовому составу ценосферы являются стеклокристаллическим материалом на основе алюмосиликатного стекла с включениями наноразмерных железосодержащих фаз шпинельной структуры, обусловливающих магнитные свойства микросферического полого носителя [Верещагина Т.А., Аншиц Н.Н., Максимов Н.Г. и др. Природа и свойства железосодержащих наночастиц, диспергированных в алюмосиликатной матрице ценосфер // Физика и химия стекла, 2004, №3 - в печати}. Это позволяет создавать процессы сорбционного извлечения благородных металлов из жидких отходов, содержащих тонкодисперсные взвеси твердых компонентов (например, из пульпы хвостов серосульфидной флотации), основанные на возможности магнитного концентрирования сорбента и его выделения из гетерогенной среды.
Открытая пористость оболочки ценосфер (перфорация) и тем самым доступность внутреннего объема достигается действием кислотных реагентов на неоднородные по химическому и фазовому составу участки стекла, связанные с тонкой вкрапленностью рудных минералов (кварц, гематит, магнетит, муллит). В частности, травление ценосфер реагентом на основе плавиковой кислоты (например, NH4F-HCI-H2O) позволяет получить в оболочке ценосфер регулярные сквозные поры округлой формы диаметром 2-20 мкм, обеспечивающие доступность внутреннего объема глобул для заполнения его активным компонентом. В зависимости от состава ценосфер и типа используемого реагента можно получить микросферический полый носитель с заданной сквозной пористостью оболочки.
Известные методы нанесения активных компонентов на пористые носители, включающие пропитку растворами солей с промежуточной сушкой насыщенного носителя, в данном случае не применимы из-за чрезвычайно низкой растворимости неорганических ионообменников в воде и большинстве органических растворителей. При нанесении соединений, растворимых в органических растворителях, но не растворимых в воде (например, органических экстрагентов), следует также избегать стадии удаления растворителя методом упаривания, поскольку при этом происходит вынос активного компонента на внешнюю поверхность микросферического носителя. В связи с этим заполнение внутренней полости ценосфер осуществляется путем синтеза вещества непосредственно во внутреннем объеме носителя или его осаждения из пересыщенного раствора.
В зависимости от решаемой задачи могут быть получены микросферические сорбенты с различным активным компонентом, включая как неорганические ионообменники (молибдофосфат аммония (АМФ), ферроцианиды и сульфиды переходных металлов (Zn, Cu, Ni и пр.), фосфаты Mg и аммония), так и органические экстрагенты (триизобутилфосфинсульфид (ТИБФС), триоктилфосфиноксид (ТОФО) и пр.). Список селективных сорбентов не ограничивается приведенными примерами.
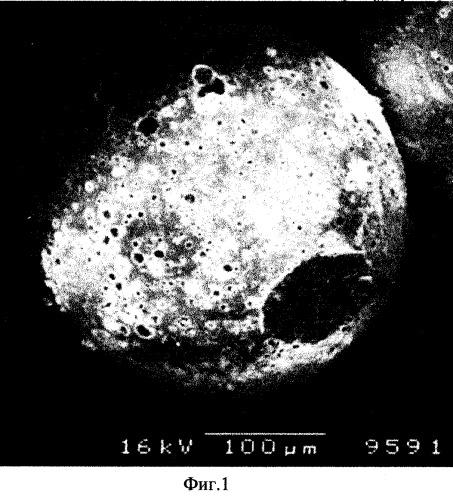
На фиг.1 изображена гранула микросферического полого носителя, полученного в результате травления ценосфер крупностью 0,4-0,315 мм реагентом NH4F-HCI-H2O (по данным сканирующей электронной микроскопии).
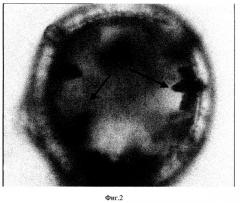
На фиг.2 изображена гранула микросферического сорбента крупностью 0,16-0,1 мм с локализованным во внутреннем объеме молибдофосфатом аммония (по данным оптической микроскопии).
Сущность изобретения демонстрируется следующими примерами.
ПРИМЕР 1. Для получения микросферического сорбента используют ценосферы стабилизированного состава с содержанием железа 3,1 мас.% в расчете на Fe2О3, крупностью 0,16-0,1 мм и насыпной плотностью 0,37 г/см3, полученные в результате разделения концентрата ценосфер летучей золы кузнецких углей методом гранулометрической классификации, гидродинамического разделения и магнитной сепарации.
Навеску ценосфер помещают в полипропиленовый стакан и обрабатывают травильным раствором следующего состава:
NH4F - 3,7 г
HCI(12 М) - 10 мл
Н2O (дист) - до 100 мл.
Время обработки 15 минут, соотношение твердая фаза : жидкость =1:10.
По окончанию обработки ценосферы разделяются на плавающий (неперфорированные ценосферы) и утонувший (перфорированные ценосферы) слои. Оба слоя собирают и сушат отдельно в вентилируемой камере при 100-110°С. Для получения сорбента используют перфорированные ценосферы.
Перфорированные ценосферы помещают в делительную воронку, которую откачивают водоструйным насосом до остаточного давления 8,0 кПа и выдерживают при этом разрежении 30-40 мин. После этого в воронку снизу путем засасывания подают горячий (60-80°С) раствор следующего состава:
(NH4)6Mo7O24·4H2O - 160 г
NH4H2PO4 - 8 г
Н2О (дист) - 500 мл.
Соотношение ценосферы : раствор =1:2.
По окончании этой процедуры воронку с ценосферами и горячим раствором выдерживают 20-30 мин, а затем через нижний кран воронку соединяют с атмосферой, в результате чего происходит заполнение раствором внутренних полостей перфорированных ценосфер.
Ценосферы, заполненные раствором, отфильтровывают от избытка жидкой фазы и помещают в установку для обработки газообразным хлороводородом в статических или динамических условиях при непрерывном вращении сосуда с ценосферами. За время обработки, которое составляет 24 часа, непосредственно во внутренней полости перфорированных ценосфер происходит образование желтого осадка молибдофосфата аммония.
Полученный продукт отмывают дистиллированной водой и сушат в вентилируемой камере при 100-120°С. В таблице 1 приведены характеристики полученного сорбента.
ПРИМЕР 2. Для получения микросферического сорбента используют ценосферы стабилизированного состава с содержанием железа 3,1 мас.% в расчете на Fe2O3, крупностью 0,315-0,2 мм и насыпной плотностью 0,34 г/см3. Обработку травильным раствором проводят как в примере 1. Перфорированные ценосферы выделяют как в примере 1, помещают в делительную воронку и под вакуумом, как описано в примере 1, заполняют горячим (60-80°С) раствором следующего состава (1 стадия заполнения ценосфер):
K4Fe[(CN)6]·3Н2O - 40 г
Н2O (дист) - 100 мл.
Ценосферы, заполненные раствором, отфильтровывают от избытка жидкой фазы и сушат в вентилируемой камере при 100-120°С.
Полученный продукт вновь вакуумируют и заполняют горячим раствором следующего состава (2 стадия заполнения ценосфер):
CuSO4·5H2O - 55 г
Н2O (дист) - 100 мл.
Ценосферы оставляют в растворе на 24 часа для кристаллизации ферроцианида меди, затем отфильтровывают от избытка жидкости, отмывают дистиллированной водой и сушат в вентилируемой камере при 100-120°С (табл.1).
ПРИМЕР 3. Для получения микросферического сорбента используют ценосферы как в примере 2. Обработку травильным раствором и выделение перфорированных ценосфер проводят как в примере 1. Навеску перфорированных ценосфер последовательно в две стадии, как описано в примере 2, заполняют растворами следующего состава:
| 1 стадия заполнения ценосфер: | 2 стадия заполнения ценосфер: |
| MgSO4·7H2O - 45 г | Na3PO4·12Н2O - 80 г |
| Н2O (дист) - 100 мл | Н2O (дист) - 100 мл. |
Ценосферы оставляют в растворе на 24 часа для кристаллизации фосфата магния, затем отфильтровывают от избытка жидкости, отмывают дистиллированной водой и сушат в вентилируемой камере при 100-120°С (табл.1).
ПРИМЕР 4. Для получения микросферического сорбента используют ценосферы как в примере 2. Обработку травильным раствором и выделение перфорированных ценосфер проводят как в примере 1. Навеску перфорированных ценосфер последовательно в две стадии, как описано в примере 2, заполняют растворами следующего состава:
| 1 стадия заполнения ценосфер: | 2 стадия заполнения ценосфер: |
| Na2S - 42 г | NiNO3·6Н2O - 96 г |
| Н2O (дист) - 100 мл | Н2O (дист) - 100 мл. |
Ценосферы оставляют в растворе на 24 часа для кристаллизации сульфида никеля, затем отфильтровывают от избытка жидкости, отмывают дистиллированной водой и сушат в вентилируемой камере при 100-120°С (табл.1).
ПРИМЕР 5. Для получения микросферического сорбента используют ценосферы стабилизированного состава с содержанием железа 3,1 мас.% в расчете на Fe2O3, крупностью 0,4-0,315 мм и насыпной плотностью 0,33 г/см3. Обработку травильным раствором и выделение перфорированных ценосфер проводят как в примере 1. Навеску перфорированных ценосфер последовательно в две стадии, как описано в примере 2, заполняют растворами следующего состава:
| 1 стадия заполнения ценосфер: | 2 стадия заполнения ценосфер: |
| Na2CO3 - 45 г | MgSO4·7H2O - 45 г |
| Н2О (дист) - 100 мл | Н2O (дист) - 100 мл. |
Ценосферы оставляют в растворе на 24 часа для кристаллизации карбоната магния, затем отфильтровывают от избытка жидкости, отмывают дистиллированной водой и сушат в вентилируемой камере при 100-120°С.
ПРИМЕРЫ 6, 7. Для получения микросферических сорбентов типа твердых экстрагентов используют ценосферы стабилизированного состава с содержанием железа 3,3 мас.% в расчете на Fe2О3, крупностью 0,16-0,125 мм и насыпной плотностью 0,38 г/см3. Обработку травильным раствором и выделение перфорированных ценосфер проводят как в примере 1. Навески перфорированных ценосфер помещают в делительную воронку и под вакуумом, как описано в примере 1, заполняют горячим (50°С) раствором следующего состава:
| Пример 6 | Пример 7 |
| триоктилфосфиноксид - 102,6 г | триизобутилфосфинсульфид - 40 г |
| С2Н5OH - 100 мл. | С2Н5ОН - 100 мл. |
Полученные продукты оставляют в растворе на 24 часа, после чего отфильтровывают от избытка жидкости, отмывают дистиллированной водой и сушат на воздухе при 20-25°С в течение суток.
Для полученных сорбентов были измерены равновесные ионообменные емкости в отношении катионов Cs, Pd и некоторых цветных металлов. Результаты сорбции представлены в таблице 1.
Таким образом, приведенные примеры подтверждают возможность воспроизводимого получения микросферических сорбентов на основе ценосфер энергетических зол, активными компонентами которых являются неорганические ионообменники и органические экстрагенты.
| Таблица 1Характеристики микросферических сорбентов на основе ценосфер | ||||||||||
| Пример | Перфорированные ценосферы | Сорбент на основе перфорированных ценосфер | Результаты сорбции | |||||||
| Размер фракции, мм | Насыпной вес, г/см3 | Удельная поверхность, м2/г | Активный компонент | Содержание активного компонента, масс.% | Насыпной вес, г/см3 | Удельная поверхность, м2/г | Сорбируемый ион | Емкость сорбента, мг/г | Состав раствора | |
| 1 | 0,16-0,1 | 0,25 | 1,5 | Молибдо-фосфат аммония | 23,0 | 0,33 | 47 | Cs | 6,4 | Cs - 68 мг/л |
| NaNO3 - 350 г/л | ||||||||||
| HNO3 - 1 моль/л | ||||||||||
| 2 | 0,315-0,2 | 0,35 | 0,6 | Ферроцианид меди | 41,3 | 0,59 | 1,9 | Cs | 6,0 | Cs - 63 мг/л |
| 3 | 0,315-0,2 | 0,27 | 0,8 | Фосфат магния | 21,8 | 0,35 | 8,8 | Ni | 10,4 | Ni - 100 мг/л |
| 4 | 0,315-0,2 | 0,27 | 0,8 | Сульфид никеля | 19,3 | 0,34 | 12,1 | Pd | 25,0 | Pd - 45 мг/л |
| Cu | 1.9 | Cu - 19 мг/л | ||||||||
| 5 | 0,4-0,315 | 0,27 | 0,7 | Карбонат магния | 40,8 | 0,46 | 1,9 | Co | 1,0 | Со - 10 мг/г |
| 6 | 0,16-0,125 | 0,30 | 1,8 | Триоктил-фосфиноксид | 19,8 | 0,51 | 0,7 | Pd | 20,8 | Pd - 340 мг/л |
| 7 | 0,16-0,125 | 0,30 | 1,8 | Триизобутил-фосфин-сульфид | 21,2 | 0,40 | 0,7 | Pd | 33,7 | Pd-340 мг/л |
1. Способ получения микросферического сорбента для очистки жидких отходов от радионуклидов, ионов цветных и тяжелых металлов, включающий введение активного компонента во внутренний объем ценосфер диаметром до 400 мкм с пористой стеклокристаллической оболочкой, отличающийся тем, что ценосферы предварительно перфорируют обработкой реагентом травления на основе минеральной кислоты, а введение активного компонента во внутренний объем осуществляют путем его осаждения непосредственно в полости ценосфер.
2. Способ по п.1, отличающийся тем, что в качестве активного компонента используют ионообменные материалы или органические экстрагенты.
3. Способ по п.2, отличающийся тем, что активный компонент выбирают из ряда, включающего молибдофосфат аммония, ферроцианиды и сульфиды переходных металлов, фосфат магния, карбонат магния, триоктилфосфиноксид или триизобутилфосфинсульфид.
4. Способ по п.1, отличающийся тем, что осаждение активного компонента проводят в процессе его синтеза.
5. Способ по п.1, отличающийся тем, что осаждение активного компонента проводят из его пересыщенных органических растворов.
6. Способ по п.1, отличающийся тем, что в качестве реагента травления используют раствор состава NF4F-HCI-H2O с содержанием F- 1 г-ион/л при мольном соотношении F-/Cl-=1,0.