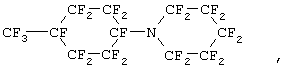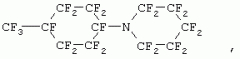Перфторированные циклосодержащие третичные амины как основа газопереносящих эмульсий (варианты) и способ их получения
Иллюстрации
Показать всеИзобретение относится к новым перфторированным циклосодержащим третичным аминам общей формулы (1)
где n=1; m=2 или 3, X является или ,
и к смеси перфторированных циклосодержащих третичных аминов общей формулы (1), где n=1; m=2 или 3,
X является или
где при n=1 Y=CF3, а при n=2 Y=F, в качестве основы газопереносящих эмульсий. Соединения настоящего изобретения являются близкими по физико-химическим свойствам, в частности по критической температуре растворения в гексане. Благодаря свойствам соединений удается достигнуть большей однородности фторуглеродной фазы эмульсий и повысить стабильность частиц эмульсий, стабилизированных блоксополимером окиси этилена и окиси пропилена, при отсутствии токсичности для мелких и крупных животных. Изобретение также относится к способу получения перфторированных циклосодержащих третичных аминов общей формулы (1) электрохимическим фторированием п-пиперидиногептафтортолуола в безводном фтористом водороде. 3 н. и 1 з.п. ф-лы, 1 ил., 3 табл.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к области химии фторорганических соединений и фармацевтической химии, а точнее к группе новых перфорированных циклосодержащих третичных аминов (ПФЦТА). Наиболее эффективно изобретение может быть использовано в качестве основы для создания газопереносящих сред, предназначенных для консервации органов, кровезамещения и лечения патологий, связанных с нарушением регионального кровотока.
Уровень техники
Известен перфторированный циклический третичный амин перфтор-N-(4-метилциклогексил)-пиперидин, имеющий следующую формулу
обладающий липофобными свойствами и используемый в качестве основы газопереносящих сред как самостоятельно, так и в сочетании с липофильными перфторорганическими соединениями (ПФОС), например перфтордекалином (ПФД) [см. С.И.Воробьев, Г.Р.Иваницкий, К.Н.Макаров, В.В.Мороз, В.П.Кутышенко // Перфторуглеродные эмульсии, стабилизированные неионогенными блоксополимерами. // В сб. «Перфторуглеродные активные среды для медицины и биологии (новые аспекты исследования)» Пущино, 1993, с.33-46].
В описании изобретения к патенту РФ №2088217, опубликованному в Бюлл. «Изобретения... (заявки...)» №24, 27.08.1998, показано, что введение в состав липофильной фторуглеродной фазы эмульсии липофобного ПФЦТА перфтор-N-(4-метициклогексил)-пиперидина обеспечивает ликвидацию у эмульсий токсичности для крупных животных, свойственную газопереносящим эмульсиям, содержащим липофильные быстровыводящиеся ПФОС. Однако при всех положительных свойствах эмульсий, полученных на основе липофильных ПФОС и липофобного перфтор-N-(4-метилциклогексил)-пиперидина, частицы такой эмульсии недостаточно стабильны. Их нестабильность при замораживании-оттаивании во время хранения и при попадании в кровоток обусловлена, согласно расчетам и модельным экспериментам [Г.Р.Иваницкий, С.И.Воробьев, А.А.Деев // «Жизнь» перфторуглеродной эмульсии. // В сб. «Физиологическая активность фторсодержащих соединений (эксперимент и клиника)» Пущино, 1995, с.5-32], тем, что резко различающиеся по липофильности ПФОС, в частности по температуре критического растворения в гексане, образуют во фторуглеродной фазе неоднородные кластеризованные структуры, характеризующиеся постоянным турбулентным движением внутри частиц эмульсии, нарушающим стабильность адсорбционного слоя поверхностно-активного компонента.
Кроме того, использование индивидуального перфтор-К-(4-метилциклогексил)-пиперидина затруднено ввиду высокой трудоемкости его получения и связанной с этим высокой стоимостью этого соединения. Все это накладывает существенные ограничения на получение этого вещества в промышленных масштабах и на широкое использование газопереносящих сред биомедицинского назначения.
Сущность изобретения
Задачей изобретения является получение новых перфторированных циклосодержащих третичных аминов, близких по физико-химическим и биологическим свойствам к перфтор-N-(4-метилциклогексил)-пиперидину, не токсичных для крупных животных и улучшающих стабильность эмульсий при замораживании-оттаивании и попадании в кровоток.
Другой задачей изобретения является упрощение и ускорение технологического процесса получения ПФЦТА, пригодных для использования в качестве основы для производства газопереносящих сред и обладающих улучшенным комплексом полезных свойств.
Поставленные задачи решаются тем, что в качестве основы для газопереносящих эмульсий предлагается использовать группу перфторированных циклосодержащих третичных аминов общей формулы (1)
(значение X и n см. далее).
Указанную группу соединений получают электрохимическим фторированием п-пиперидиногептафтортолуола. Эта группа содержит соединения, имеющие близкие физико-химические свойства, обусловливающие их успешное применение в смеси:
- два изомера перфторметилпропил(метилциклопентил)амина,
- цис/транс-перфторметилпропил(4-метилциклогексил)амин,
- перфторметилбутил-(4-метилциклогексил)амин,
- цис/транс-перфтор-N-(4-метилциклогексил)-2-метилпирролидин,
- цис/транс-перфтор-N-(4-метилциклогексил)-пиперидин.
Критическим параметром, который определяет возможность использования продуктов электрохимического фторирования п-пиперидиногептафтортолуола, является отсутствие недофторированных продуктов - водородсодержащих или непредельных соединений, обусловливающих токсичность. По параметрам токсичности индивидуальный перфтор-N-(4-метилциклогексил)-пиперидин и смесь ПФЦТА практически совпадают как в виде жидкостей, так и в составе эмульсий (табл.1, 2).
Все соединения этой группы ПФЦТА близки по липофильно-липофобным свойствам и по критической температуре растворения в гексане (КТРГ в диапазоне 34-36°С при растворении 25 мол.%). В смеси они образуют ряд соединений с градуально меняющимися характеристиками. Благодаря этому удается достигнуть большей однородности фторуглеродной фазы эмульсий, получаемых как на основе только данной группы соединений, так и в сочетании их с липофильными перфторорганическими соединениями, и тем самым повысить стабильность адсорбционного слоя частиц эмульсии, стабилизированных блоксополимером окиси этилена и окиси пропилена (табл.3). Эмульсии, получаемые на основе группы ПФЦТА, также, как и эмульсии, содержащие индивидуальный перфтор-N-(4-метициклогексил)-пиперидин, не токсичны для крупных животных (табл.2). Помимо этого они обладают лучшим комплексом свойств, проявляющихся в большей стабильности получаемых эмульсий (табл.3). Все это позволяет использовать их в качестве перфузионных сред и кровезамещающих составов.
Электрохимическое фторирование проводят в электролизере, куда загружают электролит, содержащий 10-25% исходного п-пиперидиногептафтортолуола в безводном фтористом водороде. Температуру поддерживают в интервале 20-25°С. Плотность тока варьируют от 200 до 400 А/м2 при напряжении 5-6 В. Процесс проводят в течение 10-12 часов с периодической подпиткой реакционной смеси более концентрированным раствором исходного вещества в безводном фтористом водороде. В зависимости от условий реакции выход продуктов фторирования составляет от 61 до 78% от исходного продукта. После удаления недофторированных (водородсодержащих и ненасыщенных) продуктов получают ряд перфторированных циклосодержащих третичных аминов с температурой кипения в диапазоне 179-196°С.
Все соединения идентифицируются методами хромато-масс-спектроскопии и ЯМР-спектрометрии. Основным соединением данной группы является цис/транс-перфтор-N-(4-метициклогексил)-пиперидин (выход от 60 до 70%). Остальные ПФЦТА являются продуктами частичной деструкции и изомеризации исходного вещества в процессе электрохимического фторирования. Изменения в процентном содержании соединений в смеси ПФЦТА при варьировании содержания цис/транс-перфтор-N-(4-метилциклогексил)-пиперидина в диапазоне от 60 до 70% не сказываются сколько-нибудь существенным образом на физико-химических и биологических параметрах получаемых эмульсий. На чертеже представлена типичная хроматограмма полученных перфторированных циклосодержащих третичных аминов (капиллярная колонка, сквалан, 100 м).
Описанный процесс получения ПФЦТА намного проще и дешевле, чем получение индивидуального чистого перфтор-N-(4-метилциклогексил)-пиперидина, каким бы способом его не получали, так как не требует выполнения таких трудоемких процедур как препаративная хроматография и ректификация. В литературе способ получения индивидуального перфтор-N-(4-метилциклогексил)-пиперидина не описан. Однако, по нашим оценкам, исключение из процесса неизбежных при выделении индивидуальных продуктов операций препаративной хроматографии и ректификации упрощает, ускоряет и удешевляет процесс в несколько раз.
Указанную смесь ПФЦТА используют вместо индивидуального перфтор-N-(4-метилциклогексил)-пиперидина для приготовления газопереносящих эмульсий. Упрощенная технология процесса позволяет сократить расходы на производство ПФОС и тем самым уменьшить стоимость производства газопереносящих сред при одновременном увеличении стабильности и реологических свойств этих сред. Все это открывает возможности для промышленного производства и более широкого использования эмульсий перфторорганических соединений в исследовательской и клинической практике.
Таким образом, первым объектом изобретения являются перфорированные циклосодержащие третичные амины общей формулы (1)
где n=1; m=2 или 3;
X является или
как основа газопереносящих эмульсий.
Предпочтительно такими соединениями являются перфторированные циклосодержащие третичные амины общей формулы (1), выбранные из группы, включающей цис/транс изомеры: перфторметилпропил(метилциклопентил)амина; перфторметилпропил-(4-метил-циклогексил)амина; перфторметилбутил-(4-метилциклогексил)амина и перфтор-N-(4-метилциклогексил)-2-метилпирролидина.
Другим объектом изобретения является способ получения перфторированных циклосодержащих третичных аминов общей формулы (I)
где n=1; m=2 или 3;
X является или
где при n=1 Y=CF3, а при n=2 Y=F,
электрохимическим фторированием п-пиперидиногептафтортолуола в безводном фтористом водороде.
Еще одним объектом изобретения является смесь перфторированных циклосодержащих третичных аминов общей формулы (I)
где n=1; m=2 или 3;
X является или
где при n=1 Y=CF3, а при n=2 Y=F,
как основа газопереносящих эмульсий.
Краткое описание чертежа, где изображена хроматограмма полученной смеси перфторированных циклосодержащих третичных аминов (капиллярная колонка, сквалан, 100 м), показывающая амплитуду температурного сдвига, определенную с помощью катарометрического датчика, в зависимости от времени выхода вещества:
пик 1 - два изомера перфторметилпропил(метилциклопентил)амина,
пик 2 - цис/транс-перфторметилпропил(4-метилциклогексил)амин,
пик 3 - перфторметилбутил-(4-метилциклогексил)амин,
пик 4 - цис/транс-перфтор-N-(4-метилциклогексил)-2-метилпирролидин,
пик 5 - цис/транс-перфтор-N-(4-метилциклогексил)-пиперидин.
Далее изобретение будет проиллюстрировано на примерах получения конкретных ПФТЦА. Эти примеры предназначены лишь для подтверждения возможности осуществления изобретения и не могут быть использованы для ограничения притязаний заявителя, отраженного в формуле изобретения.
Пример 1. Получение перфторированных циклосодержащих третичных аминов.
В электролизер объемом 2 л с внешней циркуляцией электролита, снабженный никелевыми электродами площадью 3000 см2, загружают 1500 мл электролита, содержащего 10% n-пиперидиногептафтортолуола в безводном фтористом водороде. Процесс электрохимического фторирования проводят при температуре 22°С и начальной плотности тока 200 А/м2 и напряжении 5 В. Периодически добавляли электролит, содержащий 60% раствор п-пиперидиногептафтортолуола в безводном фтористом водороде. В течение 10 часов фторирования плотность тока постепенно увеличивают до 400 А/м2 путем увеличения напряжения до 6 В. Всего пропускают 800 Ач тока и вводят в реакцию 330 г п-пиперидиногептафтортолуола. Жидкие продукты фторирования отделяют от электролита, промывают водой и раствором бикарбоната натрия для удаления HF. После удаления недофторированных примесей смесь продуктов фторирования перегоняют. Выход 388 г (61%) полностью фторированных соединений, имеющих температуру кипения в интервале 179-196°С. В состав полученных полностью фторированных третичных циклосодержащих аминов по данным ЯМР-спектроскопии и масс-спектрометрии входят пять видов соединений: 1-изомеры перфторметилпропил(метилциклопентил)амина (1%), 2-цис/транс-перфторметилпропил(4-метилциклогексил)амина (2%), 3-перфторметилбутил-(4-метилциклогексил)амин (8%), 4-цис/транс-перфтор-N-(4-метилциклогексил)-2-метилпирролидин (25%), 5-цис/транс-перфтор-N-(4-метилциклогексил)-пиперидин (64%) (см. хроматограмму).
Пример 2. Применение ПФЦТА.
Полученные по примеру 1 полностью фторированные продукты используют для приготовления субмикронной эмульсии, содержащей 10 об.% ПФЦТА, 3 мас.% блок-сополимера окиси этилена и окиси пропилена и водный раствор солей, изотоничных плазме крови (120 мМ NaCl, 10 мМ NaHCO3, 2 мМ КН2PO4, 5 мМ KCl 1,2 мМ CaCl2), с 10 мМ глюкозы, 1 мМ сукцината натрия, 1 мМ пирувата натрия, 1 мМ 2-гидроксибутрата натрия (рН перфузата 7,40). С помощью полученной эмульсии в рециркуляторном нормотермическом режиме перфузировали изолированную почку собаки из расчета 1 л перфузата на 40 г почки. Жизнедеятельность органа поддерживали в течение 24 часов, сменяя перфузионный состав каждые 6 часов, без явлений повреждения клеточных мембран (без отека, без существенного роста сопротивления капилляров, при сохранении рН перфузата и без падения скорости потребления кислорода).
Пример 3. Применение ПФЦТА.
Смесь полученных согласно примеру 1 ПФЦТА с перфтордекалином в соотношении 1:2 используют для приготовления субмикронной эмульсии, содержащей 10 об.% фторуглеродной фазы, 4 мас.% блоксополимера окиси этилена и окиси пропилена и водный раствор солей, изотоничных плазме крови (120 мМ NaCl, 8 мМ NaHCO3, 1,2 мМ КН2PO4, 5 мМ KCl), с 10 мМ глюкозы. Полученную эмульсию используют для изоволемического кровезамещения 65% объема циркулирующей крови у 10 крыс, находившихся под общим наркозом с предварительной премедикацией, при подаче для дыхания животных обогащенного кислородом воздуха в течение операции и в первые сутки после кровезамещения. Все животные, перенесшие кровезамещение, выжили.
Пример 4. Применение ПФЦТА.
ПФЦТА в смеси с перфтордекалином используют для получения субмикронной эмульсии, как описано в примере 3. Полученную эмульсию в дозе 20 мл на 1 кг вводят внутривенно 10 кроликам массой 2,5-3,5 кг. Отклонение температуры тела у кроликов после введения эмульсии не превышало 0,3°С. Не наблюдалось признаков аллергических реакций. Содержание лейкоцитов в периферической крови снижалось не более чем на 5% от исходного, что также свидетельствует об отсутствии реактогенности у препарата. Все кролики благополучно пережили критический период 80 дней (срок, в течение которого умирают все кролики, если им вводится эмульсия чистого перфтордекалина). В течение всего периода наблюдений (более 1 года) каких-либо патологических отклонений у животных не отмечено.
| Таблица 1Сравнение токсичности* индивидуального перфтор-N-(4-метилциклогексил)-пиперидина (ПФМЦП) и смеси перфторированных циклосодержащих третичных аминов (ПФЦТА), а также эмульсий, полученных на их основе | |||
| Вид исследуемого препарата (ИП) | Соотношение среда культивирования / ИП | Концентрация ионов фтора | Процент прироста клеток после культивирования |
| Среда культивирования | - | 1,0 | 100% |
| Смесь ПФД и индивидуального ПФМЦП | 20:1 | 1,0 | 90±15% |
| Смесь ПФД и ПФЦТА | 20:1 | 1,0 | 90±17% |
| Эмульсия на основе индивидуального ПФМЦП | 10:1 | 5,5 | 65±95% |
| Эмульсия на основе ПФЦТА | 10:1 | 5,5 | 65±95% |
| * токсичность перфторорганических соединений оценивали по подавлению роста культивируемых трансформированных лимфоидных клеток линии Raji. | |||
| Таблица 2Сравнение токсичности различных эмульсий ПФОС по величине полулетальной дозы для мышей и по выживанию кроликов | |||
| Вид исследуемого препарата | Острая токсичность для мышей, ЛД50, мл на кг | Выживание кроликов (%) через год после внутривенного введения исследуемых препаратов в дозе 20 мл на кг массы тела | |
| Эмульсия на основе индивидуального ПФМЦП | 140 | 100,0 | |
| Эмульсия на основе индивидуального ПФД | 150 | 0,0 | |
| Эмульсия на основе ПФД и индивидуального ПФМЦП (соотношение 2:1) | 140 | 100,0 | |
| Эмульсия на основе ПФД и ПФЦТА (соотношение 2:1) | 140 | 100,0 |
| Таблица 3Сравнение стабильности эмульсии на основе ПДФ/ПФМЦП и ПФД/ПФЦТА | |||||
| Вид перфторорганических соединений, входящих в состав эмульсий | Укрупнение среднего раз мера частиц при исходном размере 0,08 мкм | Оптическая плотность после смешивания эмульсии с разными концентрациями декстрана в соотношении 1:1 | |||
| Через 45 дней хранения при 4°С | После 5-кратного замораживания - оттаивания | Без декстрана | 3% декстрана | 6% декстрана | |
| ПФД и ПФМЦП в соотношении 2:1 | 0,14±0,01 | 0,15±0,02 | 0,10 | 0,35 | 0,88 |
| ПФД и ПФЦТА в соотношении 2:1 | 0,12±0,01 | 0,11±0,1 | 0,10 | 0,19 | 0,62 |
1. Перфторированные циклосодержащие третичные амины общей формулы (1)
где n=1; m=2 или 3,
X является или ,
как основа газопереносящих эмульсий.
2. Перфторированные циклосодержащие третичные амины общей формулы (1) по п.1, выбранные из группы включающей цис/трансизомеры перфторметилпропил(метилциклопентил)амина; перфторметилпропил-(4-метилциклогексил)амина; перфторметилбутил-(4-метилциклогексил)амина и перфтор-N-(4-метилциклогексил)-2-метилпирролидина.
3. Способ получения перфторированных циклосодержащих третичных аминов общей формулы (1)
где n=1; m=2 или 3,
X является или
где при n=1 Y=CF3, а при n=2 Y=F,
электрохимическим фторированием п-пиперидиногептафтортолуола в безводном фтористом водороде.
4. Смесь перфторированных циклосодержащих третичных аминов общей формулы (1)
где n=1; m=2 или 3,
X является или
где при n=1 Y=CF3, а при n=2 Y=F,
как основа газопереносящих эмульсий.