Способ формирования кардиодефибрилляционного импульса и средство для его осуществления
Иллюстрации
Показать всеИзобретения относятся к области медицины и могут быть использованы для устранения явления фибрилляции сердца пациента. Способ включает операции создания терапевтической цепи путем закрепления на теле пациента, по меньшей мере, двух рабочих терапевтических электродов, измерения и анализ пациент-зависимых электрофизических параметров, заряд емкостного накопителя энергии и последующий контролируемый блоком управления разряд емкостного накопителя энергии на рабочие терапевтические электроды. В процессе разряда подачу импульса дефибрилляции заданного количества энергии осуществляют дозированно, сначала первой частью W1 заданного количества энергии с аккумулированием второй части W2 заданного количества энергии на индуктивном накопителе энергии дефибриллятора, а затем второй частью W2 заданного количества энергии, причем соотношение первой части W1 заданного количества энергии импульса дефибрилляции ко второй части W2 заданного количества энергии импульса дефибрилляции выбирают равным одному из значений диапазона 0,01-150, а величину тока импульса дефибрилляции контролируют только при подаче первой части W1 заданного количества энергии. Кардиодефибрилляционный импульс имеет вид двухполярного импульса Гурвича, при этом заданное количество энергии для зарядки емкостного накопителя энергии дефибриллятора выбирают равным одному из значений диапазона 4-500 Дж, величину тока импульса дефибрилляции - равным одному из значений диапазона 0,005-175 А, а величину напряжения - равным одному из значений диапазона 3-30000 В. Средство для формирования кардиодефибрилляционного импульса содержит источник питания, снабженный средством контроля уровня зарядки емкостного накопителя энергии, блок формирования дефибрилляционных импульсов, коммутаторы, образованные управляемыми ключами, по меньшей мере, два рабочих терапевтических электрода, а также шунтирующих управляемые ключи диодов, резистивный датчик тока, аналого-цифровой преобразователь (АЦП) и блок управления, снабженный соответствующими функциональными связями с АЦП и управляемыми ключами, причем резистивный датчик тока помещен в токовой шине питания, имеющей наименьший потенциал относительно используемого измерительного устройства, включающего в свой состав АЦП. Способ и устройство обеспечивают безопасное для пациента воздействие и высокую его эффективность. 2 н. и 5 з.п. ф-лы, 9 ил.
Реферат
Изобретение относится к области медицинской техники, а более точно к кардиологии и предназначено для устранения фибрилляции сердца путем применения воспроизводимого способа выработки внешнего кардиодефибрилляционного импульса, а также использования соответствующего этому способу устройства для эффективной и надежной трансляции выработанного кардиодефибрилляционного импульса в тело пациента.
Предпосылки изобретения
Большая статистическая база медицинских данных достоверно свидетельствует о том, что вероятность выживания пациента после сердечного приступа прямо зависит от интервала времени до момента начала оказания пациенту специализированной кардиологической медицинской помощи. Исход сердечного приступа в прямое развитие сердечной аритмии, в частности фибрилляцию желудочков сердца, когда сердце теряет свою способность осуществлять нагнетание требуемого объема крови, имеет своим негативным результатом тяжелейшее повреждение головного мозга и почти гарантированный летальный исход, если своевременно - в пределах считанных минут - не будет восстановлен и пролонгирован нормальный сердечный ритм. В настоящее время наиболее эффективным (из успешно освоенных) способом восстановления нормального сердечного ритма у пациента является подача в его тело сильного электрического разряда, который способен почти незамедлительно подавить случившуюся аритмию сердца и способен восстановить его нормальную нагнетательную функцию. Разработка и распространение относительно недорогих портативных внешних дефибрилляторов, не требующих деятельного профессионального участия в части их применения высококвалифицированного медицинского персонала в силу высокой алгоритмизации самой процедуры терапевтического воздействия кардиодефибрилляционным импульсом на пациента, испытывающего сердечный приступ, существенно расширяет круг лиц, способных оказать пациенту эффективную и своевременную помощь. В силу указанных причин на первое место среди факторов, лимитирующих конечную результативность терапевтического применения внешних дефибрилляторов для пациентов, угнетенных хаотичной активностью (фибрилляцией) сердца, выдвигается проблема безопасной воспроизводимости параметров упомянутого электрического разряда для весьма разнообразной (по электрофизическим характеристикам, в частности по проводимости) выборки потенциальных пациентов.
Очевидным фактом является то, что с позиций электрофизических характеристик тело человека представляет собой существенно нелинейную динамическую структуру (см. "Электронная аппаратура для стимуляции органов и тканей", под ред Р.Н.Утямышева и др., М., "Энергоатомиздат", 1983, с.182-245). Ситуация также усугубляется тем, что мишенью кардиотерапевтического электроимпульсного воздействия является не тело пациента как таковое, а лишь его (тела) структурная составляющая - фибриллирующее сердце, которое также является нелинейным динамическим объектом в существенно нелинейной динамической структуре (см. эквивалентную электрическую схему на Fig 5b US Patent №5,968,080 от 10 октября 1999 г., James E. Brewer et al. "Method for determining the second phase of external defibrillator devices"), в совокупности требующими учета не только электрофизических параметров модели пациента, но и учета особенностей отклика сердца на клеточном уровне при электроимпульсном воздействии на него, а также принятие во внимание электрической модели цепи формирования кардиодефибриллируюцего импульса самого дефибриллятора. Следует принимать во внимание и то обстоятельство, что помимо учета отклика сердца на электроимпульсное воздействие на клеточном уровне (т.е. микроуровне) существует необходимость учитывать и нелинейность динамики изменения проводимости сердца пациента на макроуровне (учет гетерогенности сердца как проводника тока), поскольку установлен и доказан факт пространственной анизотропии его проводимости, в силу чего различные (миокардиальные) волокна сердечной мышцы не находятся в одинаковых условиях по отношению к стимулирующему их ипульсному току. По меньшей мере, в сердце структурируются как область с высоким электрическим сопротивлением (миокард), так и область с низким электрическим сопротивлением (кровь в лопастях желудочков и предсердий), что является причиной возникновения ситуации, когда в результате электроимпульсного терапевтического воздействия на сердце в одной из локальных его областей не исключена возможность существенного превышения пороговой плотности тока, приводящее к необратимому деструктивному изменению биотканей в указанной области (см. А.с. СССР №415840 от 9 ноября 1971 г. "Способ электроимпульсного воздействия на сердце", авторов Б.М.Цукермана и др.).
Дополнительное обстоятельство, побуждающее и усиливающее необходимость рассматривать пациента, подвергающегося терапевтическому электроимпульсному воздействию в качестве нелинейной динамической системы, заключается в том, что лишь около 4% от введенной в тело пациента энергии электрического импульса достигает сердца, т.е. только около 4% энергии выполняет собственно терапевтическую (кардиотерапевтическую) функцию. Оставшиеся 96% введенной в тело пациента электрической энергии представляют собой потенциальную угрозу электротравмы для сердца и иных тканей организма в силу возможности динамического (неконтролируемого извне) перераспределения в биотканях, обусловленного свойствами тела пациента как нелинейной динамической системы, обладающей способностью к бифуркации (см. "Нелинейные динамические системы на плоскости и их приложения", автор Р.И.Богданов, М., "Вузовская книга", 2003, стр.76.-86). Именно последствием токовой бифуркации в процессе проведения процедуры дефибрилляции является потеря устойчивости (перестройка фазового портрета) даже при незначительном изменении (см. "Теория катастроф", автор В.И.Арнольд, М., "Наука", Главная редакция физико-математической литературы, 1990 г., стр.16-102) такого управляющего характеристиками посылаемого кардиодефибрилляционного импульса параметра, как Z (импеданс тела пациента). В зависимости от дальнейшего сценария хаотизации (в представляющем для нас значение случае ею является потеря токовой устойчивости кардиодефибрилляционного импульса) происходит очень стремительная "мягкая" (так называемая "бифуркация Хопфа") и/или "жесткая" потеря устойчивости равновесия нелинейной динамической системы "дефибриллятор-пациент", приводящая к получению пациентом электротравмы тканей его организма. К сожалению, созданные на данное время способы и их аппаратурное обеспечение в части, касающейся проведения кардиореанимации при возникновении аритмии (а точнее фибрилляции) сердца, абсолютно не учитывают явления динамической бифуркации в системе "дефибриллятор-пациент", упрощая эту проблему до искусственного установления пороговых величин некоторых параметров, в частности энергии кардиодефибрилляционного импульса (см. US Patent №6,041,254 от 21 мая 200 г., автор. Joseph L. Sullivan et al.), тока упомянутого импульса (см. Walcott et al. "Comparison of monophasic, biphasic and the edmark waveform for external defibrillation", PACE, 15:563, Abstract 218, April 1992., и Kerber et al. "Energy, current and success in defibrillation and cardioversion: clinical studies using an automated impedance-based method of energy adjustment", CIRCULATION 77(5): 1038, May 1988) и импеданса тела пациента (см. US Patent №5,944,742 от 31 августа 1999 г., авт.James E.Brewer et al, "AAMI specification optimized truncated exponential waveform"), мало совместимых с реальными электрофизическими характеристиками индивидуальных представителей-пациентов народонаселения, при использовании которых гарантировался бы терапевтический успех процедуры кардиореанимации без последствий в виде электротравм тканей его организма.
Известен способ формирования терапевтического импульса дефибриллятора [1], включающий формирования рабочей электрической цепи за счет размещения на теле пациента двух электродов электроимпульсного воздействия, зарядку накопителя электрической энергии до требуемого уровня энергии на основе алгоритмизированного принятия решения о выполнении процедуры дефибрилляции по результатам прямого измерения сердечного ритма и измеренным значениям пациент-зависимых электрофизических параметров (в частности импеданса), изменение проводимости (коммутацию) высоковольтного ключа таким образом, чтобы обеспечивалась возможность посылки первой фазы двухфазного кардиодефибрилляционного импульса, контроль одновременно с посылкой в рабочую цепь энергии кардиодефибрилляционного импульса величины импеданса рабочей цепи, осуществляемое в интервале времени от начала посылки импульса до достижения соответствующим данной посылке электрической энергии току дефибрилляционного импульса пикового значения, очередное изменение проводимости (коммутацию) высоковольтного ключа в обеспечении посылки второй фазы двухфазного кардиодефибрилляционного импульса избранной длительности, измерение в процессе посылки второй фазы двухфазного кардиотерапевтического импульса величины импеданса рабочей цепи, осуществляемое в интервале времени от начала посылки указанного импульса до достижения соответствующим данной посылке электрической энергии току дефибрилляционного импульса пикового значения, и последующее прерывание проводимости высоковольтного ключа при истечении заданного времени длительности второй фазы двухфазного кардиодефибрилляционного импульса, учитывающего продолжительности первой фазы двухфазного кардиодефибрилляционного импульса.
Недостатком известного способа является то, что он не исключает риск получения пациентом электротравм тканей его организма при воздействии на тело пациента кардио-дефибрилляционным импульсным разрядом вследствие возникновения бифуркации электрического тока и как следствие неконтролируемого перераспределения энергии терапевтического импульса, особенно в интервале времени от момента достижения этим токам пикового значения до истечения времени разрешенной трансляции первой (второй) фазы двухфазного кардиодефибрилляционного импульса, поскольку измерение импеданса тела пациента в указанные промежутки времени не производится.
Известное устройство для реализации представленного способа [1] состоит из электрической батареи, взаимодействующей двумя своими контактами с высоковольтным зарядным устройством, которое подвержено контролю со стороны блока управления (выполненного в виде микроконтроллера) посредством связи по соответствующей линии контроля зарядки, а также включает цепь накопления электрической энергии, с одной стороны, подключенную к высоковольтному зарядному устройству, а с другой стороны, взаимодействующую с высоковольтным ключом (например, выполненным в виде Н-мостовой схемы), содержащую в своем составе емкостной накопитель электрической энергии, измерители тока и напряжения, индуктивный накопитель электрической энергии, включенный последовательно в рабочую цепь емкостного накопителя энергии, диода, шунтирующего индуктивный накопитель энергии, необходимые токопроводящие шины соединения элементов и шин обеспечения измерительно-управляющих функций.
Недостатком известного устройства является его непредсказуемая способность нанесения пациенту в процессе терапии сердечной аритмии электрической травмы тканей организма, что обусловлено особенностью схемотехнического построения известного устройства, а именно полным необеспечением подавления токовой бифуркации кардиодефибриллирующего импульса даже в форме бифуркации Хопфа.
Наиболее близким к предложенному способу является способ формирования кардиодефибрилляционного импульса [2], включающий зарядку емкостного накопителя энергии (конденсатора) от источника питания до напряжения, превышающего в 1,5-2,0 раза избранное напряжение импульса дефибрилляции, подключение рабочих электродов к пациенту, принятие решения о проведении процедуры дефибрилляции в форме подачи команды оператором (врачом) на запуск задающего генератора, последующий запуск задающего генератора, вырабатывающего на выходе масштабированный импульс (отображающий мощность), по своей форме идентичный кардиодефибрилляционному импульсу, подаваемому на электроды, закрепленные на теле пациента. Затем масштабированный импульс с выхода задающего генератора транслируют на вход компаратора, который будучи предварительно настроенным, восстанавливает электрическую проводимость ключа, отсутствие которой вначале препятствовало перемещению энергии кардиодефибрилляционного импульса из емкостного накопителя энергии (конденсатора) в тело пациента.
При этом производят непрерывный контроль величины энергии кардиодефибрилляционного импульса по значению вычисленной перемножителем мощности. В один из предшествующих моментов процедуры дефибрилляции, когда произведение тока на напряжение приобретает значение большее, чем значение предварительно заданного управляющего сигнала, поступающий от задающего генератора на блок управления ключом (функцию которого выполняет компаратор) сигнал размыкает ключ. В один из последующих моментов процедуры дефибрилляции, когда произведение тока на напряжение приобретает значение меньшее, чем значение предварительно заданного управляющего сигнала, поступающий от задающего генератора на блок управления ключом (функцию которого выполняет компаратор) сигнал опять замыкает ключ. В промежуток времени между состоянием, когда ключ разомкнут, и по достижении состояния, когда ключ снова замыкают, ток дефибрилляции через тело пациента поддерживается благодаря отдаче энергии, накопленной в последовательно установленном в рабочей цепи индуктивном накопителе электрической энергии. Завершение подачи импульса задающего генератора приводит к окончанию процедуры дефибрилляции с некоторым временным сдвигом, величина которого обусловлена и величиной сопротивления индуктивного накопителя энергии (дросселя), и импедансом тела пациента.
Недостатком наиболее близкого способа (избранного в качестве прототипа) является то, что успешный терапевтический результат производимого им электроимпульсного воздействия на любого пациента без ограничений, обремененного внезапной сердечной аритмией, равно как и безопасность в части недопущенния электротравм тканей его организма, в значительной мере зависят от свойств электрофизических характеристик тела пациента (включая такой параметр как импеданс), что способом-прототипом совершенно не учитывается. Кроме того, обобщенный (опосредствованный) контроль посылки кардиодефибрилляционного импульса в тело пациента через вычисляемый аналоговыми методами параметр обратной связи "мощность" способствует увеличению нелинейности системы "дефибриллятор - пациент", что провоцирует возникновение в ней, по меньшей мере, токовой бифуркации Хопфа собственно кардиодефибрилляционного импульса.
Известное устройство-прототип для осуществления способа-прототипа [2] состоит из источника питания, снабженного средством контроля уровня зарядки, при этом оба вывода источника питания подключены к цепи питания, образуемой конденсатором (в роли емкостного накопителя энергии), первый и второй выводы которого снабжены соответственно первой и второй токовыми шинами, терапевтической цепи, содержащей пару рабочих электродов, контактирующих с ними первой и второй терапевтических шин, диода, соединяющего первую и вторую терапевтические шины, управляемого ключа, с входом которого взаимодействует одна из токовых шин, а с выходом - та из терапевтических шин, с которой контактирует минусовой вывод диода, дросселя (в роли индуктивного накопителя энергии), введенного в эту же терапевтическую цепь последовательно, составных (включающих по два элемента) резистивных датчиков тока и напряжения, взаимодействующих с терапевтическими шинами, и блока управления, взаимодействующего со средством контроля уровня зарядки конденсатора, составными резистивными датчиками тока и напряжения и ключом, причем блок управления выполнен из взаимодействующих между собой по проводникам задающего генератора, компаратора и перемножителя.
Недостатком устройства-прототипа является то, что он не исключает в процессе применения нанесения пациенту электротравм тканей его организма, поскольку схемотехническое решение, заложенное в конструкцию устройства-прототипа, не обеспечивает подавление возможности возникновения токовой бифуркации кардиодефибрилляционного импульса, а также не учитывает присущие разным пациентам вариации электрофизических характеристик (в основном импеданса) их тела. Помимо данного недостатка формируемый устройством-прототипом кардиодефибрилляционный импульс однофазен, что также является причиной известного уменьшения (см., например, Патент РФ №2153901 от 08 февраля 1999 г., кл. A 61 N 1/39, "Дефибриллятор", авт. Верещагин A.M. и др.) эффективности терапевтического электроимпульсного воздействия на пациента.
В основу изобретения положена задача разработки для пациента из практически неограниченной выборки реальных пациентов безопасного способа формирования кардиодефибрилляционного импульса и создания средства для его надежного осуществления.
Техническим результатом настоящего изобретения является повышение эффективности и безопасности терапевтического электроимпульсного воздействия на любого пациента без ограничений, обремененного внезапной сердечной аритмией, сопровождающихся подавлением возможности возникновения токовой бифуркации кардиодефибрилляционного импульса и существенным снижением риска получения данным пациентом электротравм тканей его организма.
Указанный технический результат достигается тем, что способ формирования кардиодефибрилляционного импульса согласно изобретению включает создание терапевтической цепи путем закрепления на теле пациента, по меньшей мере, двух электродов, измерение и анализ пациент-зависимых электрофизических параметров, формирование цепи питания дефибриллятора посредством зарядки его емкостного накопителя заданным количеством энергии дефибрилляции и последующую подачу импульса дефибрилляции заданного количества энергии в тело пациента при контроле величины тока импульса дефибрилляции измерительным устройством, при этом подачу импульса дефибрилляции заданного количества энергии в тело пациента осуществляют дозированно, сначала первой частью W1 заданного количества энергии с аккумулированием второй части W2 заданного количества энергии на индуктивном накопителе энергии дефибриллятора, а затем второй частью W2 заданного количества энергии, причем соотношение первой части W1 заданного количества энергии импульса дефибрилляции ко второй части W1 заданного количества энергии дефибрилляции выбирают равным одному из значений диапазона 0,01-150, а величину тока импульса дефибрилляции контролируют только при подаче первой части W1 заданного количества энергии.
Кроме того, имеет значение, чтобы кардиодефибрилляционный импульс имел вид двухполярного импульса Гурвича.
Желательно величину тока импульса дефибрилляции первой части W1 заданного количества энергии контролировать в шине цепи питания, имеющей наименьший потенциал относительно используемого измерительного устройства.
Целесообразно заданное количество энергии для зарядки емкостного накопителя дефибриллятора выбрать равным одному из значений диапазона 4-500 Дж.
Рекомендуется на тело пациента воздействовать кардиодефибрилляционным импульсом с величиной тока, выбираемой равной одному из значений диапазона 0,005-175 А.
Предпочтительно на тело пациента воздействовать импульсом дефибрилляции с величиной напряжения, выбираемой равной одному из значений диапазона 3-30000 В.
Указанный технический результат достигается также тем, что средство для формирования кардиодефибрилляционного импульса согласно изобретению содержит источник питания, снабженный средством контроля выработанной электрической энергии и первой и второй токовыми шинами, подключенную параллельно ему цепь питания, образованную емкостным накопителем энергии, первый вывод которого соединен с первой токовой шиной, а второй вывод соединен со второй токовой шиной, терапевтическую цепь, состоящую, по меньшей мере, из первого и второго рабочих электродов, снабженных первой и второй терапевтическими шинами соответственно, индуктивного накопителя энергии, включенного последовательно в цепь одной из терапевтических шин, а также диод, первый ключ, резистивный датчик тока и блок управления, связанный со средством контроля выработанной электрической энергии источника питания и первым ключом, при этом оно дополнительно снабжено, по меньшей мере, вторым, третьим и четвертым ключами, электрически связанными с блоком управления, и, по меньшей мере, вторым, третьим и четвертым диодами, при этом выход первого ключа соединен с первой токовой шиной, вход первого ключа соединен с выходом второго ключа, вход второго ключа соединен с второй токовой шиной, выход третьего ключа соединен с первой токовой шиной, вход третьего ключа соединен с выходом четвертого ключа, вход которого соединен со второй токовой шиной, причем первый ключ шунтирован первым диодом, второй ключ шунтирован вторым диодом, третий ключ шунтирован третьим диодом, четвертый ключ шунтирован четвертым диодом, а первая терапевтическая шина связана с входом первого ключа и выходом второго ключа, вторая терапевтическая шина связана с входом третьего ключа и выходом четвертого ключа, при этом резистивный датчик тока включен последовательно между вторым выводом емкостного накопителя энергии и входом четвертого ключа и соединен через аналого-цифровой преобразователь с блоком управления.
Представленные в настоящей заявке признаки необходимы и достаточны для получения указанного выше технического результата.
Проведенный анализ существующего уровня техники не выявил технических решений, содержащих сходные отличительные признаки, которые позволяли бы добиться получения заявленного в настоящем предмете притязаний технического результата, что позволяет сделать заключение о соответствии предложенных объектов изобретения критериям "новизна" и "изобретательский уровень"
Сущность изобретения иллюстрируется следующими чертежами, где:
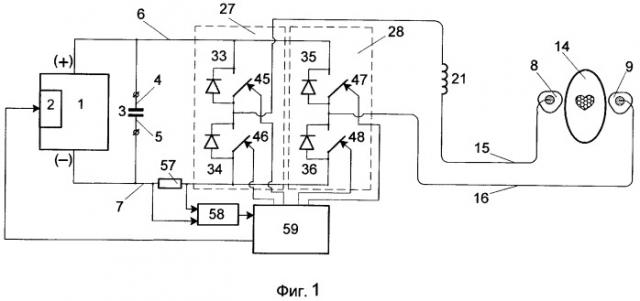
- на Фиг.1 представлена структурная схема предлагаемого средства, оснащенного двумя рабочими электродами;
- на Фиг.2 - структурная схема предлагаемого средства, оснащенного тремя рабочими электродами;
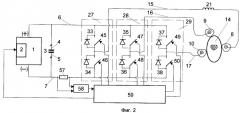
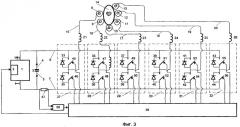
- на Фиг.3 - структурная схема предлагаемого средства, оснащенного шестью рабочими электродами;
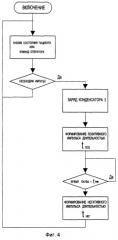
- на Фиг.4 изображена общая последовательность формирования двухфазного кардиодефибрилляционного импульса;
- на Фиг.5 схематично изображена последовательность формирования позитивной составляющей двухфазного кардиодефибрилляционного импульса;
- на Фиг.6 схематично изображена последовательность формирования негативной составляющей двухфазного кардиодефибрилляционного импульса;
- на Фиг.7 схематично изображен внешний вид двухфазного кардиодефибрилляционного импульса в соответствии с изобретением;
- на Фиг.8 представлен фрагмент Вид А позитивной и негативной составляющих двухфазного кардиодефибрилляционного импульса из Фиг.7;
на Фиг.9 изображена временная последовательность подачи двухфазного составного терапевтического импульса на шесть рабочих электродов в соответствии с конструкцией средства для формирования кардиодефибрилляционного импульса, представленного на Фиг.3.
Перечень позиций:
1. Источник питания.
2. Средство контроля количества выработанной источником питания электрической энергии.
3. Конденсатор.
4. Первый вывод конденсатора.
5. Второй вывод конденсатора.
6. Первая токовая шина.
7. Вторая токовая шина.
8. Первый рабочий электрод.
9. Второй рабочий электрод.
10. Третий рабочий электрод.
11. Четвертый рабочий электрод.
12. Пятый рабочий электрод.
13. Шестой рабочий электрод.
14. Пациент.
15. Первая терапевтическая шина.
16. Вторая терапевтическая шина.
17. Третья терапевтическая шина.
18. Четвертая терапевтическая шина.
19. Пятая терапевтическая шина.
20. Шестая терапевтическая шина.
21. Первый индуктивный накопитель энергии.
22. Второй индуктивный накопитель энергии.
23. Третий индуктивный накопитель энергии.
24. Четвертый индуктивный накопитель энергии.
25. Пятый индуктивный накопитель энергии.
26. Шестой индуктивный накопитель энергии.
27. Первый коммутатор.
28. Второй коммутатор.
29. Третий коммутатор.
30. Четвертый коммутатор
31. Пятый коммутатор.
32. Шестой коммутатор.
33. Первый диод.
34. Второй диод.
35. Третий диод.
36. Четвертый диод.
37. Пятый диод.
38. Шестой диод.
39. Седьмой диод.
40. Восьмой диод.
41. Девятый диод
42. Десятый диод.
43. Одиннадцатый диод.
44. Двенадцатый диод.
45. Первый управляемый ключ.
46. Второй управляемый ключ.
47. Третий управляемый ключ.
48. Четвертый управляемый ключ.
49. Пятый управляемый ключ.
50. Шестой управляемый ключ.
51. Седьмой управляемый ключ.
52. Восьмой управляемый ключ.
53. Девятый управляемый ключ
54. Десятый управляемый ключ.
55. Одиннадцатый управляемый ключ.
56. Двенадцатый управляемый ключ.
57. Резистивный датчик тока.
58. Аналого-цифровой преобразователь.
59. Блок управления.
60. Позитивная составляющая двухфазного кардиодефибрилляционного импульса терапевтического разряда.
61. Негативная составляющая двухфазного кардиодефибрилляционного импульса терапевтического разряда.
62. Терапевтический ток первой доли электрической энергии W1 любой (позитивной или негативной) составляющей двухфазного кардиодефибрилляционного импульса.
63. Терапевтический ток второй доли электрической энергии W2 любой (позитивной или негативной) составляющей двухфазного кардиодефибрилляционного импульса.
64. Ток I8-13 первой части электрической энергии позитивной составляющей двухфазного кардиодефибрилляционного импульса.
65. Ток I9-12 второй части электрической энергии позитивной составляющей двухфазного кардиодефибрилляционного импульса.
66. Ток I10-11 третьей части электрической энергии позитивной составляющей двухфазного кардиодефибрилляционного импульса.
67. Ток I8-13 первой части электрической энергии негативной составляющей двухфазного кардиодефибрилляционного импульса.
68. Ток I9-12 второй части электрической энергии негативной составляющей двухфазного кардиодефибрилляционного импульса.
69. Ток I10-11 третьей части электрической энергии негативной составляющей двухфазного кардиодефибрилляционного импульса.
70. Общая длительность позитивной составляющей двухфазного кардиодефибрилляционного импульса.
71. Общая длительность негативной составляющей двухфазного кардиодефибрилляционного импульса.
Средство для формирования кардиодефибрилляционного импульса содержит источник питания 1 (Фиг.1 - Фиг.3). Цепь источника питания снабжена средством контроля 2 (Фиг.1 - Фиг.3), которое обеспечивает выработку источником питания 1 (Фиг.1 - Фиг.3) требуемого для зарядки конденсатора 3 (Фиг.1 - Фиг.3) количества электрической энергии. В качестве средства контроля 2 (Фиг.1 - Фиг.3) может быть использован любой измеритель напряжения с цифровым выходом, поскольку при известной емкости конденсатора С (параметр, который определяется конструктивным исполнением используемого в дефибрилляторе в качестве емкостного накопителя конденсатора) и получении результата измерения напряжения U между пластинами этого конденсатора, энергия заряженного конденсатора W определяется из выражения: W=CU2/2 ("Справочник по физике", Х.Кухлинг, перевод с немецкого под редакцией Е.М.Лейкина, Москва, "Мир", 1982 г., стр.333). Конденсатор 3 (Фиг.1 - Фиг.3) выполняет роль емкостного накопителя энергии, первый 4 и второй 5 выводы (Фиг.1 - Фиг.3) которого соединены соответственно с первой 6 и второй 7 (Фиг.1 - Фиг.3) токовыми шинами. В составе рассматриваемого средства могут также присутствовать как первый 8 и второй 9, так третий 10, а также четвертый 11, пятый 12 и шестой 13 электроды, накладываемые на тело пациента 14 (Фиг.1 - Фиг.3). К каждому из указанных рабочих электродов 8-13 (Фиг.1 - Фиг.3) присоединена соответственно первая 15 (Фиг.1 и Фиг.2), вторая 16 (Фиг.1 и Фиг.2), третья 17 (Фиг.2), четвертая 18, пятая 19 и шестая 20 (Фиг.3) терапевтические шины. В цепь терапевтических шин 15-20 (Фиг.3) входят включенные последовательно им первый 21, второй 22, третий 23, четвертый 24, пятый 25 и шестой 26 (Фиг.3) индуктивные накопители энергии, подключенные соответственно к одному из шести коммутаторов, а именно: первому 27, второму 28, третьему 29, четвертому 30, пятому 31 и шестому 32 коммутаторам (Фиг.3). Коммутаторы 27-32 (Фиг.3) образованы первым 33, вторым 34, третьим 35, четвертым 36, пятым 37, шестым 38, седьмым 39, восьмым 40, девятым 41, десятым 42, одиннадцатым 43 и двенадцатым 44 диодами (Фиг.3), а также первым 45, вторым 46, третьим 47, четвертым 48, пятым 49, шестым 50, седьмым 51, восьмым 52, девятым 53, десятым 54, одиннадцатым 55 и двенадцатым 56 управляемыми ключами (Фиг.3), причем каждый из упомянутых коммутаторов 27-32 (Фиг.1 - Фиг.3) содержат по два последовательно соединенных между собой управляемых ключа, при этом входы управляемых ключей второго 46, четвертого 48, шестого 50, восьмого 52, десятого 54 и двенадцатого 56 (Фиг.3) соединены со второй токовой шиной 7 (Фиг.1 - Фиг.3), а выходы управляемых ключей первого 45, третьего 47, пятого 49, седьмого 51, девятого 53 и одиннадцатого 55 (Фиг.3) соединены с первой токовой шиной 6 (Фиг.1 - Фиг.3). Все управляемые ключи 45-56, образующие коммутаторы 27-32, шунтированы диодами 33-44 (Фиг.3), причем узел соединения выхода любого из управляемых ключей с входом дополняющего его в коммутаторе управляемого ключа является выводом, контактирующим с одной из терапевтических шин 15-20 (Фиг.3), в том числе (как вариант) и через один из индуктивных накопителей 21-26 (Фиг.3). Средство для формирования кардиодефибрилляционного импульса также содержит резистивный датчик тока 57 (Фиг.1 - Фиг.3), который размещен в электрической цепи между вторым выводом 5 конденсатора 6 (Фиг.1 - Фиг.3) и входом четвертого ключа (Фиг.1 - Фиг.3). Выводы резистивного датчика тока 57 (Фиг.1 - Фиг.3) соединены с входом аналого-цифрового преобразователя 58 (Фиг.1 - Фиг.3), выход которого в свою очередь соединен с входом блока управления 59 (Фиг.1 - Фиг.3), который конструктивно может быть выполнен в виде микропроцессора. Кроме того, блок управления 59 (Фиг.1 - Фиг.3) электрически связан в части реализации функции управления со средством контроля количества выработанной энергии 2 (Фиг.1 - Фиг.3) и всеми управляемыми ключами 45-56 (Фиг.1 - Фиг.3), а также содержит в своем составе анализатор пациент-зависимых параметров (не показан), в наиболее простом случае технически реализуемый как измеритель импеданса.
Средство для формирования дефибрилляционного импульса работает следующим образом:
Пример 1.
Первый рабочий электрод 8 (Фиг.1) и второй рабочий электрод 9 (Фиг.1) закрепляют на теле пациента 14 (Фиг.1) в области грудной клетки. После этого производят включение источника питания 1 (Фиг.1) и устанавливают ручной или автоматический режим управления его работой. Блок управления 59 (Фиг.1) производит анализ состояния пациента или анализ команд оператора (в том случае, если выбран ручной режим работы). При установлении необходимости терапевтического электроимпульсного воздействия на пациента (выход "да" блока "необходим импульс" на Фиг.4) производится зарядка конденсатора 3 (Фиг.1) до достижения предварительного выбранного на основе измерения пациент-зависимых параметров (сердечного ритма и импеданса тела пациента) блоком управления 59 (Фиг.1) значения энергии, например 200 Дж. Контроль зарядки емкостного накопителя энергии производят под управлением средства контроля количества выработанной источником питания электрической энергии 2 (Фиг.1). По окончании заряда конденсатора 3 (Фиг.1) до предварительно выбранного значения, равного 5000 В, наступает этап формирования позитивного импульса tпоз (Фиг.4). По команде из блока управления 59 (Фиг.1) производится замыкание (включение) ключа 45 и ключа 48 (Фиг.1 и Фиг 5), что обеспечивает формирование замкнутой электрической цепи: первый вывод конденсатора 4 (Фиг.1), первая токовая шина 6 (Фиг.1), первый управляемый ключ 45 (Фиг.1), первый индуктивный накопитель энергии 21 (Фиг.1), первая терапевтическая шина 15 (Фиг.1), первый рабочий электрод 8 (Фиг.1), пациент 14 (Фиг.1), второй рабочий электрод 9 (Фиг.1), вторая терапевтическая шина 16 (Фиг.1), четвертый управляемый ключ 48 (Фиг.1), резистивный датчик тока 57 (Фиг.1), вторая токовая шина 7 (Фиг.1), второй вывод конденсатора 5 (Фиг.1). Возникший в результате коммутации терапевтический ток первой доли электрической энергии W1 62 (Фиг.8) позитивной составляющей двухфазного кардиодефибрилляционного импульса терапевтического разряда 60 (Фиг.7) создает на резистивном датчике тока 57 (Фиг.1) пропорциональное его значению падение напряжения, преобразуемое аналого-цифровым преобразователем 58 (Фиг.1) в цифровой управляющий сигнал, подаваемый на блок управления 59 (Фиг.1). Таким образом происходит измерение силы тока в данной цепи, при этом блок управления 59 (Фиг.1) контролирует выполнение условия:
При наступлении условия {1} (текущий ток достигает значения, например, 80 А) посредством управляющего сигнала из блока управления 59 (Фиг.1) происходит разрыв созданной электрической цепи за счет выключения четвертого управляемого ключа 48 (Фиг.1 и Фиг.5). Однако выключение четвертого управляемого ключа 48 (Фиг.1) не приводит к прекращению протекания тока позитивной составляющей двухфазного кардиодефибрилляционного импульса терапевтического разряда 60 (Фиг.7) через пациента 14 (Фиг.1), так как в соответствии с известными законами электротехники электрическая энергия, накопленная в первом индуктивном накопителе энергии 21 (Фиг.1), стремится поддержать величину этого терапевтического тока, т.е. терапевтический ток второй доли электрической энергии W2 (например, 20 Дж) 63 (Фиг.8) позитивной составляющей двухфазного кардиодефибрилляционного импульса терапевтического разряда 60 (Фиг.7) протекает по следующей электрической цепи: первый индуктивный накопитель энергии 21 (Фиг.1), первый рабочий электрод 8 (Фиг.1), пациент 14 (Фиг.1), второй рабочий электрод 9 (Фиг.1), вторая терапевтическая шина 16 (Фиг.1), третий диод 35 (Фиг.1), электрическое соединение первого 27 и второго 28 коммутаторов (Фиг.1), замкнутый первый управляемый ключ 45 (Фиг.1). Образованная таким образом электрическая цепь исключает измерение протекающего через нее терапевтического тока второй доли электрической энергии W2 (Фиг.8) тока позитивной составляющей двухфазного кардиодефибрилляционного импульса терапевтического разряда 60 (Фиг.7), но дозирование заданного количества электрической энергии второй доли W2 в этом случае производится путем расчета tотк (Фиг.5) времени выключения четвертого управляемого ключа 48 (Фиг.1), по прошествии которого блоком управления 59 (Фиг.1) снова подается сигнал на включение четвертого управляемого ключа 48 (Фиг.1 и Фиг.5). Процедура включения и выключения четвертого управляемого ключа 48 (Фиг.1 и Фиг.5) происходит до тех пор, пока не закончится предварительно заданное в результате расчета блоком управления 59 (Фиг.1) время прохождения позитивной составляющей двухфазного кардиодефибрилляционного импульса терапевтического разряда 60 (Фиг.7), после чего первый управляемый ключ 45 (Фиг.1) выключается, а второй 46 и третий 47 управляемые ключи (Фиг.1 и Фиг.4) включаются, обеспечивая тем самым посылку пациенту 14 (Фиг.1) негативной составляющей двухфазного кардиодефибрилляционного импульса терапевтического разряда 61 (Фиг.7), причем время паузы (Фиг.4 и Фиг.7) между обоими указанными составляющими 60 и 61 (Фиг.7) двухфазного кардиодефибрилляционного терапевтического разряда определяется только переходными процессами в электрических цепях средства для формирования кардиодефибрилляционного импульса и выбором элементной базой первого и второго коммутаторов, которое должно быть как можно меньше (в идеальном случае стремится к нулю).
После того, как по команде из блока управления 59 (Фиг.1) произошло замыкание (включение) ключа 46 и ключа 47 (Фиг.1 и Фиг 6), происходит формирова