Способ дентальной имплантации верхней челюсти
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к стоматологии, и может быть применимо для дентальной имплантации верхней челюсти. Вводят эндоскоп в верхнечелюстной синус через ложе глубиной, соответствующей или превышающей длину имплантата. Укладывают под контролем эндоскопа на дно синуса через оставшиеся ложа биоматериал в виде аутоостеогенной ткани, содержащей остеобласты и хондробласты в комбинации с мелкогранулированным пористым никелидом титана с размером частиц от 1 до 1000 мкм. Устанавливают имплантаты. Способ позволяет уменьшить травматичность, обеспечить формирование органотипичного регенерата, обеспечить интеграцию имплантата с пересаженной тканью и реципиентной зоной. 3 ил.
Реферат
Изобретение относится к медицине, в частности к стоматологии, и может быть использован для лечения адентии премолярно-молярного сегмента верхней челюсти в условиях дефицита костной ткани и низком расположении дна верхнечелюстного синуса.
Известен способ дентальной имплантации верхней челюсти, включащий формирование ложа для дентальных имплантатов путем сверления, заканчивающихся на 1-2 мм выше дна верхнечелюстного синуса, с последующим их удлинением с помощью долота, поднятием дна верхнечелюстного синуса, укладкой на дно биоматериала (ауто-, аллокостную ткань, гидроксилапатит или их комбинации), последующим контролем глубиномером состояния трансплантационного материала и вкручивание имплантатов в челюсть [1].
Недостатком данного способа является невозможность зрительного контроля локализации биоматериала, низкая эффективность, обусловленная дисгармоничным взаимодействием трансплантационного или имплантационного материала с реципиентными тканями, что ведет к их отторжению или резорбции.
Наиболее близким техническим решением является способ дентальной имплантации верхней челюсти, включающий введение в верхнечелюстной синус жесткого эндоскопа с углом обзора 70° через естественное отверстие, пункцию верхнечелюстного синуса через нижний носовой ход, отслаивание слизистой оболочки в области дна синуса после гидропрепаровки при помощи троакара и элеватора, помещение с помощью шприца биоматериала в виде текучей консистенции на дно синуса под контролем эндоскопа, формирование ложа для имплантатов и их установку [2].
Недостатком известного способа является высокая травматичность вмешательства за счет необходимости увеличения естественного отверстия, соединяющего верхнечелюстной синус и средний носовой ход, пункции верхнечелюстного синуса в области нижнего носового хода.
Задачей предлагаемого изобретения является снижение травматичности и повышение эффективности дентальной имплантации в области премолярно-молярного сегмента верхней челюсти в условиях низко расположенного дна верхнечелюстного синуса.
Поставленная задача достигается тем, что в способе дентальной имплантации верхней челюсти, включающем введение эндоскопа в верхнечелюстной синус, укладку биоматериала на дно синуса, формирование ложа для имплантатов и последующую их установку, новым является то, что эндоскоп вводят через ложе, глубина которого соответствует или превышает длину имплантата, под контролем которого на дно синуса через оставшиеся ложа укладывают биоматериал в виде аутоостеогенной ткани, содержащей остеобласты и хондробласты в комбинации с мелкогранулированным пористым никелидом титана с размером частиц от 1 до 1000 мкм.
Предлагаемый способ дентальной имплантации позволяет в значительной степени снизить травматичность вмешательства за счет отсутствия необходимости введения эндоскопа в верхнечелюстной синус через средний носовой ход и пунктирования верхнечелюстного синуса через нижний носовой ход, повысить эффективность данной операций, поскольку пересадка аутоостеогенной ткани, структура которой находится между гиалиновым хрящом и грубоволокнистой костной тканью, в комбинации с мелкогранулированным пористым никелидом титана обеспечивает оптимальную регенерацию и формирование органотипичного костного регенерата в проекции дна верхнечелюстного синуса. Мелкогранулированный пористый никелид титана с размером частиц от 1 до 1000 мкм позволяет получить заданный объем регенерата с минимальным количеством остеогенной ткани.
Способ осуществляют следующим образом. После выкраивания и мобилизации слизисто-надкостничного лоскута в зоне отсутствующих зубов заднего и/или среднего отдела верхней челюсти образуют ложа для имплантатов путем сверления на 0,2-0,3 мм меньше диаметра дентальных имплантируемых конструкций с перфорацией дна верхнечелюстного синуса. Через отверстие, имеющее наибольшую глубину (чаще в области бугра верхней челюсти), в верхнечелюстной синус вводят эндоскоп, под контролем которого через оставшиеся ложа на дно синуса помещают остеогенную ткань в комбинации с мелкогранулированным пористым никелидом титана с размерами частиц от 1 до 1000 мкм и устанавливают дентальные имплантаты. При помощи эндоскопа проводят контроль состояния корневой части имплантатов, трансплантационного и имплантационного материалов. После извлечения эндоскопа в это отверстие устанавливают дентальную имплантирующую конструкцию, слизисто-надкостничный лоскут укладывают на прежнее место и рану ушивают наглухо.
Пример. Больной Ч., 58 лет, обратился с целью протезирования зубов конструкциями с опорой на дентальные имплантаты. Зубы потерял в течение последних 10 лет по поводу хронического пародонтита и осложненного кариеса. Объективно: Конфигурация лица не нарушена. Рот открывал свободно. Определялась частичная вторичная адентия верхних и нижней челюстей, атрофия альвеолярной кости. На ортопантомограмме видны признаки неравномерной атрофии альвеолярных отростков нижней, правой и левой верхних челюстей, низкое расположение дна левого и правого верхнечелюстного синуса. Перед операцией проведено лечение патологии внутренних органов, нормализованы реологические свойства крови, устранены иммунологические нарушения организма, удалены разрушенные 22, 37, 44 и 48 зубы. Под местной анестезией выкроены трапециевидные слизисто-надкостничные лоскуты с вестибулярной стороны альвеолярного отростка в проекции отсутствующих зубов верхней и нижней челюсти, последние отслоены от кости и мобилизованы. С помощью бормашины и специальных фрез сформированы костные ложа вглубь альвеолярных отростков по диаметру на 0,2-0,3 мм меньше диаметра дентальных имплантируемых конструкций. В проекции отсутствующих моляров и премоляров правой верхней челюсти образованы 3 ложа с перфорацией дна верхнечелюстного синуса. Через переднее перфорированное ложе, глубина которого составляла 12 мм, в синус введен 2-миллиметровый эндоскоп, под контролем которого через два дистально расположенных ложа на дно синуса помещена остеогенная ткань, "выращенная" в толще гребня подвздошной кости, в комбинации с мелкогранулированным пористым никелидом титана с размерами частиц от 1 до 1000 мкм, после чего в них установлены пористые никелид-титановые имплантаты с пористой шейкой длиной 10 мм. Проведен эндоскопический контроль состояния корневой части имплантатов, трансплантационного и имплантационного материалов. После извлечения эндоскопа в это и оставшиеся отверстия установлены дентальные имплантирующие конструкции. Аналогичная операция выполнена слева. Слизисто-надкостничные лоскуты уложены на прежнее место, раны ушиты наглухо. В проекции отсутствующих правых и левых моляров нижней челюсти установлено по два дентальных имплантата с каждой стороны. Швы сняты спустя 10 суток. Заживление ран первичное. Зубное протезирование осуществлено через 3,5 месяца. При осмотре через 3 года функциональных нарушений со стороны зубочелюстного аппарата не выявлено.
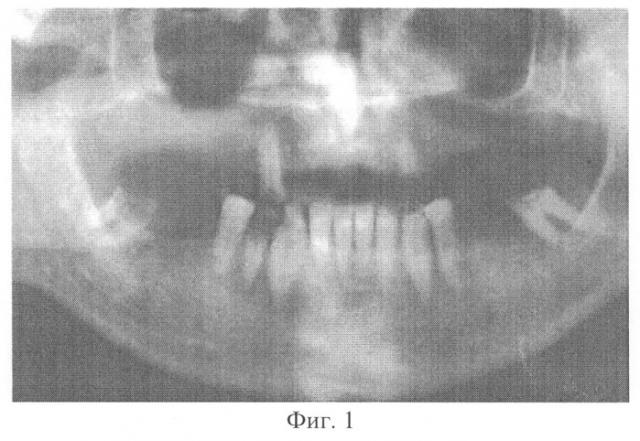
На фиг.1 показано состояние зубочелюстного аппарата больного Ч. до лечения;
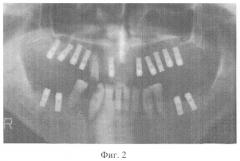
На фиг.2 показано состояние зубочелюстного аппарата больного Ч. после дентальной имплантации;
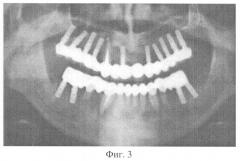
На фиг.3 показано состояние зубочелюстного аппарата больного Ч. после дентальной имплантации и зубного протезирования через 3 года.
Преимущества предлагаемого способа заключается в том, что в результате использования в качестве трансплантационного материала аутоостеогенной ткани происходит остеоинтеграция имплантата с пересаженной тканью и реципиентной зоной. Аутоостеогенная ткань, являясь высокоиндуктивной за счет наличия клеточных элементов мезенхимального происхождения, обладает свойствами интерстициального роста и анаэробного гликолиза и после трансплантации более жизнеспособна в условиях тканевой гипоксии по сравнению с другими ауто-, алло-, ксенотрансплантационными и имплантационными материалами, быстро прорастает сосудами, что способствует образованию в операционной ране органотипичного регенерата в соответствии с дальнейшими закономерностями непрямого остеогенеза. Благодаря биомеханической и биохимической совместимости пористого никелида титана с тканями организма ткань прорастает между гранулами и сквозь его пористую структуру. Остеогенная ткань и пористый никелид титана в виде мелких гранул удобны в применении, так как дают возможность восстанавливать изъяны любой конфигурации. Успешность применения данного имплантационного материала для восстановления дефектов в комбинации с аутотрансплантатом следует объяснить тем, что для получения заданного объема регенерата необходимо меньшее число остеогенных клеток или низкодифференцированных клеточных элементов мезенхимального происхождения, в сравнении с трансплантацией без имплантационного материала.
Клинические испытания предлагаемого способа осуществлены на 5 больных, которым установили 18 имплантатов. В результате наблюдения за пациентами в течение 3-4 лет, каких либо анатомо-функциональных нарушений со стороны зубочелюстного аппарата не выявлено, состояние дентальных имплантатов удовлетворительное.
Источники информации
1. Робустова Т.Г. Имплантация зубов (хирургические аспекты). М.: Медицина, 2003, с.482-483.
2. Робустова Т.Г. Имплантация зубов (хирургические аспекты). М.: Медицина, 2003, с.484.
Способ дентальной имплантации верхней челюсти, включающий введение эндоскопа в верхнечелюстной синус, укладку биоматериала на дно синуса, формирование ложа для имплантатов и последующую их установку, отличающийся тем, что эндоскоп вводят через ложе, глубиной, соответствующей или превышающей длину имплантата, под контролем которого на дно синуса через оставшиеся ложа укладывают биоматериал в виде аутоостеогенной ткани, содержащей остеобласты и хондробласты в комбинации с мелкогранулированным пористым никелидом титана с размером частиц от 1 до 1000 мкм.