Способ пульсометрической оценки функционального состояния и характера вегетативной регуляции сердечно-сосудистой системы человека
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к кардиологии, и может быть использовано для оценки функционального состояния сердечно-сосудистой системы (ССС) человека и характера ее регуляции вегетативной нервной системой и другими регуляторными системами гомеостаза. Способ позволяет с помощью компьютера и пьезоэлектрического датчика с высокой точностью, непрерывно в течение необходимого времени и не сложно по выполнению регистрировать дифференциальные сфигмограммы и по ним, используя метод определения "кодирующих" точек, проводить экспресс-анализ одновременно двух основных характеристик пульса - а) ритмичности и б) пульсовых колебаний артериального давления, вызванных периодическим выбросом ударного объема крови в аорту. Специально разработанный алгоритм обработки данных обеспечивает автоматическую расстановку "кодирующих" (расчетных) точек на усредненном графике кардиоцикла, что в сочетании с дополнительной визуальной корректировкой локализации этих точек повышает точность определения амплитудно-временных параметров на каждой распознанной нормальной пульсации выбранного фрагмента пульсограммы. По этому фрагменту длительностью не менее 2 мин (стандартная длительность - 5 мин) измеряют и анализируют временные показатели, характеризующие сердечный ритм и его вариабельность. Затем вычисляют калибровочный коэффициент для перевода условных единиц компьютерной "оцифровки" в общепринятые единицы измерения артериального давления крови (АД, мм рт.ст.) и путем интегрирования по соответствующим площадям кардиоциклов на выбранном фрагменте пульсограммы определяют в мм рт.ст. величины пульсового прироста АД крови на различных этапах сердечного цикла. По этим величинам рассчитывают все амплитудно-временные кардиогемодинамические показатели, зависящие от АД крови и характеризующие сократительную способность миокарда левого желудочка и упруго-эластические свойства стенок сосудов артериального русла. Обеспечивается непрерывный мониторинг изменений амплитудно-временных параметров пульсограммы, получение расчетных данных практически в реальном масштабе времени, а также быстрое выполнение сложных математических преобразований для проведения спектрального анализа вариабельности сердечного ритма и выбранных амплитудно-временных кардиогемодинамических показателей для определения их суммарной и дифференцированной по стандартным частотным диапазонам спектральной мощности колебаний. По результатам статистического и спектрального анализов вариабельности измеренных показателей оценивают функциональное состояние и характер вегетативной регуляции ССС обследуемого путем сравнения измеренных величин показателей со среднестатистическими числовыми значениями этих же показателей, установленными для ССС определенных по возрасту, полу, состоянию здоровья и другим признакам групп людей, которые выбраны в качестве контрольных. Способ обеспечивает повышение точности и расширение числа информативных показателей для оценки ССС человека. 8 ил., 2 табл.
Реферат
Изобретение относится к медицине, а именно к кардиологии, и может быть использовано для неинвазивного экспресс-анализа функционального состояния сердечно-сосудистой системы (ССС) человека и характера ее регуляции вегетативной нервной системой и другими регуляторными системами гомеостаза. На основе изобретения разработано новое диагностическое устройство для комплексного и, в то же время, простого по выполнению обследования ССС человека с использованием компьютерной регистрации и анализа сердечного ритма и колебаний артериальных стенок при прохождении пульсовой волны. Изобретение может быть использовано для диагностики сердечно-сосудистых заболеваний в клинике, при проведении оперативного медицинского контроля за состоянием здоровья различных групп населения, а также в медицинских прогностических исследованиях с целью оценки тенденций развития функциональных доклинических изменений в ССС и вероятности их выхода за допустимые пределы.
Разработка и совершенствование методологии и технических средств ранней диагностики состояния ССС человека является чрезвычайно актуальной задачей в современных условиях, поскольку эта система - наиболее уязвимая по отношению к физическим и эмоциональным (стрессовым) нагрузкам часть организма и именно сердечно-сосудистая патология в структуре заболеваемости, инвалидизации и смертности занимает устойчивое первое место в развитых странах. Важнейшую роль в регуляции ССС и в адаптации ее функций к меняющимся условиям внешней и внутренней среды играет вегетативная нервная система (ВНС). Поэтому современные системы комплексного обследования ССС должны включать и оценку характера вегетативной регуляции этой системы.
До последнего времени системы такого обследования ССС строились преимущественно на основе вариационно-статистического и спектрального анализа кардиоинтервалограммы, получаемой с помощью метода электрокардиографии (ЭКГ) (например, такие известные системы, как «Анкар», «Инкарт», "Holter for Windows", "SphygmoCor Px" и др.).
Известен запатентованный способ диагностики по кардиоритму, использующий ЭКГ для регистрации и накопления кардиоинтервалов за определенный промежуток времени с последующим их анализом [1].
Однако используемый в таких системах и способах метод ЭКГ, несмотря на его высокую информативность при изучении динамики электрического возбуждения сердца и широкую применяемость при проведении спектрального анализа вариабельности сердечного ритма, не может в достаточной мере оценивать кардиогемодинамику, сократительные свойства миокарда и состояние сосудистого тонуса. В то же время у больных очень часто функциональные нарушения, происходящие в миокарде и кровеносных сосудах, предшествуют изменениям, выявляемым с помощью ЭКГ. Поэтому в последние годы активно разрабатываются системы, в которых используются и другие способы неинвазивного изучения состояния ССС.
Широкое распространение получил метод ультразвуковой эхокардиографии, позволяющий проводить неинвазивную оценку ряда важных кардио- и гемодинамических характеристик ССС. Тем не менее, использование этого метода требует сложной и дорогостоящей аппаратуры, высокой квалификации оператора и значительного времени обследования, что снижает его значимость как метода получения экспресс-информации.
Дальнейший прогресс в этом направлении был связан с созданием специализированных систем анализа ССС, в основе которых лежит регистрация амплитудно-временных параметров пульсовых волн в виде электрических сигналов, возникающих в результате преобразования специальными датчиками механических сигналов от перемещающихся под воздействием волны пульсового давления стенок артерий - сфигмография (СФГ) или от изменяющихся под воздействием пульсирующего притока крови объемов тканей - плетизмография. На основе фото- и импедансных плетизмографических и других датчиков (например, с использованием компрессионной манжеты) были созданы такие системы, как "DynaPuls", "Finapres", "Portapres" и др. [2], во многом объединяющие плетизмографию со сфигмографией, а сам метод получил название объемной сфигмографии (ОСФГ). В то же время сохраняются высокая стоимость этих устройств и сложность процедуры расшифровки результатов. Например, при использовании относительно недорогой (499 долларов США) системы "DynaPuls" требуется передать первичную информацию по сети «Интернет» в специальный коммерческий аналитический центр в Калифорнии для ее интерпретации, что создает дополнительные трудности и существенно увеличивает стоимость обследования.
Близким к заявленному является «Способ оценки функционального состояния сердечно-сосудистой системы», который осуществляется путем измерения артериального давления крови (АД) и регистрации СФГ в течение одного дыхательного цикла с целью определения средней длительности одного кардиоцикла и времени нарастания пульсового давления (t, мс) [3]. Этот способ позволяет с помощью предложенных эмпирических формул по величине «t», диастолическому и пульсовому давлениям дать приблизительную оценку в условных единицах степени выраженности функционального стресса под влиянием физической нагрузки. Однако, он не может быть использован в качестве метода комплексного обследования ССС из-за ограниченного числа изучаемых параметров и невозможности выявления динамики изменения во времени важных для диагностики показателей, ограничиваясь при анализе лишь несколькими пульсовыми волнами одного дыхательного цикла. По этой же причине запатентованный способ не может быть применен для спектрального анализа вариабельности амплитудно-временных параметров при определении характера вегетативной регуляции ССС.
Наиболее близким по своей сущности к заявленному способу является метод, использующий датчики для регистрации ОСФГ с последующим математическим дифференцированием пульсовых кривых [4]. Недостатком этого метода является то, что регистрируемый при этом сигнал отражает пульсовые изменения и артериального, и капиллярного, и венозного кровенаполнения тканей, по разному изменяющих их объем. Это приводит к демпфированию сигнала, сглаживанию или, наоборот, усложнению контура графика кардиоцикла и к потере ряда существенных деталей на регистрируемой кривой. Дифференцирование такой пульсограммы облегчает процедуру временного анализа графика по «кодирующим» точкам, но не повышает точность и информативность обследования, что в дальнейшем приводит к неопределенности в оценке состояния ССС, а ограниченное число регистрируемых кардиоциклов не позволяет анализировать воздействия регуляторных систем организма на состояние ССС.
Анализ современного состояния проблемы пульсовой диагностики ССС привел к выводу о предпочтительности и перспективности использования генераторных (индукционных и пьезоэлектрических) датчиков для непосредственной регистрации дифференциальных сфигмограмм (ДСФГ) с пульсирующего участка тела над артерией [5]. Эта возможность появилась в последние годы в связи с промышленным созданием малогабаритных и высокочувствительных пьезоэлектрических преобразователей с широкой полосой рабочих частот и высокой собственной резонансной частотой (более 2000 Гц) [6]. Такие датчики принадлежат к числу наиболее точных и позволяют преобразовывать механические воздействия на датчик непосредственно в аналоговый электрический сигнал, который может быть зарегистрирован графически в виде кривой скорости изменения силы воздействия. Развитие вычислительной техники открыло возможность преодоления трудностей, возникающих при количественной обработке и анализе больших массивов получаемой пульсометрической информации [7]. Стало возможным проведение непрерывного мониторинга изменений амплитудно-временных параметров пульсограммы, получение расчетных данных практически в реальном масштабе времени, а также быстрое выполнение сложных математических преобразований для выявления периодических составляющих в колебаниях амплитудно-временных параметров пульсовых кривых с целью оценки значимости их вклада в обеспечение необходимой кардиогемодинамики.
Задачей изобретения явилось создание способа неинвазивного обследования функционального состояния ССС человека, позволяющего с высокой точностью, непрерывно в течение необходимого времени и не сложно по выполнению регистрировать пульсовые кривые и по ним проводить экспресс-анализ одновременно двух основных характеристик пульса - а) ритмичности и б) пульсовых колебаний артериального давления, вызванных периодическим выбросом ударного объема крови в аорту. С этой целью нами был разработан компьютерный вариант метода ДСФГ, в котором в качестве датчика было использовано не применяемое ранее в этих целях простое и удобное для закрепления на пульсирующем участке тела техническое устройство другого назначения, выпускаемое промышленностью (звуковой преобразователь типа «ЗП» с металлической мембраной, на внутреннюю сторону которой наклеен пьезокерамический элемент, обеспечивающий такому датчику чувствительность около 0,5 мм рт.ст./с при собственной резонансной частоте более 2600 Гц). Специально разработанные программное обеспечение (ПО) и алгоритм обработки данных сделали несложным для оператора (а также для любого лица, не имеющего медицинского образования, но внимательно соблюдающего инструкцию для пользователя) проведение в автоматизированном режиме регистрации кривой ДСФГ, измерение по выбранному фрагменту пульсограммы ее амплитудно-временных параметров и получение результатов анализа широкого спектра показателей, совокупно характеризующих функциональное состояние ССС и особенности ее регуляции со стороны ВНС и других регуляторных систем.
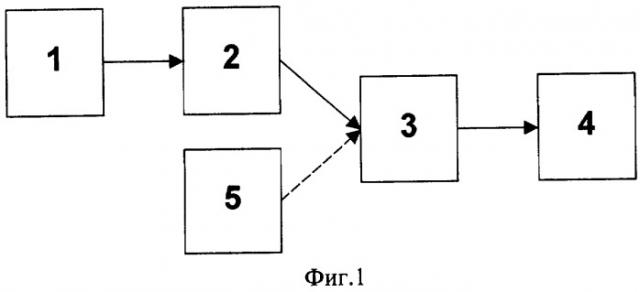
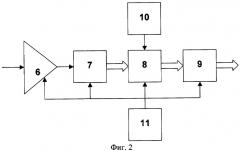
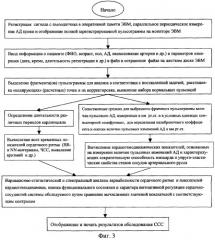
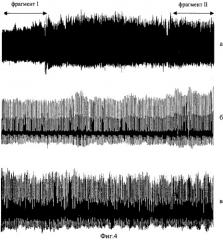
Изобретение поясняется прилагаемыми чертежами и графиками, на которых изображены: на фиг.1 - структурная схема устройства для пульсометрического обследования; на фиг.2 - функциональная схема устройства сопряжения сигнала с ЭВМ; на фиг.3 - блок-схема алгоритма обработки данных; на фиг.4 - пример полной пульсограммы и выбранных из нее фрагментов; на фиг.5 - фрагмент ДСФГ с выделенным набором индивидуальных пульсаций и графиком усредненного кардиоцикла; на фиг.6 - примеры трех основных типов графиков кардиоцикла.
Устройство для осуществления способа пульсометрического обследования сердечно-сосудистой системы содержит (фиг.1) пьезодатчик 1, выход которого соединен с входом устройства сопряжения 2, подключенного к ЭВМ 3. Информация выводится на монитор 4. Второй вход ЭВМ 3 соединен с выходом сфигмоманометра 5.
Устройство сопряжения 2 состоит из усилителя 6 (фиг.2), выход которого соединен с входом аналого-цифрового преобразователя 7 (АЦП), связанного с блоком преобразования 8, выход которого через блок согласования 9 соединен с ЭВМ. Тактовые импульсы с выхода генератора тактовых импульсов 10 (ГТИ) подаются на блок преобразования 8. Питание всей схемы осуществляется от источника питания 11. Аналоговый сигнал с датчика, усиленный до необходимой амплитуды, поступает на вход АЦП, где он квантуется с определенной частотой дискретизации (в нашем устройстве используется частота, равная 200 Гц, и, соответственно, интервал времени между отсчетами или длительность дискрета квантования - Δt=5 мс) и оцифровывается. Далее информация передается на блок преобразования 8, который по тактовым импульсам от ГТИ вырабатывает сигналы управления АЦП и подготавливает данные для передачи через блок согласования 9 по последовательному каналу на вычислитель ЭВМ с соответствующим ПО.
Способ пульсометрического обследования ССС осуществляется следующим образом (фиг.3). У обследуемого неинвазивно с помощью пьезодатчика, установленного над пульсирующей, поверхностно расположенной центральной (например, сонной) или периферической (например, пальцевой или височной) артерией, снимают сигнал и непрерывно регистрируют его в оперативной памяти ЭВМ. На фиг.4а в качестве примера представлен растянутый во весь экран монитора график ДСФГ длительностью 25 мин, зарегистрированный с пальцевой артерии большого пальца левой руки молодого (23 г.) мужчины при изучении влияния ортостатической нагрузки на его ССС. В таком виде пульсограмма сохраняется на жестком диске ЭВМ в виде файла для последующего анализа. После этого в этот файл записывают данные о пациенте (ФИО, возраст, пол, артериальное давление, анамнез, предварительный диагноз и др.) и параметры измерения (дата, время, длительность регистрации и др.). На следующем этапе в соответствии с задачей исследования (в представленном случае - при изучении влияния ортостатической нагрузки на ССС) выбирают фрагменты ДСФГ. На фиг.4б представлен выбранный пятиминутный фрагмент пульсограммы, зарегистрированной в положении лежа (фрагмент 1, условный контроль, 5 мин до подъема), на фиг.4в - также пятиминутный фрагмент в положении стоя (фрагмент 2, с 15 по 20 минуту ортостатической нагрузки). Эти фрагменты длительностью обычно не менее 2-х минут (стандартная длительность - 5 минут) могут быть сохранены в виде отдельных файлов для последующего анализа. Для повышения точности сравнительного анализа характеристик отдельно выбранных фрагментов ДСФГ с помощью ПО задают временные границы этих фрагментов, что позволяет вычислять строго соответствующие им показатели.
График ДСФГ отражает скорость изменения АД на разных этапах сердечного цикла в течение всего периода обследования и представляет каждый кардиоцикл в виде сложного контура с характерными перегибами. Это позволяет в соответствии с теорией информации с помощью специального компьютерного алгоритма на графике ДСФГ выделять определенные точки: нулевые (пересечение с изолинией), экстремальные и точки перегиба в качестве «кодирующих» (расчетных, опорных) точек и по ним измерять и затем вычислять все амплитудно-временные параметры и показатели. Правильная расстановка таких точек является основным условием точности и достоверности результатов измерения и требует процедуры дополнительного уточнения. С этой целью из выбранного в качестве примера фрагмента ДСФГ (фиг.5-I) с помощью ЭВМ выделяют все индивидуальные пульсации и укладывают их на график одного кардиоцикла, совмещая по координате максимального положительного экстремума (фиг.5-II). Затем по этому набору автоматически строят график усредненной пульсации (фиг.5-III) и на нем проставляют «кодирующие» точки, которые пользователь проверяет визуально и, в случае ошибки, корректирует. Выявляют нормальные зубцы на графике ДСФГ и отбрасывают ложные зубцы из набора пульсаций. Для этого вычисляют порог амплитуды (горизонтальная линия на фиг.5-II), относительно которого производят поиск абсолютного систолического максимума (наибольший положительный экстремум) графика ДСФГ, находящегося выше данного порога. Критерием отбрасывания является резкое отклонение амплитудно-временных параметров анализируемого зубца от средних значений (более чем на 3 среднеквадратичных отклонения). Оставшийся после процедуры отбрасывания набор зубцов считается набором пульсаций, отражающим скорость изменения АД крови обследуемого. Затем принцип уточненной расстановки расчетных точек на графике усредненной пульсации автоматически переносится на каждую распознанную нормальную пульсацию (фиг.5-IV).
По положению «кодирующих» точек на графике ДСФГ определяют все временные параметры и показатели. Вычисление амплитудных характеристик сигнала, содержащих информацию о величине АД крови, требует дополнительной процедуры калибровки данных для их перевода в общепринятые единицы измерения АД (мм рт.ст.). Для этого компьютерная регистрация сигнала от датчика в виде кривой ДСФГ сопровождается параллельным периодическим измерением величин систолического (САД) и диастолического (ДАД) давлений крови с помощью сфигмоманометра. Эти величины вводятся в компьютер для расчета среднего значения ПАД (=САД-ДАД) для выбранного периода обследования. Соотнесение этой непосредственно измеренной в мм рт.ст. величины ПАД со средней величиной ПАД, вычисленной в этот же период в условных единицах компьютерной «оцифровки» путем интегрирования по соответствующим площадям выбранного фрагмента кривой ДСФГ, позволяет определить калибровочный коэффициент пропорциональности АД. С учетом этого коэффициента вычисляют в мм рт.ст. величины пульсового прироста АД крови на различных этапах сердечного цикла и по ним рассчитывают все показатели, зависящие от АД крови и характеризующие кардиогемодинамику и упруго-эластические свойства стенок сосудов артериального русла. Это позволяет проводить длительный и непрерывный во времени мониторинг динамики пульсовых колебаний АД крови в течение всего периода обследования в общепринятых единицах измерения - мм рт.ст. Обеспечивается необходимый уровень достоверности при статистической обработке измеренных амплитудно-временных показателей, становится возможным проведение спектрального анализа их вариабельности, в том числе, - при различных воздействиях на организм (нагрузочные тесты, прием лекарственных средств и др.), а также сравнение результатов обследований, выполненных в разное время.
На фиг.6 показаны примеры трех основных типов встречающихся графиков отдельного кардиоцикла и варианты расположения на этих графиках «кодирующих» точек.
Типы (1) и (3) графиков - соответствуют ССС молодых и пожилых людей, тип (2) характерен для большинства взрослых (от 25 до 55 лет) людей.
Графики ДСФГ представляют собой первые производные графиков зависимости изменения АД от времени (СФГ) при прохождении пульсовой волны, что определяет математически однозначное расположение точки А как точки начала анакротической фазы изгнания крови, соответствующей моменту открытия аортального клапана. В этой точке АД=ДАД и первая производная СФГ равна нулю, что позволяет провести через эту точку горизонтальную изолинию, определяющую площадь под и/или над кривой графика и отражающую прирост или уменьшение давления крови в артериях при прохождении пульсовой волны, обусловленной выбросом ударного объема крови из левого желудочка. Точка В соответствует моменту достижения максимальной скорости систолического прироста АД (абсолютный положительный экстремум ДСФГ); точка С - моменту достижения максимальной величины АД в результате изгнания крови из левого желудочка в период систолы (точка пересечения изолинии нисходящей частью систолической волны давления, первая производная СФГ в этой точке равна нулю); точка D - моменту окончания изгнания крови (закрытие аортального клапана, отрицательный экстремум ДСФГ, предшествующий росту дикротического АД) [4]; точка F - моменту достижения максимальной скорости прироста АД, вызванного в начале диастолы дикротической волной давления крови, отраженной от закрытого аортального клапана; точка G - моменту достижения максимальной величины вторичного систолического прироста АД за счет ранней (до закрытия аортального клапана) отраженной от периферии первичной волны пульсового давления крови.
Учитывая «Международные стандарты» [8], а также официальные методические рекомендации группы российских кардиологов [9], во временной области по «кодирующим» точкам измеряют и анализируют все основные показатели, характеризующие сердечный ритм и его вариабельность: среднюю длительность выявленных кардиоинтервалов (между смежными точками «В» на фиг.6), среднюю длительность нормализованных кардиоинтервалов - TNN, а также длительности отдельных фаз кардиоцикла; оценивают вариабельность выбранных для измерения временных показателей (вычисляют SD, DX, CV, RMSSD, pNN50 и др.).
«Кодирующие» точки используют и для определения (см. фиг.6) в условных единицах компьютерной «оцифровки» средней для выбранного фрагмента ДСФГ величины ПАД - интегрированием по площадям, покрываемым ординатами между точками А и С, если площадь между точками С и G меньше или равна нулю, или между точками А и G, если площадь между точками С и G больше нуля. Как уже было сказано, сравнение этой величины ПАД со средней величиной ПАД, измеренной с помощью сфигмоманометра, позволяет перевести условные единицы «оцифровки» в общепринятые единицы - мм рт.ст. и вычислять в этих единицах все показатели, отражающие пульсовые изменения АД крови в определенные периоды кардиоцикла в течение всего времени обследования:
- величину ускоренного анакротического прироста АД в период систолического выброса крови в аорту из левого желудочка - ΔАДАуск [мм рт.ст.] (интегрированием по площади, покрываемой ординатами между точками А и В, на фиг.6 выделена штриховкой с наклоном влево);
- величину замедленного анакротического прироста АД в период систолы - ΔАДАзам [мм рт.ст.] (интегрированием по площади, покрываемой ординатами между точками В и С или В и G, см. ниже);
- величину дикротического прироста АД крови в фазе его ускоренного возрастания в начальный период диастолы - ΔАДДуск [мм рт.ст.] (интегрированием по площади, покрываемой ординатами между точками D и F, на фиг.6 выделена штриховкой с наклоном вправо). Эта величина, четко выявляемая на всех кривых ДСФГ, отражает тонус стенок сосудов артериального русла, определяющий периферическое сопротивление на уровне артериол, являющееся причиной возникновения отраженных пульсовых волн;
- величину вторичного волнообразного прироста АД за счет ранней отраженной от периферического сопротивления волны пульсового давления в период систолы - ΔАДОС [мм рт.ст.], проявляющегося или в период катакроты, или в фазе замедленного анакротического выброса крови (определяется интегрированием по площади, покрываемой ординатами между точками С и G). Отрицательная или нулевая величина интеграла этой площади, соответствующая волнообразному катакротическому изменению АД на графике ДСФГ отдельного кардиоцикла (на фиг.6-2 эта площадь выделена горизонтальной штриховкой), характерна для здоровых взрослых людей с упругими и в то же время эластичными аортальными стенками. У молодых и, особенно, у физически тренированных людей с очень эластичными стенками аорты эта волна гасится и может быть практически незаметной (фиг.6-1). Положительные значения интеграла площади CG (ΔАДОС больше нуля), увеличивающие САД и ПАД и удлинняющие замедленную анакротическую фазу систолы (на фиг.6-3 эта площадь выделена также горизонтальной штриховкой), указывают на превышение нормальной упругости (жесткость) стенок аорты, появляющееся с возрастом и под воздействием факторов риска сердечно-сосудистых заболеваний (например, таких, как диабет, курение). Этот прирост АД обусловлен тем, что снижение эластичности стенок препятствует расширению аорты под воздействием приходящей отраженной от периферического сопротивления волны давления крови, а возросшая при этом скорость распространения волны по сосудистой стенке [10] обеспечивает более быстрый ее возврат и более раннее наложение на первичную систолическую волну. С учетом изложенного, в случае, если ΔАДОС больше нуля, в целях проведения сравнительных оценок сократительной способности миокарда левого желудочка разных обследуемых определяют величину нормализованного пульсового артериального давления - ПАДн=ПАД-ΔАДОС [мм рт.ст.].
По этим величинам рассчитывают производные кардиогемодинамические показатели:
- среднюю скорость систолического прироста АД в период ускоренного анакротического выброса крови в аорту - [мм рт.ст./с],
где tAB - длительность периода АВ;
- максимальную скорость этого прироста - VmaxАДА [мм рт.ст./с], определяемую по ординате точки В. На эти величины не оказывает заметного влияния (не накладывается) отраженная от периферического сопротивления пульсовая волна давления крови и, поэтому, они вместе с нормализованной величиной ПАДн отображают именно сократительную способность миокарда левого желудочка и состояние аортального клапана, т.е. характеризуют эффективность насосной (нагнетательной) функции сердца;
- кардиогемодинамический индекс - , который также характеризует эффективность сократительной (насосной) функции миокарда левого желудочка и может служить индикатором развития стеноза аортального клапана и ужесточения стенок аорты. Определяют показатели, характеризующие упруго-эластические свойства стенок сосудов артериального русла:
- индекс жесткости стенок аорты - , если ΔАДОС больше нуля;
- индекс тонуса артериальных стенок - ,
где ΔАДДуск - ускоренный дикротический прирост АД крови в начальный период диастолы.
В качестве примера в Таблице 1 приведены результаты, полученные с помощью заявляемого метода и характеризующие влияние ортостатической нагрузки на сердечный ритм, кардиогемодинамику и упруго-эластические свойства сосудов артериального русла практически здоровых молодого (обследуемый - I, 23 г.) и пожилого (обследуемый - II, 69 л.) мужчин. Из полученных результатов видно, что ортостатическая нагрузка влияет на функциональное состояние ССС и молодого, и пожилого мужчины и характер этого влияния изменяется с возрастом. Нагрузка приводит к возрастанию частоты сердечных сокращений у обоих обследуемых, но у молодого человека это увеличение выражено сильнее и сопровождается повышением вариабельности ритма (существенно снижается амплитуда моды длительности NN интервалов на гистограмме). У обоих обследуемых при сохранении средней скорости анакротического прироста АД в фазе ускоренного изгнания крови из левого желудочка заметно возрастает максимальная скорость прироста АД. При этом выявляется разная направленность изменений кардиогемодинамического индекса (КГДИ) у обследуемых: у I-го (КГДИ уменьшился от 1,51 до 1,08) при сохранении величины нормализованного ПАД ортостатическая нагрузка привела к перераспределению относительного вклада ускоренного и замедленного анакротических приростов АД за счет снижения доли ΔАДАуск (от 28 до 24 мм рт.ст.); у II-го обследуемого (КГДИ увеличился от 0,47 до 0,69) в условиях такой нагрузки необходимый уровень ПАДн был сохранен путем возрастания относительного вклада ΔАДАуск (от 15 до 19 мм рт.ст.). На основании этих единичных, приведенных в качестве примера данных, можно высказать предположение о том, что отмеченные возрастные особенности изменения показателей кардиогемодинамики функционально сопряжены с изменениями упруго-эластических свойств стенок сосудов артериального русла у обследуемых. У молодого человека стенки и аорты, и артерий эластичны (величина ИЖАО меньше нуля) и адекватное кровообращение при нагрузке обеспечивается повышением тонуса стенок артерий (величина ИТАр возрастает с 0,308 до 0,743). У пожилого человека с жесткими стенками сосудов адекватное кровообращение в условиях ортостатической нагрузки обеспечивается снижением сосудистого тонуса (величина ИТАр снижается с 0,632 до 0,497). Приведенный пример иллюстрирует преимущества применения заявляемого метода, по сравнению, например, с широко используемым в кардиологической практике методом ЭКГ, возможности которого ограничены получением информации лишь о временных характеристиках сердечного ритма.
Используя алгоритм преобразований Фурье, проводят спектральный анализ кривой ДСФГ как по вариабельности сердечного ритма (по изменчивости длительности NN интервалов - TNN), так и по вариабельности показателей, характеризующих кардиогемодинамику и тонус артериальных сосудов: ПАДн, VmaxАДА, ΔАДДуск и др., в зависимости от задачи исследования. В качестве примера на фиг.7 и 8 представлены графики спектров мощности колебаний ряда показателей обследуемого - I (смотрите выше и в Таблице 2), полученные при изучении влияния ортостатической нагрузки на организм в положении лежа (фон, фиг.7) и стоя (нагрузка, фиг.8). Определяли суммарную (ТР, 0.003÷0.4 Гц) и дифференцированную по стандартным частотным диапазонам (HF, 0.15÷0.4 Гц; LF, 0.04+0.15 Гц; VLF, 0.015÷0.04 Гц; ULF, 0.003÷0.015 Гц) спектральную мощность колебаний выбранных показателей. В Таблице 2 приведены результаты спектрального анализа вариабельности сердечного ритма (по величине TNN) и нормализованного пульсового артериального давления (ПАДн) у молодого (I) и пожилого (II) обследуемых. Видно, что в условиях ортостатической нагрузки на организм возрастает вклад симпатического звена ВНС в регуляцию сердечного ритма относительно парасимпатического влияния, и у молодого человека это перераспределение выражено в значительно большей степени, по сравнению с пожилым мужчиной (индекс симпатовагального баланса- SVI у первого возрастает от 1,5 до 8,8, а у второго от 2,6 только до 3,9). Менее значительны по величине и обратны по знаку выявленные изменения симпатовагального баланса вегетативной регуляции ПАДн у этих же обследуемых. Ортостатическая нагрузка не оказала существенного влияния на суммарную спектральную мощность (ТР) вариабельности ПАДн молодого человека, но более чем в 2 раза увеличила ТР у пожилого человека (от 10,3 до 24,0 [мм рт.ст.]2). При этом можно видеть, что у обоих обследуемых в условиях ортостатической нагрузки происходит значительное перераспределение относительного участия регуляторных систем в поддержании необходимого уровня гемодинамики. Относительно медленная гуморально-метаболическая регуляция, выявляемая в положении лежа в основном в диапазоне ULF (70% и 65% от величин ТР у I и II обследуемого, соответственно) уступает место более быстрой нейрогенной регуляции (в диапазоне LF, например, спектральная мощность колебаний величины ПАДн у обследуемого - I возрастает от 11% до 41%).
Таким образом, заявляемый способ расширяет диапазон изучения характера вегетативной и гуморально-метаболической регуляции ССС человека, открывая возможности исследования физиологических механизмов регуляции кровообращения, в основе которых лежит контроль не только сердечного ритма, но и параметров гемодинамики, сопряженных с пульсовыми изменениями АД крови. Сопоставление результатов спектрального анализа вариабельности разных показателей позволяет получить качественно новую информацию о роли и относительном вкладе симпатического и парасимпатического отделов вегетативной (автономной) нервной системы, а также других регуляторных систем гомеостаза в регуляцию как сердечного ритма, так и функциональных характеристик миокарда и гладкомышечных структур стенок сосудов артериального русла, совместно определяющих динамику пульсового изменения АД для обеспечения физиологически адекватного кровообращения.
По результатам статистического и спектрального анализов вариабельности измеренных показателей (выбранных в зависимости от задачи исследования) оценивают функциональное состояние и характер вегетативной регуляции ССС обследуемого путем сравнения измеренных величин показателей со среднестатистическими числовыми значениями этих же показателей, установленными для ССС определенных по возрасту, полу, состоянию здоровья (анамнезу) и условиям внешней среды групп людей, выбранных в качестве контроля. На основе применения специальных методов статистического анализа (дискриминантного, дисперсионного или факторного) эти результаты могут быть использованы для решения вопросов дифференциальной диагностики состояния ССС пациентов.
Таким образом, использование пьезокерамического датчика в сочетании с применением компьютерной регистрации и анализа ДСФГ позволило разработать простой по выполнению автоматизированный способ точного количественного экспресс-анализа широкого спектра уже известных и ряда новых показателей, совокупно характеризующих функциональное состояние ССС и особенности ее регуляции со стороны ВНС.
На основе разработанного способа может быть создан образец артериального пьезопульсометра, который в виде автономной компактной и недорогой приставки к компьютеру или в виде составной компоненты универсальной многофункциональной системы кардиоскрининга может обеспечить потребность в оснащении этими приборами отечественных поликлиник, диагностических и спортивно-оздоровительных центров, специализированных санчастей и аналогичных по профилю медицинских учреждений. Простота обслуживания автономного варианта пульсометрической приставки к персональному компьютеру позволяет использовать это устройство как для регулярного индивидуального обследования пациентов, так и для крупномасштабного наблюдения за состоянием ССС у различных групп населения (например, учащихся, военнослужащих, работников предприятий повышенного риска, контингента, работающего в отдаленных точках, и т.д.). Предлагаемый способ делает возможным проведение оперативного контроля состояния ССС человека при стрессорных воздействиях, в условиях неблагоприятной экологической обстановки, а также мониторинг состояния ССС у представителей профессий, связанных с непрерывной и напряженной работой, - авиадиспетчеров, пилотов, космонавтов и др.
| Таблица 1 | ||||
| Влияние ортостатической нагрузки на показатели, характеризующие функциональное состояние сердечно-сосудистой системы молодого и пожилого человека. | ||||
| Показатели | Обследуемый - I (23 г.) | Обследуемый - II (69 л.) | ||
| Лежа | Стоя | Лежа | Стоя | |
| Сердечный ритм: | ||||
| Частота сердечн. сокращений (ЧСС), уд/мин | 56 | 80 | 57 | 61 |
| Средн. длит-сть NN-интервалов (TNN), мс | 1070 | 750 | 1060 | 980 |
| Станд. отклон-е NN интервалов (SDNN), мс | 51 | 59 | 26 | 21 |
| Мода NN интервалов (MoNN), мс | 1080 | 765 | 1045 | 970 |
| Амплитуда моды NN-интерв-ов (AMoNN), % | 44,1 | 28,0 | 67,5 | 51,5 |
| Доля отлич-хся соседн. интерв-ов (pNNSO), % | 30,8 | 8,9 | 0 | 0 |
| Кардиогемодинамика: | ||||
| Нормализованное ПАД (ПАДн), мм рт.ст. | 47 | 47 | 45 | 46 |
| Станд. отклон-е ПАДн (SDПАДн), мм рт.ст | 5,5 | 4,6 | 5,2 | 7,5 |
| Ускор. анакрот. прирост АД (ΔАДАуск), мм рт.ст. | 28 | 24 | 15 | 19 |
| Средн. скор. прироста АДА (VАДАуск), мм рт.ст./с | 335 | 352 | 210 | 214 |
| Макс.скор. прироста ПАД (VmaxАДА), мм рт.ст./с | 703 | 801 | 437 | 519 |
| Кардиогемодинамический индекс (КГДИ) | 1,51 | 1,08 | 0,47 | 0,69 |
| Упруго-эластические свойства сосудов: | ||||
| Индекс жесткости аорты (ИЖАо), % | - | - | 38,5 | 23,2 |
| Индекс тонуса артериальных стенок (ИТАр) | 0,308 | 0,743 | 0,632 | 0,497 |
| Таблица 2 | ||||
| Влияние ортостатической нагрузки на показатели спектрального анализа, характеризующие особенности вегетативной регуляции сердечно-сосудистой системы молодого и пожилого человека. | ||||
| Показатели спектрального анализа вариабельности | Обследуемый - I (23 г.) | Обследуемый - II (69 л.) | ||
| лежа | стоя | лежа | стоя | |
| а) сердечного ритма: | ||||
| Суммарная спектральная мощность (ТР), мс2 | 4000 | 6681 | 1297 | 885 |
| Спектр. мощность высоких частот (HF), мс2 | 1255 | 407 | 100 | 77 |
| Спектр. мощность высоких частот (HF), % | 31 | 6 | 8 | 9 |
| Спектр. мощность низких частот (LF), мс2 | 1845 | 3576 | 258 | 296 |
| Спектр. мощность низких частот (LF), % | 46 | 54 | 20 | 33 |
| Спектр. мощн-ть сверхнизких частот (VLF), мс2 | 391 | 1738 | 456 | 203 |
| Спектр. мощн-ть сверхнизких частот (VLF), % | 10 | 26 | 35 | 23 |
| Спектр. мощн-ть ультранизких частот (ULF), мс2 | 510 | 960 | 483 | 309 |
| Спектр.мощн-ть ультранизких частот (ULF), % | 13 | 14 | 37 | 35 |
| Симпатовагальный индекс (SVI) | 1,5 | 8,8 | 2,6 | 3,9 |
| б) величины ПАДн: | ||||
| Суммарн. спектр, мощность (ТР), [мм Hg]2 | 29,6 | 31,9 | 10,3 | 24,0 |
| Спектр. мощн-сть высоких частот (HF), [мм Hg]2 | 2,9 | 8,5 | 1,1 | 8,0 |
| Спектр. мощность высоких частот (HF), % | 9,9 | 27 | 11 | 33 |
| Спектр. мощ-сть низких частот (LF), [мм Hg]2 | 3,2 | 13,1 | 1,8 | 9,9 |
| Спектр. мощность низких частот |