Способ лечения и профилактики глазных болезней, связанных с ишемией тканей глаза
Иллюстрации
Показать всеИзобретение относится к медицине, в частности к офтальмологии, и касается лечения и профилактики глазных болезней, связанных с ишемией тканей глаза. Для этого при индуцированной патологии, сопровождающейся ишемией тканей глаза, в качестве лекарственных средств вводят ингибиторы ангиотензин-превращающего фермента в виде инстилляций или местных инъекций. Способ обеспечивает ускорение васкуляризации и сокращение площади зоны ишемии. 4 ил.
Реферат
Изобретение относится к области медицины и ветеринарии и может быть использовано для лечения и профилактики патологий глаза, связанных с ишемией тканей глаза.
Ишемия - наиболее частый патологический процесс, сопровождающий или вызывающий глазную патологию. Ишемия тканей глаза является важным патогенетическим звеном таких заболеваний как диабетическая ретинопатия, травматические повреждения глаза, дистрофические заболевания сетчатки, атрофия зрительного нерва сосудистого генеза, ишемическая нейропатия, нарушение кровообращения в ветвях центральной артерии сетчатки. Все эти заболевания обусловлены в основном местным нарушением кровообращения. Ликвидация ишемии достигается за счет расширения сосудов, развития коллатерального кровообращения, неоваскуляризации, раскрытия резервных капилляров [1, 2].
В настоящее время в мировой практике для лечения подобных состояний применяют сосудорасширяющие препараты, фибринолитики, антикоагулянты, ангиопротекторы, биогенные стимуляторы, витамины, иммуномодуляторы, антиоксиданты [3-11].
Лечение вышеперечисленными препаратами не всегда бывает достаточно успешным, что обеспечивает актуальность проблемы по расширению арсенала лекарственных средств для лечения глазных болезней, связанных с ишемическими состояниями.
В качестве прототипа предлагаемого способа выбран способ лечения глазных заболеваний, связанных с ишемией тканей глаза, включающий местное введение 1% раствора эмоксипина, обладающего ангиопротекторной и антигипоксической активностью. В офтальмологии при лечении больных с травматическими повреждениями глаза и при патологии сетчатки, включая заднюю ишемическую нейропатию и диабетическую ретинопатию, действие эмоксипина направлено на улучшение микроциркуляции, что приводит к снятию отека и оживлению обменных процессов [3, 12].
Задачей изобретения является как разработка нового средства, позволяющего эффективно лечить круг патологий, связанных с ишемией тканей глаза, так и поиск более эффективного препарата.
Поставленная задача решается тем, что в известном способе лечения и профилактики глазных болезней, связанных с ишемией тканей глаза, путем местного введения лекарственных средств в качестве лекарственных средств используют ингибиторы ангиотензин-превращающего фермента, которые вводят местно путем инстилляций или местных инъекций.
Одним из патогенетических звеньев, объединяющих заболевания, связанные с ишемией тканей, является нарушение баланса компонентов общей и локальной (в глазу) ренин-ангиотензиновых систем (РАС). Ренин-ангиотензиновая система является одной из важнейших регуляторных систем организма. Центральным регулирующим звеном РАС является ангиотензин-превращающий фермент (АПФ). АПФ - это цинкзависимая пептидаза, катализирующая гидролитическое отщепление дипептидов с карбоксильного конца ряда физиологически активных олигопептидных субстратов, в частности ангиотензина I и брадикинина. В результате ограниченного протеолиза, осуществляемого АПФ, ангиотензин I превращается в мощный вазоконстриктор ангиотензин II, вызывающий спазм сосудов, а вазодилятор брадикинин, вызывающий расширение сосудов, напротив, инактивируется. Ингибиторы АПФ блокируют активность АПФ и препятствуют тем самым образованию ангиотензина II и деструкции брадикинина. В результате действия ингибиторов понижается кровяное давление и увеличивается приток крови и кислорода к сердцу. В настоящее время ингибиторы АПФ широко применяются только перорально или внутривенно для лечения гипертонии и сердечно-сосудистой недостаточности [3], хотя есть сведения о положительном эффекте при пероральном введении ингибиторов АПФ при атеросклерозе [13], при инсулин-зависимом сахарном диабете [14], при старческой дегенерации сетчатки [15] и диабетической ретинопатии [16].
Локальная РАС глаза может играть значительную роль в патогенезе различных заболеваний глаза, что является основанием местного применения ингибиторов АПФ для лечения широкого круга глазных заболеваний [17, 18]. В офтальмологии возможное местное применение ингибиторов АПФ предложено только для снижения внутриглазного давления при глаукоме [19] и лечения язв роговицы [20].
Однако авторы не обнаружили работ по местному применению ингибиторов АПФ для лечения глазных болезней, связанных с ишемией тканей глаза.
Авторами установлено, что у экспериментальных животных в слезной жидкости, метаболизм которой отражает характер течения биохимических процессов в глазу, при ишемии тканей глаза, в том числе при диабете и травматическом повреждении глаза, возрастает активность АПФ. Установлена корреляция между активностью АПФ в слезе и выраженностью клинических проявлений патологического процесса, связанного с ишемией тканей глаза. Этот факт послужил предпосылкой для местного применения ингибиторов АПФ для лечения и профилактики глазных болезней, связанных с ишемией тканей глаза.
Сущность изобретения заключается в применении ингибиторов АПФ в качестве лекарственного средства при лечении глазных болезней, связанных с ишемией тканей глаза. Терапевтически эффективное количество ингибитора АПФ вводится местно в виде глазных капель или местных инъекций. В некоторых случаях может быть показано сочетание перорального и местного применения. Предложенный метод может быть использован при лечении таких заболеваний как травматические повреждения глаза (механические, химические, термические, радиационные, вызванные воздействием лазера), диабетическая ретинопатия, дистрофические заболевания сетчатки, атрофия зрительного нерва сосудистого генеза, ишемическая нейропатия, нарушение кровообращения в ветвях центральной артерии сетчатки.
Для лечения указанных патологий могут применяться различные ингибиторы АПФ, такие как каптоприл, лизиноприл, эналаприлат, трандолаприлат, фозиноприлат и т.д.
Согласно представленному изобретению ингибиторы АПФ могут применяться местно у млекопитающих, таких как люди, домашние животные, домашний скот и т.д.
Для применения способа в представленном изобретении местные композиции являются предпочтительными и могут содержать ингибиторы АПФ в концентрации от 10 мкМ до 0,1 М, которые вводятся в глаз от 2-х раз в неделю до 4-х раз в день. В некоторых случаях может быть рекомендовано сочетание перорального и местного применения. Конкретные дозы и режим введения подбираются в зависимости от заболевания и его тяжести.
Местные препараты могут содержать в качестве среды известные офтальмологические носители, включая воду, содержащую буферный агент, изотонические смеси, антибактериальные компоненты, антиоксиданты, консерванты, пролонгаторы, загустители, гели.
Были проведены исследования на экспериментальных животных с ожоговой травмой глаза различной локализации, сопровождающейся ишемией тканей глаза, а также на животных с экспериментальным диабетом, при развитии которого в тканях глаза отмечается наличие ангиопатий, нарушения микроциркуляции в конъюнктиве, образование неперфузированных капиллярных зон (зон ишемии) [1, 2].
Сочетанный ожог конъюнктивы, роговицы и части лимба (сосудистая и бессосудистая ткань) и ожог конъюнктивы (только сосудистая ткань) под наркозом и местной анестезией моделировали с помощью круга из хлопчатобумажной ткани (диаметр 7 мм), пропитанной 10% NaOH. Было задействовано 50 кроликов (100 глаз). 20 кроликов получали инстилляции раствора лизиноприла в концентрации 10 мкМ - 0,1 М 4 раза в день в течение 14-28 дней, 20 кроликов получали инстилляции раствора каптоприла в концентрации 10 мкМ - 0,1 М 4 раза в день в течение 14-28 дней, 10 кроликов получали инстилляции 0,05 М фосфатного буфера, рН 7,5, содержащего 0,15 М NaCl, 4 раза в день в течение 14-28 дней.
У 30 кроликов моделировали диабет путем внутривенного введения 5% раствора аллоксана в дозе 130-150 мг аллоксана на 1 кг массы. В течение 3-х месяцев 10 кроликов получали инстилляции эналаприлата в концентрации 10 мкМ - 0,1 М 2 раза в день, 10 кроликов в течение 3-х месяцев получали субконъюнктивальные инъекции эналаприлата в концентрации 10 мкМ - 0,1 М 2 раза в неделю, 5 кроликов получали инстилляции 0,05 М фосфатного буфера, рН 7,5, содержащего 0,15 М NaCl, 2 раза в день, 5 кроликов получали субконъюнктивальные инъекции 0,05 М фосфатного буфера, рН 7,5, содержащего 0,15 М NaCl, 2 раза в неделю.
У обожженных кроликов без лечения и в различные сроки лечения ингибиторами АПФ определяли уровень активности АПФ в слезной жидкости и оценивали клиническую картину течения болезни (динамика уменьшения площади зоны ишемии, степень отека и инфильтрации ткани, рост сосудов, степень изъязвления). У кроликов с аллоксановым диабетом следили за уровнем активности АПФ в слезной жидкости, а также проводили биомикроскопию, фоторегистрацию сосудов лимба, офтальмоскопию и калиброметрию сосудов.
В первой серии экспериментов сравнивали клинический характер течения болезни после ожоговой травмы глаза и активность АПФ у кроликов, получавших инстилляции раствора ингибитора АПФ с первого дня после ожога, и у кроликов, которым закапывали растворитель, - фосфатный буфер. Оказалось, что у кроликов, получивших лечение, во все периоды наблюдения активность АПФ в слезной жидкости была значительно ниже (в 3-4 раза), чем у животных, получавших буфер. Сравнение клинической картины течения ожоговой болезни показало, что между группами, получавшими и не получавшими лечение ингибиторами АПФ, имеются достоверные различия.
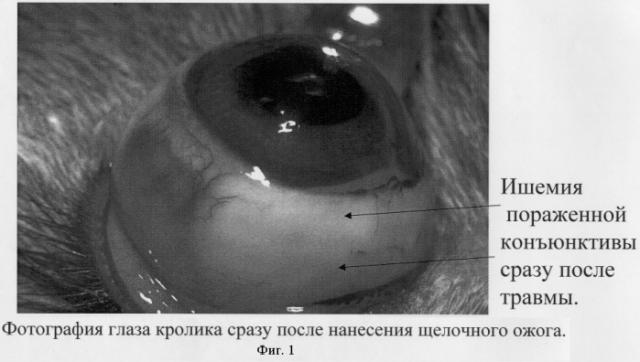
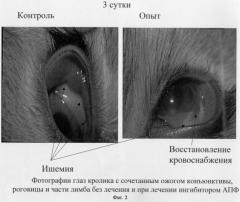
Сразу после ожога в глазах обеих групп кроликов образовывалась зона ишемии, ишемизированная ткань имела бледно-розовый - белый цвет. Площадь зоны ишемии оценивали планиметрически, во всех случаях площадь зоны ишемии превышала площадь исходного ожогового поражения ткани. При биомикроскопии в ишемизированных тканях не просматривались сосуды (фиг.1). На фиг.2 представлены фотографии глаз кролика с сочетанным ожогом конъюнктивы, роговицы и части лимба после травмы без лечения и при лечении ингибитором АПФ. Видно, что уже на 3-й день после травмы у кролика, получавшего лечение ингибитором АПФ, начинается прорастание сосудов в ишемизированную зону. Наблюдение за группами кроликов, получавшими и не получавшими лечение ингибиторами АПФ, в динамике показало, что уменьшение площади зоны ишемии при лечении происходило значительно быстрее (фиг.3А) и полностью завершалось к 20 суткам после ожоговой травмы, в то время как у нелеченных животных на 31 сутки еще сохранялись единичные дефекты. Васкуляризация зоны лимба и роговицы на фоне лечения ингибиторами АПФ проходила быстрее (фиг.3Б) и достигала максимума на 20 сутки, после чего начиналось запустевание сосудов в роговице. В отсутствие лечения интенсивность васкуляризации на 20 сутки была в 2 раза меньше и сохранялась на том же уровне до 31 суток, т.е. запустевания сосудов не происходило. Динамика распространения отека за пределы участка поражения также была различной в двух группах (фиг.3В). В группе, получавшей лечение ингибиторами АПФ, зона отека резко сокращалась к 11 суткам, а начиная с 20 суток отек отсутствовал. В группе нелеченных животных зона отека уменьшалась постепенно, начиная с 15 суток, небольшой отек сохранялся и на 31 сутки.
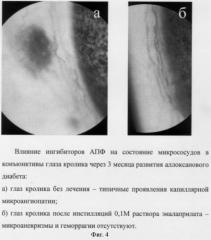
Во второй серии экспериментов изучено влияние ингибиторов АПФ на состояние микрососудов глаза кролика через 3 месяца развития диабета, индуцированного аллоксаном. Активность АПФ в слезной жидкости у кроликов, не получавших лечение, через 40 дней после развития диабета увеличивалась вдвое, в то время как у кроликов, леченных ингибиторами АПФ, активность фермента практически оставалась в норме на протяжении всего времени проведения эксперимента (3 месяца). При офтальмологическом исследовании кроликов через 40 дней после развития диабета в сетчатке не выявлено кровоизлияний, микроаневризм, появления извитых сосудов сетчатки, что совпадает с данными литературы [21]. У 30% животных определено небольшое расширение центральной вены сетчатки в ответ на локальную ишемию и сужение просвета центральной артерии сетчатки. В то же время при биомикроскопии лимбальной зоны конъюнктивы зафиксированы типичные проявления капиллярной микроангиопатии у всех животных с диабетом без лечения (фиг.4): выраженная сеть расширенных перилимбальных сосудов, наличие неперфузируемых капиллярных зон (зон ишемии), венулы неравномерного калибра с единичными микроаневризмами, микро- и макрогеморрагии, что является признаком прогрессирующего поражения капилляров, связанным с исчезновением интрамуральных перицитов, в основном в венозном отделе капиллярной сети. Все эти проявления капиллярной ангиопатии, свойственные диабету, являются причиной развития ишемии тканей [22], в данном случае ткани конъюнктивы.
В группе животных, получавших местное лечение раствором ингибитора АПФ, степень расширения перилимбальных сосудов была менее выраженной, в лимбальной зоне отсутствовали микроаневризмы и геморрагии, неперфузируемые капиллярные зоны не обнаруживались (фиг.4). Изменений в состоянии центральной вены сетчатки и центральной артерии сетчатки не отмечено.
В результате проведенного исследования показано, что лечение местными инстилляциями или местными инъекциями ингибиторов АПФ позволило при ожоговой травме глаза сократить сроки заживления и улучшить исходы за счет снижения площади ишемии конъюнктивы уже в первые дни после травмы, а на ранних стадиях экспериментального диабета снизить выраженность проявлений микроангиопатии конъюнктивы и тем самым уменьшить ишемию этой ткани.
Изобретение поясняется следующими примерами:
Пример 1. Кролику на оба глаза был нанесен сочетанный ожог конъюнктивы, роговицы и части лимба вышеописанным методом. После нанесения ожога с первых суток кролик получал инстилляции 0,05 М фосфатного буфера, рН 7,5, содержащего 0,15 М NaCl, по 2 капли в каждый глаз 4 раза в день в течение 14 дней. Сразу после нанесения ожога на месте повреждения образовывалась область белого цвета. Площадь ишемизированной зоны была вдвое больше площади ожога, при биомикроскопии не просматривались сосуды. Активность АПФ в слезной жидкости после ожога увеличивалась и достигала максимума на 14 сутки, затем сохранялась на повышенном уровне вплоть до 28 суток. Инфильтрация роговицы сохранялась на третьей неделе наблюдения. У кролика на 14 день после ожога образовалась глубокая язва роговицы до десцеметовой оболочки. К 28 суткам образовалась грубая рубцовая ткань, половина площади роговицы полностью непрозрачна. Отек прилегающих к ожогу тканей сохранялся до 28 суток. Зона ишемии конъюнктивы начала медленно уменьшаться после 14 суток, но небольшой участок ишемизированной ткани сохранялся вплоть до 30 суток.
Пример 2. Кролику на оба глаза был нанесен сочетанный ожог конъюнктивы, роговицы и части лимба вышеописанным методом. После нанесения ожога с первых суток кролик получал инстилляции раствора лизиноприла в концентрации 1 мМ по 2 капли в каждый глаз 4 раза в день в течение 14 дней. Сразу после нанесения ожога на месте повреждения образовывалась область белого цвета вдвое больше площади ожога, в которой не просматривались сосуды. Активность АПФ в слезной жидкости после нанесения ожога увеличивалась в 1-е сутки, затем постепенно снижалась и достигала нормы к 7 суткам. Инфильтрация роговицы слабой интенсивности (рисунок радужки просматривается) выявлена в первые две недели эксперимента. На 14 день после ожога отмечалась небольшая язва поверхностных слоев стромы роговицы, которая зарубцевалась к 21 суткам. К этому сроку практически исчез отек роговицы и конъюнктивы, роговица полностью прозрачна. Зона ишемии конъюнктивы начала уменьшаться, начиная с 5 суток, и к 21 суткам полностью исчезла. Сокращение зоны ишемии происходило за счет прорастания сосудов из конъюнктивы, окружающей область ишемии.
Пример 3. Кролику на оба глаза был нанесен ожог конъюнктивы вышеописанным методом. После нанесения ожога с первых суток кролик получал инстилляции 0,05 М фосфатного буфера, рН 7,5, содержащего 0,15 М NaCl, по 2 капли в каждый глаз 4 раза в день в течение 28 дней. Сразу после ожога, помимо травмированной области, вокруг нее образовалась светлая область полулунной формы шириной до 3 мм, в которой отсутствовало кровоснабжение. Уровень активности АПФ в слезе увеличивался сразу после ожога в 3 раза и оставался повышенным вплоть до 21 суток. Площадь ишемии обожженной области конъюнктивы и интенсивность отека необожженной области конъюнктивы начали медленно уменьшаться на 14 сутки. К 30 суткам все еще сохранялись ишемизированные участки, в которых ткань конъюнктивы была некротизирована.
Пример 4. Кролику на оба глаза был нанесен ожог конъюнктивы вышеописанным методом. После нанесения ожога с первых суток кролик получал инстилляции раствора каптоприла в концентрации 10 мкМ по 2 капли в каждый глаз 4 раза в день в течение 28 дней. Сразу после ожога, помимо травмированной области, вокруг нее образовалась светлая область полулунной формы шириной до 3 мм, в которой отсутствовало кровоснабжение. Активность АПФ в слезной жидкости после нанесения ожога увеличивалась в 1-е сутки в 3,5 раза. Затем постепенно снижалась и достигала нормы к 21 суткам. Область ишемии обожженной конъюнктивы и отек необожженной области начали уменьшаться на 5 сутки. К 21 суткам зона ишемии исчезла, микроциркуляция в конъюнктиве полностью восстановилась, а отек спал.
Пример 5. Кролику моделировали диабет вышеописанным методом. С первых суток кролик получал субконъюнктивальные инъекции 0,05 М фосфатного буфера, рН 7,5, содержащего 0,15 М NaCl, no 0,3 мл в каждый глаз 2 раза в неделю в течение 3-х месяцев. Через 3 месяца при биомикроскопии лимбальной зоны конъюнктивы зафиксированы типичные проявления капиллярной микроангиопатии: выраженная сеть расширенных перилимбальных сосудов, наличие неперфузируемых капиллярных зон (зона ишемии), венулы неравномерного калибра с единичными микроаневризмами, микро- и макрогеморрагии. Активность АПФ в слезной жидкости увеличилась вдвое через 40 дней от начала эксперимента и оставалась повышенной вплоть до прекращения эксперимента.
Пример 6. Кролику моделировали диабет вышеописанным методом. С первых суток кролик получал субконъюнктивальные инъекции раствора эналаприлата в концентрации 10 мкМ по 0,3 мл в каждый глаз 2 раза в неделю в течение 3-х месяцев. Через 3 месяца в лимбальной зоне отсутствовали микроаневризмы и геморрагии, степень расширения перилимбальных сосудов была слабо выраженной, неперфузируемые капиллярные зоны не определялись, активность АПФ в слезной жидкости практически оставалась на уровне нормы в течение всего эксперимента.
Представленные данные указывают на эффективность местного применения ингибиторов АПФ для улучшения микроциркуляции при ишемических состояниях, стимулирования восстановления собственных тканей, снижения проявлений воспаления, улучшения исходов и ускорения течения репаративных процессов после травмы.
Учитывая, что физиологические особенности глаза кролика и человека идентичны, данный метод можно рекомендовать к использованию в клинике.
Учитывая высокую степень стабильности ингибиторов АПФ, их лекарственная форма в виде глазных капель может быть использована для применения в полевых условиях (горячих точках) для оказания экстренной эффективной помощи пострадавшим от различного вида воздействий, повреждающих глаза.
ЛИТЕРАТУРА
1. Т.О.Елисеева, Н.А.Бишеле. Применение вазоактивных препаратов для лечения ишемических заболеваний зрительного нерва и сетчатки. Русский мед. журнал, 2000, 8, 16-20.
2. Т.О.Елисеева, А.В.Свирин. Методы лечения ишемических состояний зрительного нерва и сетчатки. Клиническая офтальмология, 2002, 3, 106-112.
3. М.Д.Машковский. Лекарственные средства. ООН «Новая Волна», М., 2002, т.1, 420-425.
4. S.C.Brodovsky, C.A.McCarty, G.Snibson et al. Management of alkali burns. Ophtalmology (2000), 107, 1829-1835.
5. Патент RU 2145229 С1 (1997).
6. Патент RU 2073523 С1 (1977).
7. В.И.Морозов, А.А.Яковлев. Фармакотерапия глазных болезней: справочник. Москва, 2001, 336 с.
8. Patent ЕР 1297849 A1 (2001).
9. Patent US 4795423 (1989).
10. Patent US 5431907 (1995).
11. Patent US 2003|0027801 A1.
12. E.A.Егоров, Ю.С.Астахов, Т.В.Ставицкая. Офтальмофармакология. Руководство для врачей. М., «ГЭОТАР-МЕД», 2004, 413.
13. Jacobsson L., Persson K., Aberg G., Anderson R., Karlberg В., Olsson A.J. Antiatherosclerotic effects of the angiotensin-converting enzyme inhibitors captopril and fosinopril in hypercholesterolemic minipigs. Cardiovasc. Pharmacol. (1994), 24, 670-677.
14. L.H.Opie. Angiotensin-converting enzymes inhibitors: the advance continius. N.-Y., 1999, 275 p.
15. Patent US 4656188 (1987).
16. Chaturvedi H., Sjolie A.K., Stephenson J.M. et al. Effect of lisinopril on progression of retinopathy in normotensive people with type 1 diabetes. The EUCLID Study Group. EURODIAB Controlled Trial of Lisinopril in Insulin-Dependent Diabetes Mellitus. Lancet (1998), 351, 28-31.
17. Н.Б.Чеснокова, А.В.Григорьев, Т.А.Павленко и др. Роль компонентов ренин-ангиотензиновой системы в тканях глаза в норме и патологии. Вестник РАМН (2003), №9, 29-31.
18. О.А.Кост, Н.Б.Чеснокова, Т.П.Кузнецова. Активность ангиотензин-превращающего фермента в слезной жидкости кроликов после ожога роговицы. Вопр. Мед. Химии (1996), 42, 130-134.
19. Patent EUR. 0099239 (1984).
20. Патент РФ 2119314 (1996).
21. Баранов Б.Б. Экспериментальный диабет. Роль в клинической диабетологии. Л., «Наука», 1983.
22. И.И.Дедов, В.В.Фатеев. Введение в диабетологию. Руководство для врачей. М., «Берег», 1998, 147-148.
Способ лечения и профилактики глазных болезней, связанных с ишемией тканей глаза путем местного введения лекарственных средств, отличающийся тем, что в качестве лекарственных средств используют ингибиторы ангитензин-превращающего фермента, которые вводят инстилляцией или местными инъекциями.