Способ определения оксибензола и его монометильных производных в биологическом материале
Иллюстрации
Показать всеИзобретение относится к способу определения оксибензола и его монометильных производных в биологическом материале, заключающемуся в том, что анализируемые вещества извлекают из объекта с использованием этилацетата, вытяжки упаривают, остаток растворяют в смеси растворителей гексан-диэтиловый эфир (6:4) и хроматографируют в колонке с силикагелем, отбирая при этом фракции, содержащие оксибензол и его монометильные производные, которые после этого обрабатывают нитрующим агентом, предварительно разделив полученные нитросоединения оксибензола и его монометильных производных с помощью экстракции диэтиловым эфиром при рН 1 и рН 4, определяют их качественное и количественное содержание по содержаниям соответствующих полинитропроизводных, определенным по данным хроматограмм, полученных методом ВЭЖХ, с использованием подвижной фазы гексан-диоксан-пропанол-2 (40:5:1) для растворов, содержащих полинитропроизводные 2 метилоксибензола и 4 метилоксибензола, и с ипользованием подвижной фазы гексан-диоксан-муравьиная кислота (5:3:0,2) для растворов, содержащих полинитропроизводные оксибензола и 3 метилоксибензола. Технический результат: повышение чувствительности и селективности определения оксибензола и его монометильных производных при их совместном присутствии, сокращение продолжительности анализа. 6 табл., 2 ил.
Реферат
Изобретение относится к биологии и токсикологической химии, а именно к способам определения оксибензола и его монометильных производных в биологическом материале, и может быть использовано в практике санэпидстанций, химико-токсикологических и ветеринарных лабораторий. Способ относится к числу массовых.
Известен способ определения оксибензола в биологическом материале путем измельчения биологического объекта, подкисления раствором виннокаменной кислоты, прибавления сульфата кадмия, проведения дистилляции с использованием парообразователя, отбора дистиллята, встряхивания дистиллята с оксидом алюминия с последующей обработкой дистиллята водно-этанольным раствором 2,6-дибромхинонхлоримида в присутствии боратного буфера с рН 10,5 и фотометрированием образующегося окрашенного раствора на фоне воды. (Гадаскина И.Д., Филов В.А. Превращения и определение промышленных органических ядов в организме. Л.: Медицина, 1970. - С.38-39). Способ малоселективен, характеризуется недостаточной высокой точностью.
Известен способ определения фенола (оксибензола) и его монометильных производных (крезолов) в биологических объектах путем измельчения биологической ткани, смешивания ее с водой, подкисления органической кислотой и осуществления дистилляции с водяным паром с последующим сбором дистиллята, экстракцией анализируемых веществ из дистиллята диэтиловым эфиром, отгонкой экстрагента и определением исследуемых соединений методом броматометрического титрования (Швайкова М.Д. Токсикологическая химия. - М.: Медицина, 1975. - С.67-69, 111-114).
Способ малоселективен, отличается недостаточно высокой чувствительностью.
Наиболее близким является способ определения 4-метилоксибензола в моче, заключающийся в том, что анализируемую пробу подкисляют серной кислотой, перегоняют с водяным паром, полученный дистиллят обрабатывают 65% азотной кислотой, выдерживают при 37°С в течение 24 часов, нейтрализуют 20% раствором гидроксида натрия, прибавляют к реакционной смеси буферный раствор с рН 12 и проводят полярографическое определение (Гадаскина И.Д., Филов В.А. Превращения и определение промышленных органических ядов в организме. Л.: Медицина, 1970. - С.204).
Способ характеризуется длительностью выполнения, недостаточно высокой чувствительностью, не может обеспечить селективное определение оксибензола и его монометильных производных при их совместном присутствии.
Задачей настоящего изобретения является повышение чувствительности и селективности определения, сокращение продолжительности анализа.
Поставленная задача достигается с помощью предлагаемого способа, который заключается в том, что биологическую ткань (например, ткань печени) измельчают, двукратно по 30 минут обрабатывают этилацетатом, этилацетатные извлечения объединяют, обезвоживают, этилацетат испаряют при 16-20°С, остаток растворяют в смеси растворителей гексан-диэтиловый эфир (8:2), хроматографируют в колонке с силикагелем с использованием подвижной фазы гексан-диэтиловый эфир (8:2), фракции элюата, содержащие оксибензол и его монометильные производные, объединяют, обезвоживают, элюент испаряют, остаток обрабатывают смесью азотной (65%-ной) и серной (94%-ной) кислот при кипячении на водяной бане, реакционную смесь разбавляют водой, подщелачивают до рН 4, экстрагируют диэтиловым эфиром, подкисляют до рН 1 и повторно экстрагируют диэтиловым эфиром, экстракт из раствора с рН 4 упаривают до сухого остатка, остаток растворяют в системе растворителей гексан-диоксан-пропанол-2 (40:5:1) и хроматографируют методом ВЭЖХ в колонке с сорбентом "Силасорб-600", используя подвижную фазу гексан-диоксан-пропанол-2 (40:5:1), экстракт из раствора с рН 1 упаривают до сухого остатка, остаток растворяют в системе растворителей гексан-диоксан-муравьиная кислота (5:3:0,2) и хроматографируют методом ВЭЖХ в колонке с сорбентом "Силасорб-600", используя подвижную фазу гексан-диоксан-муравьиная кислота (5:3:0,2).
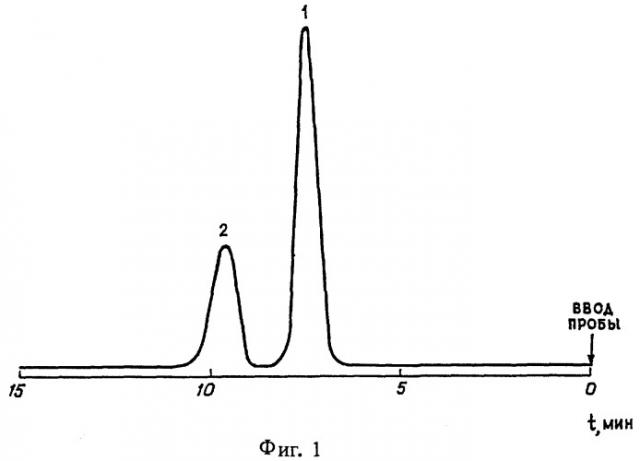
Изобретение поясняется чертежами. На фигуре 1 представлена хроматограмма смеси полинитропроизводных 2-метилоксибензола и 4-метилоксибензола (соответственно 2-метил-4,6-динитрооксибензола и 4-метил-2,6-динитрооксибензола). На фигуре 2 представлена хроматограмма смеси полинитропроизводных оксибензола и 3-метилоксибензола (соответственно 2,4,6-тринитрооксибензола и 3-метил-2,4,6-тринитрооксибензола).
Способ осуществляется следующим образом: биологическую ткань, содержащую смесь оксибензола и его монометильных производных, измельчают, дважды настаивают с этилацетатом при перемешивании (каждый раз в течение 30 минут), извлечение отделяют от твердых частиц биоматериала, объединяют, обезвоживают безводным сульфатом натрия, экстрагент испаряют в токе воздуха при 16-20°С, остаток растворяют в смеси растворителей гексан-диэтиловый эфир (8:2), хроматографируют в колонке с силикагелем с использованием подвижной фазы гексан-диэтиловый эфир (8:2), фракции элюата, содержащие оксибензол и его монометильные производные, объединяют, обезвоживают безводным сульфатом натрия, элюент испаряют, остаток обрабатывают смесью азотной (65%-ной) и серной (94%-ной) кислот, взятых в соотношении 1:1 по объему, при кипячении на водяной бане, реакционную смесь разбавляют водой, подщелачивают до рН 4, экстрагируют диэтиловым эфиром, водный слой подкисляют до рН 1 и повторно экстрагируют диэтиловым эфиром, экстракт из раствора с рН 4 упаривают до сухого остатка, остаток растворяют в системе растворителей гексан-диоксан-пропанол-2 (40:5:1) и хроматографируют методом ВЭЖХ в колонке с сорбентом "Силасорб-600", используя подвижную фазу гексан-диоксан-пропанол-2 (40:5:1), экстракт из раствора с рН 1 упаривают до сухого остатка, остаток растворяют в системе растворителей гексан-диоксан-муравьиная кислота (5:3:0,2) и хроматографируют методом ВЭЖХ в колонке с сорбентом "Силасорб-600", используя подвижную фазу гексан-диоксан-муравьиная кислота (5:3:0,2). Способ иллюстрируется следующими примерами.
Пример 1
Качественное определение оксибензола и его монометильных производных в ткани печени
К 10 г мелкоизмельченной ткани свежей трупной печени человека прибавляют смесь оксибензола, 2-метилоксибензола, 3-метилоксибензола и 4-метилоксибензола по 5 мг каждого из веществ, тщательно перемешивают биологическую ткань с веществами и оставляют на сутки при температуре 16-20°С. По истечении указанного времени смесь заливают 20 мл этилацетата и выдерживают 30 минут, периодически перемешивая. Извлечение отделяют, операцию настаивания повторяют в указанных условиях. Вытяжки объединяют, экстрагент испаряют в токе воздуха при температуре 16-20°С, остаток растворяют в 10 мл смеси растворителей гексан-диэтиловый эфир (8:2). 2 мл полученного раствора вносят в колонку размером 490×11 мм, заполненную 10 г силикагеля типа L 40/100 μ. Хроматографируют, используя подвижную фазу гексан-диэтиловый эфир (8:2). Элюат собирают отдельными фракциями по 2 мл каждая. Фракции с 5 по 13 включительно объединяют, элюент испаряют в токе воздуха над 1 г безводного сульфата натрия при температуре 16-20°С. К остатку прибавляют 4 мл воды, остаток обрабатывают смесью азотной (65%-ной) и серной (94%-ной) кислот, взятых в соотношении 1:1 по объему, при кипячении на водяной бане в течение 5 минут, к реакционной смеси прибавляют 20%-ный раствор гидроксида натрия до рН 4. Образующийся раствор доводят буферным раствором с рН 4 до 50 мл и экстрагируют диэтиловым эфиром дважды порциями по 50 мл каждая. Эфирные экстракты объединяют, экстрагент испаряют (остаток А). Водный раствор подкисляют 24%-ным раствором хлороводородной кислоты до рН 1, доводят буферным раствором до объема 75 мл и экстрагируют образующийся раствор дважды порциями диэтилового эфира по 75 мл каждая. Эфирные экстракты объединяют, экстрагент испаряют (остаток Б). Остаток А растворяют в 25 мл системы растворителей гексан-диоксан-пропанол-2 (40:5:1). 8 мкл полученного раствора вводят в жидкостный хроматограф типа "Милихром". Процесс хроматографирования осуществляют в колонке размером 64×2 мм, заполненной сорбентом с гидроксилированной поверхностью "Силасорб-600", используя в качестве подвижной фазы систему растворителей гексан-диоксан-пропанол-2 (40:5:1). Скорость подачи элюента составляет 50 мкл/мин, скорость диаграммной ленты - 720 мм/час. Оптическую плотность регистрируют при длине волны 266 нм. Качественное определение 2-метилоксибензола и 4-метилоксибензола осуществляют по величинам характерных объемов или времени удерживания их соответствующих полинитропроизводных (2-метил-4,6-динитрооксибензола и 4-метил-2,6-динитрооксибензола).
Общий вид хроматограммы смеси 2-метил-4,6-динитрооксибензола и 4-метил-2,6-динитрооксибензола представлен на фиг.1. Первый пик (с меньшим временем удерживания) на хроматограмме соответствует 4-метил-2,6-динитрооксибензолу, второй (с большим временем удерживания) соответствует 2-метил-4,6-динитрооксибензолу.
Значения объемов и времени удерживания полинитропроизводных 2-метилоксибензола и 4-метилоксибензола представлены в таблице 1.
Остаток Б растворяют в 25 мл системы растворителей гексан-диоксан-муравьиная кислота (5:3:0,2). 8 мкл полученного раствора вводят в жидкостный хроматограф типа "Милихром". Процесс хроматографирования осуществляют в колонке размером 64×2 мм, заполненной сорбентом с гидроксилированной поверхностью "Силасорб-600", используя в качестве подвижной фазы систему растворителей гексан-диоксан-муравьиная кислота (5:3:0,2). Скорость подачи элюента составляет 100 мкл/мин, скорость диаграммной ленты 720 мм/час. Оптическую плотность регистрируют при длине волны 334 нм. Качественное определение оксибензола и 3-метилоксибензола осуществляют по величинам характерных объемов или времени удерживания их соответствующих полинитропроизводных (2,4,6-тринитрооксибензола и 3-метил-2,4,6-тринитрооксибензола).
Общий вид хроматограммы смеси 2,4,6-тринитрооксибензола и 3-метил-2,4,6-тринитрооксибензола представлен на фиг.2. Первый пик (с меньшим временем удерживания) на хроматограмме соответствует 3-метил-2,4,6-тринитрооксибензолу, второй (с большим временем удерживания) соответствует 2,4,6-тринитрооксибензолу.
Значения объемов и времени удерживания полинитропроизводных оксибензола и 3-метилоксибензола представлены в таблице 1.
Пример 2
Количественное определение 2-метилоксибензола в ткани печени в присутствии оксибензола, 3-метилоксибензола и 4-метилоксибензола
К 10 г мелкоизмельченной ткани свежей трупной печени человека прибавляют смесь оксибензола, 2-метилоксибензола, 3-метилоксибензола и 4-метилоксибензола по 5 мг каждого из веществ, тщательно перемешивают биологическую ткань с веществами и оставляют на сутки при температуре 16-20°С. По истечении указанного времени смесь заливают 20 мл этилацетата и выдерживают 30 минут, периодически перемешивая. Извлечение отделяют, операцию настаивания повторяют в указанных условиях. Вытяжки объединяют, встряхивают с 7 г безводного сульфата натрия, фильтруют через стеклянный фильтр с безводным сульфатом натрия, фильтр дополнительно промывают 20 мл этилацетата, фильтраты объединяют, экстрагент испаряют в токе воздуха при температуре 16-20°С, остаток растворяют в 10 мл смеси растворителей гексан-диэтиловый эфир (8:2). 2 мл полученного раствора вносят в колонку размером 490×11 мм, заполненную 10 г силикагеля L 40/100 μ. Хроматографируют, используя подвижную фазу гексан-диэтиловый эфир (8:2). Элюат собирают отдельными фракциями по 2 мл каждая. Фракции с 5 по 7 включительно объединяют, элюент испаряют в токе воздуха над 1 г безводного сульфата натрия при температуре 16-20°С. К остатку прибавляют 4 мл воды и 4 мл смеси азотной (65%-ной) и серной (94%-ной) кислот, взятых в соотношении 1:1 по объему, и кипятят реакционную смесь на водяной бане в течение 5 минут, после чего к реакционной смеси прибавляют 20%-ный раствор гидроксида натрия до рН 4. Образующийся раствор доводят буферным раствором с рН 4 до 50 мл и экстрагируют диэтиловым эфиром дважды порциями по 50 мл каждая. Эфирные экстракты объединяют, экстрагент испаряют. Остаток растворяют в 25 мл системы растворителей гексан-диоксан-пропанол-2 (40:5:1). 8 мкл полученного раствора вводят в жидкостный хроматограф типа "Милихром". Процесс хроматографирования осуществляют в колонке размером 64×2 мм, заполненной сорбентом "Силасорб-600", используя в качестве подвижной фазы систему растворителей гексан-диоксан-пропанол-2 (40:5:1). Скорость подачи элюента составляет 50 мкл/мин, скорость диаграммной ленты 720 мм/час. Оптическую плотность регистрируют при длине волны 266 нм.
Пик на хроматограмме с временем удерживания 7,40 мин (объемом удерживания 370 мкл) соответствует полинитропроизводному 2-метилоксибензола-2-метил-4,6-динитрооксибензолу.
Количественное содержание 2-метилоксибензола определяют исходя из площади хроматографического пика 2-метил-4,6-динитрооксибензола по уравнению калибровочного графика и пересчитывают на навеску 2-метилоксибензола, внесенную в биологический материал.
Построение калибровочного графика
В ряд пробирок вносят по 0,5 мл 0,0375%, 0,0750%, 0,15%, 0,30%, 0,45%, 0,60%, растворов 2-метилоксибензола, по 0,5 мл воды и прибавляют к содержимому каждой пробирки 1 мл смеси азотной (65%-ной) и серной (94%-ной) кислот, взятых в соотношении 1:1 по объему и кипятят на водяной бане в течение 5 минут, после чего к каждой реакционной смеси прибавляют 20%-ный раствор гидроксида натрия до рН 4 и доводят объем образующегося раствора буферным раствором с рН 4 до 10 мл.
Полученный раствор экстрагируют диэтиловым эфиром дважды порциями по 10 мл каждая. Эфирные экстракты объединяют, экстрагент испаряют. Остаток растворяют в 50 мл системы растворителей гексан-диоксан-пропанол-2 (40:5:1). 8 мкл полученного раствора вводят в хроматограф. Хроматографирование осуществляют в колонке размером 64×2 мм, заполненной сорбентом "Силасорб-600", используя в качестве подвижной фазы систему растворителей гексан-диоксан-пропанол-2 (40:5:1). Скорость подачи элюента составляет 50 мкл/мин, скорость диаграммной ленты 720 мм/час. Оптическую плотность регистрируют при длине волны 266 нм. По результатам измерения на хроматографе строят график зависимости площади пика от концентрации определяемого вещества. График линеен в интервале концентраций 0,03-0,48 мкг. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое имеет вид:
S=34,9774·С+0,1096,
где S - площадь хроматографического пика 2-метил-4,6-динитрооксибензола, см2,
С - условная концентрация 2-метилоксибензола в анализируемой пробе, мкг.
Результаты количественного определения 2-метилоксибензола в ткани печени представлены в таблице 2.
Пример 3
Количественное определение 4-метилоксибензола в ткани печени в присутствии оксибензола, 2-метилоксибензола и 3-метилоксибензола
К 10 г мелкоизмельченной ткани свежей трупной печени человека прибавляют смесь оксибензола, 2-метилоксибензола, 3-метилоксибензола и 4-метилоксибензола по 5 мг каждого из веществ, тщательно перемешивают биологическую ткань с веществами и оставляют на сутки при температуре 16-20°С. По истечении указанного времени смесь заливают 20 мл этилацетата и выдерживают 30 минут, периодически перемешивая. Извлечение отделяют, операцию настаивания повторяют в указанных условиях. Вытяжки объединяют, встряхивают с 7 г безводного сульфата натрия, фильтруют через стеклянный фильтр с безводным сульфатом натрия, фильтр дополнительно промывают 20 мл этилацетата, фильтраты объединяют, экстрагент испаряют в токе воздуха при температуре 16-20°С, остаток растворяют в 10 мл смеси растворителей гексан-диэтиловый эфир (8:2). 2 мл полученного раствора вносят в колонку размером 490×11 мм, заполненную 10 г силикагеля L 40/100 μ. Хроматографируют, используя подвижную фазу гексан-диэтиловый эфир (8:2). Элюат собирают отдельными фракциями по 2 мл каждая. Фракции с 10 по 13 включительно объединяют, элюент испаряют в токе воздуха над 1 г безводного сульфата натрия при температуре 16-20°С. К остатку прибавляют 4 мл воды и 4 мл смеси азотной (65%-ной) и серной (94%-ной) кислот, взятых в соотношении 1:1 по объему, и кипятят реакционную смесь на водяной бане в течение 5 минут, после чего к реакционной смеси прибавляют 20%-ный раствор гидроксида натрия до рН 4. Образующийся раствор доводят буферным раствором с рН 4 до 50 мл и экстрагируют диэтиловым эфиром дважды порциями по 50 мл каждая. Эфирные экстракты объединяют, экстрагент испаряют. Остаток растворяют в 25 мл системы растворителей гексан-диоксан-пропанол-2 (40:5:1). 8 мкл полученного раствора вводят в жидкостный хроматограф типа "Милихром". Процесс хроматографирования осуществляют в колонке размером 64×2 мм, заполненной сорбентом "Силасорб-600", используя в качестве подвижной фазы систему растворителей гексан-диоксан-пропанол-2 (40:5:1). Скорость подачи элюента составляет 50 мкл/мин, скорость диаграммной ленты 720 мм/час. Оптическую плотность регистрируют при длине волны 266 нм.
Пик на хроматограмме с временем удерживания 9,92 мин (объемом удерживания 496 мкл) соответствует полинитропроизводному 4-метилоксибензола-4-метил-2,6-динитрооксибензолу.
Количественное содержание 4-метилоксибензола определяют исходя из площади хроматографического пика 4-метил-2,6-динитрооксибензола по уравнению калибровочного графика и пересчитывают на навеску 4-метилоксибензола, внесенную в биологический материал.
Построение калибровочного графика
В ряд пробирок вносят по 0,5 мл 0,05%, 0,1%, 0,2%, 0,3%, и 0,4% растворов 4-метилоксибензола, 0,5 мл воды и прибавляют к содержимому каждой пробирки 1 мл смеси азотной (65%-ной) и серной (94%-ной) кислот, взятых в соотношении 1:1 по объему, и кипятят на водяной бане в течение 5 минут, после чего к каждой реакционной смеси прибавляют 20%-ный раствор гидроксида натрия до рН 4 и доводят объем образующегося раствора буферным раствором с рН 4 до 10 мл.
Полученный раствор экстрагируют диэтиловым эфиром дважды порциями по 10 мл каждая. Эфирные экстракты объединяют, экстрагент испаряют. Остаток растворяют в 50 мл системы растворителей гексан-диоксан-пропанол-2 (40:5:1). 8 мкл полученного раствора вводят в хроматограф. Хроматографирование осуществляют в колонке размером 64×2 мм, заполненной сорбентом "Силасорб-600", используя в качестве подвижной фазы систему растворителей гексан-диоксан-пропанол-2 (40:5:1). Скорость подачи элюента составляет 50 мкл/мин, скорость диаграммной ленты 720 мм/час. Оптическую плотность регистрируют при длине волны 266 нм. По результатам измерений на хроматографе строят график зависимости площади пика от концентрации определяемого вещества. График линеен в интервале концентраций 0,04-0,32 мкг. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое имеет вид:
S=26,0663·C+0,00804,
где S - площадь хроматографического пика 4-метил-2,6-динитрооксибензола, см2,
С - условная концентрация 4-метилоксибензола в анализируемой пробе, мкг.
Результаты количественного определения 4-метилоксибензола в ткани печени представлены в таблице 3.
Пример 4
Количественное определение оксибензола в ткани печени в присутствии 2-метилоксибензола, 3-метилоксибензола и 4-метилоксибензола
К 10 г мелкоизмельченной ткани свежей трупной печени человека прибавляют смесь оксибензола, 2-метилоксибензола, 3-метилоксибензола и 4-метилоксибензола по 5 мг каждого из веществ, тщательно перемешивают биологическую ткань с веществами и оставляют на сутки при температуре 16-20°С. По истечении указанного времени смесь заливают 20 мл этилацетата и выдерживают 30 минут, периодически перемешивая. Извлечение отделяют, операцию настаивания повторяют в указанных условиях. Вытяжки объединяют, встряхивают с 7 г безводного сульфата натрия, фильтруют через стеклянный фильтр с безводным сульфатом натрия, фильтр дополнительно промывают 20 мл этилацетата, фильтраты объединяют, экстрагент испаряют в токе воздуха при температуре 16-20°С, остаток растворяют в 10 мл смеси растворителей гексан-диэтиловый эфир (8:2). 2 мл полученного раствора вносят в колонку размером 490×11 мм, заполненную 10 г силикагеля L 40/100 μ. Хроматографируют, используя подвижную фазу гексан-диэтиловый эфир (8:2). Элюат собирают отдельными фракциями по 2 мл каждая. Фракции с 5 по 8 включительно объединяют, элюент испаряют в токе воздуха над 1 г безводного сульфата натрия при температуре 16-20°С. К остатку прибавляют 4 мл воды и 4 мл смеси азотной (65%-ной) и серной (94%-ной) кислот, взятых в соотношении 1:1 по объему и кипятят реакционную смесь на водяной бане в течение 5 минут, после чего к реакционной смеси прибавляют 20%-ный раствор гидроксида натрия до рН 4. Образующийся раствор доводят буферными растворами с рН 4 до 50 мл и экстрагируют диэтиловым эфиром дважды порциями по 50 мл каждая.
Эфирные извлечения отделяют, водный слой подкисляют 24%-ным раствором хлороводородной кислоты до рН 1, доводят буферным раствором до объема 75 мл и экстрагируют образующийся раствор дважды порциями диэтилового эфира по 75 мл каждая.
Эфирные экстракты объединяют, экстрагент испаряют. Остаток растворяют в 25 мл системы растворителей гексан-диоксан-муравьиная кислота (5:3:0,2). 8 мкл полученного раствора вводят в жидкостный хроматограф типа "Милихром". Процесс хроматографирования осуществляют в колонке размером 64х2 мм, заполненной сорбентом "Силасорб-600", используя в качестве подвижной фазы систему растворителей гексан-диоксан-муравьиная кислота (5:3:0,2). Скорость подачи элюента составляет 100 мкл/мин, скорость диаграммной ленты 720 мм/час. Оптическую плотность регистрируют при длине волны 334 нм.
Пик на хроматограмме с временем удерживания 9,12 мин (объемом удерживания 912 мкл) соответствует полинитропроизводному оксибензола-2,4,6-тринитрооксибензолу.
Количественное содержание оксибензола определяют исходя из площади хроматографического пика 2,4,6-тринитрооксибензола по уравнению калибровочного графика и пересчитывают на навеску оксибензола, внесенную в биологический материал.
Построение калибровочного графика
В ряд пробирок вносят по 1 мл 0,075%, 0,15%, 0,3%, 0,6%, 1,2%, 2,2% растворов оксибензола и 1 мл смеси азотной (65%-ной) и серной (94%-ной) кислот, взятых в соотношении 1:1 по объему, и кипятят на водяной бане в течение 5 минут, после чего к каждой реакционной смеси прибавляют 20%-ный раствор гидроксида натрия до рН 4 и доводят объем образующегося раствора буферным раствором с рН 4 до 10 мл.
Полученный раствор экстрагируют диэтиловым эфиром дважды порциями по 10 мл каждая. Эфирные извлечения отделяют, водный слой подкисляют 24%-ным раствором хлороводородной кислоты до рН 1, доводят буферным раствором до объема 15 мл и экстрагируют образующийся раствор дважды порциями диэтилового эфира по 15 мл каждая.
Эфирные экстракты объединяют, экстрагент испаряют. Остаток растворяют в 50 мл системы растворителей гексан-диоксан-муравьиная кислота (5:3:0,2). 8 мкл полученного раствора вводят в хроматограф. Хроматографирование осуществляют в колонке размером 64×2 мм, заполненной сорбентом "Силасорб-600", используя в качестве подвижной фазы систему растворителей гексан-диоксан-муравьиная кислота (5:3:0,2). Скорость подачи элюента составляет 100 мкл/мин, скорость диаграммной ленты 720 мм/час. Оптическую плотность регистрируют при длине волны 334 нм.
По результатам измерений на хроматографе строят график зависимости площади пика от концентрации определяемого вещества. График линеен в интервале концентраций 0,12-3,36 мкг. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое имеет вид:
S=4,3334·C+0,0095,
где S - площадь хроматографического пика 2,4,6-тринитрооксибензола, см2,
С - условная концентрация оксибензола в анализируемой пробе, мкг.
Результаты количественного определения оксибензола в ткани печени представлены в таблице 4.
Пример 5
Количественное определение 3-метилоксибензола в ткани печени в присутствии оксибензола, 2-метилоксибензола и 4-метилоксибензола
К 10 г мелкоизмельченной ткани свежей трупной печени человека прибавляют смесь оксибензола, 2-метилоксибензола, 3-метилоксибензола и 4-метилоксибензола по 5 мг каждого из веществ, тщательно перемешивают биологическую ткань с веществами и оставляют на сутки при температуре 16-20°С. По истечении указанного времени смесь заливают 20 мл этилацетата и выдерживают 30 минут, периодически перемешивая. Извлечение отделяют, операцию настаивания повторяют в указанных условиях. Вытяжки объединяют, встряхивают с 7 г безводного сульфата натрия, фильтруют через стеклянный фильтр с безводным сульфатом натрия, фильтр дополнительно промывают 20 мл этилацетата, фильтраты объединяют, экстрагент испаряют в токе воздуха при температуре 16-20°С, остаток растворяют в 10 мл смеси растворителей гексан-диэтиловый эфир (8:2). 2 мл полученного раствора вносят в колонку размером 490×11 мм, заполненную 10 г силикагеля L 40/100 μ. Хроматографируют, используя подвижную фазу гексан-диэтиловый эфир (8:2). Элюат собирают отдельными фракциями по 2 мл каждая. Фракции с 8 по 11 включительно объединяют, элюент испаряют в токе воздуха над 1 г безводного сульфата натрия при температуре 16-18°С. К остатку прибавляют 4 мл воды и 4 мл смеси азотной (65%-ной) и серной (94%-ной) кислот, взятых в соотношении 1:1 по объему, и кипятят реакционную смесь на водяной бане в течение 5 минут, после чего к реакционной смеси прибавляют 20%-ный раствор гидроксида натрия до рН 4. Образующийся раствор доводят буферными растворами с рН 4 до 50 мл и экстрагируют диэтиловым эфиром дважды порциями по 50 мл каждая.
Эфирные извлечения отделяют, водный слой подкисляют 24%-ным раствором хлороводородной кислоты до рН 1, доводят буферным раствором до объема 75 мл и экстрагируют образующийся раствор дважды порциями диэтилового эфира по 75 мл каждая.
Эфирные экстракты объединяют, экстрагент испаряют. Остаток растворяют в 25 мл системы растворителей гексан-диоксан-муравьиная кислота (5:3:0,2). 8 мкл полученного раствора вводят в жидкостный хроматограф типа "Милихром". Процесс хроматографирования осуществляют в колонке размером 64×2 мм, заполненной сорбентом "Силасорб-600", используя в качестве подвижной фазы систему растворителей гексан-диоксан-муравьиная кислота (5:3:0,2). Скорость подачи элюента составляет 100 мкл/мин, скорость диаграммной ленты 720 мм/час. Оптическую плотность регистрируют при длине волны 334 нм.
Пик на хроматограмме с временем удерживания 3,77 мин (объемом удерживания 377 мкл) соответствует полинитропроизводному 3-метилоксибензола-3-метил-2,4,6-тринитрооксибензолу.
Количественное содержание 3-метилоксибензола определяют исходя из площади хроматографического пика 3-метил-2,4,6-тринитрооксибензола по уравнению калибровочного графика и пересчитывают на навеску 3-метилоксибензола, внесенную в биологический материал.
Построение калибровочного графика
В ряд пробирок вносят по 1 мл 0,0625%, 0,125%, 0,25%, 0,5%, 1,0%, 1,5% растворов 3-метилоксибензола и 1 мл смеси азотной (65%-ной) и серной (94%-ной) кислот, взятых в соотношении 1:1 по объему, и кипятят на водяной бане в течение 5 минут, после чего к каждой реакционной смеси прибавляют 20%-ный раствор гидроксида натрия до рН 4 и доводят объем образующегося раствора буферным раствором с рН 4 до 10 мл.
Полученный раствор экстрагируют диэтиловым эфиром дважды порциями по 10 мл каждая. Эфирные извлечения отделяют, водный слой подкисляют 24%-ным раствором хлороводородной кислоты до рН 1, доводят буферным раствором до объема 15 мл и экстрагируют образующийся раствор дважды порциями диэтилового эфира по 15 мл каждая.
Эфирные экстракты объединяют, экстрагент испаряют. Остаток растворяют в 50 мл системы растворителей гексан-диоксан-муравьиная кислота (5:3:0,2). 8 мкл полученного раствора вводят в хроматограф. Хроматографирование осуществляют в колонке размером 64×2 мм, заполненной сорбентом "Силасорб-600", используя в качестве подвижной фазы систему растворителей гексан-диоксан-муравьиная кислота (5:3:0,2). Скорость подачи элюента составляет 100 мкл/мин, скорость диаграммной ленты 720 мм/час. Оптическую плотность регистрируют при длине волны 334 нм.
По результатам измерения на хроматографе строят график зависимости площади пика от концентрации определяемого вещества. График линеен в интервале концентраций 0,10-2,4 мкг. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое имеет вид:
S=30,9829·C+0,0217,
где S - площадь хроматографического пика 3-метил-2,4,6-тринитрооксибензола, см2,
С - условная концентрация 3-метилоксибензола в хроматографируемой пробе, мкг.
Результаты количественного определения 3-метилоксибензола в ткани печени представлены в таблице 5.
Предлагаемый способ по сравнению с прототипом в 20 раз повышает чувствительность определения в анализируемой пробе и в 2 раза - в ткани печени, в 1,2-1,5 раза увеличивает степень извлечения оксибензола и его монометильных производных из ткани печени (для 4-метилоксибензола степень извлечения увеличивается с 49,96 до 75,65%), характеризуется более высокой селективностью (позволяет в отличие от прототипа определять любое из четырех рассматриваемых веществ в присутствии трех остальных, а также в присутствии их метаболитов), сокращает продолжительность процесса определения более чем в 3 раза.
Сравнительная характеристика предлагаемого и известного способов представлена в таблице 6.
| Таблица 1 | |||
| Параметры хроматографирования полинитропроизводных оксибензола и его монометильных замещенных методом ВЭЖХ (колонка размером 64×2, заполненная сорбентом " Силасорб" -600) | |||
| Хроматографируемое вещество | Объем удерживания VR, мкг | Время удерживания tR,мин | Относительное удерживание (по отношению к удерживанию оксибензола) |
| Элюент гексан-диоксан-муравьиная кислота (5:3:0,2) | |||
| 3-метил-2,4,6-тринитрооксибензол (производное 3-метилоксибензола) | 377 | 3,77 | 1,07 |
| 2,4,6-тринитрооксибензол (производное оксибензола) | 912 | 9,12 | 2,16 |
| Элюент гексан-диоксан-пропанол-2 (40:5:1) | |||
| 2-метил-4,6-динитрооксибензол (производное 2-метилоксибензола) | 370 | 7,40 | 0,98 |
| 4-метил-2,6-динитрооксибензол (производное 4-метилоксибензола) | 496 | 9,92 | 1,31 |
| Таблица 2 | |||||||
| Результаты определения 2-метилоксибензола в ткани печени в присутствии оксибензола, 3-метилоксибензола и 4-метилоксибензола | |||||||
| N | Внесено в 10 г печени | Найдено 2-метилоксибензола | Метрологические характеристики | ||||
| 2-метилоксибензола | оксибензола | 3-метилоксибензола | 4-метил-оксибензола | мг | % | ||
| 1 | 5,0 | 5,0 | 5,0 | 5,0 | 3,39 | 67,81 | х=70,38 |
| 2 | 5,0 | 5,0 | 5,0 | 5,0 | 3,42 | 68,42 | S=2,49 |
| 3 | 5,0 | 5,0 | 5,0 | 5,0 | 3,70 | 73,80 | Sx=1,11 |
| 4 | 5,0 | 5,0 | 5,0 | 5,0 | 3,59 | 71,75 | Δx=2,86 |
| 5 | 5,0 | 5,0 | 5,0 | 5,0 | 70,02 | 70,02 | ε=4,07 |
| Таблица 3 | |||||||
| Результаты определения 4-метилоксибензола в ткани печени в присутствии 2-метилоксибензола, оксибензола и 3-метилоксибензола | |||||||
| N | Внесено в 10 г печени | Найдено 4-метилоксибензола | Метрологические характеристики | ||||
| 4-метилоксибензола | оксибензола | 2-метилоксибензола | 3-метил-оксибензола | мг | % | ||
| 1 | 5,0 | 5,0 | 5,0 | 5,0 | 3,71 | 74,12 | х=75,05 |
| 2 | 5,0 | 5,0 | 5,0 | 5,0 | 3,67 | 73,41 | S=2,06 |
| 3 | 5,0 | 5,0 | 5,0 | 5,0 | 3,83 | 76,63 | Sx=0,92 |
| 4 | 5,0 | 5,0 | 5,0 | 5,0 | 3,66 | 73,26 | Δx=2,36 |
| 5 | 5,0 | 5,0 | 5,0 | 5,0 | 13,89 | 77,83 | ε=3,16 |
| Таблица 4 | |||||||
| Результаты определения оксибензола в ткани печени в присутствии 2-метилоксибензола, 3-метилоксибензола и 4-метилоксибензола | |||||||
| N | Внесено в 10 г печени | Найдено оксибензола | Метрологические характеристики | ||||
| оксибензола | 2-метилоксибензола | 3-метилоксибензола | 4-метил-оксибензола | мг | % | ||
| 1 | 5,0 | 5,0 | 5,0 | 5,0 | 3,89 | 77,85 | х=77,81 |
| 2 | 5,0 | 5,0 | 5,0 | 5,0 | 3,68 | 73,64 | S=2,52 |
| 3 | 5,0 | 5,0 | 5,0 | 5,0 | 4,01 | 80,17 | Sx=1,13 |
| 4 | 5,0 | 5,0 | 5,0 | 5,0 | 3,97 | 79,33 | Δx=2,89 |
| 5 | 5,0 | 5,0 | 5,0 | 5,0 | 3,90 | 78,09 | ε=3,72 |
| Таблица 5 | |||||||
| Результаты определения 3-метилоксибензола в ткани печени в присутствии оксибензола, 2-метилоксибензола и 4-метилоксибензола | |||||||
| N | Внесено в 10 г печени | Найдено 3-метилоксибензола | Метрологические характеристики | ||||
| 3-метилоксибензола | оксибензола | 2-метилоксибензола | 4-метил-оксибензола | мг | % | ||
| 1 | 5,0 | 5,0 | 5,0 | 5,0 | 3,28 | 65,61 | x=68,94 |
| 2 | 5,0 | 5,0 | 5,0 | 5,0 | 3,54 | 70,75 | S=2,09 |
| 3 | 5,0 | 5,0 | 5,0 | 5,0 | 3,41 | 68,19 | Sx=0,94 |
| 4 | 5,0 | 5,0 | 5,0 | 5,0 | 3,51 | 70,21 | Δх=2,40 |
| 5 | 5,0 | 5,0 | 5,0 | 5,0 | 3,49 | 69,92 | ε=3,49 |
| Таблица 6 | ||
| Сравнительная характеристика предлагаемого и известного способов | ||
| Показатели | Предлагаемый способ | Известный способ |
| 1 | 2 | 3 |
| 1. Селективность | Позволяет определять индивидуально оксибензол и каждое из его монометильных производных при их совместном присутствии в биологическом материале.Определению не мешают основные метаболиты (продукты окисления) оксибензола и его монометильных производных (1,2-диоксибензол, 1,4-диоксибензол, 1-метил-3,4-диоксибензол, 1-метил-2,5-диоксибензол,4-оксибензойная кислота) | Не позволяет (за исключением 4-метилоксибензола) определять индивидуально оксибензол и каждое из его монометильных производных при их совместном присутствии в биологическом материале.Определению мешают основные метаболиты (продукты окисления) оксибензола и его монометильных производных. |
| 2. Чувствительность (открываемый минимум) (на примере 4-метилоксибензола) | ||
| а) в 100 г ткани печени | 0,4 мг | 0,8 мг |
| б) в анализируемой пробе | 0,04 мг | 0,91 мг |
| 3. Интервал линейности калибровочного графика (мкг в анализируемой пробе) (на примере 4-метилоксибензола) | 0,04-0,32 мкг | 0,91-9,1 мкг |
| Продолжение таблицы 6 | ||
| 1 | 2 | 3 |
| 4. Степень извлечения определяемого вещества, в процентах от предварительно внесенного в биоматериал количества (на примере 4-метилоксибензола) | 75,64% | 49,96% |
| 5. Относительная ошибка среднего результата (n=5; P=0,95) (при условии содержания 50 мг определяемого вещества в 100 г биоматериала) (на примере 4-метилоксибензола) | ±3,16% | ±7,24% |
| 6. Продолжительность одного определения | Около 8 часов | 26-27 часов |
Способ определения оксибензола и его монометильных производных в биологическом материале, заключающийся в том, что анализируемые вещества извлекают из объекта, обрабатывают нитрующим агентом и определяют их качественное и количественное содержание физико-химическим методом, отличающийся тем, что извлечение анализируемых веществ осуществляют путем обработки биологической ткани этилацетатом двукратно по 30 мин, перед обработкой нитрующим агентом этилацетатные вытяжки объединяют, обезвоживают, этилацетат испаряют при 16-20°С, остаток растворяют в смеси растворителей гексан-диэтиловый эфир (6:4), хроматографируют в колонке с силикагелем с использованием подвижной фазы гексан-диэтиловый эфир (6:4), фракции, содержащие оксибензол и его монометильные производные, отбирают, объединяют, обезвоживают, элюэнт испаряют до получения остатка, остаток разбавляют водой и обрабатывают нитрующим агентом в равном объемном соотношении, в качестве нитрующего агента применяют смесь 65%-ной азотной и 94%-ной серной кислот в соотношении 1:1 по объему, обработку ведут на водяной бане, после чего реакционную смесь подщелачивают до рН 4 и разбавляют буферным раствором с рН 4, полученный раствор двукратно экстрагируют диэтиловым эфиром в соотношении 1:1 по объему, эфирные извлечения, содержащие полинитропроизводные 2 метил-оксибензола и 4 метил-оксибензола, отделяют, а водный слой подкисляют до рН 1 и разбавляют буферным раствором, полученный раствор снова дважды обрабатывают диэт