Способ получения производного пиридина и промежуточное вещество
Иллюстрации
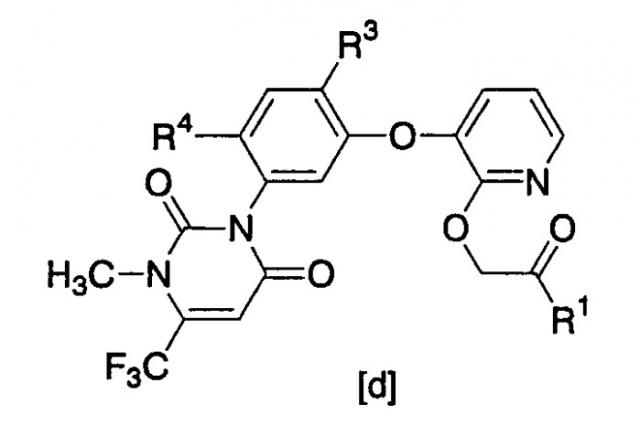
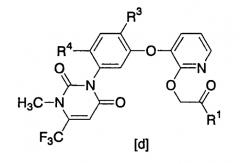
Показать всеИзобретение относится к новому способу получения производного пиридина формулы [d]
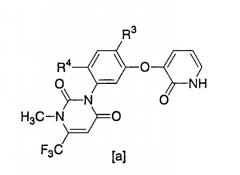
где R1, R3 и R4 являются такими, как они определены ниже, взаимодействием нового производного пиридона [а]
где R3 представляет собой атом галогена, цианогруппу или нитрогруппу и R4 представляет собой атом водорода или атом галогена, с производным α-диазоэфира [f]
N2CHCOR1, [f]
где R1 представляет собой C1-С6-алкоксигруппу, в присутствии кислоты. Описываемый способ является удобным и выгодным способом получения производных пиридина формулы [d], обладающих специфической системой заместителей и проявляющих гербицидную активность. 2 н. и 6 з.п. ф-лы, 2 табл.
Реферат
Область техники
Настоящее изобретение относится к новому способу получения производных пиридина, обладающих превосходной гербицидной активностью, и к исходным соединениям, используемым для способа.
Предшествующий уровень техники
Производные пиридина (d):
[где R1 представляет собой С1-С6-алкоксигруппу, R3 представляет атом галогена, цианогруппу или нитрогруппу и R4 представляет собой атом водорода или атом галогена] обладают превосходной гербицидной активностью. Производные пиридина [d] содержат два гетероциклических кольца, которые представляют собой урациловое кольцо и пиридиновое кольцо, и является весьма желательным выгодный способ их получения.
Задача настоящего изобретения - получить производные пиридина [d], обладающие специфической системой заместителей, и исходные соединения, используемые в этом способе.
Описание изобретения
Для создания выгодного способа получения производных пиридина [d] авторы настоящего изобретения проводили интенсивные исследования. В результате они обнаружили, что производное пиридина [d] может быть получено взаимодействием производного пиридона [a]:
[где R3 и R4 имеют значения, указанные выше] с производным α-диазоэфира [f]
N2CHCOR1 [f]
[где R1 имеет значение, указанное выше] в присутствии кислоты для осуществления региоселективного О-алкилирования, вследствие чего было создано настоящее изобретение. За счет выбора способа настоящего изобретения может быть выгодно получено производное пиридина [d], имеющее специфическую систему заместителей.
Именно, настоящее изобретение относится к способу получения производного пиридина [d] взаимодействием производного пиридона [a] с производным α-диазоэфира [f] в присутствии кислоты (далее указывается как «способ настоящего изобретения) и к производному пиридона [a], которое представляет собой необходимое исходное соединение, используемое в этом способе.
В настоящем изобретении примеры С1-С6-алкоксильной группы, данные для R1, включают метоксигруппу, этоксигруппу, пропоксигруппу и т.д. и примеры атома галогена, данные для R3 и R4, включают атом фтора, атом хлора и атом брома.
Способ настоящего изобретения осуществляется взаимодействием производного пиридона [а] с производным α-диазоэфира [f] в присутствии кислоты, и реакцию обычно проводят в растворителе. Примеры растворителя включают ароматические углеводороды, такие как бензол, толуол, ксилол и т.д.; галогенированные углеводороды, такие как 1,2-дихлорэтан, хлорбензол, дихлорбензол и т.д.; и их смеси.
В настоящем способе кислота означает кислоту, определенную Льюисом, а именно вещество, которое может принимать электронную пару, и включает апротонную кислоту и протонную кислоту (кислота Бренстеда). Примеры апротонной кислоты включают соли родия (II), трифторид бора и тетрахлорид олова и примеры протонной кислоты включают сульфоновые кислоты, такие как трифторметансульфоновая кислота, п-толуолсульфоновая кислота и т.д.; трифторуксусную кислоту и серную кислоту. Термин «соли родия (II)» означает металлическую соль, включающую катион двухвалентного родия и соответствующий анион, и, кроме того, необязательно соответствующий лиганд, и типичные примеры представляют собой димер трифторацетата родия (II) ([(CF3CO2)2Rh]2), димер ацетата родия (II) ([(CH3CO2)2Rh]2) и т.д. В качестве трифторида бора может быть использован сам BF3 или его комплекс, и примеры комплекса включают диэтилэфирный комплекс, диметилсульфидный комплекс, тетрагидрофурановый комплекс и т.д. Принимая во внимание скорость реакции, предпочтительно использовать в качестве кислоты димер трифторацетата родия (II), комплекс трифторид бора/диэтиловый эфир, тетрахлорид олова или трифторметансульфоновую кислоту.
В настоящей реакции теоретически необходим один моль производного α-диазоэфира [f] в расчете на один моль производного пиридона [a], а практически используются от 1 до 2 моль производного α-диазоэфира. В настоящей реакции кислота имеет каталитическую активность и ее используют с учетом скорости реакции в количестве, находящемся в диапазоне от 0,001 до 5 моль, предпочтительно в количестве 0,01 моль или более в расчете на моль производного пиридона [a]. Температура реакционной массы в настоящей реакции с учетом ее скорости обычно составляет от -50 до 120°С, предпочтительно -20°С или более. Время реакции обычно находится в диапазоне от мгновения до 72 часов.
Используемые для настоящей реакции реагенты добавляют в реакционный сосуд, например, в следующем порядке:
1) Способ включает предварительное смешивание производного пиридона [a], кислоты и растворителя и добавление в смесь по каплям производного α-диазоэфира [f].
2) Способ включает предварительное смешивание производного пиридона [a], производного α-диазоэфира [f] и растворителя и добавление в смесь по каплям кислоты.
3) Способ включает предварительное смешивание производного пиридона [a] и растворителя и добавление в смесь по каплям соответственно кислоты и производного α-диазоэфира [f].
Окончание настоящей реакции может быть установлено отбором части реакционной смеси, анализом пробы жидкостной хроматографией, тонкослойной хроматографией и т.д. и измерением оставшегося количества производного пиридона [a] или производного α-диазоэфира [f].
После реакции производное пиридина [d] может быть получено, например, следующими методами дополнительной обработки реакционной смеси:
1) Фильтрация реакционной смеси и концентрирование фильтрата.
2) Хроматографирование реакционной смеси на силикагеле и затем концентрирование.
3) Вливание реакционной смеси в водный раствор бикарбоната натрия, экстракция органическим растворителем, сушка и концентрирование органического слоя.
Полученное производное пиридина [d] может быть очищено таким методом, как хроматография, перекристаллизация и т.д.
В случае взаимодействия производного пиридона [а] со сложноэфирным соединением [x]:
Х1CH2COR1 [х]
[где R1 имеет значение, указанное выше, и Х1 представляет собой атом хлора, атом брома, метансульфонилоксигруппу или п-толуолсульфонилоксигруппу]
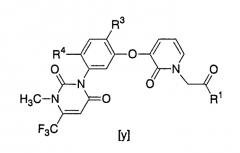
в присутствии основания, основным продуктом было производное пиридона [y]:
[где R3, R4 и R1 имеют значения, указанные выше]
Производное α-диазоэфира [f], используемое в настоящем изобретении, как таковое, имеется в продаже или может быть получено известным способом взаимодействием соединения [h]:
Н2NCH2COR1 [h]
[где R1 имеет значение, указанное выше] или его соли с минеральной кислотой (то есть гидрохлоридной соли) с нитритом натрия в кислой среде (Смотри: Organic Syntheses Collective. Volume IV, p.424-426).
Производное α-диазоэфира [f], полученное взаимодействием соединения [h] или его соли с минеральной кислотой с нитритом натрия в кислой среде, может быть использовано в качестве исходного в способе настоящего изобретения без выделения. Т.е. раствор производного α-диазоэфира [f], полученного взаимодействием производного α-диазоэфира [h] с нитритом натрия в кислой среде, экстракцией органическим растворителем, может применяться в способе настоящего изобретения после соответствующей обработки, такой как сушка безводным сульфатом магния. Примеры используемого указанного выше растворителя включают ароматические углеводороды, такие как бензол, толуол, ксилол и т.д.; и галогенированные углеводороды, такие как дихлорметан, 1,2-дихлорэтан, хлорбензол, дихлорбензол, бензотрифторид и т.д.
Производное пиридона [a], используемое в способе настоящего изобретения, может быть получено из известного соединения следующими способами:
Способ 1 получения
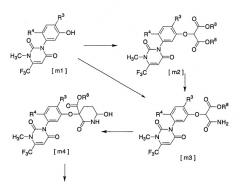
[где R3 и R4 имеют значения, указанные выше, и R8 представляет собой низшую алкильную группу, такую как метильная группа, этильная группа и т.д.]
Соединение [m1] → [соединение m2]
Соединение [m2] получают взаимодействием соединения [m1] с соединением [m7]:
[где R8 имеет значение, указанное выше, и Х представляет собой удаляемую группу, такую как атом хлора, атом брома и т.д.] в присутствии основания.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от комнатной температуры до 80°С, и время реакции обычно находится в диапазоне от мгновения до 12 часов.
В данной реакции теоретически необходимы один моль соединения [m7] и один моль основания в расчете на один моль соединения [m1], но количества могут свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции основания включают карбонат калия и примеры растворителя включают нитрилы, такие как ацетонитрил и т.д.; и амиды кислот, такие как N,N-диметилформамид, N-метил-2-пирролидон и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду или подкисленную воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m2] → соединение [m3]
Соединение [m3] получается взаимодействием соединения [m2] с аммиаком.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от -20°С до 50°С, и время реакции обычно находится в диапазоне от мгновения до 12 часов.
В данной реакции теоретически необходим один моль аммиака в расчете на один моль соединения [m2], но количество может свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции растворителя включают спирты, такие как метанол, этанол и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m1] → соединение [m3]
Соединение [m3] получается взаимодействием соединения [m1] с соединением [m8]:
[где R8 и Х имеют значения, указанные выше] в присутствии основания.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от комнатной температуры до 80°С, и время реакции обычно находится в диапазоне от мгновения до 12 часов.
В данной реакции теоретически необходимы один моль соединения [m8] и один моль основания в расчете на один моль соединения [m1], но количества могут свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции основания включают карбонат калия и примеры растворителя включают нитрилы, такие как ацетонитрил и т.д.; и амиды кислот, такие как N,N-диметилформамид, N-метил-2-пирролидон и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду или подкисленную воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m3] → соединение [m4]
Соединение [m4] получается взаимодействием соединения [m3] с акролеином в присутствии основания.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от -30 до 50°С, предпочтительно от -10 до 20°С. Время реакции обычно находится в диапазоне от мгновения до 12 часов.
В данной реакции теоретически необходимы один моль акролеина и от 0,01 до 2 моль основания в расчете на один моль соединения [m3], но количества могут свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции основания включают алкоксиды металлов, такие как трет-бутоксид калия и т.д.; и неорганические основания, такие как карбонат калия и т.д.
Примеры используемого для реакции растворителя включают простые эфиры, такие как тетрагидрофуран и т.д.; и сложные эфиры, такие как этилацетат и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m4] → соединение [m5]
Соединение [m5] получается взаимодействием соединения [m4] в присутствии кислоты.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от комнатной температуры до 150°С, и время реакции обычно находится в диапазоне от мгновения до 24 часов.
В данной реакции используется от 0,001 до 0,2 моль кислоты в расчете на один моль соединения [m4], но количество может свободно изменяться в соответствии с условиями реакции.
Примеры используемой для реакции кислоты включают органические кислоты, такие как уксусная кислота, п-толуолсульфоновая кислота и т.д.; и неорганические кислоты, такие как хлористоводородная кислота и т.д. Примеры растворителя включают простые эфиры, такие как тетрагидрофуран и т.д.; и сложные эфиры, такие как этилацетат и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m5] → соединение [m6]
Соединение [m6] получается из соединения [m5] в присутствии воды и галогенида щелочного металла, обычно в растворителе.
Температура реакции обычно находится в диапазоне от 80 до 140°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
В данной реакции используются от 0,5 до 2 моль воды и от 1 до 5 моль галогенида щелочного металла в расчете на один моль соединения [m5], но количества могут свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции галогенида щелочного металла включают хлорид лития, хлорид натрия, иодид лития и иодид натрия и примеры растворителя включают диметилсульфоксид и пиридин.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m6] → производное пиридона [а]
Производное пиридона [а] получается взаимодействием соединения [m6] с дегидрирующим реагентом.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от 60 до 190°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
Используемый для настоящей реакции дегидрирующий реагент означает хиноидные окислительные реагенты, такие как хлоранил и т.д.; и гетерогенный металлический катализатор, такой как палладий на угле и т.д.
В данной реакции используется от 1 до 3 моль хиноидного окислительного реагента, или от 10 до 30 мас.% гетерогенного металлического катализатора в расчете на один моль соединения [m6], но количество может свободно изменяться в зависимости от условий реакции.
Примеры растворителя включают ароматические углеводороды, такие как толуол, ксилол и т.д.; галогенированные ароматические углеводороды, такие как хлорбензол, дихлорбензол, бензотрифторид и т.д.; простые эфиры, такие как диоксан, тетрагидрофуран, диглим, дифениловый эфир и т.д.; и их смеси.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь разбавляют органическим растворителем, затем вливают в водный раствор бикарбоната натрия, экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m1] известно из патента США № 4859229 и может быть получено известным способом или подобными способами.
Соединение [m7] как таковое имеется в продаже или может быть получено известным способом.
Соединение [m8] может быть получено взаимодействием соединения [m7] с аммиаком при условиях реакции, представленных выше для превращения «Соединение [m2] → соединение [m3]».
Способ 2 получения
[где R3 и R4 имеют значения, указанные выше; R100 представляет собой низшую алкильную группу, такую как метильная группа, этильная группа и т.д., или фенильную группу; и n равно 1 или 2]
Соединение [m1] → [соединение n1]
Соединение [n1] может быть получено взаимодействием соединения [m1] с хлорацетонитрилом или бромацетонитрилом в присутствии основания.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от -20 до 80°С, и время реакции обычно находится в диапазоне от мгновения до 24 часов.
В данной реакции теоретически необходимы один моль хлорацетонитрила или бромацетонитрила и один моль основания в расчете на один моль соединения [m1], но количества могут свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции основания включают гидрид натрия, карбонат калия, бикарбонат натрия, гидроксид натрия и гидроксид калия и примеры растворителя включают нитрилы, такие как ацетонитрил и т.д.; амиды кислот, такие как N,N-диметилформамид, N-метил-2-пирролидон и т.д.; простые эфиры, такие как тетрагидрофуран, 1,4-диоксан, диметиловый эфир этиленгликоля, 2-метоксиэтиловый эфир и т.д.; углеводороды, такие как толуол и т.д.; и сложные эфиры, такие как метилацетат, этилацетат и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду или подкисленную воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n1] → соединение [n2]
Соединение [n2] может быть получено взаимодействием соединения [n1] с дисульфидным соединением [n6]:
(R100S)2 [n6]
[где R100 имеет значение, указанное выше] в присутствии основания.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от -50 до 10°С, и время реакции обычно находится в диапазоне от мгновения до 12 часов.
В данной реакции теоретически необходимы один моль дисульфидного соединения [n6] в расчете на один моль соединения [n1], но количество может свободно изменяться в соответствии с условиями реакции.
Примеры растворителя включают амиды кислот, такие как ДМФА, N-метилпирролидин-2-он и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n2] → соединение [n3]
Соединение [n3] может быть получено взаимодействием соединения [n2] с окислителем.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от -20 до 50°С, и время реакции обычно находится в диапазоне от мгновения до 24 часов.
Окислитель представляет собой перкислоты, такие как м-хлорпербензойная кислота и т.д.; и пероксид водорода. Примеры используемого для реакции растворителя включают галогенированные соединения, такие как хлороформ, дихлорметан и т.д.
В данной реакции теоретически необходимы один и два моля окислителя в расчете на один моль соединения [n2], когда n=1 и n=2 соответственно, но количество может свободно изменяться в соответствии с условиями реакции.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n3] → соединение [n4]
Соединение [n4] может быть получено взаимодействием соединения [n3] в присутствии воды и диоксида марганца.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от 50 до 120°С и время реакции обычно находится в диапазоне от мгновения до 24 часов.
Диоксид марганца в данной реакции используется в количестве от каталитического количества до избытка.
Примеры используемого для реакции растворителя включают воду и смеси воды с органическим растворителем (спирты, такие как метанол, этанол, изопропанол и т.д.; кетоны, такие как ацетон, метилэтилкетон, метилизобутилкетон и т.д.; и простые эфиры, такие как тетрагидрофуран, 1,4-диоксан и т.д.).
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n4] получается также взаимодействием соединения [n3] в присутствии воды и тетрабората натрия.
Соединение [n4] → производное пиридона [а]
Производное пиридона [а] может быть получено взаимодействием соединения [n4], где n равно 1, с акролеином в присутствии основания и последующим превращением в присутствии кислоты.
Реакцию обычно осуществляют в растворителе. Температура реакции на первой стадии находится в диапазоне от -20 до 50°С и температура реакции на второй стадии находится в диапазоне от комнатной температуры до 80°С. Время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры используемого для реакции основания включают гидрид натрия, трет-бутоксид калия, гидроксид натрия, карбонат калия, фторид калия и т.д. и примеры кислоты включают уксусную кислоту, трифторуксусную кислоту, метансульфоновую кислоту, п-толуолсульфоновую кислоту, трифторид бора и его комплекс (например, комплекс трифторид бора-метанол). Примеры растворителя включают простые эфиры, такие как диэтиловый эфир, метилтрет-бутиловый эфир, диметоксиэтан, тетрагидрофуран, 1,4-диоксан и т.д.; галогенированные соединения, такие как хлороформ, дихлорметан и т.д.; и углеводороды, такие как толуол и т.д.
В данной реакции теоретически необходимы количества основания и кислоты, равные соответственно от каталитического количества до одного эквивалента и от каталитического количества до избытка, и один моль акролеина в расчете на один моль соединения [n4], но количества могут свободно изменяться в соответствии с условиями реакции.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n4] → соединение [n5]
Соединение [n5] может быть получено взаимодействием соединения [n4], где n равно 2, с акролеином в присутствии основания и последующим превращением в присутствии кислоты.
Реакцию обычно осуществляют в растворителе. Температура реакции первой стадии находится в диапазоне от -20 до 50°С и температура реакции второй стадии находится в диапазоне от комнатной температуры до 50°С. Время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры используемого для реакции основания включают гидрид натрия, трет-бутоксид калия, гидроксид натрия, карбонат калия, фторид калия и т.д. и примеры кислоты включают уксусную кислоту, трифторуксусную кислоту, метансульфоновую кислоту, п-толуолсульфоновую кислоту, трифторид бора и его комплекс (например, комплекс трифторид бора-метанол). Примеры растворителя включают простые эфиры, такие как диэтиловый эфир, метилтрет-бутиловый эфир, диметоксиэтан, тетрагидрофуран, 1,4-диоксан и т.д.; галогенированные соединения, такие как хлороформ, дихлорметан и т.д.; и углеводороды, такие как толуол и т.д.
В данной реакции теоретически необходимы количества основания и кислоты, равные соответственно от каталитического количества до одного эквивалента и от каталитического количества до избытка, и один моль акролеина в расчете на один моль соединения [n4], но количества могут свободно изменяться в соответствии с условиями реакции.
Соединение [n5] → производное пиридона [а]
Производное пиридона [а] может быть получено взаимодействием соединения [n5] в присутствии кислоты.
Реакцию обычно осуществляют в растворителе. Температура реакции находится в диапазоне от 50 до 130°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры кислоты включают уксусную кислоту, трифторуксусную кислоту, метансульфоновую кислоту, п-толуолсульфоновую кислоту, трифторид бора и его комплекс (например, комплекс трифторид бора-метанол). Примеры растворителя включают соединения серы, такие как диметилсульфоксид и т.д.; производные простых эфиров, такие как диметоксиэтан, тетрагидрофуран, 1,4-диоксан и т.д.; и углеводороды, такие как толуол и т.д.
В данной реакции кислота используется в количестве от каталитического количества до избытка.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Кроме того, соединение [n4] получают также следующим способом:
[где R3, R4 и R100 имеют значения, указанные выше]
2-Хлорацетамид → соединение [n7]
Соединение [n7] может быть получено взаимодействием соединения [n10]
NaSR100 [n10]
[где R100 имеет значения, указанные выше] с 2-хлорацетамидом.
Реакцию обычно осуществляют в растворителе. Температура реакции находится в диапазоне от комнатной температуры до 50°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры растворителя включают спирты, такие как метанол, этанол, изопропанол и т.д.; воду и их смеси.
В данной реакции теоретически необходим один моль соединения [n10] в расчете на один моль 2-хлорацетамида, но количество может свободно изменяться в соответствии с условиями реакции.
После реакции саму реакционную смесь концентрируют; или после взаимодействия одного моля 2-хлорацетамида реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n7] → соединение [n8]
Соединение [n8] может быть получено взаимодействием соединения [n7] с хлорирующим реагентом.
Реакцию обычно осуществляют в растворителе. Температура реакции находится в диапазоне от -10 до 30°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры растворителя включают галогенированные соединения, такие как хлороформ, дихлорметан и примеры хлорирующего реагента включают сульфурилхлорид.
В данной реакции теоретически необходим один моль хлорирующего реагента в расчете на один моль соединения [n7], но количество может свободно изменяться в зависимости от условий реакции.
После реакции саму реакционную смесь концентрируют; или после взаимодействия одного моля хлорирующего реагента реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n8] → соединение [n9]
Соединение [n9] может быть получено взаимодействием соединения [n8] с соединением [m1] в присутствии основания и необязательно дополнительно иодидной соли.
Реакцию обычно осуществляют в растворителе. Температура реакции находится в диапазоне от -10 до 80°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры растворителя включают кетоны, такие как ацетон, метилэтилкетон, метилизобутилкетон и т.д.; соединения серы, такие как диметилсульфоксид и т.д.; простые эфиры, такие как диэтиловый эфир, метилтрет-бутиловый эфир, диметоксиэтан, тетрагидрофуран, 1,4-диоксан и т.д.; и углеводороды, такие как толуол. Примеры основания включают гидрид натрия, карбонат калия, бикарбонат натрия, гидроксид натрия и трет-бутоксид калия и примеры иодидной соли включают иодид натрия и иодид калия.
В данной реакции теоретически необходим один моль соединения [m1] в расчете на один моль соединения [n8] и теоретически необходим один моль основания в расчете на один моль соединения [m1], но количества могут свободно изменяться в зависимости от условий реакции.
После реакции саму реакционную смесь концентрируют; или после взаимодействия одного моля соединения [n8] реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n9] → соединение [n4]
Соединение [n4] может быть получено взаимодействием соединения [n9] с окислителем.
Реакцию обычно осуществляют в растворителе. Температура реакции находится в диапазоне от -30 до 50°С, и время реакции обычно находится в диапазоне от мгновения до 24 часов.
Окислитель представляет собой перкислоты, такие как м-хлорпербензойная кислота и т.д.; и пероксид водорода. Примеры используемого для реакции растворителя включают галогенированные соединения, такие как хлороформ, дихлорметан и т.д.
В данной реакции теоретически необходимы один и два моля окислителя в расчете на один моль соединения [n9], когда n=1 и n=2 соответственно, но количество может свободно изменяться в зависимости от условий реакции.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Способ 3 получения
[R4 имеет значение, указанное выше, R31 представляет собой атом галогена или цианогруппу и L1 представляет собой атом фтора или атом хлора]
Соединение [р1] → соединение [р3]
Соединение [р3] может быть получено взаимодействием соединения [р1] и соединения [р2] с основанием, таким как карбонат калия, обычно в растворителе.
Соединение [р3] → соединение [р4]
Соединение [р4] может быть получено взаимодействием соединения [р3] в атмосфере водорода в присутствии катализатора, такого как палладий на угле и т.д., обычно в растворителе или взаимодействием с порошком железа в смешанном растворителе, состоящем из уксусной кислоты и воды.
Соединение [р4] → соединение [р5]
Соединение [р5] может быть получено взаимодействием соединения [р4] с диазотирующим реагентом, таким как нитрит натрия и т.д., и последующего взаимодействия с хлоридом меди, бромидом меди или цианидом меди в растворителе.
Соединение [р5] → соединение [а-1]
Производное пиридона [а], где R3 представляет собой атом галогена или цианогруппу, а именно производное пиридона [а-1], может быть получено взаимодействием соединения [р5] с трибромидом бора, обычно в растворителе.
Соединение [р3] → соединение [а-2]
Производное пиридона [а], где R3 представляет собой нитрогруппу, а именно производное пиридона [а-2], может быть получено взаимодействием соединения [р3] с трибромидом бора, обычно в растворителе.
Соединение [р2] может быть получено следующим способом:
2-Хлор-3-бензилоксипиридин → соединение [р6]
Соединение [р6] может быть получено взаимодействием 2-хлор-3-бензилоксипиридина с метанолом в присутствии