Способ получения суспензий субмикронных частиц
Иллюстрации
Показать всеИзобретение относится к области фармацевтики и касается способа получения субмикронных частиц водонерастворимого или плохо водорастворимого органического фармацевтического соединения путем растворения этого соединения в смешиваемом с водой первом растворителе, смешивания полученного раствора со вторым растворителем для создания предсуспензии и гомогенизации полученной предсуспензии или воздействия на нее ультразвуком. Способ позволяет получить частицы размером менее 2 мкм. 2 н. и 30 з.п. ф-лы, 18 ил., 2 табл.
Реферат
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Техническая область
Данное изобретение относится к препарату фармацевтически активного соединения. Более конкретно, данное изобретение относится к производству наносуспензий фармацевтически активного соединения для парентеральной или оральной доставки.
Известный уровень техники
Существует все увеличивающееся число лекарственных веществ, которым нужно создать лекарственную форму и которые плохо растворимы или нерастворимы в водных растворах. Такие лекарственные вещества представляют проблемы в отношении их доставки в инъецируемой форме, такой как посредством парентерального введения. Лекарственные вещества, которые нерастворимы в воде, могут обладать значительными преимуществами, когда изготовлены в виде стабильных суспензий субмикронных частиц. Точный контроль размера частиц является существенным для безопасности и эффективного использования этих препаратов. Частицы должны быть менее семи микрон диаметром для безопасного прохода через капилляры, не вызывая эмболии (Allen et al., 1987; Davis and Taube, 1978; Schroeder et al., 1978; Yokel et al., 1981).
Один из подходов к доставке нерастворимого лекарственного вещества описан в патенте США № 2745785. В данном патенте описан способ получения кристаллов пенициллина G, пригодных для парентерального введения. Данный способ включает стадию перекристаллизации пенициллина G из раствора формамида путем добавления воды для снижения растворимости пенициллина G. B патенте '785 дополнительно раскрывается, что частицы пенициллина G могут быть покрыты увлажняющими веществами, такими как лецитин, или эмульгаторами, поверхностно-активными и пеноуничтожающими веществами, или неполными сложными эфирами высших жирных кислот и сорбитана или полиоксиалкилена и их производными, или арилалкилполиэфирами спиртов или их солями. В патенте '785 дополнительно описано микронизирование пенициллина G с помощью струи воздуха под давлением с образованием кристаллов, находящихся в интервале от примерно 5 до 20 микрон.
Другой подход описан в патенте США № 5118528, в котором описан способ получения наночастиц. Данный способ включает стадии (1) получения жидкой фазы вещества в растворителе или смеси растворителей, к которым могут быть добавлены одно или более поверхностно-активных веществ, (2) получения второй жидкой фазы нерастворителя или смеси нерастворителей, причем нерастворитель является смешиваемым с растворителем или смесью растворителей для данного вещества, (3) добавления вместе растворов (1) и (2) при перемешивании и (4) удаления нежелательных растворителей с получением коллоидной суспензии наночастиц. В патенте '528 описано, что получаются частицы вещества менее 500 нм без подачи энергии. В частности, в патенте '528 установлено, что нежелательно использовать высокоэнергоемкое оборудование, такое как ультразвуковые излучатели и гомогенизаторы.
В патенте США № 4826689 описан метод получения частиц однородного размера из нерастворимых в воде лекарств или других органических соединений. Сначала соответствующее твердое органическое вещество растворяют в органическом растворителе, и раствор может быть разбавлен нерастворителем. Затем вливают водную осаждающую жидкость, осаждают неагрегированные частицы с одинаковым (однородным) по существу средним диаметром. Затем частицы отделяют от органического растворителя. В соответствии с данным изобретением, в зависимости от органического соединения и требуемого размера частиц, параметры температуры, отношения нерастворителя к органическому растворителю, скорость вливания, скорость перемешивания и объем могут изменяться. В патенте '689 раскрывается, что при данном процессе образуется лекарственное вещество в метастабильном состоянии, которое является термодинамически нестабильным и которое, в конечном счете, превращается в более стабильное кристаллическое состояние. В патенте '689 описано отделение лекарственного вещества в метастабильном состоянии, при котором свободная энергия занимает место между энергией раствора исходного лекарственного вещества и стабильной кристаллической формы. В патенте '689 описано использование ингибиторов кристаллизации (например, поливинилпирролидона) и поверхностно-активных веществ (например, поли(оксиэтилен)-со-оксипропилен) для получения осадка, достаточно стабильного для выделения центрифугированием, мембранной фильтрацией или обратным осмосом.
В патентах США №№ 5091188; 5091187 и 4725442 описываются (а) или покрытие мелких частиц лекарственного вещества природными или синтетическими фосфолипидами, или (b) растворение лекарственного вещества в подходящем липофильном носителе и формирование эмульсии, стабилизированной природными или полусинтетическими фосфолипидами. Один из недостатков этих подходов состоит в том, что они зависят от качества сырьевого материала лекарственного вещества, и не раскрываются стадии изменения морфологии сырьевого материала для приведения данного материала в хрупкое, более легкое для обработки состояние.
Другой подход для получения нерастворимых лекарственных веществ для парентеральной доставки описан в патенте США № 5145684. В патенте '684 описан влажный размол нерастворимого лекарственного вещества в присутствии модификатора поверхности для получения частиц лекарственного вещества, имеющих средний эффективный размер частиц менее 400 нм. В патенте '684 подчеркивается нежелательность использования каких-либо растворителей в этом способе. В патенте '684 описан модификатор поверхности, который адсорбируется на поверхности частицы лекарственного вещества в количестве, достаточном для предотвращения агломерации в более крупные частицы.
Еще одна попытка получить нерастворимые лекарственные средства для парентеральной доставки описана в патенте США №5992355. В патенте '355 описано получение частиц субмикронного размера нерастворимых лекарственных веществ с использованием комбинации модификаторов поверхности и фосфолипида с последующим снижением размера частиц при использовании таких методик, как обработка ультразвуком, гомогенизация, размол, микрофлюидизация, осаждение или перекристаллизация. В патенте '355 нет описания изменения условий процесса для получения кристаллов в более хрупкой форме.
В патенте США № 5780062 описан способ получения мелких частиц нерастворимых лекарственных веществ путем (1) растворения лекарственного вещества в смешиваемом с водой первом растворителе, (2) получения второго раствора полимера и амфифильного вещества во втором водном растворителе, в которой лекарство по существу нерастворимо, посредством чего образуется полимеро/амфифильный комплекс и (3) смешивания растворов с первой и второй стадий для осаждения агрегата лекарственного вещества и полимеро/амфифильного комплекса.
В патенте США № 5858410 описана фармацевтическая наносуспензия, пригодная для парентерального введения. В патенте '410 описана гомогенизация под высоким давлением в поршневом щелевом гомогенизаторе, по меньшей мере, одного твердого терапевтически активного соединения, диспергированного в растворителе, с образованием частиц, имеющих средний диаметр, определенный с помощью фотонной корреляционной спектроскопии (ФКС), равный от 10 до 1000 нм, причем доля частиц более 5 мкм от всего их числа составляет менее 0,1% (число распределения, определяемое с помощью счетчика частиц), без предварительного превращения в расплав, причем активное соединение является твердым при комнатной температуре и нерастворимо, только слабо растворимо или умеренно растворимо в воде, водной среде и/или органических растворителях. В примерах в патенте '410 описано струйное измельчение перед гомогенизацией.
В патенте США № 4997454 описан способ изготовления частиц однородного размера из твердых соединений. Способ по патенту '454 включает стадии растворения твердого соединения в подходящем растворителе с последующим вливанием осаждающей жидкости, причем осаждаются неагрегированные частицы с по существу однородным средним диаметром. Затем частицы отделяют от растворителя. В патенте '454 создаются помехи образованию частиц в кристаллическом состоянии, так как во время процедуры осаждения кристаллы могут растворяться и перекристаллизовываться, расширяя тем самым интервал распределения частиц по размеру. В патенте '454 поддерживаются условия во время процедуры осаждения для улавливания частиц в метастабильном состоянии.
В патенте США № 5605785 описан способ получения наноаморфных дисперсий, пригодных для фотографии соединений. Способ получения наноаморфных дисперсий включает любой известный способ эмульгирования, который дает дисперсную фазу, имеющую аморфные частицы.
КРАТКОЕ ИЗЛОЖЕНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение предлагает способ получения частиц субмикронного размера органического соединения, растворимость которого больше в смешиваемом с водой первом растворителе, чем во втором растворителе, который является водным. Данный способ включает стадии (i) растворения органического соединения в смешиваемом с водой первом растворителе с образованием раствора, причем первый растворитель выбирается из группы, состоящей из N-метил-2-пирролидинона, 2-пирролидона, диметилсульфоксида, диметилацетамида, молочной кислоты, метанола, этанола, изопропанола, 3-пентанола, н-пропанола, глицерина, бутиленгликоля, этиленгликоля, пропиленгликоля, моно- и диацилированных моноглицеридов, диметилизосорбида, ацетона, диметилформамида, 1,4-диоксана, полиэтиленгликоля, сложных эфиров полиэтиленгликоля, полиэтиленгликольсорбитанов, моноалкилэфиров полиэтиленгликоля, полипропиленгликоля, полипропиленальгината, ППГ-10 бутандиола, эфира ППГ-10 и метилглюкозы, эфира ППГ-20 и метилглюкозы, стеарилового эфира ППГ-15, пропиленгликоля дикаприлага, пропиленгликоля дикапрата, пропиленгликоля лаурата; (ii) смешивания раствора со вторым растворителем для создания предсуспензии (предварительной суспензии) и (iii) подвода энергии к предсуспензии для образования частиц, имеющих средний эффективный размер частиц менее чем примерно 2 мкм.
Способ получения частиц субмикронного размера органического соединения, растворимость которого больше в смешиваемом с водой первом растворителе, чем во втором растворителе, который является водным, причем способ включает стадии (i) растворения органического соединения в смешиваемом с водой первом растворителе с получением раствора, причем первый растворитель выбирается из группы, состоящей из N-метил-2-пирролидинона, 2-пирролидона, диметилсульфоксида, диметилацетамида, молочной кислоты, метанола, этанола, изопропанола, 3-пентанола, н-пропанола, глицерина, бутиленгликоля, этиленгликоля, пропиленгликоля, моно- и диацилированных моноглицеридов, диметилизосорбида, ацетона, диметилформамида, 1,4-диоксана, этилацетата, пропилацетата, полиэтиленгликоля, сложных эфиров полиэтиленгликоля, полиэтиленгликольсорбитанов, моноалкилэфиров полиэтиленгликоля, полипропиленгликоля, полипропиленальгината, ППГ-10 бутандиола, эфира ППГ-10 и метилглюкозы, эфира ППГ-20 и метилглюкозы, стеарилового эфира ППГ-15, пропиленгликоля дикаприлата, пропиленгликоля дикапрата, пропиленгликоля лаурата; (ii) смешивания раствора со вторым растворителем для создания предсуспензии, где органическое соединение находится в аморфной форме, полукристаллической форме или в виде переохлажденной жидкости, как определено ДСК, и имеющей средний эффективный размер частиц, и (iii) отжига предсуспензии с образованием частиц, имеющих по существу тот же самый средний эффективный размер частиц предсуспензии и в более стабильной форме.
Данное изобретение дополнительно предлагает способ получения частиц субмикронного размера органического соединения, растворимость которого больше в смешиваемом с водой первом растворителе, чем во втором растворителе, который является водным. Данный способ включает стадии (i) растворения органического соединения в смешиваемом с водой первом растворителе с образованием раствора, причем первый растворитель выбирается из группы, состоящей из N-метил-2-пирролидинона, 2-пирролидона, диметилсульфоксида, диметилацетамида, молочной кислоты, метанола, этанола, изопропанола, 3-пентанола, н-пропанола, глицерина, бутиленгликоля, этиленгликоля, пропиленгликоля, моно- и диацилированных моноглицеридов, диметилизосорбида, ацетона, диметилформамида, 1,4-диоксана, полиэтиленгликоля, сложных эфиров полиэтиленгликоля, полиэтиленгликольсорбитанов, моноалкилэфиров полиэтиленгликоля, полипропиленгликоля, полипропиленальгината, ППГ-10 бутандиола, эфира ППГ-10 и метилглюкозы, эфира ППГ-20 и метилглюкозы, стеарилового эфира ППГ-15, пропиленгликоля дикаприлата, пропиленгликоля дикапрата, пропиленгликоля лаурата; (ii) смешивания раствора со вторым растворителем для создания предсуспензии частиц в хрупкой форме и (iii) подвода энергии к предсуспензии для образования частиц, имеющих средний эффективный размер частиц менее чем примерно 2 мкм.
Данное изобретение также предлагает способ получения суспензии фармацевтически активного соединения, растворимость которого больше в смешиваемом с водой первом органическом растворителе, чем во втором растворителе, который является водным. Способ включает стадии (i) растворения первого количества фармацевтически активного соединения в смешиваемом с водой первом органическом растворителе с образованием первого раствора; (ii) смешивания первого раствора со вторым растворителем для осаждения фармацевтически активного соединения; (iii) затравливание (внесение затравки) первого раствора или второго растворителя или предсуспензии. Способ дополнительно включает стадию формирования требуемого полиморфа фармацевтически активного соединения. В предпочтительной форме данного изобретения стадия затравливания включает стадию добавления затравочного соединения в первый раствор, во второй растворитель и/или в предсуспензию.
Данное изобретение, кроме того, предлагает способ получения суспензии фармацевтически активного соединения, растворимость которого больше в смешиваемом с водой первом растворителе, чем во втором растворителе, который является водным. Данный способ включает стадии (i) добавления некоторого количества фармацевтически активного соединения в первый органический растворитель для создания пересыщенного раствора, (ii) старения пересыщенного раствора для формирования обнаруживаемых кристаллов для получения затравочной смеси и (iii) смешивания затравочной смеси со вторым растворителем для осаждения фармацевтически активного соединения для создания предсуспензии.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
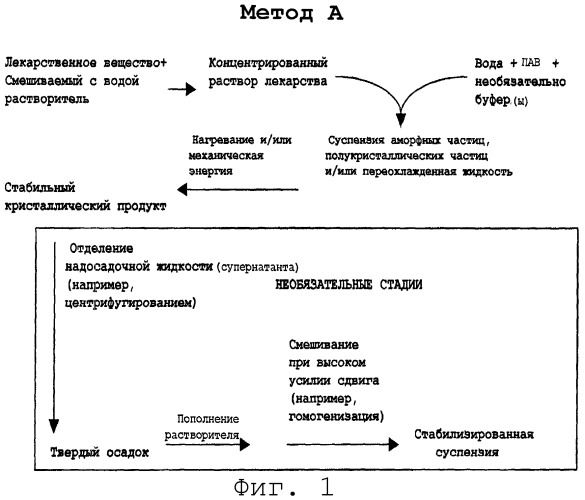
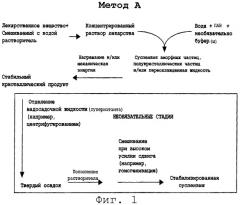
На фиг.1 и 2 представлены два варианта способов: А и В.
На фиг.3 представлены аморфные частицы перед гомогенизацией (пример 1).
На фиг.4 представлены частицы после отжига гомогенизацией.
На фиг.5 представлена рентгеновская дифрактограмма микроосажденного итраконазола с полиэтиленгликоль-660-12-гидроксистеаратом до и после гомогенизации (пример 5).
На фиг.6 представлены кристаллы карбамазепина перед гомогенизацией (пример 6).
На фиг.7 представлены микрочастицы карбамазепина после гомогенизации (Avestin С-50).
На фиг.8 представлена диаграмма способа микроосаждения для преднизолона (примеры 9-12).
На фиг.9 представлена микрофотография суспензии преднизолона перед гомогенизацией (модуляция контраста по Гофману, увеличение 1250х).
На фиг.10 представлена микрофотография суспензии преднизолона после гомогенизации (модуляция контраста по Гофману, увеличение 1250х).
На фиг.11 представлено сравнение распределения по размеру наносуспензий (данное изобретение) и коммерческой масляной эмульсии (пример 13).
На фиг.12 представлена порошковая рентгенограмма сырьевого материала итраконазола (верхний) и SMP-2-PRE (нижний) по примеру 16. Картина сырьевого материала смещена вверх для ясности.
На фиг.13а представлены данные ДСК сырьевого материала итраконазола (пример 16).
На фиг.13b представлены данные ДСК для SMP-2-PRE (пример 16).
На фиг.14 представлены данные ДСК для SMP-2-PRE, показывающие плавление менее стабильного полиморфа при нагревании до 160°С, явление перекристаллизации при охлаждении и последующее плавление более стабильного полиморфа при повторном нагревании до 180°С (пример 16).
На фиг.15 представлено сравнение образцов SMP-2-PRE после гомогенизации(пример 16). Сплошная линия = образец после затравливания сырьевым материалом итраконазола. Пунктирная линия = образец без затравливания. Сплошная линия смещена на 1 Вт/г для ясности.
На фиг.16 представлен эффект затравливания во время осаждения (пример 17). Пунктирная линия = образец без затравливания, сплошная линия = образец после затравливания сырьевым материалом итраконазола. Данные для образца без затравливания (пунктирная линия) сдвинуты вверх на 1,5 Вт/г для ясности.
На фиг.17 представлены эффект затравливания концентрата лекарственного вещества посредством старения. Верхняя рентгенограмма лучей относится к кристаллам, полученным из свежего концентрата лекарственного вещества, и соответствует стабильному полиморфу (см. фиг.12, верхний). Нижний вид относится к кристаллам, полученным для подвергнутого старению (затравленного) концентрата лекарственного вещества и соответствует метастабильному полиморфу (см. фиг.12, нижний). Верхний вид сдвинут вверх для ясности (пример 18).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение допускает осуществление во многих различных формах. Предпочтительные варианты осуществления данного изобретения описаны при понимании того, что данное описание должно рассматриваться в качестве иллюстраций принципов данного изобретения и не предназначено для ограничения аспектов данного изобретения в широком смысле до проиллюстрированных вариантов осуществления.
Данное изобретение предлагает методы и способы формирования частиц органического соединения, имеющих средней эффективный размер частиц, подходящий для парентерального введения, и в наиболее предпочтительной форме данного изобретения, равен менее примерно 2 мкм. Данное изобретение также пригодно для получения частиц органического соединения в форме, пригодной для орального введения. Размер частиц для оральных лекарственных форм может быть свыше 2 мкм и обычно менее примерно 7 мкм. Однако частицы могут превышать 7 мкм при условии, что частицы обладают достаточной биодоступностью и другими свойствами оральной лекарственной формы. Оральные лекарственные формы включают таблетки, капсулы, каплеты, мягкие и твердые гелевые капсулы или другие носители для доставки лекарственного вещества при оральном введении.
Способы могут быть разделены на три основных вида. Каждый из видов способов имеет стадии (1) растворения органического соединения в смешиваемом с водой органическом растворителе для получения первого раствора, (2) смешивания первого раствора со вторым водным растворителем для осаждения органического соединения для получения предсуспензии и (3) подача энергии к предсуспензии в виде перемешивания с высоким усилием сдвига или нагревания для получения стабильной формы органического соединения, имеющего желаемые пределы размера, указанные выше.
Три вида способов отличаются по физическим свойствам органического соединения, что определено исследованием с помощью дифракции рентгеновского излучения, исследованием дифференциальной сканнирующей калориметрией или другим подходящим исследованием, проводимым перед стадией подведения энергии и после стадии подведения энергии. При способе первого вида перед стадией подведения энергии органическое соединение в предсуспензии принимает аморфную форму, полукристаллическую форму или форму переохлажденной жидкости и имеет средний эффективный размер частиц. После стадии подачи энергии органическое соединение находится в кристаллической форме, имеющей средний эффективный размер частиц по существу такой же, как и размер в предсуспензии (т.е. от менее примерно 2 мкм).
При способе второго вида перед стадией подведения энергии органическое соединение находится в кристаллической форме и имеет средний эффективный размер частиц. После стадии добавления энергии органическое соединение находится в кристаллической форме, имеющей по существу тот же самый средний эффективный размер частиц, что и перед стадией добавления энергии, но кристаллы после стадии подведения энергии менее способны агрегировать. Более низкая склонность органического соединения агрегировать наблюдается с помощью рассеяния лазерного динамического света и световой микроскопии.
При третьем виде способа перед стадией подачи энергии органическое соединение находится в кристаллической форме, которая является хрупкой и имеет средний эффективный размер частиц. Под термином «хрупкая» подразумевается то, что частицы являются хрупкими и легче ломаются на более мелкие частицы.
После стадии подачи энергии органическое соединение находится в кристаллической форме, имеющей средний эффективный размер частиц, меньший, чем у кристаллов предсуспензии. Пользуясь стадиями, необходимыми для приведения органического соединения в кристаллическую форму, которая является хрупкой, последующая стадия подачи энергии может быть проведена более быстро и эффективно, по сравнению с органическим соединением с менее хрупкой кристаллической морфологией.
Стадия подачи энергии может быть осуществлена любым способом, при котором предсуспензия подвергается воздействию сил кавитации, сдвига или удара. В одной из предпочтительных форм изобретения стадия подачи энергии является стадией обжига. Отжиг в данном изобретении определяется как процесс превращения вещества, которое термодинамически нестабильно, в более стабильную форму путем единственного или повторного применения энергии (прямого нагревания или механического воздействия) с последующей тепловой релаксацией. Это снижение энергии может быть достигнуто превращением твердой формы из менее упорядоченной в более упорядоченную кристаллическую структуру. Альтернативно эта стабилизация может совершаться переупорядочением молекул поверхностно-активных веществ на поверхности раздела жидкости и твердого вещества.
Эти три вида способов (процессов) будут обсуждены отдельно ниже. Должно быть понятно, однако, что условия процесса, такие как выбор поверхностно-активных веществ или комбинация поверхностно-активных веществ, количество используемого поверхностно-активного вещества, температура реакции, скорость перемешивания растворов, скорость осаждения и тому подобное, могут выбираться так, чтобы дать возможность обработки любого лекарственного вещества при использовании любого одного из видов, обсуждаемых далее.
Способы первого вида, а также способы второго и третьего вида могут быть дополнительно разделены на два подвида, метод А и В, представленные в виде диаграммы на фиг.1 и 2.
Органическое соединение для использования в способе данного изобретения является любым органическим химическим соединением, растворимость которого снижается от одного растворителя к другому. Данное органическое соединение могло бы быть фармацевтически активным соединением из разных групп, таких как, но не ограничиваясь ими, антигиперлипидемические средства, антимикробные средства, например антибактериальные средства, такие как сульфадиазин, противогрибковые средства, такие как итраконазол; нестероидные противовоспалительные средства, например индометацин; антигиперхолестеринемические средства, например пробукол, и стероидные соединения, например дексаметазон; иммунодепрессанты, например циклоспорин А, такролимус и микофенолят мофетил. Или органическое соединение могло бы быть из группы, используемой в качестве адъювантов или эксципиентов в фармацевтических препаратах и косметических средствах, таких как, но не ограничиваясь этим, консерванты, например пропилпарабен.
Первый растворитель по данному изобретению является растворителем или смесью растворителей, в которых органическое соединение, представляющее интерес, является относительно растворимым, и которые смешиваются со вторым растворителем. Примеры таких растворителей включают, но не ограничиваются этим, поливинилпирролидон, N-метил-2-пирролидон (также называемый N-метил-2-пирролидин), 2-пирролидон, диметилсульфоксид, диметилацетамид, молочная кислота, метанол, этанол, изопропанол, 3-пентанол, н-пропанол, глицерин, бутиленгликоль (бутандиол), этиленгликоль, пропиленгликоль, моно- и диацилированные моноглицериды (такие как глицерилкаприлат), диметилизосорбид, ацетон, диметилформамид, 1,4-диоксан, полиэтиленгликоль (например, ПЭГ-4, ПЭГ-8, ПЭГ-9, ПЭГ-12, ПЭГ-14, ПЭГ-16, ПЭГ-120, ПЭГ-75, ПЭГ-150, сложные эфиры полиэтиленгликоля (например, такие как ПЭГ-4 дилаурат, ПЭГ-20 дилаурат, ПЭГ-6 изостеарат, ПЭГ-8 пальмитостеарат, ПЭГ-150 пальмитостеарат), полиэтиленгликольсорбитаны (такие как ПЭГ-20 сорбитанизостеарат), моноалкиловые простые эфиры полиэтиленгликоля (например, такие как диметиловый эфир ПЭГ-3, диметиловый эфир ПЭГ-4), полипропиленгликоль (ППГ), полипропиленальгинат, ППГ-10 бутандиол, простой эфир ППГ-10 и метилглюкозы, простой эфир ППГ-20 и метилглюкозы, простой стеариловый эфир ППГ-15, пропиленгликоля дикаприлат/дикапрат, пропиленгликоля лаурат.
Метод А
В способе А (см. фиг.1) органическое соединение («лекарство») сначала растворяют в первом растворителе с получением первого раствора. Органическое соединение может быть добавлено в количестве от примерно 0,1% (вес/об) до примерно 50% (вес/об), в зависимости от растворимости органического соединения в первом растворителе. Для обеспечения полного растворения соединения в первом растворителе может быть необходимо нагревание концентрата от примерно 30°С до примерно 100°С.
Второй водный раствор получают с добавлением к нему одного или более необязательных поверхностно-активных модификаторов, таких как анионное поверхностно-активное вещество (ПАВ), катионное ПАВ, неионное ПАВ или биологические поверхностно-активные молекулы. Подходящие анионные ПАВ включают, но не ограничиваются этим, лаурат калия, лаурилсульфат натрия, додецилсульфат натрия, сульфаты алкилполиоксиэтилена, альгинат натрия, диоктилнатрия сульфосукцинат, фосфатидилхолин, фосфатидилглицерин, фосфатидилинозин, фосфатидилсерин, фосфатидную кислоту и ее соли, сложные эфиры глицерина, натрийкарбоксиметилцеллюлозу, холевую кислоту и другие желчные кислоты (например, холевая кислота, дезоксихолевая кислота, гликохолевая кислота, таурохолевая кислота, гликодезоксихолезая кислота и ее соли (например, дезоксихолат натрия и т.д.). Подходящие катионные ПАВ включают, но не ограничиваются этим, соединения четвертичного аммония, такие как бензалкония хлорид, цетилтриметиламмония бромид, лаурилдиметилбензиламмония хлорид, ацилкарнитина гидрохлориды или алкилпиридиния галогениды. В качестве анионных ПАВ можно использовать фосфолипиды. Подходящие фосфолипиды включают, например, фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, фосфатидилинозин, фосфатидилглицерин, фосфатидная кислота, лизофосфолипиды, яичный или соевый фосфолипид или их сочетание. Фосфолипид может быть солевой или обессоленный, гидрированный или частично гидрированный, или природный, полусинтетический или синтетический.
Подходящие неионные ПАВ включают простые эфиры полиоксиэтилена и жирных спиртов (Macrogol и Brij), сложные эфиры полиоксиэтиленсорбитана и жирных кислот (полисорбаты), сложные эфиры полиоксиэтилена и жирных кислот (Myrj), сложные эфиры сорбитана (спен. Span), глицерина моностеарат, полиэтиленгликоли, полипропиленгликоли, цетиловый спирт, цетостеариловый спирт, стеариловый спирт, арилалкилполиэфирные спирты, полиоксиэтиленополиоксипропиленовые сополимеры (полоксамеры), полаксамины, метилцеллюлоза, гидроксицеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, некристаллическая целлюлоза, полисахариды, включая крахмал и производные крахмала, такие как гидроксиэтилкрахмал (ГЭК, HES), поливиниловый спирт и поливинилпирролидон. В предпочтительном варианте данного изобретения неионное ПАВ является сополимером полиоксиэтилена и полиоксипропилена и предпочтительно блоксополимером пропиленгликоля и этиленгликоля. Такие полимеры продаются под торговым названием «Poloxamer» (полоксамер), иногда также называемым PLURONIC® (плуроник), и продаются несколькими поставщиками, включая Spectrum Chemical and Ruger. В сложные эфиры полиоксиэтилена и жирных кислот включены и те, которые имеют короткие алкильные цепи. Одним из примеров такого ПАВ является SOLUTOL® HS 15 (солутол HS 15), полиэтилен-660-гидроксистеарат, производимый фирмой BASF Aktiengesellschaft.
Поверхностно-активные биологические молекулы включают такие молекулы, как альбумин, казеин, гепарин, гирудин и другие подходящие белки.
Может быть также желательно добавлять рН регулирующее средство ко второму раствору, такое как гидроксид натрия, соляную кислоту, трис-буфер или цитрат, ацетат, лактат, меглумин и тому подобное. Второй раствор должен иметь рН в интервале от примерно 3 до примерно 11.
Для оральных лекарственных форм могут использоваться один или более из следующих эксципиентов: желатин, казеин, лецитин (фосфатиды), камедь акации, холестерин, трагакант, стеариновая кислоты, бензалкония хлорид, стеарат кальция, глицерилмоностеарат, цетостеариловый спирт, цетомакроголевый эмульгирующий воск, сложные эфиры сорбитана, полиоксиэтиленалкиловые эфиры, например простые эфиры макрогола, такие как цетомакрогол 1000, производные полиоксиэтилена и касторового масла, сложные эфиры полиоксиэтиленсорбитана и жирных кислот, например доступные для приобрегения твины ТМ, полиэтиленгликоли, полиоксиэтиленстеараты, коллоидный силикондиоксид, фосфаты, додецилсульфат натрия, кальцийкарбоксиметилцеллюлоза, натрийкарбоксиметилцеллюлоза, метилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, фталат гидроксипропилметилцеллюлозы, некристаллическая целлюлоза, алюмосиликат магния, триэтаноламин, поливиниловый спирт (PVA, ПВС) и поливинилпирролидон (ПВП). Большинство из этих эксиципиентоз подробно описаны в Handbook of Pharmaceutical Excipients, опубликованном совместно American Pharmaceutical Association и The pharmaceutical Society of Great Britain, The Pharmaceutical Press, 1986. Модификаторы поверхности коммерчески доступны и/или могут быть получены методами, известными в данной области. Два или более модификаторов поверхности можно использовать в комбинации.
В предпочтительном варианте данного изобретения способ получения частиц органического соединения субмикронного размера включает стадии добавления первого раствора ко второму раствору. Скорость добавления зависит от размера партии и кинетики осаждения органического соединения. Обычно для процесса небольшого лабораторного масштаба (получения 1 литра) скорость добавления составляет от примерно 0,05 см3 в минуту до примерно 10 см3 в минуту. Во время добавления растворы должны постоянно перемешиваться. С помощью световой микроскопии наблюдали, что при изготовлении предсуспензии образуются аморфные частицы, полукристаллические вещества или переохлажденные жидкости. Данный способ дополнительно включает стадию проведения отжига предсуспензии для превращения аморфных частиц, переохлажденной жидкости или полукристаллического твердого вещества в кристаллическое более стабильное твердое состояние. Полученные частицы будут иметь средний эффективный размер частиц, который измеряли методами динамического рассеяния света (например, фотокорреляционной спектроскопией, лазерной диффракцией, рассеяния лазерного излучения при низком угле падения (LALLS), рассеивания лазерного света при среднем угле падения (MALLS), методы матирования света (например, метод Coulter), методом реологии или микроскопии (световой или электронной), в интервалах, представленных выше.
Стадия подведения энергии включает поставку энергии посредством воздействия ультразвуком, гомогенизации, гомогенизации в противотоке, микроожижения или другими методами получения усилия удара, сдвига или сил кавитации. Образец может охлаждаться или нагреваться во время этой стадии. В одном из предпочтительных вариантов данного изобретения стадия отжига осуществляется с помощью поршневого щелевого гомогенизатора, такого как продаваемый фирмой Avestin Inc. в виде продукта под названием EmulsiFlex-C160. В другом предпочтительном варианте данного изобретения отжиг может выполняться путем обработки ультразвуком с использованием ультразвукового процессора, такого как Vibra-Cell Ultrasonic Processor (600 Вт), производимого Sonics and Materials, Inc. В еще одном предпочтительном варианте данного изобретения отжиг может выполняться путем применения аппарата для эмульгирования, как описано в патенте США № 5720551, который включен в описание в виде ссылки и составляет часть этого.
В зависимости от скорости отжига может быть желательно регулировать температуру обрабатываемого образца до уровня в интервале от примерно -30 до 30°С. Альтернативно, чтобы выполнить желаемое фазовое изменение у обрабатываемого твердого вещества, может быть также необходимо нагреть предсуспензию до температуры в интервале от примерно 30°С до примерно 100°С во время стадии отжига.
Метод В
Метод 3 отличается от метода А в следующих отношениях.
Первое отличие состоит в том, что ПАВ или комбинацию ПАВ добавляют в первый раствор. ПАВ могут быть выбраны из групп анионных, неионных и катионных ПАВ, представленных выше.
Сравнительный пример метода А и метода В и US 5780062
В патенте США № 5780062 описан способ получения мелких частиц органического соединения путем первоначального растворения соединения в подходящем смешиваемом с водой первом растворителе. Второй раствор получают растворением полимера и амфифильного соединения в водном растворе. Первый раствор затем добавляют во второй раствор с образованием осадка, который состоит из органического соединения и комплекса полимер-амфифильное соединение. В патенте '062 не описано использования стадии подведения энергии из данного изобретения в методах А и В. Об отсутствии стабильности обычно свидетельствует быстрая агрегация и рост частиц. В некоторых случаях аморфные частицы перекристаллизовывались в виде больших кристаллов. Подведение энергии к предсуспензии способом, описанным выше, обычно дает частицы, которые проявляют сниженную скорость агрегации и роста частиц, а также отсутствие перекристаллизации при хранении продукта.
Методы А и В, кроме того, отличаются от способа патента '062 отсутствием стадии формирования комплекса полимер-амфифильное соединение перед осаждением. В методе А такой комплекс не может формироваться, так как никакого полимера не добавляется к растворителю (водной фазе). В методе В ПАВ, которое может также действовать как амфифильное соединение, или полимер, растворяют с органическим соединением в первом растворителе. Это предотвращает формирование любых комплексов амфифильного соединения-полимера перед осаждением. В патенте '062 успешное осаждение мелких частиц зависит от образования комплекса амфифильного соединения-полимера перед осаждением. В патенте '062 описано, что комплекс амфифильного соединения-полимера образует агрегаты во втором водном растворе. В патенте '062 объясняется, что гидрофобное органическое соединение взаимодействует с комплексом амфифильного соединения-полимера, снижая тем самым растворимость этих агрегатов и вызывая осаждение. В данном изобретении было продемонстрировано, что добавление ПАВ или полимера в первый раствор (метод В) приводит, при последующем добавлении во второй раствор, к формированию более однородных, более тонких частиц, чем те, которые получают по способу, описанному в патенте '062.
С этой целью были получены и проанализированы два препарата. При каждом из получений этих препаратов имеется два раствора, концентрат и водный растворитель, которые смешивают вместе и затем обрабатывают ультразвуком. Концентрат при каждом изготовлении содержит органическое соединение (итраконазол), смешиваемый с водой растворитель (N-метил-2-пирролидинон или NMP) и, возможно, полимер (полоксамер 188). Водный растворитель содержит воду, трис-буфер и, возможно, полимер (полоксамер 188) и/или ПАВ (дезо