Полипептид ожирения (ов)(варианты), его аналог (варианты) и слитый белок (варианты), изолированная молекула нуклеиновой кислоты, молекула днк, рекомбинантный вектор клонирования, рекомбинантный вектор экспрессии, фармацевтическая композиция, моноклональное и поликлональное антитело
Иллюстрации
Показать всеИзобретение относится к области биотехнологии и может быть использовано в медицине при диагностике и лечении патологических состояний, связанных с нарушением регуляции веса тела человека, а также в животноводстве и ветеринарии. В изобретении раскрыты аминокислотные последовательности двух изоформ полипептида ожирения (ОВ) человека, обладающих способностью модулировать вес тела животного, их предшественники, содержащие сигнальный пептид, аналоги, получаемые в результате вставок, делеции и аминокислотных замен, которые сохраняют активность, присущую немодифицированным формам ОВ-полипептидов, а также поликлональные и моноклональные антитела, специфически взаимодействующие с новыми модуляторами веса тела. Охарактеризованы последовательности ДНК, кодирующие названные полипептиды и их аналоги; описаны содержащие эти последовательности векторные конструкции, с помощью которых получены рекомбинантные формы полипептидов OB по изобретению. Предлагается использовать новые полипептиды и их аналоги в качестве активного начала в фармацевтических композициях. Применение настоящего изобретения может внести существенный вклад в решение задачи обеспечения медицины, ветеринарии и животноводства эффективным средством для снижения веса тела. 18 с. и 5 з.п., 35 ил., 12 табл.
Реферат
ОБЛАСТЬ ИСПОЛЬЗОВАНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение в целом относится к контролированию веса млекопитающих, включая животных и человека, и более конкретно, к реагентам, которые идентифицированы здесь как модуляторы веса, а также к диагностическому и терапевтическому применению модуляторов.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ УРОВЕНЬ ТЕХНИКИ
Ожирение рассматривается как избыток жировых отложений по отношению к мышечной массе тела и связано со многими важными физиологическими и медицинскими нарушениями, в том числе гипертензией, повышенным содержанием липидов в крови, диабетом типа II или инсулин-независимым сахарным диабетом (NIDDM). В США NIDDM страдают 6-10 млн человек, включая 18% населения в возрасте около 65 лет (Harris et al., Int. J. Obes., 11: 275-283 (1987)). Примерно 45% мужчин и 70% женщин, больных NIDDM, страдают от ожирения, и тяжесть их заболевания существенно снижается или элиминируется при уменьшении веса (Harris, Diabetes Care, 14 (3): 639-648 (1991)). Как описано ниже, и NIDDM, и ожирение строго наследуются несмотря на то, что гены предрасположенности к данным заболеваниям еще не идентифицированы. Молекулярно-генетические процессы, лежащие в основе указанных метаболических нарушений, составляют важную, плохо изученную проблему.
Ассимиляция, запасание и использование энергии питательных веществ образуют сложную гомеостатическую систему, обеспечивающую выживание многоклеточных организмов. Среди наземных млекопитающих запасание в жировой ткани больших количеств метаболического «топлива» в форме триглицеридов является критическим фактором выживания в условиях нехватки пищи. Необходимость поддержания определенного уровня запасов энергии без постоянных изменений размеров и формы тела требует достижения заданного равновесия между потреблением и расходом энергии. Однако молекулярные механизмы, регулирующие энергетический баланс, остаются неизученными. Получение молекул, которые передают информацию о питательных компонентах и контролируют энергетический баланс, является ключевым моментом понимания механизмов регулирования веса тела, столь важных для развития заболеваний и поддержания здоровья.
Степень ожирения индивидуума в значительной степени генетически детерминирована. Изучение соответствия веса тела и ожирения у монозиготных и дизиготных близнецов и их биологических родителей позволяет предположить, что степень наследования ожирения (0.4-0.8) превышает соответствующие величины для других нарушений, в развитие которых (как считается общепринятым) вовлечен значимый генетический компонент, например шизофрении, алкоголизма и атеросклероза (StunKard et al., N. Engl. J. Med., 322: 1483-1487 (1990)). Сообщалось также о семейном сходстве в уровнях расходования энергии (Bogardus et al., Diabetes, 35: 1-5 (1986)). Генетический анализ в географически ограниченных популяциях позволяет высказать предположение, что относительно небольшое количество генов может обусловливать 35-50% вариации состава тела (Moll et al., Am. J. Hum. Genet., 49: 1243-1255 (1991)). Однако ни один из генов, ответственных за ожирение в популяции в целом, не картирован в каком-либо хромосомальном локусе.
Модели ожирения на грызунах включают семь явных мутаций в отдельных генах. Наиболее изученными у мышей мутациями, связанными с ожирением, являются мутации в ob (ожирение)- и db (диабет)-генах. При функционировании на одном генетическом фоне гены ob и db приводят к возникновению метаболически и поведенчески неразличимых фенотипов, позволяя предположить, что указанные гены могут функционировать сходным физиологическим путем (Coleman et al., Diabetologia, 14: 141-148, 1978). Мыши, гомозиготные по двум мутациям, отличаются гиперфагичностью и гипометаболизмом, что приводит к фенотипу ожирения, выявляемому в возрасте одного месяца. Вес этих животных стабилизируется на уровне 60-70 г (в сравнении с 30-35 г у контрольных животных). Ob и db животные обнаруживают огромное число других гормональных и метаболических нарушений, которые определенным образом мешают выявить первичный дефект, обусловленный мутацией (Bray et al., Am. J. Clin. Nutr., 50: 891-902 (1989)).
Каждая из моделей ожирения на грызунах характеризуется изменениями углеводного метаболизма, напоминающими диабет типа II у человека. В некоторых случаях тяжесть диабета частично зависит от фона, свойственного данной линии мышей (Leiter, Endocrinology, 124: 912-922 (1989)). Как у ob, так и у db конгенных мышей C57BL/Ks развивается тяжелый диабет с некрозом b-клеток и атрофией островков, что приводит к относительной инсулинопении. В противоположность этому ob и db конгенные мыши C57BL/6J характеризуются транзиторным инсулин-устойчивым диабетом, который полностью компенсируется гипертрофией b-клеток, свойственной диабету типа II человека.
Фенотип ob и db мышей при сопоставлении с ожирением у человека проявляется иным образом, чем развитие диабета. Мутантные мыши едят больше и тратят меньше энергии, чем контрольные животные (так же, как и люди, страдающие ожирением). Такой фенотип практически совпадает с фенотипом животных с нарушениями вентромедиального гипоталамуса. Это позволяет предположить, что обе мутации способны взаимодействовать со способностью надлежащим образом объединять или отвечать на информацию о питательных компонентах в пределах центральной нервной системы. В поддержку этой гипотезы свидетельствуют результаты экспериментов по парабиозу (Coleman, Diabetologia, 9: 294-298 (1973)), из которых следует, что ob мыши дефектны по циркулирующему в крови фактору насыщения, а db мыши устойчивы к воздействиям ob фактора (возможно за счет дефекта ob-рецептора). Указанные эксперименты позволяют заключить, что ожирение у мутантных мышей может являться результатом различных дефектов в афферентной петле и/или интегрированном центре механизма обратной связи, контролирующем состав тела.
При использовании молекулярных и классических генетических маркеров ob и db гены картированы на проксимальной хромосоме 6 и средней хромосоме 4 соответственно (Bahary et al., Proc. Natl. Acad. Sci. USA, 87: 8642-8646 (1990); Friedman et al., Genomics, 11: 1054-1062 (1991)). В обоих случаях мутации картированы в участках мышиного генома, аналогичных таковым человека, позволяя предположить, что если существуют человеческие аналоги ob и db, они с большей вероятностью будут картированы на хромосомах человека 7q и 1р соответственно. Дефекты гена db могут приводить к ожирению других видов млекопитающих: в генетических сращиваниях между крысами Zucker fa/fa и крысами Brown Norway +/+ мутация fa (хромосома 5 крысы) фланкирована тем же самым локусом, который фланкирует db-ген мыши (Truett et al., Proc. Natl. Acad. Sci. USA, 88: 7806-7809 (1991)).
Поскольку многочисленные факторы влияют на вес тела, практически невозможно предсказать, какие факторы и, что более важно, какие гомеостатические механизмы в первую очередь определяют вес тела. Таким образом, принципиальная проблема, лежащая в основе настоящего изобретения, связана с получением модуляторов веса тела, которые обеспечивают контроль ожирения и содержания жира у млекопитающих.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В соответствии с настоящим изобретением проблема контроля ожирения и содержания жира у животных, особенно у млекопитающих, решается посредством получения полипептидов ожирения (OB) и молекул нуклеиновых кислот, кодирующих указанные полипептиды. Настоящее изобретение относится в первую очередь к выделенным полипептидам, полезным для модуляции, т.е, контроля и регулирования веса тела и ожирения, а также к нуклеиновым кислотам, кодирующим указанные полипептиды, которые не только обеспечивают возможность получения рекомбинантных полипептидов OB, но и сами по себе могут использоваться для модуляции веса тела.
Полипептиды ожирения (ОВ), согласно настоящему изобретению имеющие примерно от 145 до около 167 аминокислот, способны к модуляции веса тела животных, в особенности млекопитающих, и включают аллельные варианты или аналоги, в том числе фрагменты, обладающие сходной биологической активностью. Полипептиды могут быть получены рекомбинантным путем или в результате химического синтеза. Предпочтительные полипептиды ОВ включают соединения, имеющие аминокислотные последовательности SEQ ID NOS: 2, 4, 5 или 6 или их аллельные варианты или аналоги, в том числе фрагменты.
Имуногенные фрагменты полипептидов ОВ согласно данному изобретению включают: Val-Pro-Ile-Gln-Lys-Val-Gln-Asp-Asp-Thr-Lhs-Thr-Leu-Ile-Lys-Thr (SEQ ID NO:18); Leu-His-Pro-Ile-Leu-Ser-Leu-Ser-Lys-Met-Asp-GIn-Thr-Leu-Ala (SEQ ID NO:19); Ser-Lys-Ser-Cys-Ser-Leu-Pro-Gln-Thr-Ser-Gly-Leu-Gln-Lys-Pro-Glu-Ser-Leu-Asp (SEQ ID NO:20); и Ser-Arg-Leu-Gln-Gly-Ser-Leu-Gln-Asp-Ile-Leu-Gln-Gln-Leu-Asp-Val-Ser-Pro-Glu-Cys (SEQ ID NO:21). Аналоги полипептида ОВ человека имеют аминокислотные последовательности SEQ ID NOS: 4 и 6 при том, что одна или более аминокислот в положениях 53, 56, 71, 85, 89, 92, 95, 98, 110, 118, 121, 122, 126, 127, 128, 129, 132, 157, 159, 163 и 166 (в соответствии с нумерацией последовательности SEQ ID NO:4) замещены другими аминокислотами, такими как дивергентные аминокислоты полипептида ОВ мыши, в соответствии с SEQ ID NO:2 или аланин. Указанные аналоги также включают следующие: (а) остаток серина в положении 53 замещен на глицерин, аланин, валин, цистеин, метионин или треонин; (б) остаток серина в положении 98 замещен на глицин, аланин, валин, цистеин, метионин или треонин; и (в) остаток аргинина в положении 92 замещен на аспарагин, лизин, гистидин, глутамин, глутаминовую кислоту, аспарагиновую кислоту, серин, треонин, метионин или цистеин. Аналог полипептида ОВ в соответствии с изобретением предпочтительно на 83% и более гомологичен по аминокислотной последовательности полипептиду ОВ с аминокислотной последовательностью SEQ ID NO:2, 4, 5 или 6. Дополнительные аналоги полипептида ОВ человека в соответствии с данным изобретением имеют аминокислотные последовательности SEQ ID NOS: 4 и 6 при том, что: (а) один или более остатков аспарагиновой кислоты замещены глутаминовой кислотой; (б) один или более остатков изолейцина замещены лейцином; (в) один или более остатков глицина или валина замещены аланином; (г) один или более остатков аргинина замещены на гистидин; (д) один или более остатков тирозина или фенилаланина замещены на триптофан; (е) один или более остатков в положениях 121-128 (в соответствии с нумерацией последовательности SEQ ID NO:4) замещены на глицин или аланин и (ж) один или более остатков в положениях 54-60 или 118-166 (в соответствии с последовательностью SEQ ID NO:4) замещены на лизин, глутаминовую кислоту, цистеин или пролин. Предпочтительные усеченные аналоги полипептидов ОВ человека, согласно настоящему изобретению, включают следующие соединения (в соответствии с нумерацией последовательности SEQ ID NO:4): (а) один или более остатков в положениях 121-128 делетированы; (б) остатки 1-116 делетированы; (в) остатки 1-21 и 54-167 делетированы; (в) остатки 1-21 и 54-167 делетированы; (г) остатки 1-60 и 117-167 делетированы; (д) остатки 1-60 делетированы; (е) остатки 1-53 делетированы и (ж) аналог в соответствии с (а) при том, что остатки 1-21 делетированы. Полипептиды ОВ и аналоги полипептида ob, полученые согласно настоящему изобретению, утратившие 21 аминокислоту сигнальной последовательности (например, аминокислоты 1-21 последовательности SEQ ID NO:4), могут иметь N-концевую аминокислоту или аминокислотную последовательность, такую как (1) метионин, (2) глицин-серин-гистидин-метиониновую последовательность (SEQ ID NO:38), (3) метионин-глицин-серин-серин-гастидин-гистидин-гистидин-гистидин-гистидин-гистидин-серин-серин-глицин-лейцин-валин-пролин-аргинин-глицин-серин-гистидин-метиониновую последовательность (SEQ ID NO:98), (4) лейцин-глутаминовая кислота-лизин-аргинин-глутаминовая кислота-аланин-глутаминовая кислота-аланиновую последовательность (SEQ ID NO:26), (5) глутаминовая кислота-аланин-глутаминовая кислота-аланиновую последовательность (SEQ ID NO:27), (6) лейцин-глутаминовая кислота-лизин-аргининовую последовательность (SEQ ID NO:28), (7) метионин-глицин-серин-серин-гистилин-гистидин-гистидин-гистидин-гистидин-гистидин-серин-серин-глицин-лейцин-валин-пролин-аргинин-глицин-серин-пролиновую последовательность (SEQ ID NO:99) и (8) глицин-серин-пролиновую последовательность.
Производные полипептида ОВ в соответствии с изобретением имеют одну или более прикрепленных химических групп, включая водорастворимые полимеры, такие как полиэтиленгликоль. Производные, полученные с помощью полиэтиленгликоля, могут быть моно-, ди-, три- или тетрапэгированными, например, монопэгированы на N-концевом участке.
Предпочтительные монопэгированные на N-концевом участке производные полипептидов ob, согласно настоящему изобретению, включают полипептиды OB, содержащие аминокислотные остатки 22-167 последовательности SEQ ID NO:4 или остатки 22-166 последовательности SEQ ID NO:6 и факультативно содержащие (пэгированный) метионин в положении 21.
Выделенные молекулы нуклеиновых кислот, полученные согласно настоящему изобретению, кодируют полипептид OB, аллельный вариант или аналог, в том числе фрагменты, как описано выше. Особо важные ДНК-молекулы для использования с целью обеспечения безопасной экспрессии полипептида ОВ обладают биологической активностью, модулирующей вес тела млекопитающих, и выбраны из группы, включающей: (а) ДНК- молекулы с последовательностями SEQ ID NO:1 и 3 или их фрагменты, (б) ДНК-молекулы, способные гибридизоваться с ДНК-молекулами, определенными в (а) или с их фрагментами, и (в) ДНК-молекулы, определяющие экспрессию аминокислотной последовательности, кодируемую любой из указанных выше ДНК-молекул. Примерами таких молекул служат геномные ДНК-молекулы с последовательностями SEQ ID NOS: 22 и 24. Предпочтительные ДНК-молекулы, согласно настоящему изобретению, кодируют полипептид, имеющий следующую аминокислотную последовательность: (a) SEQ ID NO:2, (б) аминокислоты 22-167 последовательности SEQ ID NO:2, (в) SEQ ID NO:4, (г) аминокислоты 22-167 последовательности SEQ ID NO:4, (д) SEQ ID NO:5, (e) аминокислоты 22-166 последовательности SEQ ID NO:5, (ж) SEQ ID NO:6 и (з) аминокислоты 22-166 последовательности SEQ ID NO:6. Кроме того, указанные ДНК-молекулы кодируют полипептиды, имеющие N-концевую аминокислоту или аминокислотную последовательность, приведенную ранее. Например, предпочтительная ДНК-молекула имеет последовательность, представленную как белок-кодирующая последовательность SEQ ID NO:3, и, в особенности, последовательность, кодирующая аминокислоты 22-167.
Кроме того, изобретение относится к нуклеиновым кислотам с выявляемой меткой, которые гибридизуются с заявленными нуклеиновыми кислотами. Такие нуклеиновые кислоты, в частности, гибридизуются с некодирующим участком нуклеиновой кислоты OB, выбранным из группы, включающей интрон, 5'-некодирующий участок и 3'-некодирующий участок. Настоящее изобретение также относится к олигонуклеотилным праймерам для амплификации геномной ДНК человека, кодирующей полипептид ob, например, олигонуклеотилам 29-32 последовательности SEQ ID NOS:29.
Заявленные согласно настоящему изобретению векторы содержат ДНК-молекулу, полученную в соответствии с изобретением, как описано выше, и предпочтительно представляют собой векторы экспрессии, включающие ДНК-молекулу, функционально связанную с последовательностью, контролирующей экспрессию. Одноклеточные клетки-хозяева в соответствии с изобретением трансформированы или трансфицированы ДНК-молекулами или векторами, описанными выше. Предпочтительные клетки-хозяева включают бактерии, дрожжи, клетки млекопитающих, клетки растений, клетки насекомых и клетки человека в культуре тканей. Например, такие клетки-хозяева выбирают из группы, включающей Е. Coli, Pseudomonas, Bacillus, Streptomyces, дрожжи, СНО-, R1.1-, B-W-, L-M-, COS 1-, COS7-, BSC1-, BSC40-, ВМТ10- и Sf9-клетки. Предпочтительными дрожжевыми хозяевами являются Saccharomyces, Pichia, Candida, Hansenula u Torulopsis. Объектом изобретения являются также клетки млекопитающих, содержащие ДНК-последовательность, кодирующую полипептид ob, и модифицированные in vitro для облегчения повышенной экспрессии полипептида ob путем гомологичной рекомбинации, при которой происходит встраивание регуляторной последовательности экспрессии в функциональной близости от последовательности, кодирующей полипептид ob. Регуляторная последовательность экспрессии может быть соответствующей последовательности для полипептида ob или нет и способна замещать мутантную регуляторную последовательность полипептида ob в клетке.
Настоящее изобретение относится также к способам получения полипептида ob, включающим: (а) культивирование клетки, описанной выше, в условиях, обеспечивающих экспрессию полипептида ob, и (б) выделение экспрессированного полипептида. Указанная процедура может сопровождаться следующими стадиями: (в) хроматографией полипептида на Ni-хелатирующей колонке и (г) очисткой полипептида путем гель-фильтрации. В предпочтительном варианте осуществления изобретения после стадии (в) и перед стадией (г) осуществляют хроматографию полипептида ob на сильной катионообменной колонке.
Настоящее изобретение относится также к меченным и немеченным моноклинальным и поликлональным антителам, специфическим к заявленным полипептидам ob, и бессмертным клеточным линиям, продуцирующим моноклонные антитела в соответствии с изобретением. Получение антител, согласно настоящему изобретению, включает следующие стадии: (а) конъюгацию полипептида ob с белком-носителем, (б) иммунизацию животного-хозяина конъюгатом «фрагмент полипептида ob/белок-носитель», полученным на стадии (а) и смешанным с адъювантом, и (в) выделение антитела из иммунизированного животного-хозяина.
Изобретение относится к способам определения присутствия полипептида OB в образце, включающим: (а) контактирование образца, предпочтительно содержащего полипептид OB, с антителом (предпочтительно связанным с твердой подложкой), которое специфически связывается с полипептидом OB в условиях, обеспечивающих образование реакционных комплексов, содержащих антитело и полипептид ОВ, и (б) выявление образования реакционных комплексов, содержащих антитело и полипептид ob, в образце при том, что выявление образования реакционных комплексов свидетельствует о присутствии полипептида ОВ в образце. Соответственно изобретение относится к способам оценки in vitro уровня полипептида OB в биологическом образце, включающим: (а) выявление образования реакционных комплексов в биологическом образце в соответствии со способом, описанным выше, и (б) оценку количества образовавшихся реакционных комплексов, которое соответствует уровню полипептида OB в биологическом образце. Когда выявляют или диагностируют заболевание, ассоциированное с повышенным или пониженным уровнем полипептида OB в соответствии с изобретением, оценку уровня проводят, как описано выше, и выявленное значение сравнивают со значением уровня полипептида OB у здоровых индивидуумов или же у данного индивидуума в более раннее время. Увеличение уровня полипептида ОВ по сравнению с нормальным или предшествующим уровнем свидетельствует о наличии заболевания, ассоциированного с повышенным уровнем полипептида OB, а снижение уровня полипептида OB по сравнению с нормальным свидетельствует о наличии заболевания, ассоциированного с пониженным уровнем полипептида OB. Соответственно в объем изобретения включены способы мониторинга in vitro терапевтического лечения заболевания млекопитающего, ассоциированного с повышенным или пониженным уровнем полипептида ОВ, предусматривающие оценку уровня полипептида ОВ (как описано выше) в серии биологических образцов, полученных в различные временные точки от млекопитающего, подвергающегося указанному терапевтическому лечению.
Полученные согласно настоящему изобретению фармацевтические композиции содержат полипептид ОВ, описанный выше, и фармацевтически приемлемый носитель и используются при осуществлении терапевтических способов для снижения веса тела животного. Дополнительные фармацевтические композиции, полученные согласно настоящему изобретению для использования при осуществлении терапевтических способов с целью увеличения веса тела животного, содержат антагонист полипептида ОВ, предпочтительно выбранный из группы, включающей: антитело, которое связывается с полипептидом ОВ и нейтрализует его активность, фрагмент полипептида ob, который связывается с рецептором полипептида ОВ, но не активирует его, и небольшую молекулу-антагонист полипептида OB. Кроме того, изобретение относится к соответствующим косметическим композициям, улучшающим внешний вид тела, для снижения или увеличения веса тела индивидуума, которые используются при осуществлении косметических процедур, улучшающих внешний вид тела индивидуума. Такие косметические композиции используются в количественной дозе, достаточной для моделирования веса тела индивидуума до заданного уровня.
Изобретение также относится к применению молекул нуклеиновых кислот, полученных согласно настоящему изобретению, а также молекул антисмысловых нуклеиновых кислот, способных гибридизоваться с нуклеиновой кислотой, кодирующей заявленный полипептид OB, для приготовления медикамента, модифицирующего вес тела животного (например, для генной терапии). Кроме того, изобретение относится к применению полипептида ОВ или соответствующего антагониста для получения медикамента, модифицирующего вес тела животного. Полученные таким образом медикаменты могут использоваться для модификации веса тела млекопитающего в процессе лечения заболевания, выбранного из группы, включающей диабет, высокое кровяное давление и повышенный уровень холестерина. Такая модификация является частью комбинированной терапии данного заболевания с помощью соответствующих лекарственных препаратов. Указанные выше медикаменты могут быть применимы в терапевтических способах внутривенным, внутриартериальным, интраперитонеальным, внутримышечным, подкожным, назальным, оральным или пульмональным путем.
Приведенные в настоящем описании сведения показывают, что полипептиды ОВ, полученные согласно данному изобретению, именно в такой форме первоначально секретируются из адипоцитов млекопитающих и функционируют по типу гормонов.
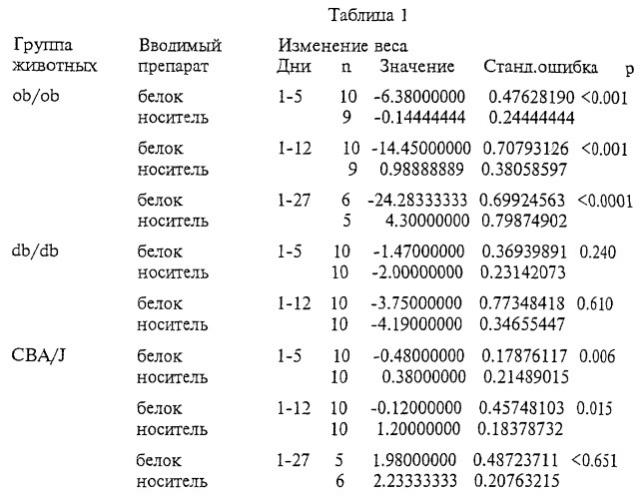
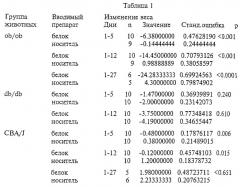
Приведенные примеры показывают, что полипептид ОВ, альтернативно обозначенный «лептином» циркулирует в плазме крови мыши, крысы и человека. Лептин отсутствует в плазме крови мышей ob/ob и обнаруживается в десятикратных концентрациях в плазме крови db/db-мышей и в двадцатикратных концентрациях в плазме крови крыс fa/fa. Более того, ежедневные инъекции рекомбинантного лептина существенно уменьшают массу тела ob/ob-мышей, в значительной степени влияют на вес тела мышей дикого типа и не оказывают эффекта на мышей db/db.
Кроме того, полипептид ob одного вида животного биологически активен в организме животного другого вида. В особенности, полипептид ОВ активен в организме мышей.
В первую очередь, модуляторы, заявленные согласно настоящему изобретению, включают молекулы нуклеиновых кислот, в том числе молекулы рекомбинантных ДНК (например, кДНК, или вектора, содержащего кДНК, или выделенной геномной ДНК) или клонированные гены (т.е. выделенные геномные ДНК) или их варианты, полученные на основе вырожденности генетического кода, которые кодируют полипептиды, являющиеся модуляторами контроля веса тела, как описано ниже, или консервативные варианты или фрагменты таких полипептидов, в особенности фрагменты полипептидов, утративших сигнальный пептид (альтернативно называемых здесь зрелыми полипептидами ОВ). Указанные полипептиды имеют аминокислотные последовательности, приведенные на фиг. 1А-Е (SEQ ID NO:2), фиг. 3 (SEQ ID NO:4), фиг. 5 (SEQ ID NO:5) и фиг. 6 (SEQ ID NO:6). В особом варианте осуществления изобретения получают аминокислотные последовательности для ob-полипептидов человека и мыши. Оба полипептида обнаруживаются в форме, утратившей глутамин в положении 49, что может являться следствием аномального сплайсинга мРНК. Полипептиды ОВ различных видов животных могут обладать высокой степенью гомологии. Как показано на фиг. 4, полипептиды ОВ человека и мыши обладают более чем 80%-ной гомологией.
Молекулы нуклеиновых кислот, рекомбинантные ДНК-молекулы или клонированные гены могут иметь нуклеотидные последовательности или могут быть комплементарны ДНК-кодирующими последовательностям, приведенным на фиг. 1А-Е (SEQ ID NO:1) и фиг. 2А и В (SEQ ID NO:3). В частности, такие ДНК-молекулы могут быть молекулами кДНК или геномными ДНК, выделенными из хромосом. Нуклеиновые кислоты, полученные в соответствии с изобретением, могут также соответствовать 5'- и 3'-фланкирующим последовательностям ДНК и интронным ДНК-последовательностям. В связи с этим настоящее изобретение относится также к идентификации нуклеиновой кислоты, имеющей нуклеотидную последовательность, выбранную из группы, включающей последовательности на фиг. 1А-Е (SEQ ID NO:1) и фиг. 2А и В (SEQ ID NO:3), а также их варианты, полученные с учетом вырожденности генетического кода, аллельные варианты и подобные им родственные молекулы.
В соответствии с настоящим изобретением молекулы нуклеиновой кислоты могут быть ДНК и РНК, в том числе их синтетические варианты, имеющие фосфат или аналог фосфата, например, тиофосфатные связи. При этом указанные молекулы могут быть как одноцепочечные, так и двухцепочечные.
Изобретение также относится к молекулам нуклеиновой кислоты, используемым в качестве молекулярных проб или праймеров для амплификации с помощью полимеразной цепной реакции (PCR), т.е. к природным или синтетическим олигонуклеотидам, имеющим последовательность, соответствующую участку последовательностей, приведенных на фиг. 1А -Е (SEQ ID NO:1), фиг. 2А и В (SEQ ID NO:3) и фиг. 20А-С (SEQ ID NO:22), или 5'- и 3'-фланкирующим последовательностям кодирующих последовательностей или интронным последовательностям геномной ДНК. В частности, изобретение относится к молекуле нуклеиновой кислоты, имеющей по крайней мере около 10 нуклеотидов, при том что последовательность молекулы нуклеиновой кислоты соответствует нуклеотидной последовательности из того же количества нуклеотидов в нуклеотидных последовательностях, представленных на фиг. 1А-Е (SEQ ID NO:1), фиг. 2А и В (SEQ ID NO:3) и фиг. 20А-С (SEQ ID NO:22) или последовательности, комплементарной указанным. Более предпочтительно, последовательность молекулы нуклеиновой кислоты имеет по крайней мере 15 нуклеотидов. Наиболее предпочтительно, последовательность нуклеиновой кислоты имеет по крайней мере 20 нуклеотидов. В одном варианте осуществления изобретения, когда олигонуклеотид используется в качестве пробы, он содержит выявляемую метку, например радионуклидную (такую, как 32P) или ферментную.
Далее изобретение относится к клонирующему вектору, содержащему заявленные нуклеиновые кислоты, кодирующие полипептид ob, а также к вектору экспрессии, активному в клетках бактерий, насекомых или млекопитающих, содержащему заявленные нуклеиновые кислоты, а также к вектору экспрессии, активному в клетках бактерий, насекомых или млекопитающих, содержащему заявленные нуклеиновые кислоты, кодирующие полипептид ob, функционально связанные с последовательностью, контролирующей экспрессию. Соответственно изобретение относится к клетке-хозяину, например бактериальной, дрожжевой, клетке насекомых или млекопитающих, трансфицированной или трансформированной подходящим вектором экспрессии, а также к применению указанных выше конструктов для получения модуляторов согласно изобретению.
Изобретение также относится к антителам, которые связываются с полипептидом ob. Такие антитела могут быть получены к полипептиду полной длины или его антигенным фрагментам. В одном случае такие антитела ингибируют функциональную активность полипептида ob. В другом случае антитела могут использоваться для определения уровня циркулирующего полипептида ob в плазме крови или сыворотке. Кроме того, антитела, специфичные по отношению к какому-либо участку полипептида ОВ, в частности моноклональные антитела, могут использоваться в качестве «структурных» проб данного полипептида.
Все описанные выше соединения могут рассматриваться как модуляторы веса тела и содержания жира и, таким образом, могут использоваться различным образом, как указано выше. В частности, изобретение может найти диагностические и терапевтические применения, а также использоваться в сельском хозяйстве. В основе таких применений лежит использование описанных выше модуляторов, в том числе молекул нуклеиновых кислот и пептидов. Более того, модуляция веса тела подразумевает применение специфических терапевтических подходов таким образом, что ожирение или, наоборот, кахексия, отражающие нежелательные в организме нарушения, могут быть скорригированы применением одного или более модуляторов, полученных согласно настоящему изобретению.
Таким образом, изобретение относится к способу модулирования веса тела млекопитающих, включающему контролирование экспрессии белка, кодируемого нуклеиновой кислотой, имеющей нуклеотидную последовательность, выбранную из группы, включающей последовательность, приведенную на фиг. 1А-Е (SEQ ID NO:1), фиг. 2А и В (SEQ ID NO:3), а также их аллельные варианты и варианты, полученные на основе вырожденности генетического кода. Такой контроль может оказаться эффективным путем введения заявленных нуклеотидов при генной терапии в жировые клетки больного или какого-либо хозяина для контроля или редукции ожирения. В противоположность этому, получение и применение антагонистов данных нуклеотидов, например антисмысловых молекул, может оказаться полезным для устранения нарушений, включающих избыточную потерю веса, например, нервозной анорексии, рака или СПИДа, в отношении которых проводится лечение. Указанные антагонисты могут быть введены сходным образом с нуклеотидами непосредственно в жировые клетки для достижения заданных изменений.
Соответственно белки, определенные с помощью фиг. 1А-Е, 3, 5 и 6 (SEQ ID NO:1, SEQ ID NO:4, SEQ ID NO:5 и SEQ ID NO:6), их консервативные варианты, активные фрагменты и родственные небольшие молекулы могут быть получены для непосредственного применения с терапевтическими целями для редукции или контроля избытка жира или веса тела. Антитела и другие антагонисты указанных белков, например, их фрагментов, могут быть получены и сходным образом применены для достижения обратного эффекта. В связи с этим изобретение относится к фармацевтическим композициям, содержащим заявленный полипептид ОВ или, альтернативно, его антагонист в смеси с фармацевтически приемлемым носителем или наполнителем.
Кроме того, полученный согласно изобретению полипептид ОВ может быть использован для обеспечения косметических эффектов, например улучшения внешнего вида тела за счет редукции жировых отложений. Полипептид ОВ может использоваться независимо или в комплексе с другими косметическими методиками, например хирургическими, для достижения желаемых результатов.
Диагностические применения указанных нуклеотидов и соответствующих пептидов также подразумевают использование нуклеиновых кислот для идентификации возможных мутаций или аллельных вариантов указанных соединений с целью расширения набора активных нуклеотидных молекул, полезных в диагностике и терапии. В частности, гомозиготные и гетерозиготные мутации нуклеотидов могут быть идентифицированы в количественном отношении и более точно свидетельствовать о каком-либо нарушении, выявляя возможную степень риска индивидуумов, связанную с ожирением. Более точно, гетерозиготные мутации в настоящее время рассматриваются как ассоциированные со слабой или средней степенью ожирения, в то время как гомозиготные мутации ассоциированы с более выраженным и тяжелым ожирением. Соответствующее ДНК-тестирование может быть осуществлено при использовании вышеуказанных соединений в качестве маркеров уровня для получения точного долговременного прогноза определенных тенденций, так чтобы оказались возможным предсказать изменения в питании и других индивидуальных привычках индивидуума или характер непосредственного терапевтического вмешательства для устранения заданных нарушений.
Диагностическое применение настоящего изобретения включает способы определения присутствия и уровня заявленных модуляторов в клеточных образцах или биологических экстрактах (или образцах), полученных от соответствующих индивидуумов, так что может быть установлено содержание в таких тестируемых образцах нуклеиновых кислот (геномной ДНК или мРНК) и/или белка. Принимая во внимание, что увеличенная активность нуклеиновой кислоты и наличие соответствующего белка отражает способность организма ингибировать ожирение, врач, анализирующий полученные результаты такого рода исследований больного, страдающего ожирением, будет иметь возможность заключить, что причиной ожирения скорее является дисфункция, а не наличие или повышенная активность нуклеиновой кислоты, полученной согласно данному изобретению. В противоположность этому, пониженные уровни нуклеиновой кислоты и/или экспрессируемого белка позволяют предположить, что такие уровни могут быть повышены для лечения данного типа ожирения, и необходимо применить соответствующую терапевтическую систему.
Кроме того, нуклеотиды, представленные на Фиг.1А-Е и 2А и В, относятся к кДНК, которая, как вкратце указано выше, используется для определения соответствующей РНК. Сходным образом, рекомбинантные белки, соответствующие полипептидам на Фиг.1А-Е и 3, получают и надлежащим образом метят для использования, например, в радиоиммунологических анализах с целью определения содержания полипептида ОВ в плазме крови или же с целью определения содержания уровня ОВ-рецептора в тканях, скажем, в тканях гипоталамуса. Далее, изобретение относится не только к идентификации нуклеотидов и соответствующих белков, но и к выявлению рецепторов данных соединений. В данном контексте, полипептиды, представленные на Фиг.1А-Е, 3, 5 и/или 6, могут быть получены и использованы для скрининга соответствующей экспрессионной библиотеки для выделения активных рецепторов. Затем рецепторы могут быть клонированы и сами по себе или в комплексе с лигандом использованы для отбора небольших молекул, способных проявлять сходную активность по отношению к модуляторам.
Изобретение также относится к фармацевтическим композициям, содержащим некоторые из указанных модуляторов, предпочтительно полипептиды с последовательностями, представленными SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:5 и SEQ ID NO:6, а также соответствующие антитела, небольшие молекулы агонистов и антагонистов или активные фрагменты, находящиеся в форме, пригодной для различных способов введения при необходимой терапии. Такие рецепторы могут включать фармацевтически приемлемые носители или другие адъюванты и быть использованы в эффективной дозе, которая определяется специалистом в каждом конкретном случае.
В соответствии с изложенным, наиболее важным объектом настоящего изобретения являются модуляторы веса тела, полученные в очищенной форме, которые обладают определенными характеристиками и свойствами, позволяющими контролировать и наменять степень ожирения и содержания жира у млекопитающих.
Другие объекты настоящего изобретения относятся к способам определения и выявления модуляторов контроля веса, как здесь указано, с целью эффективной диагностики и мониторинга патологических состояний, когда вариации в уровне таких модуляторов являются или могут быть прогнозом на будущее.
Объектом изобретения также являются способ и соответствующая аналитическая система для скрининга соединений, например лекарственных препаратов, реагентов и т.д., которые обладают потенциальной возможностью имитировать или ингибировать активность модуляторов, полученных согласно данному изобретению, у млекопитающих.
Еще одним объектом изобретения является способ воздействия на млекопитающих для контроля веса тела и содержания жира и/или способ лечения некоторых патофизиологических состояний, для которых аномальный вес тела (повышенный или пониженный) является характерным признаком.
Объектом изобретения также являются генетические конструкции для использования в генно-терапевтических методиках и/или фармацевтические композиции для соответствующих терапевтических методик, которые содержат или основаны на одном или более модуляторе, связывающем агенте или реагенте, способном контролировать образование модуляторов или же имитировать или противодействовать их активности.
Другие объекты и преимущества настоящего изобретения для специалиста в данной области исследований очевидным образом следуют из приведенного описания, которое подкрепляется ссылками на соответствующие фигуры.