Лекарственное средство (настойка мелиссы), обладающее седативным и противовоспалительным действием
Иллюстрации
Показать всеИзобретение относится к созданию седативного и противовоспалительного средства растительного происхождения для лечения различных заболеваний. Средство, обладающее седативным и противовоспалительным действием, содержит спиртовую настойку травы мелиссы лекарственной (Melissea officinalis L.), полученную при соотношении сырья и экстрагента 1:5 и содержащую фенилпропаноиды в пересчете на розмариновую кислоту, при следующем соотношении ингредиентов в готовой настойке, мас.%: фенилпропаноиды в пересчете на розмариновую кислоту 0,1-0,9, экстрактивные вещества травы мелиссы лекарственной 1,0-5,5, 35-45% спирт этиловый остальное. Средство не обладает раздражающим и сенсибилизирующим действием и не токсично. 18 табл., 2 ил.
Реферат
Изобретение относится к химико-фармацевтической промышленности, к средству на основе экстрактивных веществ растительного происхождения, используемого в качестве седативного и противовоспалительного средства для лечения различных заболеваний, вызываемых вирусными и микробными инфекциями.
Все существующие препараты на основе Мелиссы лекарственной (Melissea officinalis L.), зарубежные аналоги и препараты, в состав которых входит мелисса, дорогостоящие, что значительно ограничивает возможности их широкого применения в медицинской практике.
В настоящее время отмечается тенденция к росту уровня психопатологических расстройств, особенно различных психогенных невротических нарушений. В России сложившуюся ситуацию потенциируют различные социально-психологические и биологические факторы (социально-экономические проблемы, глобальная информационная перенасыщенность, хроническая усталость, экологическая ситуация, ухудшение качества жизни), что приводит к дистрессу, проявляющемуся повышенной утомляемостью, снижением работоспособности, раздражительностью, напряженностью, тревогой, снижением настроения, потерей привычных интересов, немотивированными страхами, нарушением сна.
В настоящее время для лечения невротических состояний наиболее оптимальными являются седативные средства. Повышенный интерес к седативным препаратам со стороны пациентов и врачей обусловлен возможностью самолечения, простотой дозировки, минимум противопоказаний и побочных эффектов. Эти свойства обусловлены, в первую очередь, растительным происхождением большинства компонентов, относительно невысокой концентрацией активных веществ (в комплексных седативных препаратах), что практически исключает возможность передозировки, а также широким спектром показаний к их применению: легкие неврозы, проблемы с засыпанием, повышенная возбудимость, невростения.
Психоседативные препараты должны снижать ощущение тревоги, обладать успокаивающим эффектом, проявляя при этом минимальное действие на двигательную и мыслительную функции. Степень угнетения ЦНС, вызванная этими средствами, должна быть минимальной. Указанным требованиям наиболее соответствуют седативные препараты растительного происхождения.
Основной задачей современной фитотерапии является внедрение в медицинскую практику максимального количества стандартизированных фитофармацевтических средств (в том числе обладающих седативным эффектом) с подтвержденным действием и дозировкой. По данным экспертов ВОЗ и ЕС, несмотря на успехи синтетической химии, считается целесообразным реализация программ по разработке и производству стандартизированных эффективных и безопасных лекарственных средств на основе накопленного опыта традиционной и современной медицины мира.
Оптимальный методологический подход при разработке современных лекарственных средств природного происхождения заключается в использовании отдельных видов лекарственного растительного сырья. При этом рецептура разрабатывается с учетом последних представлений об этиологии и патогенезе заболевания, а также химических и фармакологических данных об ингредиентах препарата, состоянии сырьевой базы и ряда других факторов.
Опыт применения многокомпонентных растительных лекарственных средств в народной и традиционной медицине разных стран мира показывает, что выделенное в чистом виде из растения одно биологически активное вещество или несколько очищенных фракций действуют совсем иначе, чем галеновые препараты, которые содержат практически все группы биологически активных веществ, входящих в состав данного растения, причем в более или менее натуральных соотношениях. Исходя из этого, в настоящее время при разработке лекарственных препаратов природного происхождения наблюдается возврат к использованию лекарственных растений в целом и комплексных препаратов из них.
Современными исследованиями доказано, что благодаря взаимодействию лекарственные растения могут более полно проявлять фармакологическое действие, ограничивая при этом свою токсичность.
Наиболее популярными во всем мире традиционными многокомпонентными лекарственными средствами растительного происхождения являются сборы и экстракционные препараты, при этом последние среди галеновых препаратов наиболее удобны и хорошо стандартизированы.
На протяжении последних десятилетий отмечается увеличение спроса населения на седативные средства растительного происхождения. Их потребление растет с каждым годом, особенно четко это прослеживается в развитых странах и в странах с так называемой кризисной экономикой.
Современные данные (химический состав, виды фармакологического действия, применение в медицинской практике) позволяют оценить эти растения с точки зрения целесообразности их использования, как самостоятельных источников получения лекарственных средств и в качестве ингредиентов для создания на их основе комплексного фитохимического препарата с преимущественно седативным действием.
Одним из таких растений стала Мелисса лекарственная (Melissea officinalis). Мелисса лекарственная входит в состав зарубежных препаратов: "Алталекс", "Ново-Пассит", "Калмидорм", "Фитосед", "Нервогран".
По данным отечественных и зарубежных ученых в листьях Мелиссы лекарственной содержатся различные группы биологически активных соединений: эфирные масла, фенилкарбоновые кислоты и их депсиды (розмариновая, кофейная, хлорогеновая). По литературным данным в листьях мелиссы содержание розмариновой кислоты составляет от 0,54 до 1,79%.
Известно, что различные технологические приемы и режимы оказывают значительное влияние на содержание извлекаемых из растительного сырья веществ и соединений и их фармакологическую активность и фармакологический эффект (Чуешов В.И. Промышленная технология лекарств, т.1,2. Харьков, НФАУ МТК-Книга, 2002. Багирова В.Л., Северцев В.А. Настойки, экстракты, эликсиры и их стандартизация С-Пб, СпецЛит, 2001).
Задачей настоящего изобретения является создание препарата в иде настойки мелиссы с широким спектром фармакологического действия в качестве эффективного седативного средства, обладающего противовоспалительной активностью.
Поставленная задача решена следующим образом. Предложено средство, обладающее седативным, противовоспалительным действием и представляющее собой 35-45% спиртовую настойку, полученную при соотношении сырья и экстрагента 1:5, при этом она содержит фенилпропаноиды в пересчете на розмариновую кислоту в количестве 0,1-0,9 мас.% и экстрактивных веществ травы мелиссы лекарственной 1,0-5,5 мас.% от общей массы настойки. Примером изобретения иллюстрируется экстрагирование травы Melissea officinalis L. 35-45% спиртом этиловым. Измельченную траву Melissea officinalis L. закладывают в камеру, выполненную из нержавеющей сетки с перфорированным дном, и помещают в экстрактор, добавляют рассчитанное количество 35-45% спирта этилового, общее соотношение сырье - экстрагент 1:5 до зеркала и оставляют для набухания на 5 часов. Спирт 35-45% готовят в отдельном реакторе из 95% спирта этилового (ФС 42-3072-00) и воды очищенной (ФС 42-2619-97). После положенного времени набухания добавляют опять 35-45% этилового спирта до зеркала и включают перемешивание при помощи насоса, экстрагент, в данной ситуации спирт этиловый 35-45% может циркулировать (подаваться) как снизу экстрактора, так и сверху. Экстрактор снабжен элементами подогрева. Подогревание может производится в зависимости от ситуации, но не более 40°С. Периодически меняют направление перемешивания с настаиванием, проводятся заборы проб для определения содержания экстрактивных и действующих веществ.
Полученный водно-спиртовой экстракт сливают из экстрактора и перемещают в сборник для отстаивания. Процесс отстаивания производят в холодильной камере при температуре 4-8С°, не менее 30 часов. Полученную настойку проверяют по показателям и согласно нормативной документации и фильтруют через пресс-фильтр.
Полученная настойка представляет собой прозрачную жидкость от желтого цвета с коричневым оттенком до коричневого цвета с красным оттенком с запахом лимона. При хранении возможно выпадение осадка. Препарат применяют по 15-20 капель 3 раза в день. Курс лечения 2-3 недели. Курс может быть продлен по согласованию с врачом.
Изучение седативного и транквилизирующего действия препарата было проведено в соответствии с показателями, характеризующими транквилизирующую (анксиолитическую) активность, по "Методическим указаниям по изучению транквилизирующего (анксиолитического) действия фармакологических веществ" ("Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ" (М., Ремедиум, 2000 г., с.126-130). В качестве препарата сравнения использовали настойку валерианы производства OOO "Росбио" (г.Санкт-Петербург) серии 40603, годна до 07.2006 г. (per. №001741/01-2002). Настойка валерианы выбрана в качестве препарата сравнения, так как на данный момент из препаратов растительного происхождения она наиболее известна и обладает выраженным седативным действием на ЦНС.
Влияние на суммационно-пороговый показатель
Данные по влиянию препарата на суммацию подпороговых импульсов представлены в таблице 1. Препараты вводились внутрижелудочно крысам средней массой 160-180 г в дозах 50 и 100 мг/кг в течение недели (1 г принимали за 1 мл).
| Таблица 1Влияние "Мелиссы настойки" и аналога на порог возбудимости у белых крыс (В, М±м) | ||||||
| Сроки исследования (дни) | Экспериментальная группа и пол | |||||
| Контроль | 50 мг/кг | 100 мг/кг | ||||
| М | F | М | F | М | F | |
| "Мелиссы настойка" | ||||||
| Фон | 9.0±1.1 | 9.2±1.0 | 8.9±1.1 | 8.0±0.5 | 8.5±0.7 | 9.3±0.5 |
| 7-й день* | 9.0±0.8 | 9.1±1.0 | 12.6±1.3 | 11.9±1.0* | 14.6±1.2* | 14.8±1.5* |
| Прирост | 0.0 | -0.1 | 3.7±2.2 | 3.9±1.4 | 6.1±1.7 | 5.5±1.8 |
| "Валерианы настойка" | ||||||
| Фон | 9.0±1.1 | 9.2±1.0 | 9.5±0.8 | 8.4±0.5 | 8.8±0.8 | 9.0±0.8 |
| 7-й день* | 9.0±0.8 | 9.1±1.0 | 12.7±1.0 | 12.0±0.9* | 14.3±1.0* | 14.2±1.3* |
| Прирост | 0.0 | -0.1 | 3.2±1.7 | 3.6±1.2 | 5.5±1.6 | 5.7±1.8 |
| * - достоверное отличие от контроля и от фона (Р>0.95) |
Из таблицы видно, что в опытных группах наблюдалось увеличение величины СПП по отношению как к фону, так и контролю, причем это увеличение имело явно дозозависимый характер. Величины приращений для обоих препаратов практически совпадают.
Влияние на статико-силовую выносливость (мышечную силу)
Влияние препаратов на статико-силовую выносливость изучали, регистрируя время висения крыс на вертикальной сетке. Критерием истощения статической силы считали время, когда крыс уже не могла удерживать вес своего тела и падала с сетки вниз. Результаты эксперимента представлены в таблице 2
| Таблица 2Продолжительность физической выносливости крыс (минуты) в тесте статической силовой нагрузки собственным весом | ||||||
| Сроки исследования (дни) | Экспериментальная группа и пол | |||||
| Контроль | 50 мг/кг | 100 мг/кг | ||||
| М | F | М | F | М | F | |
| "Мелиссы настойка" | ||||||
| Фон | 21.6±1.8 | 19.2±2.0 | 20.3±1.6 | 18.0±2.0 | 17.5±2.7 | 19.3±2.4 |
| 7-й день* | 19.0±2.2 | 19.1±2.5 | 13.4±2.3 | 12.7±1.5 | 10.5±2.2 | 9.8±1.5 |
| Сокращение | 2.6±2.9 | 0.1±3.2 | 6.7±2.8 | 5.3±2.5 | 7.1±3.2 | 9.5±3.0 |
| "Валерианы настойка" | ||||||
| Фон | 21.6±1.8 | 19.2±2.0 | 18.4±2.1 | 24.3±2.0 | 19.3±1.8 | 18.4±2.1 |
| 7-й день* | 19.0±2.2 | 19.1±2.5 | 12.8±1.9 | 14.5±2.1 | 11.6±1.8 | 10.6±1.7 |
| Сокращение | 2.6±2.9 | 0,1±3.2 | 5.6±2.8 | 9.9±2.8 | 8.0±2.4 | 7.8±2.7 |
Результаты эксперимента свидетельствуют о достоверном снижении статико-силовой выносливости крыс, получавших препараты, по сравнению как с фоном, так и с контролем; различий между препаратами не выявлялось.
Влияние на двигательную и исследовательскую активность
В таблицах 3 и 4 представлены данные по влиянию "Мелиссы настойки" и препарата сравнения на спонтанную двигательную активность крыс (С ДА). Крысы по одной помещались в регистрационную камеру автоматического регистратора "Coulburn Instruments", где за каждые 5 минут на протяжении 35 минут у них регистрировалось количество движений.
| Таблица 3Влияние "Мелиссы настойки" на СДА белых крыс (М±m) | ||||||
| Период | Экспериментальная группа и пол | |||||
| наблюде | Контроль | 50 мг/кг | 100 мг/кг | |||
| ния (мин) | М | F | М | F | М | F |
| Фон | ||||||
| 0-5 | 50.0±18.8 | 92.2±20.1 | 85.0±41.9 | 75.4±26.5 | 78.4±23.8 | 44.0±8.2 |
| 6-10 | 45.4±29.1 | 75.4±12.0 | 70.8±25.7 | 43.3±21.6 | 68.3±25.5 | 75.6±14.5 |
| 11-15 | 45.2±21.2 | 45.2±18.8 | 21.6±12.0 | 40.1±23.6 | 71.0±30.7 | 45.7±16.8 |
| 16-20 | 22.8±5.1 | 25.4±15.4 | 30.5±16.1 | 28.4±14.5 | 30.2±22.4 | 28.3±10.5 |
| 21-25 | 30.5±12.0 | 5.8±2.6 | 12.6±6.8 | 19.3±10.5 | 17.0±8.6 | 17.0±11.9 |
| 26-30 | 32.0±14.1 | 11.2±9.2 | 42.4±11.1 | 18.3±9.1 | 24.0±12.0 | 12.5±4.4 |
| 31-35 | 18.0±14.1 | 5.2±2.6 | 17.6±7.5 | 22.1±9.2 | 21.2±13.7 | 16.4±10.5 |
| 0-35 | 243.8±66.1 | 260.5±42.2 | 280.3±65.7 | 247.0±52.5 | 310.1±44.1 | 239.7±40.9 |
| 7-й день | ||||||
| 0-5 | 72.2±20.1 | 75.4±23.5 | 44.6±18.0 | 52.1±18.3 | 64.8±24.6 | 43.7±14.1 |
| 6-10 | 45.0±12.0 | 43.3±11.6 | 27.8±11.2 | 35.3±15.7 | 27.5±11.2 | 24.6±11.0 |
| 11-15 | 36.2±18.8 | 26.5±13.4 | 24.2±8.0 | 28.4±11.3 | 19.3±9.0 | 38.9±10.3 |
| 16-20 | 26.4±11.0 | 28.4±5.7 | 21.4±10.7 | 22.7±10.5 | 26.6±7.3 | 20.6±8.7 |
| 21-25 | 5.8±2.6 | 10.5±2.4 | 14.2±4.1 | 18.3±9.3 | 23.6±10.6 | 14.2±5.3 |
| 26-30 | 11.2±4.2 | 8.3±2.1 | 11.3±6.7 | 10.2±4.6 | 13.8±3.1 | 7.3±2.1 |
| 31-35 | 5.2±2.6 | 22.1±7.2 | 6.3±1.8 | 5.3±1.2 | 15.0±5.4 | 9.4±2.3 |
| 0-35 | 202.0±42.2 | 214.5±62.5 | 149.8±52.9 | 172.3±43.5 | 190.9±31.1 | 158.7±44.8 |
| Таблица 4Влияние "Валерианы настойки" на СДА белых крыс (М±m) | ||||||
| Период | Экспериментальная группа и пол | |||||
| наблюде | Контроль | 50 мг/кг | 100 мг/кг | |||
| ния (мин) | М | F | М | F | М | F |
| Фон | ||||||
| 0-5 | 50.0±18.8 | 92.2±20.1 | 81.9±32.0 | 42.4±26.5 | 72.9±23.8 | 81.8±28.2 |
| 6-10 | 45.4±29.1 | 75.4±12.0 | 68.7±25.7 | 76.3±31.6 | 44.1±25.5 | 68.6±24.1 |
| 11-15 | 45.2±21.2 | 45.2±18.8 | 73.1±12.0 | 44.5±23.6 | 39.0±20.7 | 21.3±12.8 |
| 16-20 | 22.8±5.1 | 25.4±15.4 | 29.5±16.1 | 27.7±14.5 | 28.5±16.4 | 30.5±10.5 |
| 21-25 | 30.5±12.0 | 5.8±2.6 | 17.0±6.8 | 16.9±10.5 | 19.3±7.6 | 12.5±11.9 |
| 26-30 | 32.0±14.1 | 11.2±9.2 | 23.5±11.1 | 12.6±9.1 | 17.6±8.0 | 40.7±4.4 |
| 31-35 | 18.0±14.1 | 5.2±2.6 | 21.0±7.5 | 16.4±9.2 | 21.9±10.7 | 17.5±10.5 |
| 0-35 | 243.8±66.1 | 260.5±42.2 | 314.5±65.7 | 236.8±52.5 | 244.0±44.1 | 272.9±40.9 |
| Продолжение таблицы 4 | ||||||
| 7-й день | ||||||
| 0-5 | 72.2±20.1 | 75.4±23.5 | 64.1±28.0 | 52.2±22.3 | 44.9±24.6 | 42.7±14.1 |
| 6-10 | 45.0±12.0 | 43.3±11.6 | 27.2±11.2 | 34.8±15.7 | 28.3±11.2 | 33.8±11.0 |
| 11-15 | 36.2±18.8 | 26.5±13.4 | 19.5±8.0 | 24.4±11.3 | 24.9±9.0 | 28.0±10.3 |
| 16-20 | 26.4±11.0 | 28.4±5.7 | 25.6±10.7 | 22.9±10.5 | 21.4±7.3 | 15.6±8.7 |
| 21-25 | 5.8±2.6 | 10.5±2.4 | 23.6±4.1 | 14.0±9.3 | 24.0±10.6 | 14.2±5.3 |
| 26-30 | 11.2±4.2 | 8.3±2.1 | 13.9±6.7 | 9.9±4.6 | 11.3±3.1 | 7.3±2.1 |
| 31-35 | 5.2±2.6 | 22.1±7.2 | 15.0±1.8 | 15.3±1.2 | 6.1±5.4 | 9.2±2.3 |
| 0-35 | 202.0±42.2 | 214.5±62.5 | 189.1±52.9 | 174.5±43.5 | 151.2±31.1 | 150.6±44.8 |
Данные по контрольным животным свидетельствуют, что на протяжении исследования имело место общее снижение СДА (типичное явление в условиях длительных исследований). Однако на фоне этой общей тенденции имеется дополнительный эффект обоих препаратов - снижение СДА в опытных группах было достоверно выше, чем в контроле. Достоверной дозовой зависимости этого эффекта препаратов не выявляется.
Данные по влиянию "Мелиссы настойки" и препарата сравнения на структуру поведения крыс в "открытом поле" представлены в таблицах 5 и 6.
| Таблица 5Влияние "Мелиссы настойки" на поведение белых крыс (М±m) | ||||||
| Показатели | Экспериментальная группа и пол | |||||
| Контроль | 50 мг/кг | 100 мг/кг | ||||
| М | F | М | F | М | F | |
| Фон | ||||||
| Латентный период | 103±19 | 113±14 | 91±12 | 93±22 | 98±21 | 108±19 |
| Горизонтальная активность | 2.4±0.5 | 2.0±0.7 | 3.4±1.2 | 2.1±1.6 | 1.7±0.7 | 2.6±1.5 |
| Вертикальная активность | 2.6±0.7 | 2.9±0.5 | 2.2±0.9 | 2.1±0.6 | 2.0±1.1 | 2.8±0.9 |
| Заглядывания | 4.5±0.6 | 3.1±0.5 | 3.0±0.5 | 4.1±0.5 | 3.2±0.9 | 4.1±0.5 |
| Груминг | 0 | 1.3±1.3 | 2.7±1.3 | 0 | 3.0±2.2 | 1.5±0.7 |
| Болюсы | 2.1±0.6 | 1.9±0.8 | 1.7±0.8 | 2.0±0.9 | 2.3±1.2 | 2.4±1.4 |
| Продолжение таблицы 5 | ||||||
| 7-й день | ||||||
| Латентный период | 115±26 | 121±30 | 114±33 | 130±35 | 130±32 | 116±29 |
| Горизонтальная активность | 2.6±1.2 | 1.2±0.2 | 0 | 1.7±0.3 | 0.7±0.2 | 0.8±0.5 |
| Вертикальная активность | 2.4±1.2 | 1.2±0.5 | 0 | 0.3±0.1 | 0.5±0.2 | 0.1±0.1 |
| Заглядывания | 1.6±0.5 | 2.1±1.3 | 1.3±0.7 | 3.3±1.1 | 0.7±0.5 | 1.4±0.5 |
| Груминг | 0.5±0.5 | 0 | 0 | 0.5±0.3 | 0 | 0.2±0.2 |
| Болюсы | 2.0±0.9 | 3.6±0.5 | 1.9±0.7 | 2.7±0.7 | 1.8±0.7 | 3.2±1.3 |
| Таблица 6Влияние препарата сравнения на поведение белых крыс (М±m) | ||||||
| Показатели | Экспериментальная группа и пол | |||||
| Контроль | 50 мг/кг | 100 мг/кг | ||||
| М | F | М | F | М | F | |
| Фон | ||||||
| Латентный период | 103±19 | 113±14 | 95±20 | 107±18 | 94±11 | 104±20 |
| Горизонтальная активность | 2.4±0.5 | 2.0±0.7 | 1.6±0.5 | 2.5±1.3 | 3.1±1.0 | 2.1±1.4 |
| Вертикальная активность | 2.6±0.7 | 2.9±0.5 | 1.9±1.1 | 2.7±0.7 | 2.2±0.7 | 2.0±0.5 |
| Заглядывания | 4.5±0.6 | 3.1±0.5 | 3.1±0.7 | 4.6±0.2 | 3.0±0.2 | 3.8±0.5 |
| Груминг | 0 | 1.3±1.3 | 2.9±1.9 | 1.3±0.6 | 2.5±1.1 | 0 |
| Болюсы | 2.1±0.6 | 1.9±0.8 | 2.1±1.1 | 2.3±1.2 | 1.4±0.5 | 1.7±0.8 |
| 7-й день | ||||||
| Латентный период | 115±26 | 121±30 | 120±27 | 128±31 | 119±34 | 130±32 |
| Горизонтальная активность | 2.6±1.2 | 1.2±0.2 | 0.6±0.5 | 0.6±0.1 | 1.6±0.1 | 0.5±0.1 |
| Вертикальная активность | 2.4±1.2 | 1.2±0.5 | 0.2±0.1 | 0.5±0.1 | 0.3±0.1 | 0 |
| Заглядывания | 1.6±0.5 | 2.1±1.3 | 1.4±0.3 | 0.6±0.3 | 3.2±1.1 | 1.3±0.7 |
| Груминг | 0.5±0.5 | 0 | 0.2±0.1 | 0 | 0.2±0.1 | 0 |
| Болюсы | 2.0±0.9 | 3.6±0.5 | 3.1±1.2 | 1.7±0.7 | 2.5±0.6 | 1.7±0.6 |
Как видно из представленных данных, практически во всех экспериментальных группах животных (включая контрольные группы) отмечается достоверное удлинение длительности латентного периода, а также уменьшение активности, оцениваемое по количеству вертикальных стоек, пересечений и заглядываний по сравнению с фоновыми данными.
Изучение противосудорожной активности
Учитывая седативную направленность действия препарата, сравнение противосудорожной эффективности исследовали на моделях коразоловых судорог и коразолового киндлинга (Т.А.Воронина, Л.Н.Неробкова. Методические указания по изучению противосудорожной активности фармакологических веществ. Руководство по экспериментальному доклиническому изучению новых фармакологических веществ. М., Ремедиум, 2000 г., с.138-146).
Опыты проводились на белых беспородных мышах-самцах массой 18-22 г. Для моделирования коразоловых судорог коразол вводили подкожно в дозе 120 мг/кг. Определяли латентные периоды клонических, тонических судорог, время жизни и процент животных, у которых возникали судороги. Препараты вводили внутрижелудочно за 30 минут до введения коразола в дозе 100 мг/кг. Результаты экспериментов представлены в таблице 7.
| Таблица 7Влияние "Мелиссы настойки" и препарата сравнения на коразоловые судороги у мышей, (М±m) | ||||||
| Вещество, мг/кг | Клонические судороги | Тонические судороги | Время жизни, мин | Летальность, % погибших животных | ||
| Латентный период, мин | % мышей с судорогами | Латентный период, мин | % мышей с судорогами | |||
| Коразол | 10,5±1,5 | 100 | 18,5±2,5 | 50 | 22,5±1,5 | 60 |
| Коразол + Мелиссы настойка OOO "Росбио" | 13,5±1,5 | 80 | 20,5±1,5 | 50 | 30,5±2,5 | 40 |
| Коразол+"Валерианы настойка" | 12,0±1,5 | 70 | 21,5±1,5 | 50 | 29,5±2,5 | 40 |
Оказалось, что у обоих препаратов наблюдался антагонизм с коразолом, который проявлялся в увеличении латентных периодов судорог, времени жизни животных и снижении их летальности. Достоверных различий в эффективности препаратов не обнаружилось, что может свидетельствовать об их равной эффективности.
Для моделирования коразолового киндлинга мышам ежедневно подкожно на протяжении 10 дней вводили коразол в дозе 30 мг/кг. В последний день введения опытным животным за 1 час до коразола в/ж ввели препараты в дозе 100 мг/кг. Оценку судорожной готовности проводили по балльной шкале:
0 баллов - отсутствие судорожной реакции;
1 балл - вздрагивание головы или отдельных мышц туловища;
2 балла - повторные клонические судороги всего тела;
3 балла - клонико-тонические судороги передних лап;
4 балла - клонико-тонические судороги с падением на бок и депрессией поведения;
5 баллов - повторные клонико-тонические судороги с гибелью. Полученные результаты представлены в таблице 8.
| Таблица 8Влияние "Мелиссы настойки" и препарата сравнения на судорожную готовность мышей в тесте коразолового киндлинга | ||
| Препарат | Количество животных | Судорожная готовность в баллах (М±m) |
| Коразол + вода | 10 | 4,25±0,25 |
| Коразол + "Мелиссы настойка" | 10 | 2,5±0,25 |
| Коразол + "Валерианы настойка" | 10 | 2,5±0,5 |
Оказалось, что оба препарата проявляли защитное противосудорожное действие, достоверно не отличаясь при этом друг от друга.
Влияние на пролонгирование снотворного эффекта гексенала
Опыты проводили на мышах-самцах массой 20-22 г. Препараты вводили внутрижелудочно за 30 минут до подкожного введения гексенала (60 мг/кг) в дозах 50 мг/кг. Отмечали длительность бокового положения мышей (от момента утраты до восстановления рефлекса переворачивания). Результаты приведены в таблице 9.
"Мелиссы настойка" и препарат сравнения оказывали одинаковый потенциирующий эффект на действие гексенала.
| Таблица 9Влияние сравниваемых препаратов на длительность снотворного действия гексенала (60 мг/кг) | |
| Препараты | Длительность бокового положения мышей, мин (М±m) |
| Контроль (вода) | 19±5.6 (n=20) |
| "Мелиссы настойка", 50 мг/кг | 66±12.4* (n=20) |
| "Валерианы настойка", 50 мг/кг | 78±15.1* (n=20) |
| * - статистически достоверные различия между препаратами и контролем р≤0.05 |
Оба препарата более чем втрое увеличивают длительность снотворного эффекта гексенала.
Исследование анксиолитических свойств препарата
Опыты проводили на мышах по методу Boissier. Мышей-самцов массой 20-22 г помещали в пластмассовую камеру с полом, состоящим из четырех металлических пластин. В момент перемещения мышей с пластины на пластину им наносили электроболевое раздражение. Препараты вводили внутрижелудочно в дозе 50 мг/кг. Спустя 20 минут мышей помещали в камеру и в течение двух минут считали число пробежек.
Результаты представлены в таблице 10.
Как видно из таблицы, электроболевое раздражение заметно снизило активность мышей. "Мелиссы настойка" и препарат сравнения уменьшали тормозной эффект электроболевого раздражения: несмотря на него число пробежек мышей заметно возросло. Анксиолитические свойства "Мелиссы настойки" и препарата сравнения практически не различались.
| Таблица 10Анксиолитическое действие сравниваемых препаратов | |
| Препараты | Число пробежек на 1 мышь в течение 2 мин пребывания в камере (М±m) |
| Вода (без электроболевого раздражения) | 16.5±3.8a (24) |
| Вода (с электроболевым раздражением) | 5.0±0.8б (24) |
| "Мелиссы настойка" | 13.9±2.4в (24) |
| "Валерианы настойка" | 14.1±1.9в (24) |
Различия статистически достоверны между а и б и б и в при р<0.05.
Уменьшение гипертермии, вызванной амфетамином (фенамином)
Гипертермию у мышей вызывали подкожным введением фенамина в дозе 10 мг/кг. Ректальную температуру измеряли при помощи электротермометра ТПЭМ-1. Препараты в дозе 50 мг/кг вводили внутрижелудочно за 30 минут до введения фенамина. Влияние на гипертермию оценивали через 1 и 2 часа после введения фенамина. Результаты представлены в таблице 11.
| Таблица 11Влияние сравниваемых препаратов на гипертермический эффект фенамина | ||
| Препараты и дозы | Ректальная температура (°С) | |
| Через 1 час | Через 2 часа | |
| Вода | 38.2±0.16 | 38.5±0.2 |
| "Мелиссы настойка", 50 мг/кг | 36.6±0.18* | 36.5±0.12* |
| "Валерианы настойка", 50 мг/кг | 36.7±0.18* | 36.6±0.2* |
| * - статистически достоверные различия между препаратами и контролем (р≤0.05) |
Данные таблицы свидетельствуют о том, что оба препарата достоверно снижают температуру, повышенную фенамином, причем антигипертермическое действие отчетливо выражено в течение 2 часов. По влиянию на действие фенамина сравниваемые препаратм не различаются.
Изучение противовоспалительных свойств "Мелиссы настойки"
Изучение противовоспалительной активности препарата проводили в соответствии с "Методическими указаниями по изучению новых нестероидных противовоспалительных препаратов" (в книге: "Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ". М., Минздрав РФ, ЗАО "ИИА "Ремедиум", 2000, с.234-241) [Шварц Г.Я., Сюбаев Р.Д. Методические указания по изучению новых нестероидных противовоспалительных препаратов. В кн. "Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ". М., Минздрав РФ, ЗАО "ИИА "Ремедиум", 2000, с.234-241].
Моделями патологических воспалительных процессов служили каррагениновый отек лапы и формалиновый артрит у крыс.
Острую воспалительную реакцию (отек) вызывали субплантарным (подплантарный апоневроз) введением 0,1 мл 1% раствора каррагенина.
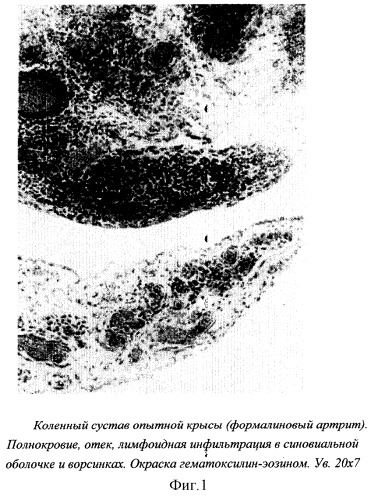
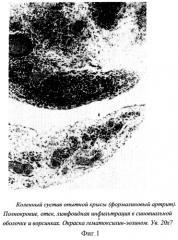
Модель артрита вызывали введением в полость коленного сустава 0,1 мл 2% раствора формалина. Спустя 1 сутки получали модель острого артрита, на которой можно было испытывать противовоспалительное и обезболивающее действия изучаемых экстрактов [Шварц Г.Я., Сюбаев Р.Д. Методические указания по изучению новых нестероидных противовоспалительных препаратов. В кн. "Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ". М., Минздрав РФ, ЗАО "ИИА "Ремедиум", 2000, с.234-241. Бабаян Э.А., Лепахин В.К. и др. Руководящие методические материалы по экспериментальному и клиническому изучению новых лекарственных средств. Издание официальное, часть 6, М., 1986, с.51-56].
Показателями противовоспалительного эффекта служили антиэкссудативное, анальгезирующее и жаропонижающее действия.
Противоотечное действие оценивалось онкометрическим методом [Гацура В.В. Методы первичного фармакологического исследования биологически активных веществ. М., Мед-на. 1974, 143 с.].
Анальгезирующие свойства препаратов оценивались по изменению под их влиянием порога болевой чувствительности при контактно-тепловом раздражении. Исследования выполнялись на оптоэлектронном анальгезиметре ТФ 003 НИНТЦ "Фармаколог", Россия. Регистрируемым показателем являлось время латентного отдергивания пораженной конечности крысы в ответ на термическое болевое воздействие.
Жаропонижающее действие препаратов определялось по их способности снижать температуру кожи лапки крысы над очагом воспаления. Температура кожи измерялась электротермометром фирмы Nihon Kohden, Япония.
Кроме этого, унифицированными биохимическими и гематологическими методами оценивались общие показатели активности воспалительного процесса: СОЭ, уровни ЦРБ, сиаловых кислот, фибриногена и содержание лейкоцитов [Лабораторные методы исследования в клинике. Справочник. Под ред. В.В.Меньшикова. М., Мед-на, 1987, 368 с. Справочник по функциональной диагностике. Под ред. И.А.Кассирского. М., Мед-на, 1970, 849 с.].
Для морфологического исследования брали коленный сустав крыс. Материал фиксировали в 15% формалине, декальцинировали в азотной кислоте с последующей обработкой в алюмо-калиевых квасцах и затем заливали в парафин. Срезы окрашивали гематоксилин-эозином.
Все результаты исследований оценивались с помощью методов непараметрической и параметрической статистики.
Противовоспалительная активность на модели каррагенинового отека лапы у крыс
В экспериментах использовали крыс-самцов массой 180-200 г. Каждая экспериментальная группа включала по 10 особей.
Всего было исследовано 4 экспериментальные группы:
1. Интатктные.
2. Каррагенин + вода.
3. Каррагенин + диклофенак (8 мг/кг в виде суспензии в крахмальной слизи).
4. Каррагенин + "Мелиссы настойка" (100 мг/кг).
Препараты вводились по следующей схеме: 2 дня до воспаления 1 раз в сутки внутрижелудочно через атравматичный металлический зонд и на 3-й день за 4 часа до введения каррагенина. Оценку проводили через 3, 12 и 24 часа.
Результаты представлены в таблицах 12-15.
| Таблица 12Объем воспаленной конечности крысы (см3 ×10; n=10) в динамике после субплантарного введения каррагенина и применения тестируемых препаратов, (М±m) | ||||
| Экспериментальная группа | Время наблюдения, час | |||
| До воспаления, исходный уровень | 3 | 12 | 24 | |
| 1 | 22±1 | 22±1 | 22±1 | 22±1 |
| 2 | 21±1 | 34±2 | 31±2 | 30±2 |
| 3 | 20±1 | 28+1* | 26±1* | 24±1* |
| 4 | 21±1 | 30±2 | 28±1 | 26±2 |
| *- достоверные отличия от группы №2 (р<0.05) | ||||
| Таблица 13Время развития болевого сигнала у крыс (сек ×10; n=10) после стандартного термического раздражения на фоне каррагенинового отека и применения тестируемых препаратов, (М±m) | ||||
| Экспериментальная группа | Время наблюдения, час | |||
| До воспаления, исходный уровень | 3 ч | 12 | 24 | |
| 1 | 30±1 | 30±1 | 30±1 | 30±1 |
| 2 | 29+1 | 19+2 | 20±3 | 24±2 |
| 3 | 31±1 | 47±2* | 52±3* | 38±2* |
| 4 | 30±1 | 46±2* | 48±3* | 44±2* |
| * - достоверные отличия от группы №2 (р<0.05) |
| Таблица 14Температура (t°C) воспаленной и интактной конечностей крыс (n=10) на фоне каррагенинового отека и применения тестируемых препаратов, (M±m) | ||||||
| Экспериментальная группа | Время наблюдения, час | |||||
| До воспаления, исходный уровень | 3 | 12 | 24 | |||
| 1 | 34.5±0.5 | 34.5±0.5 | 34.5±0.5 | 34.5±0.5 | ||
| 2 | 35.0±0.3 | 42.3±0.8 | 41.2±0.6 | 40.3±0.8 | ||
| 3 | 34.9±0.5 | 39.2±0.6* | 36.3±0.5* | 36.2±0.4* | ||
| 4 | 35.1±0.5 | 40.0±0.7* | 38.6±0.7* | 37.5±0.6* | ||
| *- достоверные отличия от группы №2 (р<0.05) | ||||||
| Таблица 15Показатели активности воспалительного процесса в динамике течения каррагенинового отека и применения тестируемых препаратов (n=10), М±m | ||||||
| Экспериментальная группа | СОЭ, мм/час | ЦРБ, мм реципитации | Сиаловые кислоты, Ммоль/л | Фибриноген, г/л | Содержание лейкоцитов, 103/мм3 | |
| Час наблюдения | ||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 1 | 3 | 6±1 | 0 | 2.0±0.5 | 2.5±0.5 | 6.5±0.5 |
| 3 | 30±3 | >4 | 6.5±0.5 | 10.5±0.5 | 16.5±1.0 | |
| 2 | 12 | 30+5 | >4 | 7.5±1.5 | 10.5±1.5 | 15.5+0.5 |
| 24 | 25±5 | >4 | 6.5±1.0 | 9.5±0.5 | 15.5±0.5 | |
| 3 | 25±5 | 4±1 | 6.3±0.2 | 8.4±1.2 | 14.2±0.5* | |
| 3 | 12 | 12±3* | 1±1* | 2.5±0.5* | 3.0±1.0* | 7.8±1.2* |
| 24 | 6±2* | 1±1* | 1.8±0.2* | 2.0±0.5* | 6.3±0.6* | |
| 3 | 20±5* | 4±1 | 6.8±0.3 | 9.0±1.1 | 15.1±0.5 | |
| 4 | 12 | 18±3* | 3±1 | 5.8±0.5 | 6.0±1.3* | 8.8±1.2* |
| 24 | 15±4* | 3±1 | 4.7±0.4* | 4.5±0.6* | 7.5±0.7* | |
| *- достоверные отличия от группы №2 (р<0.05) |
Данные, представленные в таблицах, свидетельствуют о наличии у тестируемых препаратов достаточных противовоспалительных свойств.
Противовоспалительная активность на модели формалинового артрита у крыс
В экспериментах использовали крыс-самцов массой 180-200 г. Каждая экспериментальная группа включала по 10 особей.
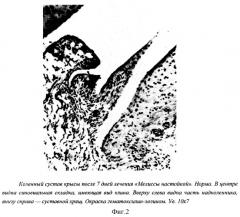
Тестируемые препараты вводились по следующей схеме: 3 дня до воспаления 1 раз в сутки внутрижелудочно через атравматичный металлический зонд и на 4-й день за 4 часа до введения формалина. Далее проводили лечение препаратами на протяжении 7 дней, вводя их 1 раз в день. Оценку проводили через сутки и на 4-й и 8-й дни.
Всего было исследовано 4 экспериментальные группы:
1. Интатктные.
2. Формалин + вода.
3. Формалин + диклофенак (8 мг/кг в виде суспензии в крахмальной слизи).
4. Формалин + "Мелиссы настойка" (100 мг/кг).
Результаты представлены в таблицах 16-18
| Таблица 16Объем воспаленной конечности крысы (см ×10; n=10) в динамике после внутрисуставного введения формалина и применения тестируемых препаратов, (М±m) | |||||||
| Экспериментальная группа (препарат) | Время наблюдения, дни | Суммарный балл активности | Терапевтический индекс по артриту | ||||
| До воспаления, исходный уровень | 1 | 4 | 8 | ||||
| 1 | см×10 | 22±1 | 21±1 | 21±1 | 22±2 | - | - |
| уменьш., % | - | - | - | - | |||
| 2 | см×10 | 22±1 | 33±2 | 34±2 | 28±2 | 15 | - |
| уменьш., % | - | - | 0 | 15 | |||
| 3 | см×10 | 22±1 | 34±2 | 25±1 | 22±2 | 63 | 4.2 |
| уменьш., % | - | - | 27 | 36 | |||
| 4 | см×10 | 22±1 | 34±2 | 30±1 | 22±2 | 48 | 3.2 |
| уменьш., % | - | - | 12 | 36 |
Суммарный балл активности - сумма процентов уменьшения объема пораженной конечности за 7 дней. Терапевтические индексы (ТИ) рассчитывались по формуле:
| Таблица 17Время развития болевого сигнала у крыс (сек ×10; n=10) после стандартного термического раздражения на фоне формалинового артрита и применения тестируемых препаратов, (М±m) |