Арилзамещенные пиразолы или триазолы, фармацевтическая композиция, способ лечения, профилактики или снижения интенсивности различных нарушений или состояний у животного (варианты)
Иллюстрации
Показать всеИзобретение относится к арилзамещенным пиразолам или триазолам общей формулы I
их фармацевтически приемлемым солям, пролекарствам или сольватам, где Х - O или S; Het - одна из групп
R1-Н, С1-С6алкил, аминокарбонил, С(O)R10; R2 и R3 независимо - Н и аминокарбонил, R5, R6, R7 и R8 независимо - Н, галоген, галоген C1-С6алкил, NO2; R10-OR11, где R11 - H, C1-С6алкил. Соединения I пригодны для лечения нейрональных повреждений, наблюдающихся в результате общей и очаговой ишемии, для лечения или профилактики нейродегенеративных состояний, таких как боковой амиотрофический склероз (БАС), и для лечения, профилактики или снижения интенсивности острых или хронических болей, в качестве агентов против шума в ушах, противосудорожных средств, а также в качестве противоманиакальных депрессантов, в качестве обезболивающих средств местного назначения, в качестве противоаритмических средств и для лечения или профилактики диабетической невропатии. 4 н. и 9 з.п. ф-лы, 1 ил.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к области медицинской химии. В частности, изобретение относится к арилзамещенным пиразолам, триазолам и тетразолам, а также к открытию противосудорожного действия этих соединений и их действия в качестве блокаторов натриевых (Na+) каналов.
Уровень техники
Показано, что несколько классов используемых в терапии лекарственных средств, включая обезболивающие средства местного назначения, такие как лидокаин и бупивакаин, противоаритмические средства, такие как пропафенон и амиокларон, и противосудорожные средства, такие как ламотригин, фенитоин и карбамазепин, характеризуются общим механизмом действия путем блокирования или модулирования активности Na+ каналов (см. статью Catterall W.A., Trends Pharmacol. Sci., 8:57-65 (1987)). Предполагают, что каждый из этих агентов действует, препятствуя быстрому притоку ионов Na+.
Недавно показано, что другие блокаторы Na+ каналов, такие как BW619C89 и лифаризин, обладают нейропротективным действием на моделях животных с общей или очаговой ишемией и в настоящее время находятся на стадии клинических испытаний (см. статьи Graham и соавт., J. Pharmacol. Exp. Ther., 269: 854-859 (1994); Brown и соавт., British J. Pharmacol., 115: 1425-1432 (1995)).
Нейропротективная активность блокаторов натриевых (Na+) каналов связана с их эффективностью в снижении внеклеточной концентрации глутамата в процессе ишемии посредством ингибирования высвобождения этого экситотоксичного (т.е. индуцирующего токсичность) аминокислотного нейромедиатора (или иначе, подавления возбудимости нервной ткани). Исследования показали, что в отличие от антагонистов глутаматного рецептора, блокаторы Na+ каналов предотвращают гипоксическое повреждение белого вещества мозга млекопитающих (см. статью Stys и соавт., J. Neurosci., 12: 430-439 (1992)). Таким образом, эти блокаторы могут представлять преимущество при лечении некоторых типов инсультов или нейрональных травм в случаях преобладания повреждений каналов белого вещества.
Другим примером клинического использования блокаторов Na+ каналов является рилузол. Показано, что это лекарственное средство продлевает жизнь в подгруппе пациентов с боковым амиотрофическим склерозом (БАС) (см. статью Bensim и соавт., New Engl. J. Med., 330: 585-591 (1994)) и позднее это лекарственное средство было утверждено Управлением по контролю пищевых продуктов и лекарственных средств (FDA) для лечения БАС. Кроме упомянутого выше клинического использования карбамазепин, лидокаин и фенитоин используют для лечения невропатической боли, такой как невралгия тройничного нерва, диабетическая невропатия и другие формы повреждения нервной ткани (см. статью Taylor and Meldrum, Trends Pharmacol. Sci., 16: 309-316 (1995)), а карбамазепин и ламотригин используют при лечении маниакальной депрессии (см. статью Denicott и соавт., J. Clin. Psychiatry, 55: 70-76 (1994). Более того, на основании ряда сходных признаков между хронической болью и звоном в ушах (см. статьи Moller A.R., Am. J. Otol., 18: 577-585 (1997); Tonndorf, J. Hear. Res., 28: 271-275 (1987)) предполагают, что шум в ушах можно рассматривать как форму ощущения хронической боли (см. статью Simpson J.J. и Davies E.W., Tip., 20: 12-18 (1999)). Действительно, показано, что лигнокаин и карбамазепин эффективны при лечении шума в ушах (см. статьи Majumdar В. и соавт., Clin. Otolaryngol., 8: 175-180 (1983); Donaldson I., Laryngol. Otol., 95: 947-951 (1981)).
Показано также, что существует по крайней мере пять-шесть участков связывания на потенциалозависимых Na+ каналах, которые специфически связываются с нейротоксинами (см. статью Catterall W.A., Science, 242: 50-61 (1988)). Дальнейшие исследования показали, что терапевтические противоаритмические средства, противосудорожные средства и обезболивающие средства местного назначения, действие которых опосредовано Na+ каналами, проявляют свою активность путем взаимодействия с внутриклеточным участком Na+ канала и аллостерического ингибирования взаимодействия с участком 2 рецептора нейротоксина (см. статью Catteral W.A., Ann. Rev. Pharmacol. Toxicol., 10: 15-43 (1980)).
Ряд авторов (см. статью Соссо М.Т., Maccioni A., Plumitallo A., Farmaco Ed. Sci., 40: 272-284 (1985)) описали два следующих соединения:
Описаны также другие арилзамещенные гетероциклы в качестве противогрибковых агентов (см. статью Stefancich G. и соавт., Arch. Pharm., (Weinheim Ger.), 323: 273-280, 1990).
До настоящего времени соединения формулы I не использовали для лечения нарушений, восприимчивых к блокированию Na+ каналов у млекопитающих.
Сущность изобретения
Настоящее изобретение относится к открытию действия арилзамещенных пиразолов, триазолов и тетразолов, представленных формулой I, в качестве блокаторов Na+ каналов.
Изобретение относится также к лечению нарушений, восприимчивых к блокированию Na+ каналов, у млекопитающих, страдающих избыточной активностью упомянутых каналов, путем введения эффективного количества соединения формулы I, как описано в данном контексте.
Другим объектом настоящего изобретения является способ лечения, профилактики или снижения степени нейрональных потерь, являющихся результатом общей и очаговой ишемии; лечения, профилактики или уменьшения интенсивности болей, включая острые и хронические боли, а также невропатические боли; лечения, профилактики или уменьшения интенсивности судорог и нейродегенеративных состояний; лечения, профилактики или уменьшения интенсивности маниакальной депрессии с использованием в качестве обезболивающих средств местного действия и противоаритмических средств, а также способа лечения шума в ушах путем введения соединения формулы I млекопитающему, нуждающемуся в таком лечении.
Другим аспектом настоящего изобретения является использование соединений формулы I в качестве блокаторов Na+ каналов.
Настоящее изобретение относится также к использованию соединения формулы I для лечения нейрональных повреждений, образовавшихся в результате общей и очаговой ишемии, и для лечения или профилактики нейродегенеративных состояний, таких как БАС, для лечения шума в ушах в качестве антиманиакальных депрессантов, обезболивающих средств местного действия, противоаритмических средств, противосудорожных средств и для лечения или профилактики диабетической невропатии и для лечения болей, включая острые и хронические боли и мигрени.
Другим объектом настоящего изобретения является фармацевтическая композиция, используемая для лечения нарушений, восприимчивых к блокированию Na+ каналов, причем композиция содержит эффективное количество соединения формулы I в смеси с по меньшей мере одним фармацевтически приемлемым носителем или разбавителем.
Ряд соединений, использованных в настоящем изобретении, до настоящего времени не опубликован. Таким образом, настоящее изобретение относится также к новым арилзамещенным пиразолам, триазолам и тетразолам формулы I.
Кроме того, настоящее изобретение относится к соединениям формулы I, содержащим радиоактивную метку 3H и 14С, и их использованию в качестве радиоактивных лигандов при их связывании с участками связывания на Na+ каналах.
Дополнительные варианты воплощения изобретения и его преимущества будут представлены ниже в подробном описании изобретения, а частично они представляются очевидными из описания или практических рекомендаций изобретения. Варианты воплощения и преимущества изобретения могут быть реализованы и получены с использованием элементов или комбинаций, которые подробно представлены в прилагаемых пунктах формулы изобретения.
Следует понимать, что представленные ниже общее описание изобретения, подробное описание и примеры приведены только в качестве иллюстрации и не ограничивают объем притязаний изобретения, как он заявлен в пунктах формулы изобретения.
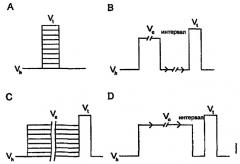
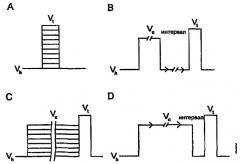
На чертеже представлены кривые импульса напряжения
А - Кривые ток-напряжение (IV-кривые);
С - Устойчивая инактивация;
В - Кинетика повторной активации;
D - Период связывания.
Сведения, подтверждающие возможность осуществления изобретения
Настоящее изобретение относится к открытию действия арилзамещенных пиразолов, триазолов и тетразолов формулы I в качестве блокаторов натриевых Na+ каналов. В связи с этим открытием соединения формулы I используют для лечения нарушений, восприимчивых к блокированию каналов ионов натрия.
Соединениями, относящимися к данному объекту настоящего изобретения, являются арилзамещенные пиразолы или триазолы, представленные формулой I
или их фармацевтически приемлемая соль, пролекарство или сольват, где
Х выбирают из группы, включающей в себя О, S;
Het означает гетероарил, который выбирают из группы, состоящей из
R1 выбирают из группы, включающей в себя водород, (С1-С6)алкил, C(O)R10;
R2 и R3 независимо выбирают из группы, включающей в себя водород и аминокарбонил;
R5, R6, R7 и R8 независимо выбирают из группы, включающей в себя водород, галоген, галоген(С1-С6)алкил и нитро;
R10 означает OR11;
R11 выбирают из группы, включающей в себя водород и (С1-С6)алкил.
Таким образом, настоящее изобретение относится к разработке способа лечения, профилактики или снижения нейрональных потерь, являющихся результатом общей или очаговой ишемии; лечения, профилактики или снижения интенсивности болей, включая острые и хронические боли, а также невропатические боли; лечения, профилактики или снижения интенсивности судорог или нейродегенеративных состояний; лечения, профилактики или снижения интенсивности маниакальной депрессии; с использованием в качестве обезболивающих средств местного назначения, антиаритмических средств, а также способа лечения звона в ушах путем введения соединения формулы I млекопитающему, нуждающемуся в подобном лечении.
R1 предпочтительно выбирают из группы, включающей в себя водород и C(O)R10;
R10 предпочтительно означает OR11, где R11 определен выше.
R2 и R3 предпочтительно независимо выбирают из группы, включающей в себя водород и аминокарбонил.
Каждая из групп R5-R8 замещает атом водорода, который в ином случае присутствует в любом положении арильного кольца, к которому присоединена группа R.
R5, R6, R7 и R8 предпочтительно независимо выбирают из группы, включающей в себя водород, галоген (предпочтительно, хлор или фтор), галоген(С1-С6)алкил, нитро.
Одна группа предпочтительных соединений, относящихся к формуле I, включает в себя соединения, в которых R1 означает С(O)R10, где R10 определен выше. В этой группе соединений Х более предпочтительно означает О или S и наиболее предпочтительно О.
Наиболее предпочтительными в этой группе являются соединения, где R5 и R6 означают водород; R2 и R3 оба означают Н; a R7 и R8 выбирают из группы, включающей в себя водород, галоген, галоген(С1-С6)алкил, нитро.
Другая группа предпочтительных соединений включает в себя соединения формулы I
или их фармацевтически приемлемую соль, пролекарство или сольват, где
Х означает О или S, предпочтительно О; Het означает гетероарил, который выбирают из группы, состоящей из
предпочтительно (i) или (iii);
R1 предпочтительно означает С(O)R10;
R2 и R3 независимо означают водород; R5 и R6 определены выше и предпочтительно означают водород; R7 и R8 независимо выбирают из группы, включающей в себя водород, галоген, галоген(С1-С6)алкил, нитро.
Примеры предпочтительных соединений, которые могут быть использованы в данном способе по настоящему изобретению, включают без ограничения нижеперечисленным:
1-[4-(4-нитрофенокси)фенил]-1Н-[1,2,4]триазол;
1-[4-(4-фторфенокси)фенил]-3-метилпиразол;
3-метил-1-(4-феноксифенил)пиразол;
1-(4-феноксифенил)-1Н-пиразол-3-карбоксамид;
1-(4-феноксифенил)-1Н-пиразол-5-карбоксамид;
1-[4-(4-фторфенокси)фенил]-1Н-пиразол-3-карбоксамид;
1-[4-(4-нитрофенокси)фенил]-1Н-[1,2,4]триазол-3-карбоксамид и
1-[4-(4-хлор-2-фторфенокси)фенил]-1Н-пиразол-3-карбоксамид.
Другая группа примеров предпочтительных соединений, которая может быть использована по настоящему изобретению, включает в себя 1-[4-(4-фторфенокси)фенил]-5-метилпиразол, 1-(4-феноксифенил)-1Н-пиразол-4-карбоксамид и 4-(4-фторфенокси)фенилпиразол.
Подходящими арильными группами являются С6-С14арил, прежде всего С6-С10арил. Типичные С6-С14арильные группы включают в себя фенил, нафтил, фенантрил, антрацил, инденил, азуленил, бифенил, бифениленил и флуоренильные группы.
Подходящими циклоалкильными группами являются С3-С8циклоалкил. Типичные циклоалкильные группы включают в себя циклопропил, циклобутил, циклопентил, циклогексил и циклогептил.
Термин "гетероарил", использованный в данном описании, относится к группам, содержащим от 5 до 14 атомов в цикле; 6, 10 или 14 п-электронов, объединенных в циклическую систему; и содержащие атомы углерода и 1, 2 или 3 гетероатомов кислорода, азота или серы (где примерами гетероарильных групп являются тиенил, бензо[b]тиенил, нафто[2,3-b]тиенил, тиантренил, фурил, бензофурил, пиранил, изобензофуранил, бензоксазонил, хроменил, ксантенил, феноксантиинил, 2Н-пирролил, пирролил, имидазолил, пиразолил, пиридил, пиразинил, пиримидинил, пиридазинил, индолизинил, изоиндолил, 3Н-индолил, индолил, индазолил, пуринил, 4Н-хинолизинил, изохинолил, хинолил, фталазинил, нафтиридинил, хиназолинил, циннолинил, птеридинил, 4аН-карбазолил, карбазолил, β-карболинил, фенантридинил, акридинил, перимидинил, фенантролинил, феназинил, тиазолил, изотиазолил, фенотиазинил, изоксазолил, фуразанил и феноксазинил.
Подходящие галогеновые группы включают в себя фтор, хлор, бром и иод.
Подходящие алкильные группы включают в себя линейные и разветвленные С1-С10алкильные группы, более предпочтительно С1-С6алкильные группы. Типичные С1-С10алкильные группы включают в себя метил, этил, пропил, изопропил, бутил, втор-бутил, трет-бутил, 3-пентил, гексил и октил. Подходящей является также триметиленовая группа, использованная в качестве заместителя в двух соседних положениях бензольного кольца соединений по настоящему изобретению.
Подходящими алкенильными группами являются С2-С6алкенильные группы, предпочтительно С2-С4алкенил. Типичные С2-С4алкенильные группы включают в себя этенил, пропенил, изопропенил, бутенил и втор-бутенил.
Подходящими алкинильными группами являются С2-С6алкинильные группы, предпочтительно С2-С4алкинил. Типичные С2-С4алкинильные группы включают в себя этинил, пропинил, бутинил и 2-бутинильную группу.
Подходящие арилалкильные группы включают в себя любые из упомянутых выше С1-С10алкильных групп, замещенных любыми упомянутыми выше С6-С14арильными группами. Подходящие значения включают в себя бензил, фенетил и нафтилметил.
Подходящие арилалкенильные группы включают в себя любые из упомянутых выше С2-С4алкенильных групп, замещенных любыми упомянутыми выше С6-С14арильными группами.
Подходящие арилалкинильные группы включают в себя любые из упомянутых выше С2-С4алкинильных групп, замещенных любыми упомянутыми выше С6-С14арильными группами. Подходящие значения включают в себя фенилэтинил и фенилпропинил.
Подходящие гетероарилалкильные группы включают в себя любые из упомянутых выше С1-С10алкильных групп, замещенных любыми упомянутыми выше гетероарильными группами.
Подходящие гетероарилалкенильные группы включают в себя любые из упомянутых выше С2-С4алкенильных групп, замещенных любыми упомянутыми выше гетероарильными группами.
Подходящие гетероарилалкинильные группы включают в себя любые из упомянутых выше С2-С4алкинильных групп, замещенных любыми упомянутыми выше гетероарильными группами.
Подходящие циклоалкилалкильные группы включают в себя любые из упомянутых выше С1-С10алкильных групп, замещенных любыми упомянутыми выше циклоалкильными группами.
Подходящие галогеналкильные группы включают в себя С1-С10алкильные группы, замещенные одним или более атомами фтора, хлора, брома или иода, например фторметил, дифторметил, трифторметил, пентафторэтил, 1,1-дифторэтил и трихлорметил.
Подходящие гидроксиалкильные группы включают в себя С1-С10алкильные группы, замещенные гидроксигруппой, например гидроксиметил, гидроксиэтил, гидроксипропил и гидроксибутил.
Подходящие алкоксигруппы включают в себя кислород, замещенный одной из С1-С10алкильных групп, упомянутых выше.
Подходящие алкилтиогруппы включают в себя серу, замещенную одной из С1-С10алкильных групп, упомянутых выше.
Подходящими ациламиногруппами являются любые С1-С6ацил(алканоил) группы, присоединенные к аминному азоту, например ацетамидо, пропионамидо, бутаноиламидо, пентаноиламидо, гексаноиламидо, а также арилзамещенные С2-С6замещенные ацильные группы.
Подходящими ацилоксигруппам и являются любые ацил(алканоил) группы, присоединенные к окси (-O-) группе, например ацетокси, пропионоилокси, бутаноилокси, пентаноилокси, гексаноилокси и т.п.
Термин "гетероцикл" использован в данном описании для обозначения насыщенной или частично ненасыщенной 3-7-членной моноциклической или 7-10-членной бициклической кольцевой системы, которая состоит из атомов углерода и из от одного до четырех гетероатомов, независимо выбранных из группы, состоящей из О, N и S, где гетероатомы серы и азота могут быть необязательно окислены, а азот может быть необязательно кватернизован, причем упомянутая система включает в себя любую бициклическую систему, в которой определенные выше гетероциклические кольца могут быть конденсироваными с бензольным кольцом, и где бициклическое кольцо может быть замещено по атому углерода или азота, при условии, что полученное соединение является стабильным. Примеры включают в себя без ограничения перечисленным пирролидин, пиперазин, морфолин, имидазолин, пиразолидин, бензодиазепины и т.п.
Подходящие гетероциклоалкильные группы включают в себя любые из упомянутых выше С1-С10алкильных групп, замещенных любыми упомянутыми выше гетероциклическими группами.
Подходящими алкиламино и диалкиламино группами являются -NHR20 и -NR20R21, где R20 и R21 являются С1-С10алкильными группами.
Аминокарбонильной группой является -С(O)NH2.
Подходящими алкиламинокарбонильными группами являются карбонильные группы, замещенные группами -NHR20 и -NR20R21, где R20 и R21 являются С1-С10алкильными группами, как определено выше.
Подходящие алкилтиольные группы включают в себя любые упомянутые выше С1-С10алкильные группы, замещенные -SH группой.
Подходящие алкилсульфинильные группы включают в себя любые упомянутые выше С1-С10алкильные группы, присоединенные к сульфинильной группе (-SO-).
Подходящие алкилсульфонильные группы включают в себя любые упомянутые выше С1-С10алкильные группы, присоединенные к сульфонильной группе (-SO2-).
Карбамоилоксигруппа означает -O-С(O)-NH2.
Карбоксигруппа означает -СООН.
Азидогруппа означает -N3.
Уреидогруппа означает -NH-С(O)-NH2.
Аминогруппа означает -NH2.
Амидная группа означает органический радикал, содержащий в качестве функциональной группы -NHC(О)-.
Изобретение, описанное в контексте данной заявки, охватывает все фармацевтически приемлемые соли описанных соединений. Фармацевтически приемлемые соли включают в себя без ограничения перечисленным соли металлов, такие как соль натрия, соль калия, соль цезия и т.п.; соли щелочноземельных металлов, такие как соль кальция, соль магния и т.п.; соли органических аминов, такие как соль триэтиламина, соль пиридина, соль пиколина, соль этаноламина, соль триэтаноламина, соль дициклогексиламина, соль N,N'-дибензилэтилендиамина и т.п.; соли неорганических кислот, такие как гидрохлорид, гидробромид, сульфат, фосфат и т.п.; соли органичесих кислот, такие как формиат, ацетат, трифторацетат, малеат, тартрат и т.п.; сульфонаты, такие как метансульфонат, бензолсульфонат, п-толуолсульфонат и т.п.; соли аминокислот, такие как аргинат, аспаргинат, глутамат и т.п.
Настоящее изобретение предназначено также для охвата пролекарств описанных соединений. Пролекарства представляют собой любые ковалентно связанные носители, высвобождающие in vivo исходное лекарственное активное средство. Примеры пролекарств включают в себя сложные эфиры или амиды формулы I, где радикалы R2-R11 означают гидроксиалкил или аминоалкил, причем эти соединения могут быть получены при их взаимодействии с ангидридами, такими как ангидрид янтарной кислоты.
Настоящее изобретение охватывает также продукты метаболизма in vivo заявленных соединений. Такие продукты могут образоваться в результате окисления, восстановления, гидролиза, амидирования, этерификации и т.д. вводимого соединения, в основном, вследствие ферментативного процесса. Соответственно изобретение включает в себя соединения, образующиеся в процессе контактирования соединения с организмом в течение времени, достаточного для образования продукта метаболизма. Такие продукты обычно идентифицируют с использованием соединения по настоящему изобретению, содержащего радиоактивную метку, которое вводят в детектируемой дозе парентеральным способом животному, такому как крыса, мышь, морская свинка, обезьяна или человек, выдерживают их в течение достаточного времени для процесса метаболизма, затем выделяют продукты превращения соединения из мочи, крови или других биологических образцов.
Изобретение, описанное в данном контексте, включает в себя соединения, содержащие изотопную метку, т.е. содержащие один или более атомов с другой атомной массой или массовым числом. Примеры изотопов, которые могут быть включены в описываемые соединения, включают в себя изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, такие как 2H, 3H, 13С, 14С, 15N, 18O, 17О, 31P, 32P, 35S, 18F и 36Cl соответственно.
Некоторые из соединений, описанных в данном контексте, могут содержать один или более асимметричных центров, что может приводить к образованию энантиомеров, диастереомеров и других стереоизомерных форм. Настоящее изобретение также включает рацемические смеси, смеси их разделенных форм, также как и индивидуальные энантиомеры, которые могут быть разделены в соответствии с методами, хорошо известными специалистам в данной области техники. Если соединения, описанные в данном контексте, содержат двойные связи или другие центры геометрической асимметрии и если это не оговорено специально, они включают в себя оба геометрических изомера Е и Z. Настоящее изобретение охватывает также все таутомеры.
Использованный в данном контексте термин "стереоизомеры" является общим термином для обозначения всех изомеров индивидуальных молекул, отличающихся только ориентацией их атомов в пространстве. Он включает в себя энантиомеры и изомеры соединений с более чем один хиральным центром, который не является зеркальным отображением другого изомера (диастереомеры).
Термин "хиральный центр" означает атом углерода, к которому присоединены 4 различных группы.
Термин "энантиомер" или "энантиомерный" означает молекулу, которая не может быть совмещена со своим зеркальным отображением и, следовательно, является оптически активной, причем энантиомер вращает плоскость поляризованного света в одном направлении, а его зеркальное отображение вращает плоскость поляризованного света в противоположном направлении.
Термин "рацемический" означает смесь равных частей энантиомеров, которая является оптически неактивной.
Термин "разделение" означает разделение или концентрирование или обеднение одной из двух энантиомерных форм молекулы. Словосочетание "энантиомерный избыток" означает смесь, в которой один из энантиомеров присутствует в большей концентрации по сравнению с молекулой его зеркального отображения.
Поскольку соединения формулы I являются блокаторами натриевых каналов, они могут быть использованы для лечения ряда заболеваний и состояний, опосредованных притоком ионов натрия. Следовательно, изобретение относится к способу лечения, профилактики или снижения нейрональных потерь, связанных с инсультом, общей или очаговой ишемией, травмами центральной нервной системы, гипогликемией или хирургией, травмами спинного мозга, а также к способу лечения и снижению интенсивности нейродегенеративных заболеваний, включающих болезнь Альцгеймера, амиотропный побочный склероз, болезнь Паркинсона, лечение или снижение интенсивности тревожных состояний, судорог, глаукомы, мигреней и мышечных спазмов. Соединения формулы I используют также в качестве лекарственных средств от звона в ушах, противоманиакальных депрессантов, обезболивающих средств местного назначения, противоаритмических средств, а также для лечения, профилактики или снижения интенсивности болей, включая послеоперационные, хронические и невропатические боли. В каждом случае согласно способу по настоящему изобретению требуется введение животному, нуждающемуся в таком лечении, эффективного количества блокатора натриевых каналов по настоящему изобретению, или его фармацевтически приемлемой соли, или пролекарства.
Изобретение также направлено на разработку способа лечения состояний, восприимчивых к блокированию натриевых каналов, у животных, подверженных таким заболеваниям. Наиболее предпочтительные варианты воплощения настоящего изобретения заключаются в использовании арилзамещенных гетероарильных соединений в способе по настоящему изобретению, представленных определенной выше формулой I.
Соединения по настоящему изобретению могут быть получены с использованием методов, известных специалистам в данной области техники.
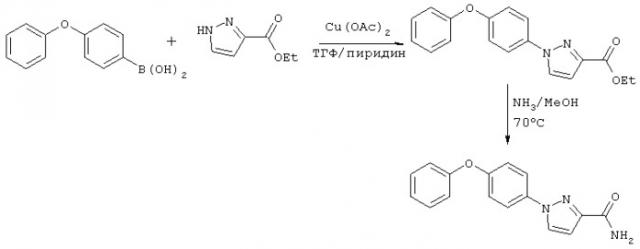
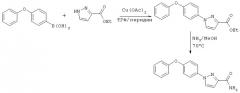
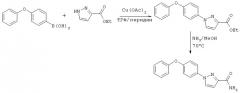
Синтез пиразолов формулы I может быть осуществлен, как показано на схемах Синтез 1 и 2. Конденсацию бороновой кислоты проводят согласно методике, описанной в статье Lam Y.S. и соавт., Tetrahedron Lett., 39: 2941-2944 (1998).
Синтез 1
Синтез 2
Триазолы формулы I могут быть получены, как показано на схеме Синтез 3, с использованием выпускаемого в промышленности 4-(1,2,4-триазол-1-ил)фенола (производства фирмы Lancaster Synthesis).
Синтез 3
Изобретение относится к соединениям формулы I, содержащим радиоактивную метку 3H и 14С, и к их использованию в качестве радиоактивных лигандов для определения участков связывания в натриевом канале. Например, одним из способов использования меченых соединений по изобретению является характеризация специфического связывания с рецептором. Другим применением меченых соединений по изобретению, наряду с испытанием на моделях животных, является изучение взаимосвязи структуры и активности. Конкурентный анализ связывания с рецепторами проводят при постоянной концентрации меченого соединения формулы I и возрастающих концентрациях тестируемого соединения.
Содержащие тритий соединения формулы I могут быть получены путем введения трития в соединение формулы I, например, методом каталитического дегалогенирования в присутствии трития. Этот способ включает в себя взаимодействие соответствующего галогензамещенного предшественника соединения формулы I в атмосфере газообразного трития в присутствии подходящего катализатора, например Pd/C, в присутствии или отсутствии основания. Другие подходящие методы описаны в книге Filer "Isotopes in the Physical and Biomedical Sciences" (Изотопы в физических и медикобиологических исследованиях) т.1, Labeled Compounds (Меченые соединения) (часть А), глава 6. 14C-меченые соединения могут быть получены с использованием исходного материала, содержащего углерод 14С.
Способность соединений по настоящему изобретению блокировать натриевые каналы исследуют путем электрофизиологического анализа диссоциированных нейронов гиппокампа. Связывание этих соединений с нейронными потенциалозависимыми натриевыми каналами может быть также исследовано с использованием мембран передней доли мозга крысы и [3H]ВХТ-В.
Натриевые каналы представляют собой высокомолекулярные трансмембранные белки, экспрессируемые в различных тканях. Эти потенциалозависимые каналы являются ответственными за быстрое возрастание проницаемости ионов Na+ в ответ на деполяризацию, связанную с потенциалом действия, во многих возбудимых клетках, включая мышечные, нервные клетки и клетки сердечной мышцы.
Аспектом настоящего изобретения является открытие механизма действия соединений, описанных в данном контексте в качестве специфических блокаторов Na+ каналов. На основании открытия такого механизма эти соединения могут быть использованы для лечения или профилактики нейрональных потерь, происходящих в результате очаговой или общей ишемии, и для лечения или профилактики нейродегенеративных нарушений, включая БАС, состояние тревоги и эпилепсию. Предполагается также, что такие соединения будут эффективными при лечении, профилактике или уменьшении интенсивности невропатических болей, послеоперационных болей, хронических болей и шума в ушах. Предполагается также, что соединения будут использованы в качестве противоаритмических средств, обезболивающих средств и противоманиакальных депрессантов.
Настоящее изобретение относится к соединениям формулы I, которые являются блокаторами потенциалозависимых натриевых каналов. Согласно настоящему изобретению такие соединения, обладающие свойствами, предпочтительно блокирующими натриевые каналы, характеризуются величиной IC50 приблизительно 100 мкМ или менее, измеренной методом электрофизиологического анализа, который описан в данном контексте. Величина IC50 соединений по настоящему изобретению предпочтительно составляет 10 мкМ или менее. Наиболее предпочтительно величина IC50 соединений по настоящему изобретению составляет 1,0 мкМ или менее. Замещенные гетероарильные соединения по настоящему изобретению могут быть исследованы для определения их блокирующей Na+ каналы активности с использованием следующих методов: электрофизиологического анализа и анализа связывающей активности.
Электрофизиологический метод анализа
Подготовка клеток: клеточная линия НЕК-293 (NaIIA-B2), стабильно экспрессирующая изоформу rBIIA Na+ каналов, получена в лаборатории. Клетки культивируют по стандартной технологии, как описано ранее (см. статью Verdoom Т.А., Neuron, 4: 919-928 (1990)). Для электрофизиологического анализа клетки наносят на предварительно покрытые поли-D-лизином чашки Петри Cellware размером 35 мм (производства фирмы BIOCOAT, Becton Dickinson) при плотности ˜104 клеток на чашку в день пересеивания из конфлуентной культуры. Эксперименты показали, что клетки пригодны для измерений в течение 2-3 суток после нанесения.
Измерение потенциалозависимых Na+ токов методом фиксации потенциала: измерения методом фиксации потенциала на целых клетках проводят с использованием стандартных методов фиксации потенциала (см. статью HamiII и соавт., Pfluegers Arch., 391: 85-100 (1981)) и усилителя Axopatch 200A amplifier (производства фирмы Axon Instruments, Foster City, CA). В измерительную камеру непрерывно подают внешний раствор (150 мМ NaCl, 5,4 мМ KCI, 1,8 мМ CaCl2, 1 мМ MgCl2, 10 мМ HEPES, 10 мМ глюкозы, рН 7,4 доводят NaOH, величина осмоляльности составляет ˜320 ммоль/кг) со скоростью приблизительно 1 мл/мин. Измерительные пипетки вытягивают из толстостенных капилляров (производства фирмы WPI, Sarasota, FI) и оплавляют в пламени. Интервал сопротивления пипетки, заполненной внутренним раствором (содержащим в мМ: 130 CsF, 20 NaCl, 2 MgCl2, 10 EGTA, 10 HEPES, рН доводят до 7,4 CsOH, осмоляльность составляет ˜320 ммоль/кг), составляет от 1 до 3 МОм. Лекарственные средства и промежуточные промывные растворы вводят через линейный пучок шлангов (производства фирмы Drummond Microcaps, 2 мкл, длина 64 мм). Соединения растворяют в диметилсульфоксиде (ДМСО) и получают исходный 30 мМ раствор, который впоследствии разбавляют внешним раствором до конечной концентрации 0,1-100 мкМ. При самой высокой концентрации (1%) ДМСО лишь незначительно ингибирует величину Na+ тока. Величину тока регистрируют при комнатной температуре (22-25°С), фильтруют при 3 кГц с использованием активного 8-полюсного фильтра Bessel (производства фирмы Frequency Devices, Haverhill, MA), переводят в цифровую форму через интервалы 10-15 мкс и сохраняют с использованием аналого-цифрового интерфейса Digidata 1200 и программного обеспечения Pclamp6/Clampex (фирмы Axon Instruments). При необходимости последовательное сопротивление обычно компенсируют примерно на 75%.
Для оценки эффективности и кинетики ингибирования Na+ каналов соединениями по изобретению используют кривые импульса напряжения, представленные на чертеже.
Для регистрации напряжения, при котором достигается максимальная величина внутреннего Na+ тока, используют зависимость тока от напряжения (IV-кривые), кривая А. При проведении эксперимента эту величину используют в качестве испытательного напряжения, Vt. Кривую устойчивой инактивации (или наличия), кривая С, используют для регистрации напряжения, при котором наблюдается практически полная (≥95%) инактивация Na+ каналов, эту величину используют на протяжении всего эксперимента в качестве кондиционирующего предварительного импульса Vc. На кривой В показано, как быстро каналы восстанавливаются после инактивации при гиперполяризованном напряжении. Эта кривая позволяет установить продолжительность интервала гиперполяризации, который используют при измерении кинетики связывания соединений с инактивированными Na+ каналами (кривая D). Повторная активация каналов в контрольных условиях происходит быстро (≥90%-ное восстановление в течение первых 5-10 мс). Если лекарственное средство значительно замедляет процесс повторной активации, то становится возможным (кривая D) точно измерить кинетику связывания ингибитора с инактивированными каналами, а также устойчивое сродство (k+ и Кi). Для определения величины k+ строят зависимость уменьшения пиков тока в последовательных экспериментах при варьировании интервала предварительного импульса от продолжительности предварительного импульса и измеряют постоянную времени (т) методом моноэкспоненциального приближения. Зависимость 1/т от концентрации антагониста позволяет рассчитать макроскопические скорости связывания антагонистов. Для определения величины Ki кривые частичного ингибирования, измеренные при фракционных откликах в устойчивом состоянии, приводили в соответствие с логистическим уравнением
где Iконтрольный означает максимальный Na+ ток в отсутствие антагонста, [антагонист] означает концентрацию лекарственного средства, Ki означает концентрацию антагониста, при которой наблюдается половина максимального ингибирования и р означает величину наклона.
Анализ связывания in vitro
Способность соединений по настоящему изобретению модулировать участок 1 и участок 2 Na+ каналов определяют с использованием следующих операций, подробно описанных в статьях Yasushi, J. Biol. Chem., 261: 6149-6152 (1986) и Creveling, Mol. Pharmacol., 23: 350-358 (1983) соответственно. В качестве источника белков Na+ каналов используют мембраны передней доли мозга крысы. Анализ связывания проводят в 130 мкМ холинхлориде при 37°С и при инкубировании в течение 60 мин в присутствии [3H]сакситоксина и [3Н]батрахотоксина в качестве радиоактивно меченных лигандов для участка 1 и участка 2 соответственно.
Фармакологические исследования in vivo
Соеди