Способ получения солей селенопирилия
Иллюстрации
Показать всеИзобретение относится к улучшенному способу получения солей селенопирилия путем взаимодействия 1,5-дикетонов с селеноводородом, который получают при растворении селенида цинка в смеси уксусной кислоты, бромистого водорода и диэтилового эфира. Реакционную среду получают путем прибавления бромангидрида уксусной кислоты к смеси диэтилового эфира и водного раствора бромистого водорода. Приведены - название, брутто-формула, температура плавления, выход целевого продукта, %: бромцинкат 2,4,6-трифенилселенопирилия, С23Н17SeZnBr3, 256-258°С, 75; бромцинкат 2,6-дифенил-4-(п-метоксифенил)-селенопирилия, C24H19SeOZnBr3, 247-252°C, 71; бромцинкат 2,6-дифенил-4-метилселенопирилия, C18H15SeZnBr3, 205-207°C, 68. Все полученные соли были переведены в соответствующие перхлораты. Способ позволяет отказаться от применения газообразного селеноводорода.
Реферат
I. Область применения
Соли селенопирилия и их производные могут применяться в качестве материалов для оптоэлектроники, полупродуктов органического синтеза, лекарственных препаратов и др.[SU 1447824, Б.И. - 1988. - №48; SU 1703649 Б.И. - 1992. - №1; Бабенко В.А., Дядюша Г.Г., Кудинова М.А. и др. // Квантовая электроника. - 1980. - т.7. - С.1796-1802; Nelen M.I., Simard T.P., Davies Sh.R.... // J.Med.Chem. - 1999. - vol.42. - P.3953-3964].
II. Предшествующий уровень техники
Известен ряд методов синтеза солей селенопирилия: с использованием газообразного селеноводорода (ПДК 0,1 мг/м3 [Вредные вещества в промышленности Т.3. Неорганические и элементорганические соединения (под ред. Лазарева Н.В.) // Лен., "Химия". - 1977. - 607 С.]) на разных стадиях реакции [Кудинова М.А., Кривун С.В., Толмачев А.И. // ХГС. - 1973. - №6. - С.857-858; SU 1051089, Б.И. - 1983. - №40; Харченко В.Г., Древко Б.И. // ЖОрХ - 1982. - т.18, вып. 12. - С.2595-2597; Харченко В.Г., Древко Б.И. // ХГС-1984. - №9. - С.1283-1284; Харченко В.Г., Древко Б.И. // ХГС-1984. - №12. - С.1634-1637] многостадийным синтезом на основе селенопиронов [Nelen M.I., Simard T.P., Davies Sh.R.... // J.Med.Chem. - 1999. - vol.42. - P.3953-3964], которые сами получаются в несколько стадий с использованием супергидрида лития [Detty M.R., Murray B.J., Seidberg M.D. //J.Org. Chem. - 1982. - vol.47. - P.1968-1969].
Наиболее приемлемым является метод синтеза солей селенопирилия, который основан на взаимодействии в условиях кислотного катализа арилалифатических или «семициклических» 1,5-дикетонов с сероводородом, получаемым непосредственно в реакционной среде из селенида цинка [SU 1816762 Б.И. - 1993. - №19; Древко Б.И., Фоменко Л.А., Смушкин М.И., Жуков О.И., Харченко В.Г. // ХГС-1994. - №4. - С.569].
Недостатком данного метода являлась трудность получения 10-13 N растворов HCl в спиртах. Данные растворы получали многочасовым насыщением абсолютных спиртов газообразным хлористым водородом с постоянным контролем процесса насыщения среды титрованием.
III. Сущность изобретения
Целью данного изобретения является создание нового метода синтеза солей селенопирилия, который не был бы связан с применением газообразного селеноводорода и не требовал трудоемкого предварительного насыщения абсолютного спирта газообразными реагентами. Этого можно достигнуть, если концентрированный водный раствор бромоводорода, выпускаемый промышленностью (8-8,4 N), смешать с диэтиловым эфиром и бромангидридом уксусной кислоты, взятым в количествах, необходимых для полного удаления воды. Реакция бромангидрида уксусной кислоты с водой идет бурно, с выделением тепла, поэтому требуется охлаждение. Как известно, галогениды цинка плохо, а галогеноводороды недостаточно растворимы в уксусной кислоте [Коган В.Б., Фридман В.М., Караров В.В. Справочник по растворимости. - М.: Изд-во АН СССР. - 1961. т.1. - кн.1], поэтому в реакционную смесь и добавляли эфир, который устранял эти недостатки.
Таким образом была получена система: СН3СООН/HBr/Et2O.
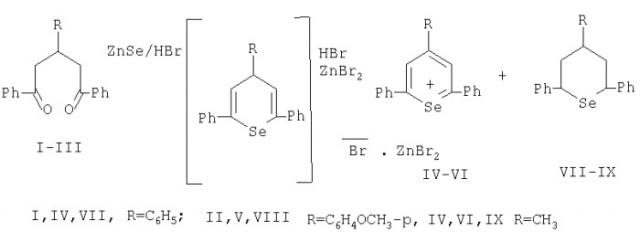
В данной реакционной среде легко проходило растворение селенида цинка с выделением селеноводорода, причем скорость образования селеноводорода не превосходила скорость его связывания в селеноорганические соединения. В результате реакции получали продукты диспропорционирования, промежуточно образующихся селенопиранов - смесь солей селенопирилия и селенациклогексанов.
Ход реакций и индивидуальность полученных соединений контролировали методом ТСХ на пластинах Silufol UV-254 в системах: гексан - эфир - хлороформ (3:1:1) и гесан - эфир (6:1, 10:1, 25:1), проявитель - пары иода.
Реакционную среду не изолировали от воздействия кислорода воздуха, что приводило к процессу солеобразования путем окисления промежуточно образующихся селенопиранов (помимо реакции диспропорционирования) [Древко Б.И., Сучков М.А., Веткин Д.О., Евдошенко Р.В., Харченко В.Г. // Сб. научн. трудов, Саратов, изд-во СГУ, 2000, с.59-60], поэтому выходы солей гетероароматических катионов были выше, чем соответствующие диспропорционированию 66,6%. Следовательно реакция частично протекала по схеме:
Все полученные соли переводили в соответствующие перхлораты (или тетрафторбораты) методом, описанным в работе [SU 1816762, Б.И. - 1993. - №19].
Для полной иллюстрации изобретения приводим конкретные методики выполнения синтеза.
Пример 1.
Получение бромцинката 2,4,6-трифенилселенопирилия (IV)
К смеси 5 мл концентрированной бромистоводородной кислоты и 20 мл диэтилового эфира при интенсивном охлаждении, по каплям прибавляют бромангидрид уксусной кислоты в количествах, необходимых для связывания всей поступившей в реакционную систему воды (обычно ˜17 мл). К полученному раствору добавляют при перемешивании 1,64 г (0,005 моль) 1,3,5-трифенилпентандиона-1,5 (I) и 0,87 г (0,006 моль) селенида цинка. Реакционную смесь перемешивают до полного исчезновения исходного дикетона по ТСХ (˜0,5 час), затем выпавшую соль селенопирилия отфильтровывают, промывают сухим эфиром (3×3 мл), сушат, получают 1,14 г (33,6%) IV. В маточный раствор добавляют 9 мл диэтилового и 17 мл диизопропилового эфира и выделяют через сутки дополнительно незначительные количества соли, которые обрабатывают аналогично, получают 0,36 г (3,9%). В маточный раствор добавляют 65 мл воды, происходит выпадение осадка, который отделяют и получают 1,05 г (31%) IV, который в значительной степени загрязнен различного рода примесями (в случае необходимости из эфирного раствора можно выделить 20-25% соответствующего селенациклогексана). Тпл=256-258°С. Выход 2,55 г (75%). ПМР спектр (CF3COOD/(CD3)2SO - 1:1) δ м.д.: 8.62 (с.,2Н,кат.); 7.28-7.73 (м.,15Н,Ph). Предполагаемая брутто-формула C23H17SeZnBr3 не сохраняется при перекристаллизации и постепенно переходит в форму С23Н17SeBr·0,5ZnBr2, поэтому соль идентифицировали через соответствующие перхлораты.
0,68 г (0.001 моль) Бромцинката IV растворяют в 10 мл 57% хлорной кислоты при нагревании на кипящей водяной бане. Гомогенный раствор охлаждают до комнатной температуры, выпавшие кристаллы отфильтровывают, промывают сухим эфиром (после добавления эфира в маточный раствор выпадает незначительное количество кристаллов X, которые отфильтровывают), сушат. Получают 0,4 г (85%) перхлората 2,4,6-трифенилселенопирилия (X), Т.пл.196-197°С. Лит. т.пл.196-197°С [Кудинова М.А., Кривун С.В., Толмачев А.И. // ХГС. - 1973. - №6. - С.857-858]. Проба смешения с достоверным образцом [SU 1816762 Б.И. - 1993. - №19] депрессии температуры плавления не дала.
При использовании соли селенопирилия X, полученной высаждением водой, выход составляет 72%.
Пример 2.
Получение бромцинката 2,6-дифенил-4-(п-метоксифенил)селенопирилия (V)
Выполняют аналогично примеру 1 исходя из 1,79 г (0,005 моль) 1,5-дифенил-4-(п-метоксифенил)пентандиона-1,5 (II). Получают 2,51 (71%) соли V. Тпл=247-252°С. ПМР спектр (CF3COOD/(CD3)2SO - 1:1) δ м.д.: 8.51 (с., 2Н, кат); 3.94 (с., 3Н, СН3); 6.82-8.09 (м., 14Н, аром.).
Предполагаемая брутто-формула C24H19SeOZnBr3 не сохраняется при перекристаллизации и постепенно переходит в форму C24H19SeOBr·0,5ZnBr2, потому соль идентифицировали через соответствующие перхлораты.
0,71 г (0.001 моль) Бромцинката V растворяют в 10 мл 57% хлорной кислоты при нагревании на кипящей водяной бане. Гомогенный раствор охлаждают до комнатной температуры, выпавшие кристаллы отфильтровывают, промывают сухим эфиром (после добавления эфира в маточный раствор выпадает незначительное количество кристаллов XI), сушат. Получают 0,46 г (91,5%) перхлората 2,6-дифнил-4-(п-метоксифенил)селенопирилия (XI), Т.пл.214-215. Лит. т.пл. 213-214°С [Кудинова М.А., Кривун С.В., Толмачев А.И. //ХГС. - 1973. - №6. - С.857-858]. Проба смешения с достоверным образцом [SU 1816762 Б.И. - 1993. - №19] депрессии температуры плавления не дала.
При использовании соли селенопирилия, полученной высаждением водой, выход составляет 74%.
Пример 3.
Получение бромцинката 2,6-дифенил-4-метилселенопирилия (VI)
Выполняют аналогично примеру 1 исходя из 1,33 г 1,5-дифенил-3-триметилпентандиона-1,5 (III). Т.пл.205-207°С. Получают 2,09 г (68%) соли VI. Тпл=205-207°С. ПМР спектр (CF3COOD/(CD3)2SO - 1:1) δ м.д.: 8.65 (с., 2Н, катион); 2.65 (с., 3Н, СН3); 7.65-8.05 (м., 10Н, аром.).
Предполагаемая брутто-формула C18H15SeZnBr3 не сохраняется при перекристаллизации и постепенно переходит в форму C18H15SeBr·0,5ZnBr2, потому соль идентифицировали через соответствующие перхлораты.
0,62 г (0.001 моль) Бромцинката VI растворяют в 10 мл 57% хлорной кислоты при нагревании на кипящей водяной бане. Гомогенный раствор охлаждают до комнатной температуры, выпавшие кристаллы отфильтровывают, промывают сухим эфиром (после добавления эфира в маточный раствор выпадает незначительное количество кристаллов XI), сушат. Получают 0,37 г (91%) перхлората 2,6-дифнил-4-метилселенопирилия (XII), Т.пл.194,5-196. Лит. т.пл.195-196°С [Кудинова М.А., Кривун С.В., Толмачев А.И. //ХГС. - 1973. - №6. - С.857-858]. Проба смешения с достоверным образцом [SU 1703649 Б.И. - 1992. - №1] депрессии температуры плавления не дала.
При использовании соли селенопирилия, полученной высаждением водой, выход составляет 71%.
Способ получения солей селенопирилия формулы I
где R= фенил, R'= фенил, возможно замещенный С1-С4алкокси, С1-С6алкил, A-=Br-.ZnBr2, ClO4 -, взаимодействием соответствующего 1,5-дикетона с селеноводородом, полученным путем растворения селенида цинка в реакционной среде, отличающийся тем, что реакционную среду создают смешением водного раствора бромистоводородной кислоты с диэтиловым эфиром и бромангидридом уксусной кислоты, взятом в количестве, необходимом для полного удаления воды.