Средство с антимутагенной активностью
Иллюстрации
Показать всеПредложено средство с антимутагенной активностью в отношении химических мутагенов. В качестве такового используется бетулиновая кислота, ранее известная как антимутаген по отношению к ультрафиолету и как антиоксидант. Показано снижение хромосомных аберраций у животных в отношении химических мутагенов диоксидина и циклофосфамида под действием бетулиновой кислоты в широком диапазоне доз. 3 табл.
Реферат
Настоящее изобретение относится к области медицины и ветеринарии и может быть использовано для подавления цитогенетического действия химических мутагенов. Более конкретно оно относится к отысканию новых и эффективных средств с антимутагенной активностью.
Сущность настоящего изобретения заключается в применении в качестве такого средства по отношению к химическим мутагенам известного и широко изученного химического соединения - бетулиновой кислоты.
В работе [1] была показана антимутагенность бетулиновой кислоты по отношению к такому физическому мутагену, как ультрафиолет. Однако антимутагенность этого вещества по отношению к химическим мутагенам не исследовалась, в то же время достоверно прогнозировать ее на основе указанной работы не представляется возможным не только в силу принципиального различия мутагенов, но и из-за характера опубликованного в [1] исследования, являвшегося единичным, проведенным в условиях in vitro с применением экзотической линии клеток. Кроме того, использовался метод оценки повреждений ДНК, в то время как для антимутагенных исследований рекомендуется [2] метод оценки хромосомных мутаций.
Антимутагенная активность бетулиновой кислоты (БК) по отношению к химическим мутагенам была обнаружена авторами изобретения при проведении исследований in vivo с использованием в качестве тестовых мутагенов таких веществ, как циклофосфамид и диоксидин, общепринятых для такого рода исследований.
Для оценки антимутагенных (мутагенмодифицирующих) свойств БК использовали метод учета хромосомных аберраций в клетках костного мозга мышей. Метод основан на визуальной микроскопической регистрации хромосомных повреждений в клетках костного мозга мелких лабораторных грызунов.
Исследование выполнено на самцах мышей линии C57BL/6 массой 18-20 г. Животных содержали при 12-часовом световом режиме, на стандартном брикетированном корме, при свободном доступе к воде в условиях вивария научно-исследовательской лаборатории фармакологической генетики НИИ фармакологии имени В. В. Закусова РАМН.
БК вводили перорально в водной суспензии твина-80 в дозах 1, 10 и 100 мг/кг. Мутагены: циклофосфамид из расчета 20 мг/кг и диоксидин в дозе 200 мг/кг вводили внутрибрюшинно в виде водных растворов. Применяли три режима обработки животных: однократное совместное введение БК с мутагеном, предварительное пятидневное введение БК, предусматривающее его сочетанное введение с мутагеном в последний день обработки животных, а также ежедневное совместное 5-дневное введение БК с мутагеном.
Цитогенетические препараты готовили через 24 часа после однократного или, в случае повторных введений, последнего введения препарата.
Во всех вариантах экспериментов животным за 2,5 часа до забоя вводили колхицин (Serva, Германия) из расчета 2,5 мг/кг с целью подавления формирования ахроматинового веретена клеточного деления и накопления метафаз.
Забой животных осуществляли смещением шейных позвонков. Затем максимально быстро выделяли бедренные кости, срезали эпифизы и вымывали клетки костного мозга гипотоническим раствором (0.55% KCl), предварительно подогретым до 37°С. После инкубации при 37°С в течение 15 минут клеточную взвесь центрифугировали 5 минут при 1000 об/мин. Надосадочную жидкость сливали, осадок ресуспензировали и добавляли 3 мл предварительно охлажденного фиксатора, состоящего из смеси этилового спирта и ледяной уксусной кислоты в соотношении 3:1. Время инкубации клеток в фиксаторе составляло 10 минут. Затем проводили повторное центрифугирование и смену фиксатора (3 мл). После этого клетки инкубировали в холодильнике еще 20 минут. Взвесь вновь центрифугировали, удаляли надосадочную жидкость, осадок ресуспендировали в 0.5 мл вновь добавленного фиксатора и наносили на мокрые предварительно обезжиренные и охлажденные стекла, которые высушивали в пламени спиртовой горелки.
Окраску производили азур-эозином. Состав красителя включал: 5 частей азура (0.1%), 2 части эозина (0.1%), 10 частей дистиллированной воды. При цитогенетическом анализе использовали микроскоп Zeiss Standart-20, 10×100.
При цитогенетическом анализе учитывали клетки с ахроматическими пробелами (гепами), одиночными и парными фрагментами хромосом, хромосомными и хроматидными обменами, а также клетки с множественными повреждениями хромосом (более 5 хромосомных повреждений в клетке). Оценку мутагенмодифицирующей активности производили путем сравнения суммарного количества клеток с гепами и структурными повреждениями хромосом в контрольных и опытных сериях исследования [3]. На каждое животное анализировали по 100 метафаз, в каждой группе было исследовано 4-5 животных. Статистический анализ проводили с помощью ϕ-критерия.
Результаты цитогенетического исследования представлены в таблицах 1-3.
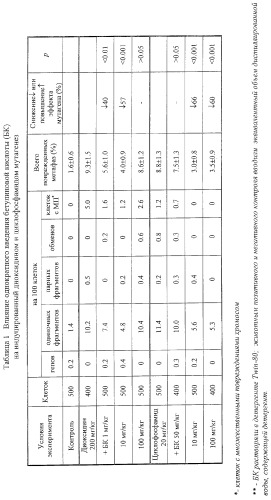
В таблице 1 представлены результаты, характеризующие влияние БК на цитогенетические эффекты диоксидина и циклофосфамида, применяемых из расчета 200 и 20 мг/кг соответственно, при однократном внутрибрюшинном введении изучаемых соединений.
Однократное введение диоксидина в дозе 200 мг/кг привело к увеличению клеток с хромосомными аберрациями до значения 9.3±1.5%, что статистически достоверно выше значения контроля (1.6±0.6%).
После введения комбинации БК в дозе 1 мг/кг и диоксидина зафиксировано 5,6±1.0% аберрантных метафаз. Полученный результат статистически достоверно отличается от значения позитивного контроля, проведенного с использованием мутагена, и свидетельствует о 40% снижении повреждающего кластогенного эффекта мутагена. Антимутагенный эффект БК в дозе 10 мг/кг возрос до 57%. В этом эксперименте было зарегистрировано 4.0±0.9% поврежденных метафаз. После использования БК в дозе 100 мг/кг также было выявлено снижение эффекта мутагена, однако оно не имело статистически значимого эффекта (табл.1).
Антимутагенные эффекты БК были подтверждены при использовании в качестве модельного мутагена циклофосфамида (табл.1).
При применении БК в дозах 10 и 100 мг/кг зарегистрирован сходный антимутагенный эффект: снижение повреждающего действия мутагена в обоих случаях составило 60-66% (уровень хромосомных аберраций соответственно 3.0±0.9% и 3.5±0.9% против 8.8±1.3% в позитивном контроле). В минимальной дозе - 1 мг/кг БК не проявил антимутагенной способности. Количество аберрантных клеток - 7.5±1.3%, выявленное в этом варианте эксперимента, не имело статистически достоверных отличий от значения позитивного контроля, характеризующего эффект мутагена,
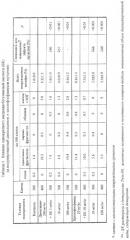
В следующей серии, результаты которой представлены в таблице 2, исследовалось влияние 5-дневной предобработки БК на проявление мутагенных эффектов диоксидина и циклофосфамида. Диапазон доз, в которых БК проявлял антимутагенность при этом режиме обработки животных, существенно сузился в сравнении с однократным введением. Снижение эффектов обеих мутагенов было выявлено только под влиянием БК, использованным в дозе 10 мг/кг. Цитогенетическая активность диоксидина была снижена на 44%, циклофосфамида на 59%. БК при использовании в дозах 1 и 100 мг/кг не вызывала достоверного изменения цитогенетических эффектов использованных мутагенов.
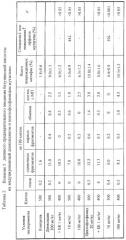
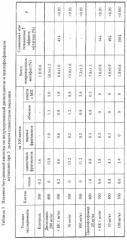
В следующей серии экспериментов исследовали влияние БК на мутагенные эффекты диоксидина и циклофосфамида в условиях 5-дневного совместного введения. Полученные результаты представлены в таблице 3.
После пятидневной обработки животных диоксидином в дозе 200 мг/кг хромосомные аберрации зарегистрированы в 10.5±1.5% исследованных метафаз. После совместного применения диоксидина и БК в дозе 1 мг/кг выявлено 6.0±1.0% поврежденных клеток, что соответствует 43% снижению эффектов мутагена. Результаты, полученные после совместного применения мутагена и БК в дозах 10 и 100 мг/кг составили соответственно 13.8±1.6% и 7.2±1.2% аберрантных метафаз. Попарное сопоставление этих результатов с данными позитивного контроля не выявило между ними статистически достоверных различий, т.е. так же, как в предыдущем случае, антимутагенная активность БК была выявлена при ее использовании только в одной дозе.
На фоне использования стандартного мутагена циклофосфамида БК проявила защитное действие во всем диапазоне исследованных доз. После совместного введения БК в дозе 1 мг/кг и мутагена зарегистрировано 3.6±0.8% аберрантных метафаз, что соответствует 54% снижению цитогенетического эффекта. При применении БК в дозе 10 мг/кг было зарегистрировано статистически значимое снижение цитогенетического эффекта мутагена до 4.0±0.9%, т.е. на 49%. Еще более выраженное антимутагенное действие БК было отмечено при ее использовании из расчета 100 мг/кг. Результат, выявленный в этом варианте эксперимента, - 1.8±0.6% аберрантных метафаз - практически совпадает с данными, выявленными у контрольных интактных животных, и указывает на полное подавление цитогенетического эффекта мутагена.
Проведенные исследования свидетельствуют о наличии у БК антимутагенной активности. Защитные эффекты БК наиболее выражены в условиях однократного введения, а также по отношению к циклофосфамиду при совместном повторном введении. Последнее наблюдение наряду с описанными данными других экспериментов, в которых антимутагенный эффект БК в количественном отношении лучше выражен по отношению к циклофосфамиду, позволяют заключить, что БК в проведенном исследовании наиболее эффективен в случае применения в качестве модельного мутагена циклофосфамида.
Таким образом, бетулиновая кислота в диапазоне доз 1-100 мг/кг обладает антимутагенной активностью, выражающейся в уменьшении цитогенетических эффектов химических мутагенов. Степень выраженности антимутагенного эффекта бетулиновой кислоты указывает на перспективу ее возможного применения в качестве фармакологического средства защиты генома.
Источники информации
1. Salti G.I., Kichina J.V., Das Gupta Т.К. et. al. Betulinic acid reduces ultraviolet-C-induced DNA breakage in congenital melanocytic naevai cells: evidence for a potential role as a chemopreventive agent // Melanoma Res, Apr. 2001; 11(2):9,9-104.
2. Методические указания по оценке канцерогенности фармакологических средств и вспомогательных веществ в краткосрочных тестах. // Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. - М. - Минздрав РФ - ИИА "Ремедиум". - 2000. - с.66-86.
3. Малашенко A.M., Суркова Н.И. и др. Определение мутагенности химических соединений (генетический скрининг) на лабораторных мышах (методические указания) - М., 1977.
Применение бетулиновой кислоты в качестве средства с антимутагенной активностью в отношении химических мутагенов.