Тетраазахлорины как фотосенсибилизаторы для фотодинамической терапии
Иллюстрации
Показать всеИзобретение относится к медицине, а более конкретно - к фотосенсибилизаторам для фотодинамической терапии (ФДТ) новообразований и ряда других заболеваний. Изобретение описывает тетраазахлорины общей формулы
где R1R2=С6H4, R3=R4=R5=CH3, М=НН (Н2ТВТАС);
R1R2=1,2-С10Н6; R3=R4=R5=СН3, M=Zn(Zn-1,2-TNTAC);
R1=R2=C6H5; R3=R4=R5=СН3, М=НН (H2TACPh6);
R1=R3=H, R2=R4=C6H5, R5R5=СН2N(СН3)СН2, М=НН (H2PyrTACPh4);
R1R2=4-C(CH3)3C6H3, R3=R4-Н, R5R5=CH2N(CH3)CH2, М=НН (H2TBtTACPyrN-Me).
в качестве фотосенсибилизаторов ближней ИК области спектра для фотодинамической терапии. Описываемые фотосенсибилизаторы обладают интенсивным поглощением в спектральной области 710-750 нм и могут быть использованы для лечения методом ФДТ глубоких опухолевых тканей. 1 ил., 5 табл.
Реферат
Настоящее изобретение относится к медицине, а более конкретно - к фотосенсибилизаторам для фотодинамической терапии (ФДТ) новообразований и ряда других заболеваний.
Метод ФДТ основан на использовании препаратов - фотосенсибилизаторов, которые обладают способностью при введении в организм накапливаться преимущественно в опухоли. При последующем световом, например лазерном, облучении патологического участка молекулы фотосенсибилизатора катализируют образование цитотоксических агентов, в частности синглетного кислорода, разрушающих опухолевые клетки.
Недостатком применяющихся в клинической практике фотосенсибилизаторов на основе производных гематопорфиринов, например HPD (hematoporphyrin derivative), фотофрин-2, является невысокая интенсивность поглощения в полосе фотовозбуждения (625-640 нм). Значительное собственное поглощение биологической ткани в этой спектральной области обусловливает малую глубину проникновения излучения и затрудняет лечение опухолей больших размеров (R. Bonnett. Photosensitizers of the porphyrin and phthalocyanine series for photodynamic therapy. Chem. Soc. Rev., 24(1), 19-33, 1995). В этом отношении преимущество имеют фотосенсибилизаторы на основе хлоринов (дигидропорфиринов), более интенсивная длинноволновая полоса поглощения которых смещена в красную область по сравнению с порфиринами. Среди них следует отметить водорастворимые моно-L-аспартилхлорин e6u (препараты NPe6, MACE) и другие различные формы хлорина e6, в частности отечественные препараты "Фотодитазин", "Радахлорин", а также синтетические хлорины - 5,10,15,20-тетракис(м-гидроксифенил)хлорин (темопорфин, m-THPC, фоскан) и производные бензопорфирина (бензопорфирин монокислота, кольцо А) с максимумом поглощения при 690 нм. Однако эти соединения весьма труднодоступны, к тому же их коэффициент экстинкции, как правило, невысок.
Весьма перспективными фотосенсибилизаторами являются производные фталоцианина, тетрабензотетраза - аналога порфиринов. Так, фотосенсибилизатор "Фотосенс" на основе сульфированного фталоцианина гидроксиалюминия, поглощающий при 675 нм с коэффициентом экстинкции, превышающим 105 л×моль-1·см-1 (E.A.Лукьянец. Новые сенсибилизаторы для фотодинамической терапии. Росс. хим. журнал, 42(5), 9-16, 1998), разрешен к клиническому применению в России для лечения ряда онкозаболеваний различных локализаций. Однако и в области поглощения "Фотосенса" собственное поглощение несенсибилизированных тканей остается значительным. Известно, что оно является минимальным только при длинах волн, превышающих 700 нм, в области так называемого "терапевтического окна". Кроме того, недостатком "Фотосенса" является длительное удерживание в коже, что требует тщательного соблюдения пациентами светового режима. "Фотосенс" является наиболее близким аналогом предлагаемых в настоящей заявке фотосенсибилизаторов.
В предлагаемом изобретении ставится задача создания фотосенсибилизаторов для ФДТ с интенсивным поглощением в спектральной области 710-750 нм. Указанная задача решается тем, что в качестве фотосенсибилизатора для ФДТ предлагаются новые соединения - производные тетраазахлорина - общей формулы
где R1R2=С6Н4, R3=R4=R5=СН3, М=НН(H2TBTAC);
R1R2=1,2-С10Н6; R3=R4=R5=СН3, М=Zn(Zn-1,2-TNTAC);
R1=R2=С6Н5; R3=R4=R5=СН3, М=НН (H2TACPh6);
R1=R3=Н, R2=R4=С6Н5, R5R5=СН2N(СН3)СН2, М=НН (H2PyrTACPh4);
R1R2=4-С(СН3)3С6Н3, R3=R4=Н, R5R5=СН2N(СН3)СН2, М=НН (H2TBtTACPyrBN-Me).
например, тетраметилтрибензотетраазахлорин (Н2ТВТАС), тетраметилтри-1,2-нафто-тетраазахлорин цинка (Zn-1,2-TNTAC), тетраметилгексафенилтетраазахлорин (Н2TACPh6), N-метилпирролидино-[3,4-b]тетрафенилтетраазахлорин (H2PyrTACPh4), N-метилпирролидино-[3,4-b]три-(4'-трет.-бутил)бензотетраазахлорин (H2TBtTACPyrN-Ме).
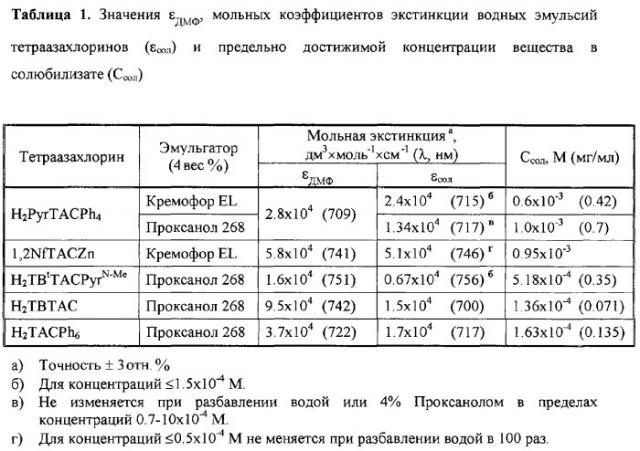
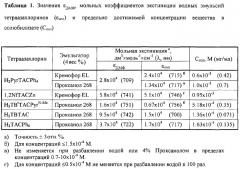
Предлагаемые производные тетраазахлорина синтезированы по разработанным нами методам. Тетраметилтрибензотетраазахлорин (Н2ТВТАС) и гексафенилтетраазахлорин (Н2TACPh6) получены конденсацией смеси тетраметилсукцинонитрила с соответствующими 1,2-динитрилами в диметиламиноэтаноле в присутствии диметиламиноэтилата лития, а три-1,2-нафтотетраазахлорин цинка (Zn-1,2-TNTAC) - аналогичной конденсацией в высококипящих органических растворителях в присутствии хлорида цинка [Патент РФ №2188200, кл. C 07 D 487/22 (2002). БИ №24 (2002)]. N-Метилпирролидино[3,4-b]тетрафенилтетраазахлорин (H2PyrTACPh4) и -три-(4'-трет.-бутил)бензотетраазахлорин (Н2ТВtACPyrN-Me) получены по аналогии с тетраарилпорфиринами (Silva A.M.G, Tome AC., Neves G.P.M.S., Silva A.M.S, Cavaleiro J.A.S., II J.Chem. Soc. Chem. Commun., 1999, р.1767) реакцией 1,3-циклоприсоединения соответствующих тетраазапорфинов с азометинилидом, генерируемым in situ из N-метилглицина и параформа. Все синтезированные тетраазахлорины нерастворимы в воде и использовались в виде их эмульсий в водных 4% растворах Кремофора EL и Проксанола 268 (таблица 1, чертеж).
Настоящее изобретение иллюстрируется следующими примерами.
ПРИМЕР 1. Синтез N-метилпирролидино[3,4-b]тетрафенилтетраазахлорина (H2PyrTACPh4). Нагревают при перемешивании раствор 50 мг (0.08 ммоль) тетрафенилтетраазапорфина в 5 мл о-дихлорбензола до 100°С в атмосфере аргона и добавляют 14 мг (0.16 ммоль) саркозина и 12 мг (0.4 ммоль) параформа. Далее реакционную смесь нагревают до 150°С и выдерживают при этой температуре в течение 1.5 ч. Затем охлажденную реакционную массу хроматографируют на силикагеле хлороформом. Вторую фракцию (смесь хлорина и изобактериохлорина) повторно хроматографируют на окиси алюминия толуолом. Собирают малиновую фракцию и после удаления растворителя получают 15 мг (27.5%) H2PyrTACPh4. Масс-спектр, m/z: 675 (М+). ЭСП, λмакс.(соотношение интенсивностей), хлороформ: 711 (1.0), 656 пл. (0.39), 547 (0.49), 358 (1.02), 333 (0.99).
Аналогично из три-(4'-трет.-бутил)бензотетраазапорфина получен N-метилпирролидино-[3,4-b]три-(4'-трет.-бутил)бензотетраазахлорин (H2TBtTACPyrN-Me).
ПРИМЕР 2. Синтез тетраметилгексафенилтетраазахлорина (H2TACPh6). Растворяют 0.01 г (14 ммоль) лития при нагревании в 20 мл диметиламиноэтанола, охлаждают до комнатной температуры. Добавляют смесь 0.82 г (3.6 ммоль) дифенилмалеонитрила и 0.49 г (3.6 ммоль) тетраметилсукцинонитрила, медленно нагревают при перемешивании до кипения и продолжают кипячение в течение 4 часов. Затем реакционную смесь охлаждают, разбавляют 100 мл воды, выпавший осадок отфильтровывают, промывают последовательно горячей водой, 50% водным этанолом, сушат на воздухе. Остаток растирают, экстрагируют этанолом для удаления примесей, затем хлорбензолом. Хлорбензольный экстракт упаривают в вакууме и хроматографируют на силикагеле хлороформом, собирают малиновую фракцию. Получают 0.025 г (3.8%) H2TACPh6. Найдено, %: С 78.45; Н 5.66; N 12.76. C56H44N8H2O. Вычислено, %: С 79.41; Н 5.47; N 13.23. Масс-спектр, m/z: 829.2 (М+). Электронный спектр поглощения. λмакс., нм (lg ε), хлороформ: 727 (4.63), 691пл. (3.85), 662пл. (3.69), 557 (4.10), 488 (3.57), 371 (4.32), 336 (4.33).
ПРИМЕР 3. Определение фототоксичности N-метилпирролидино[3,4-b]тетрафенилтетраазахлорина безметального (H2PyrTACPh4) in vitro.
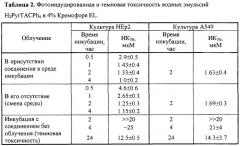
Тестирование проводили на культуре клеток эпидермоидной карциномы гортаноглотки человека НЕр2. Клетки рассевали в концентрации 40×103 кл/мл в лунки 96-луночного планшета ("Costar", США) в среде ИГЛА-МЕМ, содержащей 7% эмбриональную телячью сыворотку. Через 24 часа (начало логарифмической фазы роста культуры) вносили вещество в последовательных разведениях, инкубировали клетки в течение 2-5 часов и проводили облучение галогеновой лампой мощностью 500 Вт с использованием фильтра КС-13 (λ≥640 нм). Плотность мощности составляла 13.6-15.0 мВт/см2. Расчетная световая доза во всех экспериментах составляла 10 Дж/см2. Контролем служили: 1) клетки, не подвергавшиеся обработке красителем, растворителем и облучению, 2) клетки, подвергавшиеся облучению без предварительной инкубации с красителем, 3) клетки, инкубированные с красителем без последующего облучения, 4) клетки, обработанные 4% Кремофором с последующим облучением.
Результаты определения фототоксичности приведены в таблице 2.
ПРИМЕР 4. Определение фотодинамической активности водных эмульсий тетраазахлоринов in vivo.
Солидную форму асцитной карциномы Эрлиха (ОЭ) прививали подкожно на наружную поверхность нижней конечности мышей-самок линии СВА. Для имплантации использовали разведенную асцитическую жидкость (˜2.2×106 опухолевых клеток), взятую от мыши-донора на 7 день роста опухоли.
Образцы тетраазахлоринов в 4% Кремофоре EL или Проксаноле 268 фильтровали через мембранный фильтр 0.22 мкм и вводили животным внутривенно (в хвостовую вену) однократно на 6 день роста опухоли за 48, 24 или 0.5 часа до проведения ФДТ.
Сенсибилизированную опухоль облучали с помощью аппарата терапевтического онкологического для фотодинамической терапии АТО-1 и фильтрами КС-18 с максимумом пропускания на длине волн 700 нм и СЗС для фильтрации ультрафиолетовой части спектра. Плотность мощности излучения - 250 мВт/см2, плотность дозы - 300 Дж/см2. Перед облучением шерсть над опухолью удаляли. Продолжительность наблюдения за животными составляла 25 дней после лечения.
Эффективность воздействия оценивали по изменению объема опухоли (Vоп) и значениям торможения роста опухоли (ТРО), рассчитанным по формулам (2) и (3):
где D1, D2 и D3 - три взаимно перпендикулярных диаметра опухоли.
При исследовании фотодинамической активности in vivo водных эмульсий Н2PyrTACPh4 в 4% Кремофоре на мышах с опухолью Р-388 облучение проводили через 30 минут после введения с использованием аппарата АТО-1 с фильтрами КС-10 и СЗС. Плотность мощности излучения - 300 мВт/см2, световая доза - 270 Дж/см2.
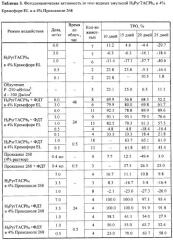
Результаты определения фотодинамической активности приведены в таблицах 3-5.
Эмульсия Н2PyrTACPh4 в 4% Кремофоре (Н2PyrTACPh4-CrEL) обладает фотоиндуцированной активностью на культуре опухолевых клеток человека (таблица 2). В стандартных условиях скрининга ИК50 при облучении составляет в среднем 1-33 мкМ (культура НЕР2) и 1.63 мкМ (культура А549), "темновая" токсичность в этом диапазоне концентраций отсутствует. Варьирование времени инкубации и условий облучения позволяет заключить, что близкая к максимуму эффективная концентрация H2PyrTACPh4 в клетках достигается к 2 часам и фототоксичность на этот срок обусловлена преимущественно внутриклеточным фотосенсибилизатором. Аналогичная эмульсия Zn-1,2-TNTAC обладает сравнительно низкой фотоиндуцированной активностью: величина ИК50 для него оказалась равной 31.0 мкМ (культура НЕР2).
Фотодинамическая активность in vivo водных эмульсий H2PyrTACPh4 изучена на мышах с солидной формой асцитной карциномы Эрлиха (ОЭ). H2PyrTACPh4 в водном растворе 4% Кремофора EL (в дозах 0.1-6.0 мг/кг) и 4% Проксанола 268 (в дозах 1.0-7.0 мг/кг) не подавлял роста опухоли в отсутствие светового воздействия, т.е. не обладал "темновой" цитотоксичностью (таблица 3). При проведении ФДТ через 48 и 24 часа после внутривенного введения Н2PyrTACPh4 в дозах 1.0, 3.0 и 6.0 мг/кг отмечен выраженный противоопухолевый эффект на всем протяжении наблюдения (ТРО=52.2-92.3%). При проведении сеанса облучения через 0.5 часа после введения фотосенсибилизатора в дозе 1.0 мг/кг терапевтический эффект регистрировался на протяжении 25 дней наблюдения (ТРО=61.9-65.1), а в дозе 0.5 мг/кг - только на 15-ый день после ФДТ (61.8%).
Раствор H2PyrTACPh4 в 4% Проксаноле 268 проявлял высокую фотодинамическую активность в отношении экспериментальной ОЭ при введении в дозах 3.5 и 7.0 мг/кг за 24 часа до сеанса ФДТ - торможение роста опухоли достигало 91.8-100% (таблица 3). При более низких дозах (1.0 и 0.5 мг/кг) биологически значимое подавление роста опухоли отмечалось при облучении через 0.5 часа после введения и составляло 52.6-70.0% на 15-25 день наблюдения. Сравнение фотодинамической активности H2PyrTACPh4 в Кремофоре EL и Проксаноле 268 не выявило существенных различий (таблица 3).
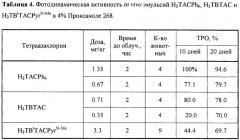
Водные эмульсии H2TACPh6, H2TBTAC и H2TBtTACPyrN-Me в 4% Проксаноле 268 в аналогичных условиях также не обладали "темновой" токсичностью и проявляли выраженную активность при проведении сеанса ФДТ через 2 часа после введения (таблица 4). Следует отметить высокую активность Н2ТВТАС, обеспечивающего высокие значения ТРО при низких дозах (до 0.35 мг/кг).
Изучена также фотодинамическая активность in vivo водных эмульсий H2PyrTACPh4 в 4% Кремофоре на мышах с опухолью Р-388. ФДТ с H2PyrTACPh4-CrEL приводило к развитию характерных тканевых реакций - отека с последующим формированием некротического струпа у всех животных через 8-9 дней после облучения. ФДТ с H2PyrTACPh4-CrEL приводила к выраженному подавлению роста опухоли Р-388 на все сроки наблюдения и увеличению продолжительности жизни животных (таблица 4). Лечебный эффект ФДТ выше при дозе фотосенсибилизатора 1.0 мг/кг, чем при дозе 0,5 мг/кг: ТРО превышало 80% при дозе 1.0 мг/кг и 70% при дозе 0.5 мг/кг; УПЖ при дозе 1.0 мг/кг составило 42.9%, при дозе 0.5 мг/кг - 24.9%.
Таким образом, предлагаемые в настоящем изобретении производные тетраазахлорина с интенсивным поглощением в спектральной области 710-750 нм представляют собой новый класс эффективных фотосенсибилизаторов ближней ИК области спектра, которые могут быть использованы для лечения методом ФДТ глубоких опухолевых тканей.
Тетраазахлорины общей формулы
где R1R2=С6H4, R3=R4=R5=CH3, М=НН (Н2ТВТАС);
R1R2=1,2-С10Н6; R3=R4=R5=СН3, M=Zn(Zn-1,2-TNTAC);
R1=R2=C6H5; R3=R4=R5=СН3, М=НН (H2TACPh6);
R1=R3=H, R2=R4=C6H5, R5R5=СН2N(СН3)СН2, М=НН (H2PyrTACPh4);
R1R2=4-C(CH3)3C6H3, R3=R4=Н, R5R5=CH2N(CH3)CH2, М=НН (H2TBtTACPyrN-Me).
как фотосенсибилизаторы для фотодинамической терапии.