Адаптоген
Иллюстрации
Показать всеПредложено: применение ацизола (бис(1-винилимидазол-N) цинка диацетата) в качестве адаптогена. Ацизол ранее был известен как антидот. Изобретение отличается тем, что ацизол превосходит элеутерококк по активности в отношении показателей функционального состояния адаптационных систем организма за счет обеспечения более высокой интенсивности тканевого дыхания, улучшения энергетического обмена и восстановительных процессов. 2 ил., 8 табл.
Реферат
Настоящее изобретение относится к медицине, в частности к новому адаптогену.
К адаптогенам относят препараты растительного происхождения (нативные или в виде чистых действующих веществ), обладающие малоспецифическим воздействием на функции ЦНС, эндокринную регуляцию, обменные процессы и повышающие адаптацию организма к неблагоприятным условиям [1].
Механизм адаптогенного воздействия (в том числе гликозидов элеутерококка) обусловлен ослаблением негативных биохимических и функциональных сдвигов при стресс-реакциях и активацией адаптивного синтеза РНК и белков, приводящей к улучшению энергетического обмена и восстановительных процессов. Для развития заметного эффекта требуется продолжительное время и регулярный прием (пик через 4-6 недель при ежедневном приеме).
Наиболее широко используемым и доступным является экстракт элеутерококка [2].
Недостатком этого известного способа является сравнительно невысокая эффективность и необходимость длительного и регулярного приема.
Задача изобретения - новое адаптогенное средство, обладающее более высокой эффективностью.
Указанная задача решается использованием ацизола в качестве адаптогена.
Известно применение ацизола - бис(1-винилимидазол-N) цинка диацетата - в качестве антидота при отравлении окисью углерода [3].
Выбор направлений изучения фармакологической активности препарата "Ацизол" определялся предполагаемыми показаниями к его применению, главным из которых является адаптация организма к неблагоприятным и экстремальным факторам окружающей среды (ионизирующее излучение и активация свободно-радикальных реакций, оксидантные повреждения, гипоксия, энергодефицитные состояния). Этими же соображениями руководствовались при выборе препаратов сравнения.
Из сравнительных нагрузочных тестов использовались модели антагонизма с гексеналом (антинаркозное действие) по продолжительности гексеналового сна [4], учет длительности восстановления способности к прямолинейному движению после вращения по К.Г.Васильеву [5], максимальной длительности статической работы (удержание белыми мышами своего тела на вертикальной сетке), длительности плавания мышей с грузом (динамической работы) [6]. Из моделей экстремальных факторов использовали моделирование гипоксии в замкнутом объеме ("баночная гипоксия") [7].
Ацизол и препарат сравнения вводили ежедневно per os на протяжении двух недель белым нелинейным мышам с помощью дозатора с атравматическим наконечником в 10 часов утра. Дозы препаратов были экстраполированы с человека на грызунов и составляли: Ацизол - 10 мг/кг, элеутерококк - 1 мл/кг.
Динамику веса животных определяли на весах ВЛР-500.
Содержание восстановленного глутатиона в печени определяли иодометрически [8], сульфгидрильных групп сыворотки крови - амперометрическим титрованием по Н.С.Рубиной [9], содержание гликогена - методом Самодьи [10].
Кровь для биохимических исследований получали после декапитации животных.
Содержание общего белка и липидов, холестерина, билирубина сыворотки крови определяли с помощью наборов Био-Ла-Тест Чешской фирмы "Лахема". Уровень глюкозы в крови и гомогенатах органов определяли ортотолуидиновым методом.
Интенсивность тканевого дыхания в гомогенатах органов определяли манометрическим методом Варбурга [11, 12]. Содержание АТФ - хроматографически [13].
Статистическую обработку результатов экспериментов проводили по Стьюденту-Фишеру.
Антагонизм с гексеналом
Антагонизм препаратов с гексеналом определялся после двух недель их ежедневного перорального введения мышам. Контрольная группа животных получала плацебо - дистиллированную воду в том же объеме. Гексенал вводился подкожно в дозе 70 мг/кг. Результаты теста представлены в табл.1.
Полученные данные свидетельствуют о достоверном наличии у Ацизола антинаркозного действия (длительность гексеналового сна сократилась), то есть препарат активирует детоксицирующую монооксигеназную систему печени.
Восстановление способности к прямолинейному движению после вращения
Тест учета длительности восстановления способности к прямолинейному движению после вращения демонстрирует эффективность препарата повышать адаптацию вестибулярного препарата к перегрузкам. Радиальное ускорение создавалось путем вращения мышей в центрифуге продолжительностью 15 с со скоростью 600 об/мин. Мыши при этом помещались в цилиндрические пластмассовые пробирки, закрытые с наружной стороны проволочной сеткой. Обычно после центрифугирования извлеченные из центрифуги мыши вращались вокруг продольной оси туловища или совершали манежные движения (перемещались по кругу).
В эксперименте использовали группы животных после ежедневного перорального введения на протяжении 14 дней исследуемого препарата и препарата сравнения. Каждую группу составляли 10 особей мужского пола. Одновременно вращали равное количество животных из каждой группы. Результаты представлены в таблице 2. Они свидетельствуют о том, что Ацизол достоверно уменьшал длительность восстановительного периода после вращения, т.е. улучшал способность вестибулярного аппарата к адаптации к радиальному ускорению.
Влияние препаратов на статико-силовую выносливость мышей
Влияние препаратов на статико-силовую выносливость изучали, регистрируя время висения мышей опытных и контрольной групп на вертикальной сетке. Животных тестировали после двухнедельного ежедневного введения препаратов. Критерием истощения статической силы считали время, когда мышь уже не могла удерживать вес своего тела и падала с сетки вниз (собственный вес мышей составлял среднем 28 г). Результаты эксперимента представлены в таблице 3. Они демонстрируют увеличение статической физической выносливости под воздействием всех препаратов.
Влияние на длительность плавания мышей
Плавание является тяжелой физической динамической нагрузкой, позволяющей оценить эффективность адаптогенов [14]. Оно осуществлялось с грузом (свинцовая трубка на резиновом кольце, прикрепляемая к корню хвоста), равным 5% от веса тела, при температуре воды 38-39°С. Критерием утомления и прекращения плавания считали первое "ныряние" с погружением носовых ходов в воду. В большой ванне одновременно плавали по 5 животных из каждой наблюдаемой группы. Тестирование мышей проводили через 14 дней после ежедневного введения препаратов (таблица 4).
Данные таблицы показывают, что препараты увеличивают продолжительность плавания, причем Ацизол не уступает зарегистрированному аналогу.
Антигипоксическое действие
Дыхание из замкнутого пространства - рересперация - является достаточно адекватной и простой моделью острой гипоксии [15, 16]. Животное, поглощая кислород из замкнутого пространства вследствие дыхания, вызывает развитие его дефицита - гипоксическую гипоксию, что позволяет оценивать исследуемый препарат по интегральным показателям летальности за определенное время наблюдения и устойчивости к дефициту кислорода (максимальной продолжительности жизни).
Животные помещались в банку объемом 250 мл, плотно закрытую стеклянной крышкой, смазанной герметиком. Фиксировали с помощью секундомера максимальную продолжительность жизни и симптомы танатогенеза. Банки с животными во время исследования находились в кондиционере, обеспечивающем постоянство условий эксперимента (температура + 20°С, влажность - 65-70%, атмосферное давление - 760±10 мм рт, ст). Контролем служили интактные животные.
После гибели у каждого животного ex tempore получали головной мозг, проводили его гемогенезацию (400 об/мин, 10 ходов пестика) [17] и определяли в гомогенате активность каталазы, уровень диеновых конъюгатов и гидроперекисей липидов [18, 19]. Эти показатели позволяют оценивать антиоксидантные свойства препарата.
Оказалось, что препараты достоверно увеличивают время жизни мышей, при этом стабилизировались показатели перекисного окисления липидов (снижались уровни малонового диальдегида и гидроперекисей липидов мозга) и восстанавливалась антиокислительная (каталазная) активность, что свидетельствует об увеличении резервной антиокислительной активности мозга (таблица 5).
Показатели функционального состояния адаптационных систем организма
Показатели, характеризующие энергетический обмен, обмен липидов и антитоксическую активность организма, представлены в таблице 6.
Представленные результаты свидетельствуют об адаптационной направленности действия изученных препаратов.
Иммобилизационный стресс
Иммобилизационный стресс моделировали на крысах-самцах после 20 дней ежедневного (включая выходные дни) введения препарата в дозе 10 мг/кг. Для этого крысы фиксировались на спине в течение 24 часов в боксах камеры Голубева. О развитии адаптационного синдрома судили по массе тела, массе тимуса, надпочечников, селезенки и количеству кровоизлияний (язв) в слизистой оболочке желудка [20]. Контролем служили интактные животные. Результаты представлены в таблице 7.
Оказалось, что после суточной иммобилизации у животных, получавших плацебо (дистиллированную воду), достоверно и значительно снизилась масса тела, на 30% увеличилась масса надпочечников, на 20% уменьшилась масса вилочковой железы и на 25% - масса селезенки. В желудке развились язвенные поражения и кровоизлияния. Это свидетельствовало о развитии адаптационного синдрома, т.е. стресса. Оба препарата предупреждали снижение массы тела, изменения массы надпочечников, вилочковой железы и селезенки. Количество язвенных поражений было в среднем на 80% меньше. Это позволяет говорить об антистрессовой активности препарата "Ацизол" при его профилактическом назначении. Положительное влияние на течение стресс-реакции еще раз подтверждает адаптогенную направленность фармакологической активности препарата "Ацизол".
Влияние Ацизола на физическую работоспособность и устойчивость организма к физическим нагрузкам
Исследование влияния Ацизола на физическую работоспособность, выносливость и устойчивость организма к продолжительным интенсивным нагрузкам проводилось при однократном и курсовом применении препарата. Состояние выраженного физического утомления достигалось прохождением кросса по пересеченной местности (10 км) с последующим преодолением полосы препятствий 100 м (в т.ч. 50 м с имитатором "пострадавшего" весом 70 кг).
Первое исследование проводилось с участием 31 здорового мужчины в возрасте от 18 до 23 лет, 17 человек в опытной группе и 14 в контрольной плацебо-группе. Прием Ацизола в дозе 120 мг (2 мл 6% раствора) и плацебо испытуемыми осуществлялся перорально двойным слепым методом непосредственно перед нагрузкой.
Сразу после кросса исследовали прямые показатели работоспособности (статический и динамический компоненты и кистевая мышечная выносливость), функциональное состояние сердечно-сосудистой системы, самочувствие. При исследовании прямых показателей работоспособности в контрольной группе после нагрузки выявлено значительное снижение показателя динамической работоспособности (до 68±5%, р<0.05) и резкое (до 23±5%, р<0.05) падение показателя статической выносливости (табл.8). Коэффициент выносливости по кистевой динамометрии снижался с 0.79±0.03 до 0.55±0.02 ед. (р<0.01).
Состояние сердечно-сосудистой системы характеризовалось утомлением миокарда (индекс Квааса увеличивался на 40% по отношению к фону). Повышалась активность симпатоадреналовой системы (частота сердечных сокращений увеличилась на 121%, индекс Робинсона на 80%). Выявлено достоверное снижение толерантности сердечно-сосудистой системы к физической нагрузке: индекс толерантности миокарда и PWC170 снижались на 40%, производительность механической работы сердца - на 27%, удельное максимальное потребление кислорода - на 17%. МОК увеличился к концу нагрузки на 23% от фонового значения.
Таким образом, интенсивная продолжительная физическая нагрузка вызвала развитие утомления, сопровождающегося значительным напряжением резервов сердечно-сосудистой системы.
Состояние ЦНС характеризовалось возрастанием субъективной оценки степени усталости почти в 3 раза (с 2,1±0,2 до 6,9±0,2 баллов по 10-балльной шкале), самочувствие и активность снизились на 12% и 9% соответственно (р<0,05.
Прием Ацизола оказал значительное влияние на показатели динамической и статической выносливости (увеличение от уровня плацебо на 43%, р<0,01 и 13% соответственно, р<0,05). Ацизол существенно повышал толерантность сердечно-сосудистой системы к нагрузкам. Он увеличивал на 15% значения показателей теста PWC170 и производительность механической работы сердца, на 18% - толерантность миокарда к нагрузкам (р<0,05). Ударный объем увеличился по сравнению с контролем на 18% при достоверном снижении метаболической потребности миокарда в кислороде (индекс Робинсона уменьшился на 38%, р<0,01) и повышении его функциональных резервов (индекс Квааса уменьшался на 17%, р<0,05), что закономерно привело к снижению частоты сердечных сокращений на 14% (р<0,01).
Такое влияние Ацизола на изученные показатели гемодинамики и физиологические индексы позволяет объяснить тот факт, что испытуемые из опытной группы прошли кросс за время на 12% быстрее (р<0,05), чем испытуемые плацебо-группы. Причем эта разница в скорости бега была наиболее выражена на последней трети маршрута, особенно во время преодоления полосы препятствий.
Полученные данные показывают, что однократное профилактическое применение Ацизола повышает выносливость и устойчивость организма к продолжительным интенсивным нагрузкам и улучшает их субъективную переносимость.
Во втором исследовании было изучено влияние курсового 10-дневного применения ацизола (перорально по 120 мг один раз в день после еды) на физическую выносливость и устойчивость организма к продолжительным интенсивным нагрузкам. Исследование проводилось с участием 34 здоровых мужчин в возрасте от 18 до 23 лет, из них 20 человек - в опытной и 14 - в плацебо-группе. Исследовали прямые показатели работоспособности (статический и динамический компоненты и кистевая мышечная выносливость), функциональное состояние сердечно-сосудистой системы, субъективную оценку самочувствия. Состояние выраженного физического утомления достигалось через 4 суток после последнего приема Ацизола и плацебо, как и в предыдущем исследовании, прохождением кросса по пересеченной местности (10 км) с последующим преодолением полосы препятствий 100 м (в т.ч. 50 м с имитатором "пострадавшего" весом 70 кг). Исследование проводилось сразу после окончания кросса.
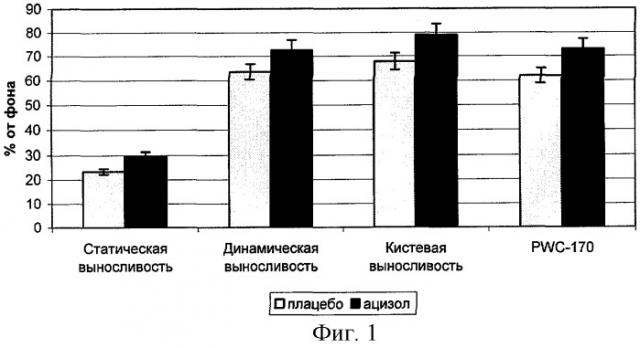
Результаты исследований показали, что после курсового применения Ацизола показатели динамической и статической выносливости в опытной группе превышают на 18 и 24% аналогичные показатели в плацебо группе (фиг.1).
Прием Ацизола оказал положительное влияние на показатели кистевой физической выносливости (увеличение от уровня плацебо на 23%, р<0,05). Было установлено, что Ацизол увеличивал на 16% значения показателей теста PWC170, производительность механической работы сердца и толерантность миокарда к нагрузкам на 11%. Выявлено достоверное повышение его функциональных резервов (индекс Квааса уменьшился на 17%), что закономерно привело к снижению частоты сердечных сокращений на 14%. Проба Штанге была на 17% выше по сравнению с плацебо-группой.
Эти данные свидетельствуют о положительном влиянии курсового применения Ацизола на толерантность сердечно-сосудистой системы к нагрузкам.
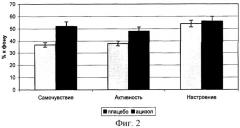
В опытной группе также отмечалось хорошее самочувствие, активность, настроение, кроме того препарат значительно облегчал переносимость физических нагрузок, что проявлялось в снижении чувства мышечной усталости, одышки во время бега, снижении болевых проявлений в правом подреберье, легче удерживался ровный темп бега (фиг.2).
Субъективная оценка чувства усталости была достоверно ниже, чем у испытуемых плацебо-группы.
Полученные данные позволяют говорить о том, что положительное влияние Ацизола на физическую работоспособность, выносливость и устойчивость организма к продолжительным интенсивным нагрузкам сохраняется через несколько суток после окончания курсового приема препарата.
Таким образом, вышеприведенные данные свидетельствуют о высокой активности Ацизола в качестве адаптогена и его преимуществах перед известным фармакологическим аналогом.
Литература
1. Регистр Лекарственных средств России. Энциклопедия лекарств, 10 выпуск, 2003 г., стр.1063.
2. Там же, стр.1064.
3. Патент № 2038079 "Антидот окиси углерода", МПК А 61 К 32/515, 1995 г.
4. Кудрин А.Н. Физиол. жур. СССР, 1953, т.39, № 3, с.309-318.
5. Васильев К.Г. Гиг. труда и проф. забол., 1957, № 2, с.19-24.
6. Брехман И.И. Женьшень. Л.: 1957, с.30-33.
7. Руководство по физиологии. Адаптация человека к экстремальным условиям среды. Под ред. О.Г.Газенко. М., "Наука", 1979, с.333-336.
8. Ellouk-Achard S. et al. Ex vivo and in vitro models in acetaminophen hepatotoxicity studies. Relationship between glutathione depletion, oxidative stress and disturbances in calcium homeostasis and energy metabolism. Archives of Toxicology. Supplement. 1995, 17, pp.209-214.
9. Тимер М., Гедрих И. Фармакология и токсикол., 1969, № 5, с.602-604.
10. Кигель Г.Б. Харабаджахьян А.В. Показатели биологической нормы для лабораторных животных. Ростов-на-Дону, 1978, 95 с.
11. Клиническая оценка лабораторных тестов. Под ред. Н.У.Тица, М., "Медицина", 1986, 480 с.
12. Умбрейт В.В., Буррис Р.Х. и др. Монометрические методы изучения тканевого обмена. М., 1957, 356 с.
13. Лабораторные методы исследования в клинике. Справочник под ред. В.В. Меньшикова. М., "Медицина", 1987, с.141-143.
14. Рылова М.Л. Методы исследования хронического действия вредных факторов среды в эксперименте. М.: "Медицина", 1964, 228 с.
15. Руководство по физиологии. Экологическая физиология человека. Адаптация человека к экстремальным условиям среды. Под ред. О.Г.Газенко. М., "Наука", 1979, с.333-336.
16. Руководство к практическим занятиям по патологической физиологи. Под ред. О.М.Павленко. М., "Медицина", 1974, с.174-175.
17. Tyson C.A., Luman K.D., Stephens R.J Age-related differences in G-SH-shuttle enzymes in NO2-or О3-exposed rat lungs Arch. Оз. Env. Health, 1982, Vol.37., No 3, pp.167-176.
18. Методы исследований в профпатологии. Под ред. О.Г.Архиповой. М., 1988, с.156-158.
19. Современные методы в биохимии. Под ред. В.Н.Ореховича. М., "Медицина", 1977, с.62-64.
20. Кигель Г.Б., Харабаджахьян А.В. и др. Показатели биологической нормы для лабораторных животных. Ростов-на-Дону, 1978, с.25-28.
| Таблица 1Продолжительность гексеналового сна мышей после предварительного введения препаратов (М±m) | |
| Группы животных | Длительность сна, мин |
| Контроль | 24.8±2.1 |
| Ацизол | 15.5±1.3* |
| Элеутерококк | 20.2±2.0 |
| * - достоверные отличия от контроля при Р<0.05 | |
| Таблица 2Длительность восстановления способности к прямолинейному поступательному движению мышей после вращения в центрифуге 15 сек со скоростью 600 об/мин (М±m) | |
| Группы животных | Время восстановления, сек |
| Контроль | 210±8 |
| Ацизол | 145±5* |
| Элеутерококк | 165±7* |
| * - достоверные отличия от контроля при Р<0.05 | |
| Таблица 3Физическая выносливость мышей в тесте статической силовой нагрузки собственным весом (М±m) | |
| Группы животных | Длительность висения, мин |
| Контроль | 22.0±1.5 |
| Ацизол | 28.5±1.0* |
| Элеутерококк | 27.5±1.0* |
| * - достоверные отличия от контроля при Р<0.05 |
| Таблица 4Длительность плавания мышей с грузом после введения препаратов (М±m) | ||||
| Группы животных | Длительность плавания, мин | |||
| Контроль | 27.8±5.5 | |||
| Ацизол | 43.8±6.6* | |||
| Элеутерококк | 40.2±6.3* | |||
| * - достоверные отличия от контроля при Р<0.05 | ||||
| Таблица 5Эффективность препаратов в тесте "баночной гипоксии" (М±m) | ||||
| Группы животных | Показатель | |||
| Продолжительность жизни, мин | Малоновый диальдегид, нмоль/мг белка | Каталаза, мкмоль Н2O2/мг мин | Гидроперекиси липидов, ед. опт. Плотности при 480 им | |
| Интактные | - | 2.77±0.26 | 9.57±0.58 | 0.11±0.01 |
| Контроль | 34.2±2.6 | 4.61±0.55 | 3.50±0.50 | 0.50±0.04 |
| Ацизол | 49.0±1.0* | 3.19±0.47* | 5.55±0.50* | 0.25±0.03* |
| Элеутерококк | 44.2±1.0* | 3.47±0.41 | 4.76±0.58* | 0.40±0.03 |
| * - достоверные отличия от контроля при Р<0.05 |
| Таблица 6Показатели функционального состояния адаптационных систем организма | |||
| Показатели | Группы животных | ||
| Контроль | Ацизол | Элеутерококк | |
| Масса тела, г | 27.0±1.4 | 26.5±1.3 | 27.2±1.1 |
| Общие липиды, сыворотка, г/л | 3.6±0.2 | 3.5±0.1 | 2.9±0.1* |
| Холестерин, сыворотка, ммоль/л | 1.64±0.32 | 1.59±0.33 | 1.60±0.28 |
| Билирубин общий, сыворотка, ммоль/л | 3.1±0.2 | 2.9±0.2 | 3.4±0.1 |
| -SHгр, сыворотка, мг % | 1634±83 | 1680±80 | 1686±79 |
| Восстановленный глутатион, печень, мг % | 165±12 | 166±10 | 153±10 |
| Гликоген, печень, мг % | 2560±110 | 2520±115 | 2400±115 |
| Глюкоза, сыворотка, мг % | 92±15 | 91±18 | 83±13 |
| Глюкоза, мышцы, мг % | 135±27 | 145±37 | 155±29 |
| АТФ, сердце, мкмоль/г | 2.5±0.2 | 3.0±0.2* | 2.3±0.1 |
| АТФ, мышцы, мкмоль/г | 5.3±0.2 | 5.9±0.4* | 5.1±0.3 |
| Интенсивность тканевого дыхания, сердце, мкл O2/100 мг/час | 63±6 | 67±6 | 60±6 |
| Интенсивность тканевого дыхания, мышцы, мкл O2/100 мг/час | 21±3 | 28±5 | 22±2 |
| * - достоверные отличия от контроля при Р<0.05 |
| Таблица 7Масса тела, надпочечников, тимуса, селезенки и количество кровоизлияний в слизистой оболочке желудка у крыс-самцов в тесте иммобилизационного стресса | |||||||||||
| Препарат | №№ животных | Масса тела, г | М±m | Надпочечники, мг | M±m | Тимус, мг | М±m | Селезенка, мг | M±m | Кровоизлияния | M±m |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| Контроль (интактные животные) | 12345678 | 160170165175180155150160 | 164±4 | 3842373540353337 | 37±1 | 131411101511109 | 12.0±1.0 | 240220230210215230210210 | 200±5 | - | 0 |
| Плацебо (стресс) | 12345678 | 140135150150145155150147 | 146±3 P1,2<0.05 | 4852565857585450 | 54±2 P1,2<0.05 | 98978578 | 8.0±0.5 P1,2<0.05 | 170200150165170175160155 | 168±6 P1,2<0.05 | 12108141510911 | 11±1 P1,2<0.05 |
| Продолжение таблицы 7 | |||||||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| Ацизол, 10 мг/кг (стресс) | 12345678 | 165170150150155170165150 | 159±3 P1,4>0.05Р2,4<0.05 | 5042394042363537 | 40±2 P1,4>0.05Р2,4<0.05 | 12141198101112 | 10.9±0.7 P1.4>0.05Р2,4>0.05 | 170190200180210230210215 | 201±8 P1,4>0.05P2,4<0.05 | 10213245 | 2±1 Р2.4<0.05 |
| Таблица 8Влияние ацизола на показатели физической выносливости, работоспособности и параметры гемодинамики после продолжительной нагрузки (% к фону) | |||
| Показатель | Плацебо N=14 | Ацизол N=17 | % к плацебо |
| Статическая выносливость, | 23±5* | 33±5 | 143** |
| Динамическая выносливость | 68±3* | 77+5 | 113* |
| Кистевая выносливость | 68±5** | 79±15 | 116 |
| PWC170 | 62±5* | 73±5 | 115* |
| МОК | 123±8* | 124±13 | 101 |
| СО | 104±5 | 123±7 | 118* |
| МПК удельное | 83±3* | 87±5 | 104 |
| Производительность механической работы сердца | 73±5* | 83±3 | 114* |
| ИТМ | 60±3** | 71±3* | 118* |
| ИК | 140±8** | 116±10 | 83 |
| ИР | 180+22* | 112±18 | 62** |
| Проба Штанге | 69±19* | 81±15 | 115* |
| Примечание: Отличие статистически достоверно: * - р<0,05, ** - р<0,01 |
Применение ацизола в качестве адаптогена.