Новые биополимеры, полученные облучением в твердой фазе в атмосфере ненасыщенных газов
Иллюстрации
Показать всеИзобретение относится к новым продуктам на основе биополимеров. Способ модификации встречающегося в природе биосовместимого биополимера, который характеризуется отсутствием каких-либо функциональных групп, включает обработку указанного биополимера в твердом или сухом состоянии источником ионизирующего излучения в присутствии опосредствующего газа. Опосредующий газ представляет собой незамещенный алкеновый или алкиновый газ, которым является этилен, пропилен или ацетилен, и отжиг полученного продукта в отсутствие кислорода при температуре от около 40 до 120°С, с последующим удалением всего оставшегося опосредствующего газа. Модифицированный биополимер получен вышеуказанным способом. Модифицированный, встречающийся в природе биосовместимый биополимер, полученный вышеуказанным способом, выбран из группы, состоящей из полисахаридов растительного или животного происхождения, белка, полученного из соединительной ткани животного, белка, полученного из других тканей животного, комбинации, по крайней мере, одного из указанных полисахаридов и, по крайней мере, одного другого белка растительного происхождения, или деминерализованной кости ("DMB"). Способ модификации ткани животного происхождения включает обработку образца указанной ткани или ее компонента в твердом или сухом состоянии источником ионизирующего излучения в присутствии опосредствующего газа и отжиг полученного продукта в отсутствие кислорода при температуре от около 40 до 120°С, с последующим удалением всего оставшегося опосредствующего газа. Изобретение позволяет получить биополимеры, обладающие хорошей биосовместимостью, при этом в исходный биополимер не вводят ни новых, ни дополнительных функциональных групп. 4 н. и 31 з.п. ф-лы, 12 табл., 43 ил.
Реферат
Область изобретения
Настоящее изобретение относится к новым продуктам; к способам их получения из сухих биологических полимеров (биополимеров) с использованием ионизирующего излучения в твердом (не жидком) состоянии в присутствии ненасыщенного газа в условиях специфических реакций, и к использованию этих продуктов.
Предпосылки изобретения
Специалистам в рассматриваемой области известно, что некоторые типы полимерных материалов подвергают облучению с целью решения ряда различных задач, хотя, насколько известно авторам, специалистам неизвестна обработка таких биополимеров излучением высоких энергий в присутствии опосредствующего газа, например ацетилена, с целью модификации биополимера таким образом, чтобы улучшить его свойства в одном или более из аспектов. Представляют интерес следующие патенты США: 3215634 (Walker); 4024073 (Shimizu); 4716224 (Sakurai); 4746514 (Warne); 4987222 (De Ambrosi); 5376692 (Park) и опубликованная иностранная заявка WO 96/03147 (Fidia,S.p.A), но они не являются значимо релевантными. Например, нигде в этих работах не сообщается об облучении полимерных материалов в твердом состоянии, включая Warne ('514), который действительно использует этиленсодержащие ненасыщенные соединения, но не в газообразном состоянии.
Sakurai ('224) раскрывает сшивку гиалуроновой кислоты с полифункциональными эпоксисоединениями в определенных условиях, но ни в одном из вариантов не упоминается использование ионизирующего излучения/ненасыщенных(алкеновых или алкиновых) газов.
Walker ('634) и Shimizu ('073) также раскрывают использование различных химических сшивающих агентов для получения продуктов - сшитых полисахаридов.
De Ambrosi ('222) раскрывает контролируемое получение низкомолекулярных глюкозаминогликанов в результате деполимеризации высокомолекулярных глюкозаминогликанов под действием гамма-излучения.
Предложение Warne ('514) направлено на обратную задачу. Warne раскрывает получение сшитых гидрогелей, обрабатывая полисахарид, со степенью высокомолекулярности, не более чем пентасахарид, ионизирующим излучением в присутствии этилен-ненасыщенных соединений (но не газов), содержащих, по крайней мере, одну гидрофильную группу.
Park ('692) раскрывает белки, например альбумин, которые функционализированы таким образом, что если альбумин связан с совместимым с кровью субстратом, и после радиационной обработки, свободные радикалы, образующиеся как на белке, так и на субстрате, химически связываются друг с другом. В этой ссылке нет указаний или предположений относительно сшивки полимеров под действием ионизирующего излучения в присутствии ненасыщенного газа, который образует часть сшивки.
Fidia (PCT заявка № WO 96/03147) раскрывает синтез химических гелей из полиэлектролитных полисахаридов, включая HA- и НА-бензиловые сложные эфиры, под действием гамма-излучения, которому предшествует функционализация для введения в их структуру олефиновых связей. Единственным раскрытым функционализирующим агентом является глицидилакрилат. Следует упомянуть другие иностранные патенты, которые имеют меньшее отношение к изобретению: EP 000038426; JP 360143991; JP 363301234; JP 401118529; DE 004123889; DE 004124338 и JP 406073102.
Не патентная литература, относящаяся к объекту настоящего изобретения, в частности, к некоторым исследованиям, проведенным на некоторых исходных материалах, использованных в настоящем изобретении, и к воздействию ионизирующего излучения на незаряженные полисахариды (такие как крахмал и целлюлоза) и на полиэлектролитные полисахариды (такие как гиалуроновая кислота и ее сшитое производное гилан, альгинаты, гепарин и т.д.) для того, чтобы вызвать разложение с разрывом основной цепи, приводящим к снижению молекулярного веса и вязкости, представлена здесь:
Описание изобретения
В настоящем изобретении предложена чрезвычайно широкая категория новых биополимеров, обладающих существенно улучшенными характеристиками по сравнению с исходными биополимерами. Молекулярные веса этих материалов можно увеличить регулируемым образом с тем, чтобы получить новые физические и химические свойства (например, эмульгирование и связывание с водой). Водные растворы новых продуктов можно получить буквально любой нужной вязкости и/или вязкоэластичности. Биополимеры можно превратить в новые гидрофильные гели (гидрогели) заданного конкретного размера и обладающие конкретными микромеханическими свойствами. Такие изменения можно осуществить без введения новых химических заместителей, и, следовательно, новые материалы сохраняют присущую им биосовместимость исходного или родительского биополимера. В способе получения новых биосополимеров можно использовать один или более из различных биополимеров.
В том смысле, как здесь использованы термины биополимер и биологический полимер, их следует понимать как полимер, полученный из биологического источника, в том числе и растения, включая микроорганизмы, или животное.
Рассматриваемые в настоящем изобретении биополимеры включают незамещенные биополимеры, охватывая всю область полисахаридов, полученных из растений и животных, независимо от того, заряжены они или не заряжены, а также белки, непосредственно полученные из источников коллагеновой ткани животных, такие как коллаген, желатин, и человеческие и животные продукты, такие как казеин, комбинации одного или более из таких полисахаридов с одним или более из белков растительного происхождения - такие как арабиногалактановые белки, биологические ткани и материалы, полученные из них, используемые для пересадки тканей и трансплантации, либо конечные продукты, либо частичные, и которые получены или сформированы из одного или более из таких биополимеров или их комбинаций с другими вышеуказанными материалами. Биополимеры, которые предстоит обработать для получения новых материалов в соответствии со способом настоящего изобретения, нет необходимости модифицировать каким либо образом до обработки, например, вводя какие-либо функционализирующие группы, которые могут быть необходимы в других процессах для активации биополимера, или для того, чтобы сделать его более реакционноспособным.
Иллюстративные примеры биополимеров, рассматриваемых в настоящем изобретении, включают:
Растительные экссудаты акаций, таких как Acacia Senegal и Acacia Seyal, содержащие арабиногалактановые белки во всех растениях; декстран и родственные бактериальные полисахариды; химически модифицированные полисахариды, такие как карбоксиметилцеллюлоза; гелеобразующие полисахариды либо бактериального происхождения (ксантан), либо растительного происхождения (каррагенан), либо фруктового происхождения (пектин); полисахариды и белки соединительных тканей животных и их комбинации, такие как гиалуронан, протеогликаны и химически модифицированные полисахариды животного происхождения, такие как хилан; и интерактивные комбинации этих материалов, которые могут быть ассоциированы, связаны и могут быть сращенными в специфических комбинациях.
При осуществлении способа настоящего изобретения для получения новых материалов из исходных биополимеров, предпочтительно, чтобы в исходном виде биополимер был в твердом состоянии, т.е. сухим, в атмосфере, включающей опосредствующий агент, предпочтительно низкомолекулярный ненасыщенный алкеновый или алкиновый газ, такой как этилен, пропилен или ацетилен, предпочтительно ацетилен. Перед введением опосредствующего газа в зону реакции эту зону необходимо очистить от любой содержащей активный кислород атмосферы. Любой опосредствующий газ удаляют после завершения процесса, и поэтому полученный в результате новый материал не содержит какого-либо опосредствующего газа.
Биополимерная система (или обработанный или частично обработанный, полученный из нее продукт) из которого была удалена активная атмосфера, насыщают затем опосредствующим газом при атмосферном давлении, и экспонируют источником ионизирующего излучения, который может быть либо изотопом, таким как 60Со (γ-лучи), либо излучением высокой энергии (250 КэВ до 10 МэВ) от ускорителя электронов, либо рентгеновскими лучами, создаваемыми ускорителем, либо любым другим подходящим устройством.
Минимальная поглощаемая доза излучения может меняться от 1 кГр до 50 кГр, в зависимости от строения биополимера, от необходимости получения разветвленного или длинноцепочечного продукта, от необходимости повышение молекулярного веса для создания легко растворимого в воде продукта или получения либо геля, либо мембранного продукта. Как правило, сильно разветвленные полисахаридные структуры могут привести к достижению 4х-кратного увеличения молекулярного веса при дозах вплоть до 10 кГр и гелей при дозах вплоть до 50 кГр, тогда как аналогичных изменений в неразветвленных структурах удается достичь при столь низких дозах, как 1-3 кГр. Белкам необходимо вплоть до 25 кГр для достижения аналогичного результата. Смеси и комбинированные адгезивные системы требуют тщательного выбора доз в зависимости от состава систем.
После стадии облучения в присутствии газообразного опосредствующего агента и для удаления всех активных агентов, образовавшихся в процессе облучения, полученную биополимерную систему или новый материал подвергают термообработке (отжигу) в отсутствие кислорода при повышенных температурах в интервале от 40 до 120°C в зависимости от термостабильности биополимерной системы, которую необходимо модифицировать. Такую стадию отжига в идеале можно осуществить в присутствии ненасыщенной газообразной атмосферы или, в другом варианте, в присутствии инертного газа, такого как азот или гелий, или в вакуумном термостате. Первое может привести к увеличению количества образования нового продукта, а последнее обеспечивает подходящий механизм окончания процесса.
После стадии отжига все оставшиеся газообразные опосредствующие агенты удаляют из модифицированной биополимерной системы путем аэрации системы, и при необходимости используют для обработки полимера вакуумный процесс. Это зависит от удерживающей способности материала в отношении газа, что зависит от пористости твердой системы.
Новые биополимеры, полученные в результате вышеописанной обработки, характеризуются изменением следующих параметров, при сравнении исходного материала с новыми биополимерами:
а) молекулярный вес может увеличиться в 4-5 раз;
b) обычно параллельно с увеличением молекулярного веса происходит повышение связывания воды;
с) используя пониженные концентрации биополимеров, удается получить эмульсию с размерами капель порядка 1 мкм;
d) интервал изменений вязкости и вязкоэластичности достигает 1000-кратного; и
е) наблюдается образование гидрогелей с размерами частиц 150-2000 мкм.
Молекулярный вес исходного биополимера можно увеличить контролируемым образом с тем, чтобы получить новое поколение продуктов с улучшенными свойствами без утраты основных функциональностей исходного биополимера. Увеличенные параметры молекул обеспечивают большее связывание с водой, улучшают физические свойства, такие как образование более мелких частиц эмульсии, новые связывающие способности и функции в отношении других полимеров, независимо от того, являются они заряженными или нет, и лучшее качество при изготовлении лекарств и небольшое выделение ионов.
Можно получить растворимые продукты с повышенной или пониженной вязкостью и/или вязкоэластичностью. Таким образом, можно получить новые пищевые, лекарственные и промышленные продукты.
Особенно важным для настоящего изобретения является тот факт, что в структуру биополимера в результате процесса изобретения не вносится никаких заметных или идентифицируемых химических изменений. Поэтому любой новый продукт, полученный в соответствии с настоящим изобретением, можно использовать на практике фактически тем же способом, что и исходный биополимер.
Гидрофильные гели (гидрогели) можно получить с определенным размером частиц и конкретными микромеханическими свойствами. Полученные продукты обладают такой же биосовместимостью, что и исходные биополимеры.
Широкий круг новых продуктов можно получить, изменяя параметры процесса, и эти параметры составляют неотъемлемую часть сути и целей настоящего изобретения и включены в объем представленной формулы изобретения. Способ не приводит к получению одного нового продукта, или даже ряда новых продуктов для конкретного типа биополимера, но скорее он предлагает возможность получения семейства новых продуктов, каждый из которых можно приспособить для конкретных применений.
Краткое описание фигур
Фигуры включают ФИГ.1-24, всего 43 ФИГ. на 27 листах. Каждая из этих перечисленных и описанных далее ФИГ. представляет графики, и они относятся к одному или более из примеров, представленных далее в разделе примеры.
ФИГ.1. Дифференциальное молярномассовое распределение контрольных и облученных образцов Acacia Senegal (высушены распылением).
| GSDA-C | Контроль | GSD2-3K | 2,3 кГр |
| GSD3-8К | 3,8 кГр | GSD6-1K | 6,1 кГр |
| GSD10-5К | 10,5 кГр | GSD13-9К | 13,9 кГр |
| GSD25А2 | 24,8 кГр | GSD50А1 | 49,8 кГр |
ФИГ.2. Увеличение образования гидрогелей при различных условиях обработки.
ФИГ.3. Сравнение содержания белка в Acacia Seyal после радиационной обработки; контроль по поглощению УФ-излучения на длине волны 214 нм.
| ТО-7А1 | 0,7 кГр | Т1-2АI | 1,2 кГр |
| TI-5А1 | 1,5 кГр | Т3-2А1 | 3,2 кГр |
| Т8-9А1 | 5,9 кГр | Т24-8А1 | 248 кГр |
| Т49-8А1 | 49,8 кГр | Т-С2 | контроль |
ФИГ.4а. Спектр 13С-ЯМР Acacia Senegal (без облучения).
ФИГ.4b. Спектр 13С-ЯМР Acacia Senegal (облучение 6,1 кГр).
ФИГ.5. Кривая вязкости сдвига как функция скорости сдвига для 33,3% (вес/вес) контроля и облученного образца Acacia Senegal (высушен распылением). (•) контроль; (о) 2,3 кГр; (▴) 2,8 кГр; (Δ) 6,1 кГр; (▪) 10,5 кГр;
ФИГ.6. График (а) модуля сохранения и (b) модуля потерь как функция частоты для 33,3% (вес/вес) контроля и облученного образца Acacia Senegal (высушен распылением). (▴) контроль (•) 2,8 кГр; (×) 3,8 кГр; (▪) 10,5 кГр;
ФИГ.7а. Дифференциальное молярномассовое распределение контрольных и облученных образцов декстрана.
| Декстран | Контроль | D0-7A1 | 0,7 кГр |
| D1-2A1 | 1,2 кГр | D1-5K1 | 1,5 кГр |
| D1-7K | 1,7 кГр | D2-3кГр | 2,3 кГр |
| D3-8K | 3,8 кГр | D5-9A1 | 5,9 кГр |
| D16-2A1 | 16,2 кГр | D24-8A1 | 24,8 кГр |
| D49-8А1 | 49,8 кГр |
ФИГ.7b. Кривые модулей сохранения (G') как функция частоты для 6,25% (вес/объем) декстрана.
(о) контроль, (•) 1,5 кГр, (+) 1,7 кГр; (Δ) 2,3 кГр; (▪) 2,8 кГр; (▴) 16,2 кГр; (×) 24,8 кГр.
ФИГ.8а. Дифференциальное молярномассовое распределение контрольного и облученных образцов СМС.
| СМС-С2 | Контроль | С1-5К | 1,5 кГр |
| С1-7К | 1,7 кГр | С2-3К | 2,3 кГр |
| С2-8К | 2,8 кГр | С3-8К | 8,3 кГр |
ФИГ.8b. Кривая вязкости сдвига как функция скорости сдвига для 2% в Н2О контрольного и облученного образцов СМС. (о) контроль; (Δ) 1,5 кГр;
ФИГ.8 с. Кривые модулей сохранения (G') как функция частоты для 2% в Н2О контрольного и облученных образцов СМС. (о) контроль; (Δ) 1,5 кГр;
ФИГ.9а. Дифференциальное молярномассовое распределение контрольных и облученных образцов пуллулана.
| Р-С2 | Контроль | Р1-2АI | 1,2 кГр |
| Р1-5К | 1,5 кГр | Р1-7К | 1,7 кГр |
| Р2-3К | 2,3 кГр | Р2-8К | 2,8 кГр |
| Р3-8К | 3,8 кГр | Р5-9А1 | 5,9 кГр |
| Р24-8А1 | 24,8 кГр | Р49-8А1 | 49,8 кГр |
ФИГ.9b. Кривая модуля сохранения (G') как функция частоты для контрольного и облученного 20% пуллулана. (○) контроль; (•) 2,3 кГр, (▪) 2,8 кГр.
ФИГ.10а. Кривая сдвига вязкости как функция скорости сдвига для образца 0,5% в Н2О облученного гиалуронана по сравнению с контрольным образцом.
ФИГ.10b. Кривая модуля потерь (G") как функция частоты для образца 0,4% в Н2О облученного гиалуронана по сравнению с контрольным образцом.
ФИГ.10с. Инфракрасный спектр волокон облученного гилана.
ФИГ.11а. Кривая модуля сохранения (G') как функция частоты для 1% в Н2О образцов контрольного и облученного ксантана. Раствор нагревают в течение 20 минут при 85°C, и измерения проводят при 25°C. (о) контроль; (•)0,7 кГр.
ФИГ.11b. Кривая модуля потерь (G") как функция частоты для 1% в Н2О образцов контрольного и облученного ксантана. Раствор нагревают в течение 20 минут при 85°C и измерения проводят при 25°C. (о) контроль; (•)0,7 кГр.
ФИГ.11с. Кривая динамической вязкости (η') как функция частоты для 1% в Н2О образцов контрольного и облученного ксантана. Раствор нагревают в течение 20 минут при 85°C и измерения проводят при 25°C. (о) контроль; (•)0,7 кГр.
ФИГ.12. Кривая вязкости сдвига как функция скорости сдвига для 1% в Н2О образцов контрольного и облученного каппа-каррагенана. Раствор нагревают в течение 20 минут при 85°C и измерения проводят при 25°C. (о) контроль; (•)16,2 кГр;(▴) 24,8 кГр.
ФИГ.13. Кривая модуля сохранения (G') как функция частоты для 3,6% (вес/объем) в Н2О образцов контрольного и облученного апельсинового пектина. (•) 3 кГр.
ФИГ.14. Кривые (а) модуля сохранения (G'), (b) модуля потерь (G") и (с) динамической вязкости как функции частоты для 10% (вес/объем) в Н2О образцов контрольного и облученного желатина. Образцы нагревают в течение 15 минут при 50°C и измерения проводят на охлажденных образцах при 25°C. (о) контроль; (•) 3 кГр;
ФИГ.15. Кривая модуля сохранения (G') как функция частоты для 4% (вес/объем) в Н2О образцов контрольного и облученной смеси 90% апельсинового пектина +10% СМС. (о) контроль,(•) 3,3 кГр, (▴) 10,4 кГр.
ФИГ.16. Кривая модуля сохранения (G') как функция частоты для 4% (вес/объем) в Н2О образцов контрольной и облученной смеси 90% апельсинового пектина +10% декстрана. (о) контроль,(•) 3,3 кГр, (▴) 10,4 кГр.
ФИГ.17. Кривая модуля сохранения (G') как функция частоты для 4% (вес/объем) в Н2О образцов контрольной и облученной смеси 50% декстрана +50% СМС. (о) контроль,(•) 3,3 кГр,(▴) 10,4 кГр.
ФИГ.18. Кривая динамической вязкости как функция частоты для 4% (вес/объем) в Н2О образцов контрольной и облученной смеси 90% поливинилпирролидона (PVP) +10% декстрана. (о) контроль, обработка совместная, (▪) 10,4 кГр, обработка раздельная.
ФИГ.19. Кривые (а) модуля сохранения (G'), (b) модуля потерь (G") и (с) динамической вязкости (η') как функции частоты для 4% (вес/объем) в Н2О образцов контрольной и облученной смеси 50% поливинилпирролидона (PVP) +50% арабиногалактанового белка (гуммиарабик). обработка совместная, обработка раздельная, (▪) 10,4 кГр, обработка совместная, обработка раздельная.
ФИГ.20. Кривые (а) модуля сохранения (G'), (b) модуля потерь (G") и (с) динамической вязкости (η')как функции частоты для 25% (вес/объем) в Н2О образцов контрольной и облученной смеси 10% карбоксиметилцеллюлозы (СМС) +90% поливинилпирролидона арабиногалактанового белка (гуммиарабик). (○) контроль, обработка совместная, обработка раздельная.
ФИГ.21. GPC-хроматограммы образцов контрольной и облученной смеси, содержащей 10% карбоксиметилцеллюлозы (СМС) +90% арабиногалактанового белка (гуммиарабик).
С-М6 контроль 3-М6 3,1 кГр 10-М6 10,4 кГр
ФИГ.22. Кривые (а) модуля сохранения (G'), (b) модуля потерь (G") и (с) динамической вязкости (η) как функции частоты для 4% (вес/объем) в Н2О образцов контрольной и облученной смеси 90% оранжевого пектина +10% декстрана. обработка совместная, (○) 3,1 кГр, обработка раздельная, (▪) 10,4 кГр, обработка совместная, обработка раздельная.
ФИГ.23. Схема превращения высокомолекулярной смолы акации в гидрогель под действием радиации.
Фиг.24. Схема превращения декстрана в гидрогель под действием радиации.
Предпочтительный вариант осуществления изобретения
Далее настоящее изобретение будет раскрыто более подробно в следующих примерах, которые ни коим образом не ограничивают его объем, но просто его иллюстрируют.
Пример 1
Арабиногалактановые белки
Авторами были предварительно исследованы строение, свойства и функциональности смолистых экссудатов Acacia Senegal и Acacia Seyal, и эти виды включены в объем примеров и настоящего изобретения. Они также включены в описание материала, известного в продаже под названием гуммиарабик коммерческий (Gum Arabic of Commerce).
Эти материалы широко используются в промышленности в качестве адгезивов, стабилизаторов, эмульгаторов, сохраняющих вкус агентов, материалов, предотвращающих кристаллизацию сахара (в кондитерской промышленности), стабилизаторов типографских красок и т.д. Этот материал представляет собой глобулярный сшитый полисахарид, состоящий из арабинозы, галактозы, рамнозы и уроновой кислоты, соединенных вместе в полисахаридные фрагменты с молекулярным весом (МВ) примерно 400000, причем все глобулярные полисахаридные фрагменты соединены вместе как шарики на струне с белковой цепочкой. Белок составляет около 3%. Арабиногалактановые белки не являются дискретными молекулярными образованиями, так как по данным гидрофобности или фракционирования с исключением по размерам можно выделить два основных компонента с МВ примерно 1·106 и 4-5·105.
Характеристика свойств, связанных с новыми полученными продуктами
Контролируемое увеличение молекулярного веса
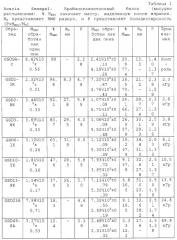
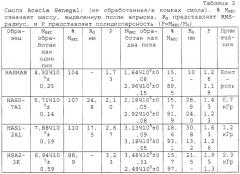
Способ настоящего изобретения позволяет осуществлять контролируемое увеличение молекулярного веса арабиногалактанов. Вначале исходный материал фракционируют, используя колонку для гельпроникающей хроматографии (GPC), соединенную с широкоугольным детектором рассеянного света лазера (MALLS), детектором концентраций (показатель преломления - RI) и детектором УФ-поглощения на длине волны 214 нм. Такая система позволяет определить молекулярно весовое распределение подлежащей измерению смолы, используя широкоугольное рассеяние света лазера, и, таким образом, используя эти три детектора, можно следить за любыми изменениями во всей структуре. Типичные изменения молекулярно-весового распределения представлены на ФИГ.1, а количественные результаты приведены в таблице 1 для представительной высушенной распылением смолы Acacia Senegal. Для того чтобы проиллюстрировать тот факт, что процесс сушки распылением не оказывает никакого влияния на общность наблюдаемых изменений, авторы провели точно такой же эксперимент, используя необработанную (в комках) смолу Acacia Senegal, и полученные результаты приведены в таблице 2, которые непосредственно оцениваются по 4 показателям. Наблюдается соответствующее увеличение среднеквадратического (RMS) радиуса для обработанной смолы.
2. Превращение в форму гидрогеля (различных размеров)
Путем создания контролируемой дозы радиации высокомолекулярную смолу акации можно превратить в гидрогель в соответствии со следующей схемой, представленной на фиг.23.
В таблицах 1 и 2 проиллюстрировано также, как можно последовательно превратить любое количество или долю растворимого арабиногалактанового белка в гидрогель. Более того, в соответствии с необходимостью можно изменять размеры частиц гидрогеля. Распределение частиц по отсечке демонстрирует, например, изменение от среднего примерно 160 мкм в сторону увеличения в системах отверждаемых гидрогелей до 2000 мкм и выше (ФИГ.2). Кривая для МВ затем постепенно повышается, причем значение для белка достигает даже 100·106, а связывание на этой стадии достигает такой степени, что частицы геля становятся хорошо видны. Эти частицы столь велики, что уже не могут попасть во фракционную колонку и представляют материал с наивысшим значение МВ, что объясняет выход на плато растворимой смолы после значения 6,1 кГр.
Увеличение доли высокомолекулярного эмульгирующего компонента
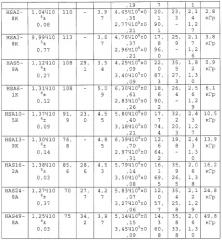
Высокомолекулярный арабиногалактановый белок (AGP), компонент смолы акации, отвечает за эффективность эмульгирования в эмульсиях типа масло-в-воде. Более высокое его содержание в Acacia Senegal по сравнению с Acacia Seyal делает эту смолу более ценной и, соответственно, более дорогостоящей. AGP покрывает капельки масла и предотвращает их повторную ассоциацию. Поэтому такие эмульсии оказываются стабильными в течение месяцев и даже лет. Увеличение количества этого компонента добавило бы ценности смоле. Авторы смогли продемонстрировать, что, используя способ радиационной обработки для Acacia Seyal, можно повысить долю высокомолекулярного компонента (AGP). Это повышение отражено в молекулярновесовом распределении и в RMS-радиусе; и таким образом получают новый материал, свойства которого приближаются к свойствам A.Senegal (таблица 3).
Таблица 3 иллюстрирует то, как молекулярный вес высокомолекулярного компонента можно повысить с 3 до 8 миллионов, при этом его количество увеличивается с 26% до 38%. Используя хроматографию гидрофобных взаимодействий (HIC), были выделены отдельные компоненты. Полученные результаты подтверждают увеличение доли AGP компонента, что отражено повышенным количеством белка по данным регистрации УФ-поглощения на длине волны 214 нм, что представлено на ФИГ.3.
Улучшенные характеристики эмульгирования
Оценивают модифицированные образцы смолы акации. Результаты оценки эффективности эмульгирования показали:
Когда Acacia Senegal превращена в новый продукт с более высоким значением молекулярного веса, доказано, что этот продукт является лучшим эмульгатором, нежели исходный, не обработанный контрольный образец.
Когда Acacia Seyal, более слабый эмульгатор по сравнению с Acacia Senegal, обрабатывают для увеличения ее молекулярного веса и для достижения того же количества высокомолекулярного компонента, что и в Acacia Senegal, ее характеристики оказываются столь же хорошими. Действительно, Acacia Seyal была превращена, по крайней мере, в отношении ее характеристик как эмульгатора, в более ценную Acacia Senegal.
Отсутствие введения новых химических групп
Используемые дозы радиации относительно низки по сравнению с теми, которые были бы необходимы для того, чтобы вызывать значительные химические изменения, если тот же материал облучают в отсутствие опосредствующего газа. Химический анализ показывает, что осуществление способа настоящего изобретения не приводит к значительным структурным изменениями, что и представлено в таблице 4.
| Таблица 4Физико-химические и химические характеристики исходной и облученной смолы (25 кГр, 10 МэВ (электронвольт) | ||
| контрольная | облученная | |
| % влаги | 12,5 | 12,4 |
| Удельное вращение | +52 | +52 |
| Предельная вязкость (см3/г) | 12 | 16 |
| % Сахаров | ||
| Рамноза | 5 | 4 |
| Арабиноза | 45 | 46 |
| Галактоза | 34 | 34 |
| Глукуроновая кислота | 15 | 15 |
| Азот | 0,15 | 0,15 |
Для точной оценки того, для которой из смол (обработанной или не обработанной) были обнаружены максимальные изменения молекулярного веса, проводилось сравнения 13С-ЯМР спектров ядерного магнитного резонанса. Между обработанной и не обработанной смолой не было обнаружено никакой разницы (ФИГ.4а и 4b). То есть в результате обработки не было введено никаких новых химических групп.
Регулируемое увеличение вязкости и вязкоэластичности
Изменения вязкости сдвига по мере изменения скорости сдвига отражают наблюдаемые изменения молекулярных весов. Вначале смола представляет собой компактную глобулярную систему, которая не оказывает заметного влияния на сдвиг. На этой стадии полисахарид ведет себя как набор маленьких компактных шариков, не уменьшая сдвига. По мере увеличения дозы радиации, используемой при обработке, образуется переплетенная сеть, которая типична для более длинных переплетенных молекул, когда можно наблюдать уменьшение сдвига (ФИГ.5). Наблюдается, по крайней мере, 1000-кратное увеличение вязкости при нулевом сдвиге после дозы 13 кГр.
Измерения колебаний также подтверждают вышеуказанные наблюдения (ФИГ.6а и 6b). Кривые зависимости модуля сохранения (G'-ФИГ.6а) и модуля потерь (G"-ФИГ.6b) построены как функции частоты. И снова, построение динамичной сети отражено в изменении от реакции разбавленного раствора (то есть G">G') до концентрированного раствора (G'>G") при смещении частоты перехода в сторону более низких частот при возрастании МВ), и наконец, до поведения плотного геля, когда G' и G" не зависят от частоты. Кривая динамической вязкости аналогична кривой сдвиговой вязкости, которые представлены на ФИГ.5, причем уменьшение сдвига проявляется как результат образования сетчатой структуры, способной создать затруднения, при увеличении дозы. Таким образом, вязкость можно увеличить как это нужно, и при необходимости систему можно превратить в гидрогель, который представляет собой высокоэластичное состояние.
Улучшенное взаимодействие с водой (Улучшенные характеристики связывания с водой)
В результате увеличения размеров молекул можно регулировать свойства связывания с водой арабиноглактанового белка. Это продемонстрировано с использованием импульсной спектрометрии ядерного магнитного резонанса.
Времена спин-спиновой релаксации (Т2) для водных растворов обработанных и не обработанных Acacia Senegal и Acacia Seyal представлены в таблице 5. Измерения проводили, используя 25 МГц импульсный ЯМР при 30°C. Был выбран полностью растворимый образец Acacia Seyal, для которого очевиден только один тип Т2. Так как Т2 объема воды меняется с 2 до 4 сек, а значения, полученные для образцов Acacia Seyal, составляли 1 сек или меньше, очевидно, что движения молекул воды ограничены смолой акации. Другими словами, образцы акации связывают воду. Исследования авторов с использованием дифференциальной сканирующей калориметрии ранее продемонстрировали эффективность связывания воды смолой акации. См. "Hydration characteristics of the gum exudate from Acacia Senegal, G.O. Phillips, et al, Food Hydrocolloids, Vol 10 (1), 1996, pp 11-19.
Как видно из таблицы 5, величина Т2 уменьшается по мере увеличения молекулярного веса. Это показывает, что количество связанной воды возрастает с увеличением молекулярного веса.
Высушенные распылением образцы Acacia Senegal демонстрируют два типа значений Т2, так как выбранные образцы смолы содержат гелевую компоненту. Однако тот же характер изменения наблюдается для увеличения связывания воды с увеличением молекулярного веса для компонента свободной воды. Обратное справедливо для гелевого компонента. С повышением молекулярного веса структура гидрогеля становится более рыхлой, и степень иммобилизации воды уменьшается с молекулярным весом.
Измеряли также величины Т2 сухих образцов, результаты представлены в таблице 6. Оба типа образцов демонстрируют два типа Т2. Т2S относится ко времени релаксации протонов ОН групп в смоле, а Т2L представляет время релаксации абсорбированной воды. И снова наблюдается эффект уменьшения времени релаксации за счет молекулярного веса, что совпадает с наблюдениями для водных растворов, и результатами, полученными на "сухих" образцах.
| Таблица 5Время спин-спиновой релаксации (Т2) для водных растворов гуммиарабика. Измерения проводились с использованием импульсного ЯМР при 30°C | ||||
| Образец | Концентрация | Т2s | Т2L | Обработка |
| Seyal (1,2) | 10,0 | - | 1000.00 (100%) | Контроль |
| Seyal (3,3) | 10,0 | - | 980,34 (100%) | 5,9 кГр |
| Seyal (3,0) | 10,0 | - | 908,18 (100%) | 49,8 кГр |
| Senegal (0,84) | 10,0 | 55,79 (5,6%) | 374,19 (94,4%) | Контроль |
| Senegal (3,1) | 9,91 | 78,13 (7,9%) | 341,91 (92,1%) | 6,1 кГр |
| Senegal (3,3) | 10,0 | 112,54 (57,2%) | 368,20 (42,8%) | 49,8 кГр |
Пример 2
Природные (незамещенные) и химически модифицированные полисахариды
Аналогичного типа модификации можно осуществить для широчайшего круга доступных полисахаридов. Здесь будут раскрыты полисахариды, типичные для различных групп. Результаты будут суммированы, но тип уже раскрытой информации доступен и составляет часть формулы изобретения.
Описанный здесь процесс модификации можно осуществить для широчайшего круга доступных полисахаридных систем. Нет возможности проиллюстрировать его для каждого отдельного полисахарида и для тех, которые были химически модифицированы. Тем не менее, авторы выбрали представительные образцы из различных групп и семейств, чтобы показать, что одинаковые изменения можно осуществить для широкого круга таких материалов, и что поведение их универсально. В этом разделе авторы предлагают иллюстративные примеры, соответствующие объему продуктов, заявленных в представленной далее формуле изобретения.
ДЕКСТРАН - бактериальный полисахарид с разветвленной цепью
Как известно, основной скелет декстрана состоит из (1-6) связанных звеньев D-глюкозы с боковыми цепями, присоединенными к 0-3 звеньям основной цепи. Степень разветвленности была определена и составляет 5%. Существуют также некоторые указания на присутствие небольшой доли α-D(1-3) разветвлений. Однако многие аспекты тонкой структуры необходимо еще определить. Декстран используют как заменитель плазмы крови, и для этой цели необходимо, чтобы он имел различные молекулярные веса. Декстраны также используют в качестве стандартов при определении молекулярного веса. По этой причине было бы желательно иметь метод, который позволил бы точно подгонять молекулярный вес к конкретным значениям.
Для примера был выбран декстран с высоким средним молекулярным весом МВ (1,44·106), причем на его хроматограмме присутствуют два пика. Определяют средневесовой молекулярный вес для каждого из пиков, и найдено, что они составляют 2,34·106 и 2,05·105. После облучения дозой 1,2 кГр происходит увеличение МВ средней компоненты (3,04·106), и компоненты с самым высоким значением МВ (4,58·106). Молярномассовое распределение иллюстрирует общее увеличение в распределении МВ (ФИГ.7а). Гель начинает образовываться после дозы 1,2 кГр, о чем свидетельствует уменьшение выделяемой массы (таблица 7). И снова, образование геля возрастает с увеличением дозы облучения. С увеличением дозы уровни МВ выравниваются, а затем уменьшаются, так как гель образуется за счет сшивок высокомолекулярного растворимого полисахарида. После дозы 49,8 кГр, примерно 83% исходного материала уже не проходит через фильтр 1 мкм, и его используют для получения геля, который можно наблюдать визуально. Значение среднеквадратического радиуса (RMS) подтверждает увеличение МВ дисперсной полисахаридной системы, увеличиваясь с начального значения 26,8 нм до примерно 43 нм при наивысшем достигнутом МВ. Аналогичным образом возрастает полидисперсность (Р), демонстрируя уширение молекулярно-весового распределения у более высокомолекулярного конца хроматограммы (с 4 до 5). Подробности количественных изменений представлены в таблице 7.
С точки зрения реологии изменения вязкости обработанного декстрана очень значительны. Вначале кривая сдвиг