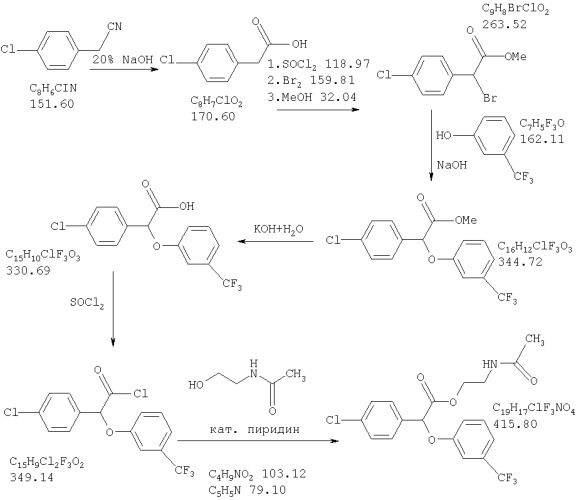
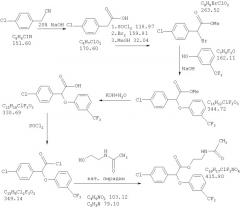
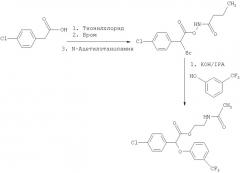
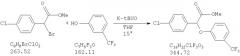
Использование производных (3-тригалометилфенокси)-(4-галофенил) уксусной кислоты для лечения резистентности к инсулину, диабета ii типа, гиперлипидемии и гиперурикемии
Иллюстрации
Показать всеИзобретение относится к усовершенствованным способам модулирования диабета II типа у млекопитающего и модулирования резистентности к инсулину, включающим введение указанному млекопитающему, нуждающемуся в этом, (-)стереоизомера соединения формулы I,
в которой R выбран из группы, состоящей из гидрокси, низшего аралкокси, ди-низшего алкиламино-низшего алкокси, низшего алканамидо низшего алкокси, бензамидо-низшего алкокси, уреидо-низшего алкокси, N'-низшего алкил-уреидо-низшего алкокси, карбамоил-низшего алкокси, галофеноксизамещенного низшего алкокси, карбамоилзамещенного фенокси, или R представляет собой гидролизуемую сложноэфирную группировку; каждый Х независимо представляет собой галоген; или его фармацевтически приемлемой соли, причем (-)стереоизомер по существу не содержит (+)стереоизомера соединения. Изобретение также относится к фармацевтическим композициям, содержащим (-)стереоизомер соединения формулы I и где композиции обладают существенно сниженным ингибирующим эффектом на цитохром Р450 2С9 по сравнению с рацемической композицией, имеющей 0% энантиомерный избыток (-)стереоизомера. 4 н. и 55 з.п. ф-лы, 21 ил., 8 табл.
Реферат
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка является частично продолжающей заявку с серийным №09/325997, зарегистрированную 4 июня 1999 г., которая включена в настоящую заявку на изобретение в качестве ссылки, для всех целей.
ОБЛАСТЬ ТЕХНИКИ
Настоящая заявка касается использования производных (-)(3-тригалометилфенокси)-(4-галофенил)уксусной кислоты и включающих их композиций в лечении резистентности к инсулину, диабета II типа, гиперлипидемии и гиперурикемии.
УРОВЕНЬ ТЕХНИКИ
Сахарный диабет, обычно называемый просто диабетом, обозначает болезненный процесс, происходящий в результате действия многих факторов и характеризующийся повышенным содержанием глюкозы в плазме крови, называемым гипергликемией. См., например, LeRoith, D. et al., (eds.). Diabetes Mellitus (Lippincott-Raven Publishers, PA U.S.A), 1996) и все содержащиеся в этой публикации ссылки. По данным Американской ассоциации диабета, сахарным диабетом больны примерно 6% населения земли. Неконтролируемая гипергликемия связана с повышенной и преждевременной смертностью из-за повышенного риска микрососудистых и макрососудистых болезней, включая нефропатию, невропатию, ретинопатию, гипертензию, заболевание сосудов головного мозга и ишемическую (коронарную) болезнь сердца. В связи с этим контроль гомеостаза глюкозы является решающей важности подходом к лечению диабета.
Существуют две основные формы диабета: диабет I типа (ранее называвшийся инсулин-зависимым диабетом, или IDDM), и диабет II типа (ранее называвшийся инсулин-независимым диабетом, или NIDDM).
Диабет I типа является результатом абсолютной недостаточности инсулина, гормона, регулирующего утилизацию глюкозы. Недостаточность инсулина обычно характеризуется разрушением β-клеток в островках Лангерганса в поджелудочной железе, что, как правило, приводит к абсолютной инсулиновой недостаточности. Диабет I типа имеет две формы: имунно-опосредованный сахарный диабет, возникающий в результате клеточно-опосредованного аутоиммунного разрушения β-клеток поджелудочной железы; и идиопатический сахарный диабет, который относится к формам болезни неизвестной этиологии.
Диабет II типа представляет собой болезнь, которая характеризуется резистентностью к инсулину, сопровождающуюся относительной, а не абсолютной инсулиновой недостаточностью. Диабет II типа может варьировать от преобладающей резистентности к инсулину с относительной инсулиновой недостаточностью до преобладающей инсулиновой недостаточности с некоторой резистентностью к инсулину. Резистентность к инсулину представляет собой уменьшенную возможность инсулина осуществлять свою биологическую функцию в широком диапазоне его концентраций. У индивидуумов с резистентностью к инсулину организм секретирует ненормально высокие количества инсулина, чтобы компенсировать этот дефект. Когда присутствуют неадекватные количества инсулина для компенсации резистентности к инсулину и адекватного контроля содержания глюкозы, то развивается состояние ослабленной толерантности к глюкозе. У значительного числа индивидуумов секреция инсулина далее снижается, а уровни содержания глюкозы в плазме крови повышаются, что приводит к клинической картине диабета. Диабет II типа может являться результатом высокой резистентности к стимулируемым инсулином регуляторным воздействиям на метаболизм глюкозы и липидов в основных чувствительных к инсулину тканях: в тканях мышц, печени и в жировых тканях. Эта резистентность к реакции на инсулин приводит к недостаточной активации инсулином поглощения глюкозы, ее окисления и отложения в мышцах, к неадекватному подавлению инсулином липолиза в жировых тканях, а также продуцирования и выделения глюкозы в печени. При диабете II типа уровни содержания свободных жирных кислот часто повышенные у тучных и у некоторых не страдающих ожирением пациентов, а окисление липидов повышено.
Преждевременное развитие атеросклероза и увеличенная частота сердечно-сосудистых болезней и заболеваний периферических сосудов характерны для пациентов, страдающих диабетом. Гиперлипидемия является важным отягощающим фактором для этих заболеваний. Гиперлипидемия представляет собой состояние, которое характеризуется главным образом ненормальным повышением содержания липидов в сыворотке крови в кровотоке и является важным фактором риска для развития атеросклероза и болезней сердца. Обзор работ по нарушениям метаболизма липидов см., например, в публикации Wilson, J. et al., (ed.). Disorders of Lipid Metabolism, Chapter 23, Textbook of Endocrinology, 9th Edition, (W.B.Sanders Company, Philadelphia, PA U.S.A. 1998); эта публикация и все цитируемые в ней работы включены в настоящую заявку в качестве ссылок. Липопротеины сыворотки крови являются носителями липидов в кровотоке. Их классифицируют на основании их плотности следующим образом: хиломикроны; липопротеины очень низкой плотности (VLDL); липопротеины средней плотности (IDL); липопротеины низкой плотности (LDL); липопротеины высокой плотности (HDL). Гиперлипидемию обычно разделяют на первичную и вторичную гиперлипидемию. Первичная гиперлипидемия обычно вызвана генетическими нарушениями, а вторичную гиперлипидемию, как правило, вызывают другие факторы, такие как различные болезненные состояния, лекарства и факторы, связанные с питанием. В качестве альтернативы, гиперлипидемия может возникнуть в результате сочетания причин, вызывающих как первичную, так и вторичную гиперлипидемию. Повышенные уровни содержания холестерина связаны с рядом болезненных состояний, включая заболевание коронарных артерий, стенокардию, заболевание сонной артерии, параличи, церебральный артериосклероз и ксантому.
Дислипидемия, или ненормальные уровни содержания липопротеинов в плазме крови, является частым нарушением у диабетиков, и доказано, что она является одной из основных причин повышенной встречаемости ишемической болезни сердца и смертности у диабетиков (см., например, Joslin, E. Ann. Chim. Med. (1927) 5: 1061-1079). Проведенные с тех пор эпидемиологические исследования подтвердили наличие этой связи и показали, что смертность от ишемической болезни сердца у диабетиков в несколько раз выше, чем у лиц, не страдающих диабетом (см., например, Garcia, M.J. et al., Diabetes (1974) 23: 105-11 (1974) и Laakso, M. et al., and Lehto, S., Diabetes Reviews (1997) 5(4):294-315). Описаны некоторые отклонения липопротеина от нормы, встречающиеся у больных диабетом (Howard В. et al., Artherosclerosis (1978) 30: 153-162).
Предыдущие исследования 1970-х годов продемонстрировали эффективность рацемического 2-ацетамидоэтил-(4-хлорфенил)-(3-трифторметилфенокси)ацетата (известного также под названием "галофенат") в качестве потенциального терапевтического средства для лечения диабета II типа, гиперлипидемии и гиперурикемии (см., например, Bolhofer, W., U.S. 3,517,050; Jain, A. et al., N. Eng. J. Med. (1975) 293:1283-1286; Kudzma, D. et al., Diabetes (1977) 25:291-95; Kohl, E. et al., Diabetes Care (1984) 7:19-24; McMahon, F.G. et al., Univ. Mich. Med. Center J. (1970) 36:247-248; Simori, С. et al., Lipids (1972) 7: 96-99; Morgan, J.P. et al., Clin. Pharmacol. Therap. (1971) 12:517-524; Aronow, W.S. et al., Clin. Pharmacol. Ther. (1973) 14:358-365 и Fanelli, G.M. et ai., J. Pharm. Experimental Therapeutics (1972) 180:377-396). В этих предшествующих исследованиях влияние рацемического галофената на диабет наблюдали в тех случаях, когда его сочетали с сульфонилмочевинами. Минимальное влияние на глюкозу наблюдали у больных диабетом пациентов, которых лечили одним рацемическим галофенатом. Однако были замечены значительные побочные действия, включая желудочно-кишечные нарушения - кровотечения из желудка и пептические язвы (см., например, Friedberg, S.J. et al., Clin. Res. (1986) Vol. 34, No. 2: 682A).
Кроме того, есть некоторые указания на существование межлекарственных взаимодействий между рацемическим галофенатом и такими агентами, как варфаринсульфат (который называется также 3-(альфа-ацетонилбензил)-4-гидроксикумарин или Кумадин™ (Dupont Pharmaceuticals, E.I. Dupont de Nemours and Co., Inc., Wilmington, DE U.S.A.) (см., например, Vesell, E.S. and Passantanti, G. T., Fed. Proc. (1972) 31(2):538). Кумадин™ представляет собой антикоагулянт, который действует путем ингибирования синтеза зависящих от витамина К факторов свертывания (включающих факторы II, VII, IX и X, а также антикоагулянтные белки С и S). Полагают, что Кумадин™ стереоспецифически метаболизируется печеночными микросомальными ферментами (ферментами цитохром Р450). Изозимы цитохрома Р450, участвующие в метаболизме кумадина, включают 2С9, 2С19, 2С8, 2С18, 1А2 и 3А4. 2С9, по-видимому, является основной формой Р450 печени человека, который модулирует метаболизм нескольких видов лекарств in vivo, включая антикоагулирующую активность Кумадина™ (см., например. Miners, J.O. et al., Bri. J. Clin. Pharmacol. (1998) 45:525-538).
Лекарства, которые ингибируют метаболизм Кумадина™, приводят к дальнейшему уменьшению количества зависящих от витамина К факторов свертывания, в результате чего у пациентов, получающих такое лечение, коагуляция уменьшается в большей степени, чем это желательно (т.е. у пациентов с риском легочной или церебральной эмболии в результате образования сгустков крови в нижних конечностях, сердце или в других участках тела). Просто уменьшить дозу антикоагулянта часто бывает трудно, поскольку пациент нуждается в поддержании соответствующего уровня антикоагуляции, чтобы предотвратить образование сгустков крови. Повышенная антикоагуляция в результате взаимодействия между лекарствами приводит к значительному риску для таких пациентов, с возможностью сильных кровотечений из повреждений мягких тканей, желудочно-кишечных кровотечений (т.е. язв желудка или двенадцатиперстной кишки) и других поражений (например, аневризмы аорты). Кровотечение в результате слишком сильной антикоагуляции требует немедленной медицинской помощи и может привести к смерти, если немедленно не было проведено соответствующее лечение.
Известно, что цитохром Р450 2С9 также участвует в метаболизме некоторых других обычно используемых лекарств, включая дилантин, сульфонилмочевины, такие как толбутамид, а также некоторых нестероидных противовоспалительных средств, таких как ибупрофен. Ингибирование этого фермента может привести к другим неблагоприятным эффектам, связанным с межлекарственными взаимодействиями, кроме тех, которые описаны выше для Кумадина™ (см., например, Pelkonen, О. et al., Xenobiotica (1998) 28:1203-1253; Linn, J.H. и Lu, A.Y., Clin. Pharmacokinet. (1998) 35 (5):361-390).
Прежде чем галофенат станет общепринятым средством для лечения резистентности к инсулину, диабета II типа, гиперлипидемии и гиперурикемии, необходимо решить вышеуказанные проблемы. Настоящее изобретение решает эту и другие задачи путем создания композиций и способов лечения резистентности к инсулину, диабета II типа, гиперлипидемии и гиперурикемии и в то же время обеспечивает улучшение профиля побочных действий.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение касается способа модулирования диабета II типа у млекопитающего. Способ включает введение млекопитающему терапевтически эффективного количества (-)стереоизомера соединения формулы I,
где R представляет собой радикал, выбранный из группы, состоящей из гидрокси, низшего аралкокси, ди-низшего алкиламино-низшего алкокси, низшего алканамидо низшего алкокси, бензамидо-низшего алкокси, уреидо-низшего алкокси, N'-низшего алкил-уреидо-низшего алкокси, карбамоил-низшего алкокси, галофенокси-замещенного низшего алкокси, карбамоилзамещенного фенокси, карбонил-низшего алкиламино, N,N-ди-низшего алкиламино-низшего алкиламино, галогензамещенного низшего алкиламино, гидрокси-замещенного низшего алкиламино, низшего алканолилоксизамещенного низшего алкиламино, уреидо и низшего алкоксикарбониламино; а Х представляет собой галоген; или его фармацевтически приемлемой соли, причем это соединение по существу не содержит своего (+)стереоизомера.
Некоторые такие способы включают также соединение формулы II:
в которой R2 представляет собой радикал, выбранный из группы, состоящей из фенил-низшего алкила, низшего алканамидо-низшего алкила и бензамидо-низшего алкила.
Некоторые такие способы включают также соединение формулы III:
Предпочтительное соединение формулы III известно как "(-)2-ацетамидоэтил-4-хлорфенил-(3-трифторметилфенокси)ацетат" или "(-)галофенат".
Настоящее изобретение обеспечивает также способ модулирования резистентности к инсулину у млекопитающего. Способ включает введение млекопитающему терапевтически эффективного количества (-)стереоизомера соединения формулы I. Некоторые такие способы включают также соединение формулы II. Некоторые такие способы включают также соединение формулы III.
Настоящее изобретение обеспечивает также способ облегчения гиперлипидемии у млекопитающего. Способ включает введение млекопитающему терапевтически эффективного количества соединения формулы I. Некоторые такие способы включают также соединение формулы II. Некоторые такие способы включают также соединение формулы III.
Настоящее изобретение обеспечивает также способ модулирования гиперурикемии у млекопитающего. Способ включает введение млекопитающему терапевтически эффективного количества соединения формулы I. Некоторые такие способы включают также соединение формулы II. Некоторые такие способы включают также соединение формулы III.
Настоящее изобретение касается также фармацевтических композиций. Фармацевтические композиции включают фармацевтически приемлемый носитель и терапевтически эффективное количество соединения формулы I, II или формулы III.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1 показывает ингибирование активности цитохрома Р450 2С9 (CYP2C9) рацемической галофеновой кислотой, (-)галофеновой кислотой и (+)галофеновой кислотой. Гидроксилирование толбутамида измеряли в присутствии увеличивающихся концентраций этих соединений. Рацемическая галофеновая кислота ингибировала активность CYP2C9 с ИК50, составляющей 0,45 мкМ, а (+)галофеновая кислота ингибировала активность CYP2C9 с ИК50, составляющей 0,22 мкМ. В противоположность этому, действие (-)галофеновой кислоты было в 20 раз меньшим с ИК50, составляющей 3,5 мкМ.
Фигура 2 показывает кривую понижения содержания глюкозы во времени после одной пероральной дозы рацемического галофената, (-)энантиомера галофената или (+)энантиомера галофената, в дозе 250 мг/кг у больных диабетом мышей линии ob/ob. Наиболее быстрое наступление действия и наиболее длительное действие продемонстрировал (-)энантиомер. Уменьшение содержания глюкозы было значимым (р<0,05) для (-)энантиомера по сравнению с контролем для всех точек кривой от 3 до 24 часов. Показатели для рацемического галофената и (+)энантиомера были также значимыми (р <0,05) для всех точек от 3 до 24 часов. Содержание глюкозы в плазме через 24 часа составляло 217±16,6 мг/дл у животных, получавших (-)энантиомер, по сравнению с 306±28,5 мг/дл и с 259,3±20,8 мг/дл у животных, получавших (+)энантиомер и рацемат, соответственно. Содержание глюкозы в плазме в контроле, где животные получали только носитель, составляло 408+16,2 мг/дл через 24 часа. Более эффективным был (-)энантиомер, при значительном (р<0,05) отличии от (+)энантиомера как через 3 часа, так и через 24 часа после введения дозы.
Фигура 3 показывает способность рацемического галофената и обоих (-) и (+)энантиомеров галофената понижать содержание глюкозы в плазме у больных диабетом мышей линии ob/ob после ежедневного перорального введения этих соединений. Рацемат давали в дозе 250 мг/кг/день, а энантиомеры давали в дозах 125 мг/г/день и 250 мг/кг/день. Значительное снижение уровней содержания глюкозы по сравнению с контрольными животными наблюдали у животных, которым вводили рацемический галофенат и оба (-) и (+)энантиомера галофената. При низкой дозе введения (125 мг/кг/день) (-) и (+)энантиомеров показатели для (-)энантиомера были значимы через 6, 27 и 30 часов, в то время как показатели для (+)энантиомера были значимы только через 6 и 27 часов после введения дозы.
Фигура 4 показывает уровни содержания инсулина в плазме крови мышей линии ob/ob, получавших рацемический галофенат и оба (-) и (+)энантиомера галофената после ежедневного перорального введения этих соединений. Рацемат давали в дозе 250 мг/кг/день, а энантиомеры давали в дозах 125 мг/г/день и 250 мг/кг/день. По сравнению с контролем, в котором животные получали только носитель, содержание инсулина было ниже у животных, которым вводили рацемический галофенат или любой из энантиомеров галофената. При высокой дозе введения наибольшее понижение содержания инсулина в плазме отмечали через 27 и 30 часов у животных, получавших оба (-) и (+)энантиомера галофената спустя два дня после его введения.
Фигура 5 показывает уровни содержания глюкозы в плазме крови мышей линии ob/ob после голодания в течение ночи, после введения в течение 5 дней носителя, рацемического галофената в дозе 250 мг/кг/день, (-)энантиомера галофената в дозах 125 мг/кг/день и 250 мг/кг/день и (+)энантиомера галофената в дозах 125 мг/кг/день и 250 мг/кг/день. У контрольных животных была гипергликемия, при содержании глюкозы в плазме на уровне 185,4±12,3 мг/дл. У всех животных, получавших галофенат, отмечено значимое (р<0,01) понижение содержания глюкозы. Высокие дозы обоих энантиомеров понижали содержание глюкозы почти до нормальных уровней в 127,3±8,0 мг/дл и 127,2±9,7 мг/дл для животных, получавших (-)энантиомер и (+)энантиомер соответственно.
Фигура 6 показывает уровни содержания инсулина в плазме крови мышей линии ob/ob после голодания в течение ночи, после введения в течение 5 дней носителя, рацемического галофената в дозе 250 мг/кг/день, (-)энантиомера в дозах 125 мг/кг/день и 250 мг/кг/день или (+)энантиомера галофената в дозах 125 мг/кг/день и 250 мг/кг/день. Значительно более низкие уровни содержания инсулина в плазме наблюдали у животных, получавших обе дозы (-)энантиомера. Низкая доза (+)энантиомера не понижала содержание в плазме инсулина, хотя высокая доза (+)энантиомера привела к понижению содержания инсулина в плазме крови.
Фигура 7А показывает уровни содержания глюкозы в плазме крови после перорального контрольного введения глюкозы крысам линии Zucker fatty, которая служит моделью резистентности к инсулину и ослабленной толерантности к глюкозе. Эти животные получали либо носитель (контроль), либо рацемический галофенат, (-)галофенат или (+)галофенат за 5,5 часов до контрольного введения глюкозы. Рацемат давали в дозе 100 мг/кг, а оба энантиомера давали в дозах 50 и 100 мг/кг. У контрольных животных содержание глюкозы повысилось до >250 мг/дл через 30 минут после введения глюкозы, что ясно указывало на ослабленную толерантность к глюкозе. Содержание глюкозы в плазме было пониженным у крыс, получавших рацемический галофенат, особенно между 30 и 60 минутами после контрольного введения глюкозы. Животные, получавшие (-)галофенат в дозе 100 мг/кг, имели самые высокие показатели понижения содержания глюкозы среди всех подопытных животных. Животные, получавшие (-)галофенат, имели более низкие уровни содержания глюкозы, которые сохранялись через 90-120 минут, по сравнению с крысами, получавшими рацемат или (+)галофенат. На фигуре 7В дается сравнение областей приращения под кривой (AUC) для животных каждой группы. Значимые изменения (р<0,05) наблюдали в группах, получавших обе дозы (-)галофената. Хотя AUC была ниже и в других группах, по сравнению с контролем, но эти изменения были незначимыми.
Фигура 8 показывает результаты экспресс-теста на толерантность к инсулину для крыс линии Zucker fatty, которые получали либо носитель (контроль), либо (-)галофенат (50 мг/кг/день) или (+)галофенат (50 мг/кг/день) в течение 5 дней. Этот тест представляет собой измерение чувствительности к инсулину у испытуемых животных, причем наклон кривой понижения содержания глюкозы представляет собой прямое измерение отвечаемости на инсулин. Животные, получавшие (-)галофенат, были существенно более чувствительны к инсулину, чем животные, получавшие носитель (р<0,01) или (+)галофенат (р<0,05).
Фигура 9А показывает уровни содержания холестерина в плазме крови крыс линии Zucker Diabetic Fatty, которые получали в течение 13 дней рацемический галофенат, (-)энантиомер или (+)энантиомер в дозах 50 мг/кг/день, 25 мг/кг/день и 25 мг/кг/день соответственно, по сравнению с животными контрольной группы, которые получали носитель. У животных, получавших как (-)энантиомер, так и рацемат, содержание холестерина в плазме крови понизилось после введения этих соединений. Содержание холестерина у получавших (+)энантиомер животных оставалось относительно постоянным, в то время как у контрольных животных содержание холестерина повышалось. На фигуре 9В приводится сравнение содержание холестерина в плазме животных контрольной группы и групп, получавших испытуемые соединения. Наиболее активным для использованного в испытании вида животных был (-)энантиомер.
Фигура 10А показывает уровни содержания холестерина в плазме крови крыс линии Zucker Diabetic Fatty, которые получали в течение 14 дней либо (-)энантиомер, либо (+)энантиомер галофената, в низкой дозе (12,5 мг/кг/день) или в высокой дозе (37,5 мг/кг/день), по сравнению с животными контрольной группы, которые получали носитель. У животных, получавших высокую дозу, (-)энантиомер привел к самому большому понижению содержания холестерина. На фигуре 10В приводится сравнение различий в содержании холестерина в плазме крови животных контрольной группы и групп, получавших испытуемые соединения. Значимые отличия от контроля наблюдались у животных, получавших (-)энантиомер, через 7 дней при использовании низкой дозы и через 7 и 14 дней при использовании высокой дозы. Для (+)энантиомера значимые отличия получены только через 7 дней после введения высокой дозы.
Фигура 11А показывает уровни содержания триглицерида в плазме крови крыс линии Zucker Diabetic Fatty, которые получали либо (-)энантиомер, либо (+)энантиомер, в низкой дозе (12/5 мг/кг/день) и в высокой дозе (37,5 мг/кг/день), по сравнению с животными контрольной группы, которые получали носитель. Животные, получавшие высокую дозу (-)энантиомера, имели самые низкие уровни содержания триглицерида из всех подопытных групп. На фигуре 11В приводится сравнение различий в содержании триглицерида в плазме крови животных контрольной группы и групп, получавших испытуемые соединения. На 7-й день высокие дозы как (+), так и (-)энантиомеров показали значимое снижение содержания в плазме триглицерида.
Фигура 12 показывает уровни содержания глюкозы в плазме крови крыс линии Zucker Diabetic Fatty, которые получали носитель, (-)галофенат или (+)галофенат, в дни 0, 2 и 3. Введение (-)галофената существенно уменьшило концентрации глюкозы в плазме крови, по сравнению с животными, получавшими носитель.
Фигура 13 показывает концентрации глюкозы в плазме крови у контрольной группы мышей линии C57BL/6J db/db по сравнению с группой, получавшей (-)галофенат. Уровни содержания глюкозы в плазме в контрольной группе прогрессирующе повышались по мере старения животных, в то время как у животных, получавших (-)галофенат, повышение содержания глюкозы в плазме не происходило либо отмечалось его существенное понижение.
Фигура 14 показывает уровни содержания инсулина в плазме крови у контрольной группы мышей линии C57BL/6J db/db по сравнению с группой, получавшей (-)галофенат. Введение (-)галофената поддерживало концентрацию инсулина в плазме, в то время как у животных контрольной группы содержание инсулина в плазме прогрессирующе понижалось.
Фигура 15 показывает процент не больных диабетом животных в контрольной группе мышей линии C57BL/6J db/db, по сравнению с группой, получавшей (-)галофенат. Примерно у 30% мышей группы, получавшей (-)галофенат, диабет не развивался (уровни содержания глюкозы в плазме <250 мг/дл), в то время как у всех животных контрольной группы к возрасту 10 недель развился диабет.
Фигура 16 показывает уровни содержания триглицерида в контрольной группе мышей линии C57BL/6J db/db, по сравнению с группой, получавшей (-)галофенат. Введение (-)галофената привело к понижению гиперлипидемии, в то время как в контрольной группе этого не произошло.
Фигура 17 показывает влияние (-)галофената и (+)галофената на содержание мочевой кислоты в плазме крови крыс, у которых с помощью оксоновой кислоты индуцировали гиперурикемию. Пероральное введение (-)галофената существенно понизило уровни содержания мочевой кислоты в плазме крови. Введение (+)галофената также понижало уровни содержания мочевой кислоты в плазме крови, но это понижение было статистически незначимым.
ОБОЗНАЧЕНИЯ
Термин "млекопитающее" включает, без ограничений, человека, домашних животных (например, собак или кошек), сельскохозяйственных животных (коров, лошадей или свиней), обезьян, кроликов, мышей и лабораторных животных.
Термин "резистентность к инсулину" можно определить в общем виде как нарушение метаболизма глюкозы. Более конкретно, резистентность к инсулину можно определить как уменьшенную способность инсулина проявлять свое биологическое действие в широком диапазоне концентраций, в результате чего его биологический эффект оказывается ниже ожидаемого (см., например, Reaven, G.M., J. Basic & Clin. Phys. & Pharm. (1998) 9:387-406, и Filer, J. Ann. Rev. Med. (1983) 34;145-60). Резистентные к инсулину индивидуумы обладают уменьшенной способностью должным образом утилизировать глюкозу и плохо реагируют или совсем не реагируют на инсулиновую терапию. Проявления резистентности к инсулину включают неэффективную активацию инсулином поглощения, окисления и запасания глюкозы в мышцах, а также неадекватное подавление инсулином липолиза в жировых тканях и продуцирования глюкозы и секретирования ее в печени. Резистентность к инсулину может явиться причиной или одной из причин синдрома поликистоза яичников, ослабленной толерантности к глюкозе (IGT), диабета беременных, гипертензии, ожирения, атеросклероза и ряда других нарушений. В конце концов, индивидуумы, резистентные к инсулину, могут постепенно дойти до состояния диабета. Связь резистентности к инсулину с нетолерантностью к глюкозе, увеличением содержания триглицеридов в плазме крови и уменьшением концентрации холестерина, представляющего собой липопротеин высокой плотности, высоким кровяным давлением, гиперурикемией, пониженной плотностью частиц липопротеинов низкой плотности и с более высокими уровнями циркуляции ингибитора-1 активатора пламиногена получила название "синдрома X" (см., например, Reaven, G.M., Physiol. Rev. (1995) 75:473-486).
Термин "сахарный диабет" или "диабет" обозначает болезнь или состояние, которое, как правило, характеризуется метаболическими дефектами продуцирования и утилизации глюкозы, приводящими к невозможности поддержания необходимых уровней сахара в теле. Результатом этих дефектов является повышенное содержание глюкозы в крови, называемое "гипергликемией". Две основные формы диабета представляют собой диабет I типа и диабет II типа. Как описано выше, диабет I типа, как правило, является результатом абсолютной недостаточности инсулина, гормона, регулирующего утилизацию глюкозы. Диабет II типа часто наблюдается на фоне нормальных или даже повышенных уровней инсулина и может являться результатом неспособности тканей правильно реагировать на инсулин. Большинство пациентов с диабетом II типа являются резистентными к инсулину и имеют относительную недостаточность инсулина, при которой секреция инсулина не может компенсировать резистентность периферических тканей по отношению к инсулину. Кроме того, многие пациенты с диабетом II типа являются тучными. Другие типы нарушений гомеостаза глюкозы включают ослабленную толерантность к глюкозе, которая представляет собой этап метаболизма, промежуточный между нормальным гомеостазом глюкозы и диабетом, и сахарный диабет беременных, который представляет собой не толерантность к глюкозе во время беременности у женщин, у которых в анамнезе ранее не было диабета I типа или II типа.
Термин "вторичный диабет" обозначает диабет, являющийся результатом действия других определенных причин, включающих: генетические дефекты функционирования β-клеток (например, начинающийся при созревании юношеский диабет, называемый "MODY", который представляет собой рано начинающийся диабет II типа с аутосомальной наследуемостью; см., например, Fajans S. et al., Diabet Med. (1996) (9 Suppl. 6): 390-5, и Bell, G. et al., Annu. Rev. Physiol. (1996) 58:171-86; генетические дефекты действия инсулина; болезни экзокринной поджелудочной железы (например, гемохроматоз, панкреатит и муковисцидоз); некоторые эндокринные болезни, при которых избыточное количество гормонов мешает действию инсулина (например, гормон роста при акромегалии и кортизол при синдроме Кушинга); некоторые лекарства, подавляющие секрецию инсулина (например, фенитоин) или ингибирующие действие инсулина (например, эстрогены и глюкокортикоиды); и диабет, вызванный инфекцией (например, краснухой, вирусом Коксаки и CMV (вирусом мозаики цветной капусты); а также другие генетические синдромы.
Рекомендации по диагностике диабета II типа, ослабленной толерантности к глюкозе и диабета беременных предложены Американской ассоциацией по диабету (см., например. The Expert Committee on the Diagnosis and Classification of Diabetes Mellitus, Diabetes Care, (1999) Vol 2 (Suppl 1): S5-19).
Термин "галофеновая кислота" обозначает форму 4-хлорфенил-(3-трифторметилфенокси)уксусной кислоты.
Термин "гиперинсулинемия" обозначает присутствие ненормально повышенного уровня содержания инсулина в крови.
Термин "гиперурикемия" обозначает присутствие ненормально повышенного уровня содержания мочевой кислоты в крови.
Термин "секретор" обозначает вещество или соединение, стимулирующее секрецию. Например, инсулиновый секретор представляет собой вещество или соединение, которое стимулирует секрецию инсулина.
Термин "гемоглобин" или "Hb" обозначает дыхательный пигмент, присутствующий в эритроцитах, который в значительной степени ответственен за транспорт кислорода. Молекула гемоглобина включает четыре полипептидных субъединицы (две системы α-цепей и две системы β-цепей, соответственно). Каждая субъединица образована ассоциацией одного белка глобина и одной молекулы гема, который представляет собой железно-протопорфириновый комплекс. Основным классом гемоглобина, содержащемся в нормальном зрелом гемолизате, является зрелый гемоглобин (называемый "HbA"; а также называемый "HbA0", для того, чтобы отличать его от гликозилированного гемоглобина, называемого "HbA1", описанного ниже), имеющий субъединицы α2β2. В нормальном зрелом гемолизате могут также находиться компоненты, содержащиеся в микроколичествах, такие как HbA2 (α2δ2).
Среди классов зрелого гемоглобина HbAs имеется гликированный гемоглобин (называемый "HbA1" или "гликозилированным гемоглобином"), который в свою очередь можно разделить на фракции HbA1a1, HbA1a2, HbA1b и HbA1c путем фракционирования на ионообменных смолах. Все эти подклассы имеют одинаковую первичную структуру, которая стабилизируется путем образования алдимина (основания Шиффа) аминогруппой N-концевого валина в цепи β-субъединицы нормального гемоглобина HbA и глюкозы (или глюкоза-6-фосфата или фруктозы), с последующим образованием кетоамина путем перегруппировки Амадори.
Термин "гликозилированный гемоглобин" (также называемый "HbA1c", "GHb", "гемоглобин-гликозилированным", "индексом контроля диабета" и "гликогемоглобином", ниже называемый "гемоглобином A1c") обозначает стойкий продукт неферментативного гликозилирования β-цепи гемоглобина глюкозой плазмы. Гемоглобином A1c представлена основная часть гликозилированных гемоглобинов крови. Содержание гликозилированного гемоглобина пропорционально содержанию в крови глюкозы. Вследствие этого, скорость образования гемоглобина A1c прямо пропорционально увеличивается с повышением содержания в крови глюкозы. Поскольку гликозилирование происходит с постоянной скоростью в течение 120 дней продолжительности жизни эритроцита, то измерение уровней содержания гликозилированного гемоглобина отражает среднее содержание в крови глюкозы для данного индивидуума во время предшествующих двух или трех месяцев. Поэтому определение количества гликозилированного гемоглобина HbA1c может служить хорошим указателем при контролировании метаболизма углеводов. В соответствии с этим, уровни содержания в крови глюкозы за последние два месяца можно установить на основании отношения количества HbA1c к общему количеству гемоглобина Hb. Анализ содержания гемоглобина A1c в крови используют в качестве измерения, позволяющего осуществлять долгосрочный контроль за уровнями содержания в крови глюкозы (см., например, Jain, S., et al., Diabetes (1989) 38:1539-1543; Peters A., et al., JAMA (1996) 276:1246-1252).
Термин "симптом" диабета включает, не ограничиваясь нижеперечисленным, полиурию, полидипсию и полифагию, как они используются в настоящей заявке, включая обычное использование этих терминов. Например, "полиурия" обозначает выделение большого объема мочи в течение определенного периода времени; "полидипсия" обозначает хроническую чрезмерную жажду; и "полифагия" обозначает чрезмерное потребление пищи. Другие симптомы диабета включают, например, повышенную восприимчивость к некоторым инфекциям (особенно к грибковым и стафилококковым инфекциям), тошноту и кетоацидоз (повышенное продуцирование кетоновых тел в крови).
Термин "осложнение" диабета включает, не ограничиваясь нижеперечисленным, микрососудистые осложнения и макрососудистые осложнения. Микрососудистые осложнения - это такие осложнения, которые в основном приводят к повреждению мелких кровеносных сосудов. Эти осложнения включают, например, ретинопатию (ослабление или потерю зрения из-за повреждения кровеносных сосудов в глазах); невропатию (повреждение нерва и болезни ног из-за повреждения нервной системы, вызванного кровеносными сосудами); и нефропатию (болезнь почек, вызванная повреждением кровеносных сосудов в почках). Макрососудистые осложнения - это такие осложнения, которые в основном происходят из-за повреждения крупных кровеносных сосудов. Эти осложнения включают, например, сердечно-сосудистые заболевания и заболевания периферической кровеносной системы. К сердечнососудистым заболевания относятся заболевания кровеносных сосудов сердца. См., например, Kaplan, R.M. et al., "Cardiovascular diseases" in "Health and Human Behavior", pp.206-242 (McGraw-Hill, New York 1993). Сердечно-сосудистое заболевание, как правило, представляет собой одну из нескольких форм, например, гипертензию (называемую также повышенным кровяным давлением), коронарную (ишемическую) болезнь сердца, стенокардию и ревматизм сердца. К заболеваниям периферической кровеносной системы относятся заболевания любых кровеносных сосудов вне сердца. Часто они представляют собой сужение кровеносных сосудов, по которым кровь поступает к мышцам ноги или руки.
Термин "атеросклероз" охватывает сосудистые заболевания и состояния, известные и понятные врачам, работающим в соответствующих областях медицины. Атеросклеротическое сердечнососудистое заболевание, коронарная болезнь сердца (известная также под названиями заболевание коронарной артерии или ишемическая болезнь сердца), заболевание сосудов мозга и заболевание периферических кровеносных сосудов - все эти заболевания являются клиническими проявлениями атеросклероза и поэтому охватываются терминами "атеросклероз" и "атеросклеротическое заболевание".
Термин "антигиперлипидемический" относится к понижению избыточных концентраций липидов в крови до желаемых уровней.
Термин "антиуремический" относится к понижению избыточных концентраций мочевой кислоты в крови до желаемых уровней.
Термин "гиперлипидемия" относится к присутствию ненормально повышенной концентрации липидов в крови. Гиперлипидемия может проявляться по меньшей мере в трех формах: (1) гиперхолестеринемия, т.е. повышенное содержание холестерина в крови; (2) гипертриглицеридемия, т.е. повышенное содержание триглицеридов; и (3) комбинированная гиперлипидемия, т.е. комбинация гиперхолестеринемии и гиперглицеридемии.
Термин "модулировать" относится к лечению, профилактике, подавлению, повышению или индуцированию функции или состояния. Например, соединения по настоящему изобретению могут модулировать гипрелипидемию путем понижения содержания холестерина в крови человека, тем самым подавляя гиперлипидемию.
Термин "лечение" обозначает помощь человеку и уход за человеком с целью борьбы с болезнью, состоянием или нарушением, и включает введение соединения