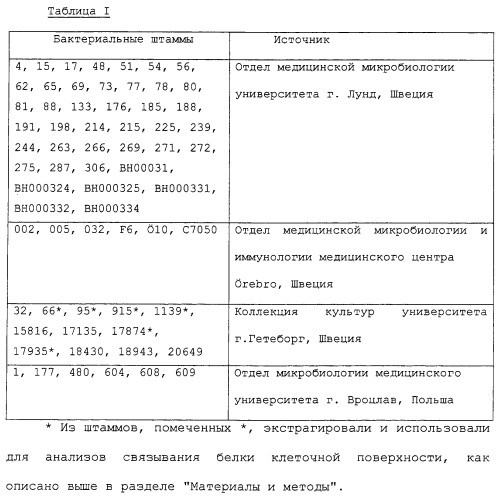
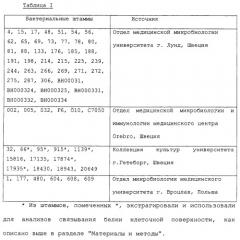
Новые вещества, связывающиеся с helicobacter pylori, и их применение
Иллюстрации
Показать всеПредложено средство формулы (1) для связывания с Helicobacter pylori ex vivo и вещество на его основе, а также фармацевтическая композиция, пищевая добавка и способ идентификации бактериального адгезина. Вещество состоит из средства формулы (1) и носителя. В частности, средство включает Galβ3GlcNAc. Средство может быть конъюгировано с олигосахаридом или с церамидом. Заявленное средство представляет собой специфически связывающий эпитоп лактотетраозы или лактотетраозилцерамид (Galβ3GlcNAcβ3Galβ-4Glcβ1Cer) с активностью, подобной таковой лактотетраозилцерамидного сфинголипида и может применяться при типировании Helicobacter pylori, для ингибирования связывания Helicobacter pylori, в немедицинских целях, для идентификации бактериального адгезина. 6 н. и 12 з.п. ф-лы, 13 ил., 3 табл.
Реферат
Область изобретения
Настоящее изобретение относится к новым веществам, связывающимся с Helicobacter pylori, и их применению, например, в фармацевтических композициях и способах лечения состояний, вызванных Helicobacter pylori.
Предпосылки к созданию изобретения
Адгезию микроорганизмов считают первым этапом патогенеза инфекций, когда специфичность адгезинов инфекционного агента, с одной стороны, и рецепторные структуры, экспрессируемые эпителиальными клетками органа-мишени хозяина, с другой, представляют собой важные определяющие факторы ряда хозяев и тканевого тропизма патогена [1].
Человеческий желудочный патоген Helicobacter pylori представляет собой этиологический агент хронического поверхностного гастрита [2] и также связан с развитием язвы двенадцатиперстной кишки, язвы желудка и аденокарциномы желудка [3-7]. Указанный микроорганизм поражает отчетливо определенный ряд хозяев и имеет выраженный тканевый тропизм, т.е. он требует наличия человеческого эпителия желудочного типа для колонизации [8]. В желудке человека большинство бактерий находят в слое слизи, но показана также избирательная ассоциация бактерий с поверхностными мукоцитами [8, 9].
Ранее было показано несколько различных связывающих специфичностей Helicobacter pylori. Так, сообщалось о связывании бактерии с такими разнообразными соединениями, как фосфатидилэтаноламин и ганглиотетраозилцерамид [10, 11], детерминанта группы крови Leb [12], гепарансульфат [13], ганглиозид GM3 [14], сульфатид [14, 15] и лактозилцерамид [16]. Зависящее от сиаловой кислоты связывание Helicobacter pylori с большим комплексом гликосфинголипидов (полигликозилцерамидов) человеческих эритроцитов, гранулоцитов и плаценты, также подтверждена документально [17, 18].
Помимо своей связи с желудочно-кишечными заболеваниями Helicobacter pylori связана с множеством заболеваний, также поражающих другие органы кроме органов желудочно-кишечного тракта [74]. Например, были показаны связи с заболеваниями сердца, особенно атеросклерозом [75], заболеваниями печени, включая аденокарциному печени [76, 77], заболеваниями кожи [78] и синдромом внезапной младенческой смерти [79, US 6083756].
Краткое описание существа изобретения
Главной целью настоящего изобретения является создание новых путей для лечения состояний, вызываемых Helicobacter pylori.
Настоящее изобретение основано на открытии специфичного рецептора Helicobacter pylori в эпителии желудка человека. Во многих случаях указанный рецептор представляет собой гликолипид, лактотетраозилцерамид, который обнаруживают исключительно в желудочно-кишечном тракте, и во время исследовательской работы было показано, что эпитоп минимального связывания представляет собой Galβ3GlcNAc или очень сходную структуру Galβ3GalNAc.
Настоящее изобретение, таким образом, относится к веществам, связывающимся с Helicobacter pylori, которые включают указанный связывающий эпитоп, или к их аналогам или производным.
Одной целью настоящего изобретения является создание фармацевтических композиций для лечения состояний, вызванных Helicobacter pylori.
Другой целью настоящего изобретения является применение упомянутых выше веществ, связывающихся с Helicobacter pylori, для производства фармацевтических композиций для лечения состояния, обусловленного присутствием Helicobacter pylori.
Другой целью настоящего изобретения является создание способа лечения состояния, обусловленного присутствием Helicobacter pylori.
Другой целью настоящего изобретения является применение упомянутых выше веществ, связывающихся с Helicobacter pylori, для идентификации бактериальных адгезинов.
Другой целью настоящего изобретения является применение упомянутых выше веществ, связывающихся с Helicobacter pylori, для ингибирования связывания с Helicobacter pylori как для терапевтических целей, так и для немедицинских целей, таких как анализы in vitro.
Другой целью настоящего изобретения является применение упомянутых выше веществ, связывающихся с Helicobacter pylori, как ведущих соединений для идентификации других веществ, связывающихся с Helicobacter pylori.
Другой целью настоящего изобретения является применение упомянутых выше веществ, связывающихся с Helicobacter pylori, в пищевых продуктах или пищевых добавках.
Другой целью настоящего изобретения является применение упомянутых выше веществ, связывающихся с Helicobacter pylori, или упомянутых выше бактериальных адгезинов для производства вакцин против Helicobacter pylori.
Другой целью настоящего изобретения является применение упомянутых выше веществ, связывающихся с Helicobacter pylori, для диагностики инфекций, вызванных Helicobacter pylori.
Еще одной целью настоящего изобретения является применение упомянутых выше веществ, связывающихся с Helicobacter pylori, для типирования Helicobacter pylori.
Подробное описание изобретения
Как упоминалось выше, настоящее изобретение относится к специфичному веществу, которое связывается с Helicobacter pylori. В работе, результатом которой стало настоящее изобретение, множество различных штаммов Helicobacter pylori метаболически пометили 35S-метионином и исследовали их связывание с рядом различных натуральных гликосфинголипидов, разделенных на пластинках для тонкослойной хроматографии. С помощью ауторадиографии были выявлены в повторностях две отличающихся друг от друга специфические формы. Как было подробно описано ранее, Helicobacter pylori связывается с лактозилцерамидом, ганглиотриаозилцерамидом и ганглиотетраозилцерамидом [16]. Единственная связывающая активность, первоначально выявленная на человеческом материале, относилась к соединению тетрагликозилцерамидного ряда в некислотной фракции мекония человека.
Гликосфинголипидный состав человеческого желудочного эпителия изучен не слишком хорошо. Однако в недавнем исследовании гликосфинголипидов клеток слизистых оболочек и подслизистой ткани желудочно-кишечного тракта человека [55] сообщалось об обогащении сульфатидами слизистой оболочки дна и антрального отдела желудка. Большая часть некислотных гликосфинголипидов на пластинках для тонкослойной хроматографии мигрировала как галактозилцерамид, лактозилцерамид, глоботриаозилцерамид и глобозид, в то время как главные ганглиозиды мигрировали как GM3, GM1 и GD3. Лактозилцерамид, связывающий Helicobacter pylori, с фитосфингозином и гидроксильными жирными кислотами, в эпителиальных клетках желудка человека также был описан [16].
Помимо этого, Cad-активный ганглиозид группы крови (GalNAcβ4 (NeuAcα3)Galβ4GlcNAcβ3Galβ4Glcβ1Cer) был идентифицирован в области дна желудка человека [56], в то время как он не был обнаружен в пилорическом отделе [57], что указывает на дифференциальную экспрессию гликосфинголипидов в различных отделах желудка человека.
В силу ограниченного доступа к ткани желудка человека авторы настоящего изобретения первоначально сосредоточились на гликосфинголипиде, связывающемся с Helicobacter pylori, выявленном в меконии человека, который представляет собой первый стерильный кал новорожденного и состоит, главным образом, из отторгнутых клеток слизистой оболочки развивающегося желудочно-кишечного тракта. После выделения указанный гликосфинголипид, связывающийся с Helicobacter pylori, был охарактеризован посредством масс-спектрометрии, протонной ЯМР-спектроскопии и анализа метилирования как Galβ3GlcNAcβ3Galβ4Glcβ1Cer (лактотетраозилцерамид). Тканевое распределение лактотетраозилцерамида весьма ограничено. До недавних пор лактотетраозилцерамид был выделен только из мекония человека [45], из тонкого кишечника индивидуума, перенесшего ранее резекцию по Бильроту II [46], из нормальной слизистой оболочки желудка человека и из ткани рака желудка человека [58]. Однако "нормальная" слизистая оболочка в 4 из 5 случаев, описанных в последнем сообщении, была получена при антрэктомии по поводу язвы двенадцатиперстной кишки или желудка. Иммуногистохимические исследования с использованием моноклонального антитела К-21 показало избирательную экспрессию последовательности Galβ3GlcNAc в поверхностных участках слизистой оболочки желудка человека (фовеолярном эпителии) у индивидуумов-несекреторов [59], которая совпадала с локализацией связывания Helicobacter pylori со срезами ткани [8, 9]. Иммуногистохимическое исследование с использованием поликлональных антител, связывающихся с последовательностью Galβ3GlcNAc, показало наличие лактотетраозилцерамида в каемочных клетках тощей и подвздошной кишки человека у индивидуумов-несекреторов, с группой крови OLe(a-b-), а также у одного индивидуума-несекретора, с группой крови OLe(a+b+) [60].
Среди 66 изолятов Helicobacter pylori, проанализированных в данном исследовании, 57 штаммов (86%), как было установлено, экспрессируют лактотетраозилцерамидсвязывающую специфичность, в то время как 9 штаммов были отрицательными. Большое преобладание свойства связывать лактотетраоэилцерамид, которое наблюдалось среди изолятов Helicobacter pylori, показывает, что оно представляет собой преобразованное свойство указанного желудочного патогена и может, таким образом, представлять важный фактор вирулентности.
Биологическая уместность лактотетраозилцерамидсвязывающей специфичности была дополнительно подтверждена связыванием Helicobacter pylori с тетрагликозилцерамидной областью некислотных гликосфинголипидов, выделенных из эпителиальных клеток-мишеней человеческого желудка. С помощью протонной ЯМР-спектроскопии и газовой хроматографии - масс-спектрометрии перметилированных тетрасахаридов, полученных гидролизом церамидгликаназой, было показано, что активная в отношении связывания фракция содержит лактотетраозилцерамид. Активный в отношении связывания лактотетраозилцерамид был выявлен только у одного из семи изученных индивидуумов, что наводит на мысль о том, что, хотя инфекция Helicobacter pylori и связанный с ней хронический гастрит является очень распространенным явлением, но только у малой части инфицированных индивидуумов развивается какое-либо из дальнейших последствий, таких как пептическая язва или аденокарцинома желудка [7]. Теоретическая предпосылка, таким образом, такова: присутствие лактотетраозилцерамида на клетках желудочного эпителия представляет собой один из кофакторов, необходимых для развития тяжелых последствий инфекции, таких как пептическая язвенная болезнь или рак желудка.
Активная в отношении связывания лактотетраозилцерамидная фракция, выделенная из мекония человека, содержала как гидроксильные, так и негидроксильные виды церамидов. Теоретически связывание может, таким образом, ограничиваться видами с гидроксицерамидами, как это описано для лактозилцерамидсвязывающей специфичности [16]. Однако лактотетраозилцерамид, выделенный из вилочковой железы кролика, с церамидом, состоящим исключительно из сфингозина и негидроксильных 16:0 и 24:0 жирных кислот (В.Lanne et al., готовится к печати), был также активен, как лактотетраозилцерамид из мекония человека (не показано), что показывает, что связывание с лактотетраозилцерамидом не зависит от состава церамида.
Профиль связывания, полученный с 125I-меченными поверхностными бактериальными белками, был идентичен профилю, полученному с 35S-меченными интактными бактериальными клетками, что наводит на мысль о том, что указанные препараты поверхностных белков можно использовать для выделения и изучения свойств адгезинов, связывающихся с углеводами.
Подводя итоги, можно сказать, что адгезия Helicobacter pylori к клеткам слизистой оболочки человеческого желудка, как представляется, является многоэлементной системой, в которой несколько бактериальных адгезинов распознают и связываются с различными рецепторами в ткани-мишени. Указанное исследование идентифицирует еще одно активное в отношении связывания соединение, т.е. лактотетраозилцерамид, выявленное по связыванию с гликосфинголипидами на пластинках для тонкослойной хроматографии. Распределение данного гликосфинголипида ограничено, и до настоящего времени он был обнаружен только в желудочно-кишечном тракте человека. В других человеческих тканях лактотетраозилцерамид замещен фукозой или сиаловой кислотой и, следовательно, при условиях применявшегося анализа не связывался.
Выделение и описание структуры указанного связывающегося с Helicobacter pylori гликосфинголипида, а также идентификация указанного соединения в клетках слизистой оболочки человеческого желудка привели к идентификации эпитопа минимального связывания, а именно Galβ3GlcNAc. Эпитоп Galβ3GalNAc является очень сходным как по структуре, так и по функции, с Galβ3GlcNAc, и они, таким образом, являются практически взаимозаменяемыми.
Настоящее изобретение, таким образом, относится к веществам, связывающимся с Helicobacter pylori, которые включают по меньшей мере одно соединение, имеющее формулу 1:
в которой:
R1 и R2 представляют собой Н или ОН, при условии, что когда R1 представляет собой Н, R2 представляет собой ОН, а когда R1 представляет собой ОН, R2 представляет собой Н;
Х представляет собой остаток моносахарида или олигосахарида, и предпочтительно Х представляет собой лактозил-, галактозил-, поли-N-ацетиллактозаминил, или образует часть олигосахаридной последовательности O-гликана или N-гликана;
Y не является ничем, либо представляет собой пространственную группу или терминальный конъюгат, такой как липидная часть церамида или связь (-O-) с Z;
Z представляет собой олиговалентный или многовалентный носитель или -Н;
n равно 0 или 1;
m представляет собой целое число, равное или превышающее 1, и m может представляет собой число до нескольких тысяч или нескольких миллионов, в зависимости от вещества,
или к их аналогам или производным, имеющим такую же или более высокую связывающую активность, как и соединение, имеющее формулу 1, в отношении Helicobacter pylori.
Когда в формуле 1 R1 представляет собой ОН, a R2 представляет собой Н, получают соединение формулы 2, а когда R1 представляет собой Н, а R2 представляет собой ОН, получают соединение формулы 3.
Настоящее изобретение также включает вещества, соответствующие формулам 1, 2 и 3, в которых -O-Х заменена на -S-X, -N-X или -С-Х, поскольку специалистам известно, что они являются взаимозаменяемыми.
Настоящее изобретение относится также к веществам, связывающимся с Helicobacter pylori, которые включают или состоят из Galβ3GlcNAc (соответствует формуле 1, в которой R1=ОН, a R2=Н) или Galβ3GalNAc (соответствует формуле 1, в которой R1=Н, а R2=ОН), или их аналогам или производным, имеющим такую же или более высокую связывающую активность, как и Galβ3GlcNAc или Galβ3GalNAc, в отношении Helicobacter pylori.
Согласно настоящему изобретению возможно использование Galβ3GlcNAc или Galβ3GalNAc per se или любого их натурального или синтезированного аналога или производного, имеющего такую же или более высокую связывающую активность в отношении Helicobacter pylori. Возможно также использование вещества, такого как лактотетраоза, лактотетраозилцерамид (Galβ3GlcNAcβ3Galβ4Glcβ1Cer) или ганглиотетраозилцерамид (Galβ3GalNAcβ4Galβ4Glcβ1Cer), включающего сайт связывания Galβ3GlcNAc или Galβ3GalNAc, или его аналога или производного, имеющего такую же или более высокую связывающую активность в отношении Helicobacter pylori. Может быть предпочтительным расположение указанного эпитопа минимального связывания или его аналога или производного на терминальном, невосстанавливающемся конце указанного вещества.
Может быть предпочтительным использование лактотетраозы или ганглиотетраозы как по одиночке, так и в поливалентной форме.
Вещество, связывающееся с Helicobacter pylori, no настоящему изобретению может также состоять из или включать носитель, к которому присоединено одно или более упомянутых выше веществ.
Вещество, связывающееся с Helicobacter pylori, no настоящему изобретению может также состоять из или включать мицеллу, включающую одно или более упомянутых выше веществ. Примером указанной мицеллы является липосома, содержащая, например, несколько молекул лактотетраозы.
Вещество, связывающееся с Helicobacter pylori, no настоящему изобретению может также быть конъюгировано с полисахаридом, таким как полилактозаминовая цепочка или ее конъюгат, или с антибиотиком, предпочтительно антибиотиком, действующим против Helicobacter pylori.
Вещества по настоящему изобретению могут, таким образом, представлять собой часть сахаридной цепочки или гликоконъюгата или смеси гликосоединений, содержащих другие известные эпитопы связывания с Helicobacter pylori, имеющих различающиеся сахаридные последовательности и конформации, как Lewis b [Fucα2Galβ3(Fucα4)GlcNAc] или NeuNAcα3Galβ4Glc/GlcNAc. Использование сразу нескольких связывающихся веществ может быть благоприятным для лечения.
Вещество по настоящему изобретению может быть конъюгировано с антибиотическим веществом, предпочтительно с антибиотиком пенициллинового ряда. Вещество по настоящему изобретению нацеливает антибиотик на Helicobacter pylori. Указанный конъюгат выгоден для лечения, поскольку для лечения или терапии против Helicobacter pylori требуется меньшее количество антибиотика, в результате чего меньше выражены побочные эффекты антибиотика. Антибиотическая часть конъюгата нацелена на уничтожение или ослабление бактерий, но конъюгат также может оказывать антиадгезионное действие, как описано ниже.
Известно, что Helicobacter pylori может связываться с несколькими видами олигосахаридных последовательностей. Некоторая часть связывания специфичными штаммами может представлять более симбиотические взаимодействия, которые не ведут к развитию злокачественной опухоли или тяжелых состояний. Настоящие данные по связыванию с эпитопами сахаридов ракового типа показывают, что вещество по настоящему изобретению может предотвращать более патологические взаимодействия, оставляя, таким образом некоторые из менее патогенных бактерий/штаммов Helicobacter pylori связанными с другими рецепторными структурами. Таким образом, для предупреждения заболеваний, связанных с Helicobacter pylori, тотальное удаление бактерий может быть необязательным. Менее патогенные бактерии могут даже оказывать пробиотическое действие в предотвращении воздействия более патогенных штаммов Helicobacter pylori.
Понятно также, что Helicobacter pylori содержит на своей поверхности последовательности Galβ3GlcNAc, которые, по меньшей мере, у некоторых штаммов находятся в нефукозилированной форме, которая может быть связана бактерией, как описано в настоящем изобретении. Вещество по настоящему изобретению может также предотвращать связывание между бактериями Helicobacter pylori и таким образом ингибировать бактерии, например, в процессе колонизации.
Вещество, связывающееся с Helicobacter pylori, no настоящему изобретению может представлять собой, например, гликолипид, гликопротеин или неогликопротеин. Оно также может представлять собой олигомерную молекулу, включающую, по меньшей мере, две олисахаридные цепочки.
Для лечения заболевания или состояния, вызванного присутствием Helicobacter pylori в желудочно-кишечном тракте пациента, возможно применение вещества по настоящему изобретению для противодействия адгезии, т.е. для ингибирования связывания Helicobacter pylori с рецепторами эпителия желудка пациента. После введения вещества или фармацевтической композиции по настоящему изобретению они будут конкурировать с рецептором за связыванием с бактериями, и все или некоторая часть бактерий, которые присутствуют в желудочно-кишечном тракте, будут связываться с веществом по настоящему изобретению, а не с рецептором на эпителии желудка. Затем бактерии будут проходить через кишечник и из организма пациента, будучи связанными с веществом по настоящему изобретению, в результате чего воздействие бактерий на организм пациента уменьшится. Предпочтительно используемое вещество представляет собой растворимое соединение, включающее сайт связывания Galβ3GlcNAc или Galβ3GalNAc, такое как растворимый аналог лактотетраозы, лактотетраозилцерамида, ганглиотетраозы или ганглиотетраозилцерамида. Возможно также и часто предпочтительно присоединять вещество по настоящему изобретению к подходящему носителю. В случае использования носителя к одному носителю можно присоединять несколько молекул вещества по настоящему изобретению, что улучшает ингибирующую эффективность.
Согласно настоящему изобретению возможно также лечение других заболеваний, вызванных присутствием Helicobacter pylori, таких как заболевания печени, сердечные заболевания или синдром внезапной младенческой смерти.
Согласно настоящему изобретению возможно инкорпорирование вещества по настоящему изобретению необязательно вместе с носителем в фармацевтическую композицию, подходящую для лечения состояния, вызванного присутствием Helicobacter pylori в желудочно-кишечном тракте пациента, или использовать вещество по настоящему изобретению в способе лечения указанного состояния. Примерами состояний, которые можно лечить по настоящему изобретению, являются хронический поверхностный гастрит, язва двенадцатиперстной кишки, язва желудка и аденокарцинома желудка.
Фармацевтическая композиция по настоящему изобретению может также включать другие вещества, такие как инертный наполнитель или фармацевтически приемлемые вспомогательные вещества, носители, консерванты и т.п., которые хорошо известны специалистам.
Помимо этого вещество по настоящему изобретению можно вводить вместе с другими лекарственными средствами, такими как лекарственные средства, применяемые для лечения заболеваний желудка, включая ингибиторы протонного насоса или лекарственные средства, регулирующие рН в желудке (омепразол, ланзопразол, ранитидин и т.п.) и антибиотики, применяемые против Helicobacter pylori.
Вещество или фармацевтическую композицию по настоящему изобретению можно вводить любым удобным путем, хотя предпочтительно использовать пероральное введение.
Термин «лечение», используемый в настоящем документе, относится как к лечению с целью излечения или облегчения заболевания или состояния, так и к лечению с целью предотвращения развития заболевания или состояния. Лечение может осуществляться как кратковременно, так и продолжительно.
Термин «пациент», используемый в настоящем документе, относится к любому человеку или млекопитающему, которое не является человеком, нуждающемуся в лечении по настоящему изобретению.
Кроме того, возможно применение вещества по настоящему изобретению с целью идентификации одного или более адгезинов путем скрининга для обнаружения последовательностей, которые связываются с веществом по настоящему изобретению. Указанные последовательности могут представлять собой, например, белки или углеводы. Белок, связывающийся с углеводами, может представлять собой лектин или фермент, связывающийся с углеводами. Скрининг можно осуществлять, например, аффинной хроматографией или способами аффинного перекрестного связывания.
Помимо этого возможно применение веществ, которые специфичным образом связываются с Galβ3GlcNAc или Galβ3GalNAc, присутствующими на тканях человека, и, таким образом, предотвращают связывание с Helicobacter pylori. Примеры указанных веществ включают моноклональное антитело К-21, специфичное в отношении Galβ3GlcNAc, и другие антитела или лектины, связывающиеся с указанной структурой, или фермент β-галактозидазу, способный расщеплять галактозы с β3-связью, или лакто-N-биозидазу, фермент эндогликозидазу, - который высвобождает терминальную часть Galβ3GlcNAc из олигосахаридных цепочек. Кроме того, для ингибирования связывания Helicobacter pylori с рецептором Galβ3GlcNAc можно использовать адгезин, связывающий GalβGlcNAc, или особенно его связывающую часть. В случае использования для человека связывающее вещество должно быть удобным для указанного использования, таким как гуманизированное антитело или рекомбинантная гликозидаза человеческого происхождения, т.е. должно быть неиммуногенным и способным отщеплять остаток/остатки терминального моносахарида от веществ по настоящему изобретению. Однако при введении через желудочно-кишечный тракт многие натуральные лектины и гликозидазы, происходящие, например, из пищи, являются толерантными.
Помимо этого возможно применение вещества по настоящему изобретению в качестве матрицы для производства вакцины, подходящей для вакцинации против Helicobacter pylori при упомянутых выше состояниях.
Помимо этого возможно применение вещества по настоящему изобретению для диагностики состояния, вызванного инфекцией Helicobacter pylori.
Помимо этого возможно применение вещества по настоящему изобретению для ингибирования связывания Helicobacter pylori в немедицинских целях, таких как система анализа in vitro, которую, например, можно использовать для идентификации других веществ, связывающихся с Helicobacter pylori.
Помимо этого возможно применение вещества по настоящему изобретению в качестве ведущего соединения для идентификации других веществ, связывающихся с Helicobacter pylori.
Помимо этого возможно применение вещества по настоящему изобретению для типирования Helicobacter pylori.
И, наконец, также возможно применение вещества по настоящему изобретению в пищевых продуктах или питательной смеси как для человека, так и для животных, например, в кормах, молоке, йогурте или других молочных продуктах, напитках и продуктах детского питания. Описанные в настоящем документе питательные смеси или продукты питания не являются натуральным человеческим молоком. Предпочтительно использовать вещество по настоящему изобретению как часть так называемой функциональной или функционализированной пищи. Указанная функционализированная пища оказывает положительное действие на здоровье человека или животного путем ингибирования или предотвращения связывания Helicobacter pylori с клетками или тканями-мишенями. Вещество по настоящему изобретению может являться частью определенной композиции пищи или функциональной пищи. Функциональная пища может содержать другие известные пищевые ингредиенты, разрешенные учреждениями, которые осуществляют контроль за продуктами питания, такими как Управление по продуктам питания и лекарственным средствам США. Вещество по настоящему изобретению может также применяться в качестве пищевой добавки, предпочтительно в качестве добавки в пищу или напитки для производства функциональной пищи или функционального напитка. Пищу или пищевую добавку можно производить также, если коровы или другие животные будут вырабатывать натуральным образом, через свое молоко, вещество по настоящему изобретению в больших количествах. Это можно осуществить, если добиться повышенной экспрессии подходящих гликозилтрансфераз в молоко животного. Можно выбрать и осуществлять селекционную работу конкретной линии или вида домашнего животного на предмет повышенной выработки вещества по настоящему изобретению. Вещество по настоящему изобретению и особенно вещество по настоящему изобретению для питательной смеси или пищевой добавки можно также производить с использованием микроорганизма/микроорганизмов, таких как бактерии или дрожжи.
Особенно полезно, если вещество по настоящему изобретению является частью продуктов питания или питательных смесей для младенцев или детей младшего возраста, предпочтительно частью смесей для младенцев. «Смеси для младенцев» в настоящем документе относятся к специальным составам для кормления младенцев, таким как состав с белковыми гидролизатами, состав для младенцев, родившихся с недостаточным весом, или дополняющий состав. Многих младенцев кормят специальными составами, которые заменяют натуральное человеческое молоко. Указанные составы могут не содержать особых олигосахаридов человеческого молока на основе лактозы, особенно удлиненных, таких как лакто-N-тетраоза, Galβ3GlcNAcβ3Galβ4Glc и его производные. Состав для кормления младенцев может быть сухим порошком, которые нужно разводить водой для получения конечного продукта, используемого для кормления младенца или ребенка младшего возраста. В предпочтительном варианте осуществления настоящего изобретения детское питание для младенца должно содержать сходную с натуральным человеческим молоком концентрацию лакто-N-тетраозы, около 0,05-5 г на литр, более предпочтительно 0,1-0,5 г на литр.
Известно, что лакто-N-неотетраоза и пара-лакто-N-гексаоза Galβ3GlcNAcβ3Galβ4GlcNAcβ3Galβ4Glc имеются в человеческом молоке и, таким образом, могут считаться безопасными добавками или ингредиентами смесей для кормления младенцев. Helicobacter pylori является особенно инфективной для младенцев и детей младшего возраста и, учитывая, какие заболевания она может впоследствии вызвать, имеет смысл предотвращать инфекцию. Известно также, что Helicobacter pylori является причиной синдрома внезапной младенческой смерти, но лечение мощными антибиотиками, которое используется для уничтожения данной бактерии, может быть особенно неподходящим для детей младшего возраста или младенцев.
Когда вещество по настоящему изобретению предназначается для диагностики или типирования, его, например, можно включать, например, в зонд или тест-карандаш, необязательно составляющими частями тест-набора. Когда указанный зонд или тест-карандаш приводят в контакт с образцом, содержащим Helicobacter pylori, бактерии связываются с зондом или тест-карандашом и, таким образом, могут быть изъяты из образца и подвергнуты дальнейшему анализу.
Номенклатура гликосфинголипидов следует рекомендациям комиссии по биохимической номенклатуре IUPAC-IUB (CBN for Lipids: Eur. J. Biochem. (1977) 79, 1121, J. Biol. Chem. (1982), 257, 3347-3351, J. Biol. Chem. (1987) 262, 13-18).
Предполагают, что Gal, Glc, ClcNAc, GalNAc, NeuAc и NeuGc имеют D-конфигурацию, Fuc-L-конфигурацию, а все сахара присутствуют в пиранозной форме.
Кроме того, лактотетраоза Galβ3GlcNAcβ3Galβ4Glc известна также как лакто-N-тетраоза.
В краткой номенклатуре жирных кислот и оснований число перед колонкой относится к длине углеводородной цепочки, а число после колонки дает общее количество двойных связей в молекуле. Жирные кислоты с 2-гидроксильной группой обозначены префиксом h перед аббревиатурой, например, h16:0. Для длинноцепочечных оснований d обозначает дигидроксил, а t - тригидроксил. Таким образом, d18:1 обозначает сфингозин(1,3-дигидрокси-2-аминооктадецен), a t18:0 - фитосфингозин(1,3,4-тригидрокси-2-аминооктадецен).
Несмотря на то что в описании, примерах и формуле изобретения упоминается только Helicobacter pylori, другие весьма сходные виды Helicobacter также включены в объем настоящего изобретения.
Настоящее изобретение далее иллюстрируется примерами, которые никоим образом не предназначены для ограничения объема настоящего изобретения.
Краткое описание фигур
В примерах, которые приведены ниже, имеются ссылки на прилагаемые фигуры, на которых:
Фиг.1 иллюстрирует связывание 35S-меченной Helicobacter pylori с гликосфинголипидами, разделенными тонкослойной хроматографией. Фиг.1А иллюстрирует гликосфинголипиды, выявленные анизальдегидным реагентом. Фиг.1В и фиг.1С иллюстрируют гликосфинголипиды, выявленные ауторадиографией после связывания меченного радиоактивными изотопами штамма 17875 Helicobacter pylori. Полоса 1 = некислотные гликосфинголипиды эритроцитов человеческой крови группы А, полоса 2 = некислотные гликосфинголипиды тонкого кишечника собаки, полоса 3 = некислотные гликосфинголипиды тонкого кишечника морской свинки, полоса 4 = некислотные гликосфинголипиды мышиных фекалий, полоса 5 = некислотные гликосфинголипиды эпителиальных клеток тонкого кишечника черно-белой крысы, полоса 6 = некислотные гликосфинголипиды человеческого мекония, полоса 7 = кислые гликосфинголипиды эритроцитов человеческой крови группы О, полоса 8 = кислые гликосфинголипиды вилочковой железы кролика, полоса 9 = ганглиозиды головного мозга теленка, полоса 10 = кислые гликосфинголипиды из гипернефромы человека. Обозначения слева от (А) указывают число углеводных остатков в полосах.
Фиг.2 иллюстрирует масс-спектр перметилированного гликосфинголипида, связывающегося с Helicobacter pylori, который был выделен из человеческого мекония. Выше спектра находится упрощенная формула, представляющая виды церамидов с сфингозином и гидроксильной 24:0 жирной кислотой.
Фиг.3 иллюстрирует аномерную область протонной ЯМР-спектрограммы гликосфинголипида из человеческого мекония. Было снято 4000 сканирований при температуре датчика 30°С. Большой дисперсионноподобный сигнал на 5,04 м.д. является инструментальным артефактом, и имеется также неидентифицированная примесь на 4,93 м.д.
Фиг.4 иллюстрирует связывание Helicobacter pylori с чистыми гликосфинголипидами, разделенными на пластинках для тонкослойной хроматографии. Полоса 1 = лактотриаозилцерамид, полоса 2 = лактотетраозилцерамид, полоса 3 = гликосфинголипид Н5 типа 1, полоса 4 = гликосфинголипид Lea-5,
полоса 5 = гликосфинголипид Leb-6,
полоса 6 = гликосфинголипид Х-5,
полоса 7 = гликосфинголипид Y-6,
полоса 8 = гликосфинголипид В6 типа 1. Фиг.4А показывает химическое детектирование с помощью анизальдегида, а фиг.4В представляет собой ауторадиограмму, полученную с помощью связывания с 35S-меченной Helicobacter pylori.
Фиг.5 иллюстрирует эффект предварительной инкубации Helicobacter pylori с олигосахаридами лактозой и лактотетраозой. Фиг.5А представляет собой тонкослойную хроматограмму, окрашенную анизальдегидом, фиг.5В показывает связывание Helicobacter pylori, инкубированной с лактозой, а фиг.5С показывает связывание Helicobacter pylori, инкубированной с лактотетраозой.
Полоса 1 = ганглиотетраозилцерамид,
полоса 2 = лактотетраозилцерамид,
полоса 3 = неолактотетраозилцерамид.
Фиг.6 иллюстрирует тонкослойную хроматограмму разделенных гликосфинголипидов, выявленных с помощью анизальдегида (фиг.6А), и ауторадиограмму, полученную с помощью связывания с 35S-меченным штаммом 002 Helicobacter pylori (фиг.6В). Полоса 1 = лактотетраозилцерамид человеческого мекония, полоса 2 = некислотные гликосфинголипиды человеческого мекония, полоса 3 = некислотные гликосфинголипиды желудка человека с группой крови A(Rh+)p, полоса 4 = некислотные гликосфинголипиды желудка человека с группой крови A(Rh+)P. Количество углеводных остатков в полосах указано обозначениями слева.
Фиг.7 иллюстрирует связывание Helicobacter pylori с некислотными гликосфинголипидами из эпителиальной клетки человеческого желудка. Полоса 1 = стандарт некислотных гликосфинголипидов тонкого кишечника собаки, полоса 2 = стандарт некислотных гликосфинголипидов мышиных фекалий, полоса 3 = стандарт некислотных гликосфинголипидов человеческого мекония, полосы 4-8 = некислотные гликосфинголипиды (80 мкг на полосу) эпителиальной клетки человеческого желудка от пяти индивидуумов (случаи 1-5 в таблице III). Фиг.7А иллюстрирует химическое обнаружение с помощью анизальдегида, а фиг.7В представляет собой ауторадиограмму, полученную путем связывания 35S-меченной Helicobacter pylori. Количество углеводных остатков в полосах указаны обозначениями слева.
Фиг.8 представляет собой тонкослойную хроматограмму, показывающую тетрагликозилцерамидсодержащие фракции, полученные из эпителиальных клеток желудка случая 4 и 5 в таблице III (А), и аномерные области протонных ЯМР-спектрограмм при 500 МГц фракции 4-II (В) и 5-II (С). Полоса 1 = общие некислотные гликосфинголипиды желудочного эпителия случая А, полоса 2 = фракция 4-I из случая 4, полоса 3 = фракция 4-II из случая 4, полоса 4 = общие некислотные гликосфинголипиды желудочного эпителия случая 5, полоса 5 = фракция 5-I из случая 5, полоса 6 = фракция 5-II из случая 5. Количество углеводных остатков в полосах указано обозначениями слева.
Фиг.9 показывает реконструированные ионные хроматограммы перметилированных олигосахаридов, высвобожденных с помощью церамидгликаназы. Прогон А = стандартная смесь глобозида, лактотетраозилцерамида и лактонеотетраозилцерамида, прогон В = тетрагликозилцерамиды из желудочного эпителия случая 4 в таблице III, прогон С = тетрагликозилцерамиды из желудочного эпителия случая 5 в таблице III. Олигосахариды стандартной смеси (прогон А) помечены.
Фиг.10 показывает масс-спектрограммы, полученные высокотемпературной газовой хроматографией и EI масс-спектрометрией перметилированных олигосахаридов, высвобожденных с помощью церамидгликаназы из стандартных гликосфинголипидов (I и II), тетрагликозилцерамидной фракции из желудочного эпителия