Соли алифатических органических аминов, соли аминокислот и соли эфиров аминокислот фосфата комбретастатина а-4 для модулирования роста опухолей или метастазов и роста доброкачественных сосудистых пролиферативных расстройств
Иллюстрации
Показать всеИзобретение относится к солям органических аминов, солям аминокислот и к солям эфиров аминокислот фосфата комбретастатина А-4. Описывается соединение, имеющее общую структуру формулы I
где один из заместителей -OR1 или -OR2 представляет собой -O-QH+, а другой представляет собой гидроксил или -O-QH+; и Q представляет собой (А) необязательно замещенный алифатический органический амин, содержащий, по меньшей мере, один атом азота, который вместе с протоном образует четвертичный аммониевый катион QH+; (В) аминокислоту, содержащую, по меньшей мере, два атома азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+; (С) аминокислоту, содержащую один или несколько атомов азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+ и где, кроме того, все карбоксильные группы аминокислоты находятся в форме эфиров. Также описываются фармацевтические композиции для модулирования роста опухолей или метастазов и роста доброкачественных сосудистых пролиферативных расстройств, применение соединения формулы (I) и способ получения соединения формулы (I). Технический результат - получены новые соли комбретастатина А-4 с полезными физико-химическими свойствами, которые повышают растворимость комбретастатина А-4. 6 н. и 21 з.п. ф-лы, 13 ил.
Реферат
По настоящей заявке испрашивается приоритет по заявке США, регистрационный номер №60/232568, поданной 14 сентября 2000 г., и по заявке США, регистрационный номер №60/251921, поданной 7 декабря 2000 г., причем обе указанные предварительные заявки включены здесь в качестве ссылки.
Область техники
Настоящее изобретение относится к новым и полезным пролекарственным моно- и ди-солям органических аминов, моно- и ди-солям аминокислот и моно- и ди-солям эфиров аминокислот фосфата комбретастатина А-4 (СА4), и эти соли имеют более высокую растворимость, чем природный комбретастатин А-4 и легко регенерируют комбретастатин А-4 при физиологических условиях.
Уровень техники
Рак считается серьезным и повсеместно распространенным заболеванием. По оценкам Национального института рака только в США 1 человек из 3 будет поражен раком в течение его жизни. Более того, приблизительно от 50 до 60% людей, заболевших раком, в конечном итоге умрет. Как следствие, с момента основания Национального института рака в начале 70-х гг. средства, затраченные на изучение рака, резко выросли.
Хотя рак, как обычно считают, является одним заболеванием, на самом деле он включает семейство заболеваний, при которых нормальная дифференциация клеток модифицируется таким образом, что она становится аномальной и неконтролируемой. В результате такие злокачественные клетки быстро разрастаются. В итоге клетки распространяются и метастазируют из своего источника и колонизируют другие органы, в конце концов убивая своего хозяина. Из-за широкого многообразия видов рака, выявленных на сегодняшний день, разработано множество стратегий искоренения рака в организме. По одному из таких способов используют цитотоксичные хемотерапевтические средства. Такие соединения вводят больным раком с целью разрушения злокачественных клеток, не затрагивая при этом живые нормальные клетки. Конкретными примерами таких соединений являются 5-фторурацил, цисплатин и метотрексат.
Комбретастатин А-4 сначала был выделен из ствола Африканского дерева Combretum caffrum (Combretaceae) и было обнаружено, что он является эффективным ингибитором микротрубчатых структур. Кроме того, комбретастатин А-4, как установлено, обладает значительной активностью в отношении линии клеток мышиного L1210 и Р338 лимфоцитарного лейкоза по классификации Национального института рака США (НИР). Помимо этого, комбретастатин А-4, как установлено, конкурирует с комбретастатином А-1, еще одним соединением, выделенным из Combretum caffrum в качестве ингибитора связывания колхицина с тубулином. Он также сильно задерживает развитие VoLo, DLD-1 и НСТ-15 рака толстой кишки человека (ED50<0,01 мкг/мл) и является одним из более сильных антимитотических агентов, найденных среди компонентов Combretum caffrum (патент США 4996237).
Соответственно были проведены исследования по определению эффективности комбретастатина А-4 в качестве хемотерапевтического агента при лечении различных видов рака человека. К сожалению, комбретастатин А-4 по существу не растворяется в воде. Такое свойство в значительной степени препятствует разработке фармацевтических композиций, содержащих комбретастатин А-4. Для повышения растворимости, а также эффективности, были предприняты попытки создания пролекарственных производных комбретастатина А-4, которые будут регенерировать комбретастатин А-4 при физиологических условиях. Например, Koji Ohsumi с соавторами описал синтез HCl-аминокислотных пролекарств аналогов комбретастатина, в которых соль аминокислоты присоединена к аминогруппе производного комбретастатина, содержащего основную аминогруппу [такие производные описаны в работе Ohsumi et.al, Anti-Cancer Drug Design, 14, 539-548 (1999)]. Хотя такие пролекарства могут иметь повышенную растворимость по сравнению с растворимостью природного комбретастатина А-4, им присуще ограничивающее их применение свойство, заключающееся в том, что регенерация комбретастатина А-4 зависит от эндогенной аминопептитазы в крови больного, которому введено пролекарство.
Свободная кислота фосфата комбретастатина А-4 ("свободная кислота СА4Р", которая имеет следующую структуру:
существует только в виде масла. Свободная кислота СА4Р по своей природе очень мало растворима (по определению Фармакопеи США) в воде при 25°С, причем растворимость в воде повышается с увеличением рН. Кислота имеет две кислотные группы со значениями рКа 1,2 и 6,2, которые способны образовывать соли. Поскольку на практике существуют проблемы при работе со свободной кислотой СА4Р из-за ее физического состояния, желательно получение кристаллической, стабильной солевой формы этого соединения.
Попытки получить производные комбретастатина А-4 включали получение солевых производных фосфата комбретастатина А-4 (солевые производные "СА4Р"). Конкретные примеры таких солей представлены в патенте США 5561122. Хотя такие пролекарственные соли обладают более высокой растворимостью, чем природный комбретастатин А-4, для них также характерны присущие им недостатки, такие как гигроскопичность.
Гигроскопичность является одним из весьма важных критериев выбора соли. См. K. Morris et al, "An Integrated Approach to the Selection of Optimal Salt Form for a New Drug Candidate", Int. J. Pharm., 105, 209-217 (1994). Степень гигроскопичности для многих лекарственных веществ оказывает сильное влияние на работу с ними и их стабильность в период срока годности лекарственного продукта.
Таким образом, существует необходимость в новых и полезных пролекарственных солях комбретастатина А-4 с полезными физико-химическими свойствами, которые повышают растворимость и предпочтительно эффективность комбретастатина А-4 при лечении широкого спектра новообразований.
Также необходимы новые и полезные пролекарственные соли комбретастатина А-4, которые легко регенерируют природный комбретастатин А-4 in vivo и не продуцируют нежелательных или потенциально вредных побочных продуктов при регенерации.
Цитирование какой-либо ссылки в данном документе не следует толковать как признание, что такая ссылка является пригодной в качестве уровня техники для данной заявки.
Сущность изобретения
В соответствии с настоящим изобретением предложены новые и полезные пролекарственные моно- и ди-соли органических аминов, моно- и ди-соли аминокислот и моно- и ди-соли эфиров аминокислот фосфата комбретастатина А-4, и эти соли имеют более высокую растворимость, чем природный комбретастатин А-4 и легко регенерируют комбретастатин А-4 in vivo. Настоящее изобретение также относится к соединениям, которые значительно менее гигроскопичны, чем известные до сих пор пролекарственные соли комбретастатина А-4 (например, они не меняют в значительной степени физическую форму в условиях обычной температуры и влажности). С этими соединениями легче работать, они более стабильны и могут образовывать растворы при значениях рН, которые сводят до минимума или исключают боль на участке инъекции. Таким образом, соединения по настоящему изобретению обеспечивают существенные преимущества при фармацевтическом применении.
Более конкретно, настоящее изобретение относится к соединению, имеющему общую структуру формулы I:
где один из заместителей -OR1 или -OR2 представляет собой -О-QH+, а другой представляет собой гидроксил или -О-QH+; и
Q представляет собой
(А) органический амин, содержащий, по меньшей мере, один атом азота, который вместе с протоном образует четвертичный аммониевый катион QH+;
(В) аминокислоту, содержащую, по меньшей мере, два атома азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+; или
(С) аминокислоту, содержащую один или несколько атомов азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+ и где, кроме того, все карбоксильные группы аминокислоты находятся в форме эфиров.
По всему описанию, когда оба заместителя -OR1 и -OR2 представляют собой -О-QH+, Q предпочтительно одинаковый в обеих группах -OR1 и -OR2.
Когда Q имеет определение (А), предпочтительный органический амин, в данном случае представляет собой трометамин (то есть, трис(гидроксиметил)аминометан, который далее обозначают сокращением ТРИС (ТРИС)).
Трометаминные соли формулы I иллюстрируются следующими формулами Ia и Ib, которые представляют моно-трометаминную и ди-трометаминную соли формулы I, соответственно:
Моно-трометаминная соль формулы Ia предпочтительна.
Когда Q имеет определение (В), любая аминокислота, содержащая, по меньшей мере, два атома азота, может использоваться в данном случае. Любые атомы азота аминокислоты могут образовывать четвертичный аммониевый катион формулы I, например любой атом азота боковой цепи аминокислоты или атом азота α-аминогруппы. Аминокислоты, которые могут использоваться в данном случае, представляют собой, но, конечно, не ограничиваются только ими, орнитин, гистидин, лизин, аргинин, триптофан и др.
Когда Q имеет определение (В), предпочтительной аминокислотой в данном случае является гистидин. Например, или атомы азота имидазольной группы боковой цепи гистидина или, с другой стороны, атом азота α-аминогруппы гистидина могут образовывать четвертичный аммониевый катион формулы I. Как можно легко увидеть, вследствие ароматической природы имидазольной группы любой атом азота имидазольной группы боковой цепи гистидина может образовывать структуру формулы (I). Предпочтительные моно-гистидиновые структуры формулы I иллюстрируются следующими формулами Ic или Id:
Когда Q имеет определение (С), любая аминокислота может использоваться в данном случае, например, такая как глицин, но этм не ограничивается. Предпочтительными эфирами являются алкиловые эфиры, такие как метиловый или этиловый эфиры.
Кроме того, настоящее изобретение относится к фармацевтической композиции, содержащей:
(а) соединения, имеющие общую структуру формулы I:
где:
один из заместителей -OR1 или -OR2 представляет собой -О-QH+, а другой представляет собой гидроксил или -О-QH+; и
Q представляет собой
(А) органический амин, содержащий, по меньшей мере, один атом азота, который вместе с протоном образует четвертичный аммониевый катион QH+;
(В) аминокислоту, содержащую, по меньшей мере, два атома азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+; или
(С) аминокислоту, содержащую один или несколько атомов азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+ и где, кроме того, все карбоксильные группы аминокислоты находятся в виде эфиров; и
(b) фармацевтически приемлемый носитель.
Конкретные примеры соединений по настоящему изобретению, используемых в таких фармацевтических композициях, описаны выше. Кроме того, любой фармацевтически приемлемый носитель находит применение в фармацевтической композиции по настоящему изобретению. Конкретные примеры описаны ниже. Конкретный вариант фармацевтической композиции по настоящему изобретению включает соединение по настоящему изобретению, в котором трометамин представляет собой органический амин и которое предпочтительно представляет собой трометаминную соль, имеющую структуру формулы Ia или Ib, наиболее предпочтительно Ia:
Другой конкретный вариант фармацевтической композиции по настоящему изобретению включает соединение по настоящему изобретению, в котором гистидин является аминокислотой и которое предпочтительно является моно-гистидиновой солью, имеющей структуру формулы Ic или Id:
Конечно, такая фармацевтическая композиция также должна включать фармацевтически приемлемый носитель.
Кроме того, настоящее изобретение также охватывает композиции, содержащие соль по настоящему изобретению. В частности, композиция по настоящему изобретению может быть получена путем смешивания соединений, включающих:
(а) свободную кислоту СА4Р, имеющую структуру:
(b) соединение Q, где Q представляет собой
(А) органический амин, содержащий, по меньшей мере, один атом азота, который способен вместе с протоном образовывать четвертичный аммониевый катион QH+;
(В) аминокислоту, содержащую, по меньшей мере, два атома азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+; или
(С) аминокислоту, содержащую один или несколько атомов азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+ и где, кроме того, все карбоксильные группы аминокислоты находятся в форме эфиров.
Необязательно композиция по настоящему изобретению также может включать фармацевтически приемлемый носитель.
Кроме того, когда Q имеет определение (А), любой органический амин, который определен в данном описании, может использоваться в композиции по настоящему изобретению. Конкретными примерами являются, но не ограничиваются только ими, трометамин, диэтаноламин, глюкамин, N-метилглюкамин, этилендиамин и 2-(4-имидазолил)этиламин. Когда Q имеет определение (В), любая аминокислота, содержащая, по меньшей мере, два атома азота, может использоваться в композиции по настоящему изобретению. Конкретными примерами являются орнитин, гистидин, лизин, аргинин, триптофан и др. Когда Q имеет определение (С), любой эфир аминокислоты, который определен в данном описании, может использоваться в композиции по настоящему изобретению. Конкретным примером является глицин.
В другом варианте настоящее изобретение относится к способу модулирования роста опухоли или метастаза у животного, который включает введение ему эффективного количества соединения, имеющего общую структуру:
где:
один из заместителей -OR1 или -OR2 представляет собой
-О-QH+, а другой представляет собой гидроксил или -О-QH+; и
Q представляет собой
(А) органический амин, содержащий, по меньшей мере, один атом азота, который вместе с протоном образует четвертичный аммониевый катион QH+;
(В) аминокислоту, содержащую, по меньшей мере, два атома азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+; или
(С) аминокислоту, содержащую один или несколько атомов азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+ и где, кроме того, все карбоксильные группы аминокислоты находятся в виде эфиров.
В конкретном варианте настоящее изобретение относится к способу модулирования роста опухоли или метастаза у животного, который включает введение ему эффективного количества соединения, в котором трометамин представляет собой органический амин и которое предпочтительно является трометаминной солью, имеющей структуру формулы Ia или Ib, наиболее предпочтительно, Ia:
В другом конкретном варианте настоящее изобретение относится к способу модулирования роста опухоли или метастаза у животного, который включает введение ему эффективного количества соединения, в котором гистидин представляет собой аминокислоту и которое предпочтительно является моно-гистидиновой солью, имеющей структуру формулы Ic или Id:
Таким образом, настоящее изобретение относится к новым и полезным пролекарственным моно- и ди-солям органических аминов, моно- и ди-солям аминокислот и моно- и ди-солям эфиров аминокислот фосфата комбретастатина А4, и эти соли более растворимы в водных растворах, чем природный комбретастатин А-4. Таким образом, эффективность этого лекарства может быть повышена.
Настоящее изобретение также относится к пролекарственным моно- и ди-солям органических аминов, моно- и ди-солям аминокислот и моно- и ди-соли эфиров аминокислот фосфата комбретастатина А4, эти соли легко регенерируют комбретастатин А4 in vivo, и эти соли при диссоциации высвобождают органический амин, аминокислоту или эфир аминокислоты в виде физиологически переносимого побочного продукта.
В наиболее предпочтительном варианте настоящее изобретение относится к новой кристаллической (1:1) пролекарственной трометаминовой (ТРИС) соли антиваскулярного противоопухолевого агента фосфата комбретастатина А4, имеющей структуру формулы Ia. Это соединение представляет собой пролекарственную соль фосфата сложного эфира, в котором фосфатный фрагмент подвергается дефосфорилированию в физиологических условиях, образуя активный лекарственный остаток комбретастатин А-4 (как упоминается ниже, олефиновая группа, соединяющая мостиком фенильные остатки ядра комбретастатина А4, находится в цисконфигурации; олефиновая группа предпочтительной моно-ТРИС соли фосфата комбретастатина А4 также находится в цисконфигурации). ТРИС-соль 1:1 (моно) СА4Р обладает хорошими свойствами в твердом состоянии и неожиданно практически негигроскопична. Эти и другие предпочтительные свойства делают ТРИС-соль СА4Р предпочтительным соединением для фармацевтического дозированного лекарственного препарата.
Краткое описание чертежей
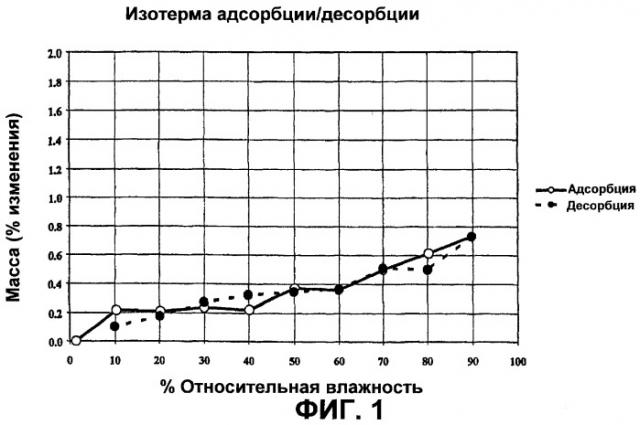
На Фиг.1 представлен график сорбции/десорбции влаги моно-ТРИС соли СА4Р (полученной в примере 1) при 25°С. Данные получены с использованием рычажных весов со шкалой, проградуированной в процентах влажности, VTI Model MB-300W, с пределами относительной влажности от 10 до 90% при интервале увеличения 10%. Максимальное время установления равновесия при каждом значении влажности установлено на 4 часа.
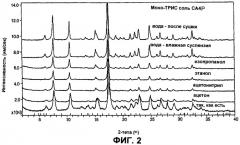
На Фиг.2 представлены спектры порошковой рентгенографии образцов моно-ТРИС соли СА4Р (полученной в примере 1), которая находится в виде суспензии в различных растворителях (вода, изопропанол, этанол, ацетонитрил и ацетон) вначале при температуре от 70 до 75°С в течение 5-10 мин, а затем при комнатной температуре в течение ночи. Рентгеновские дифрактограммы записаны с использованием рентгеновского дифрактометра Rigaku Model Miniflex с источником Cu-Kα при скорости сканирования 1° в минуту от 2° до 40° 2θ.
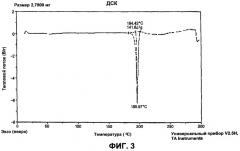
На Фиг.3 представлена термограмма дифференциальной сканирующей калориметрии (ДСК) (прибор Model DSC 2910, TA) моно-ТРИС соли СА4Р (полученной в примере 1), полученная в токе азота при скорости нагрева 10 градусов в минуту.
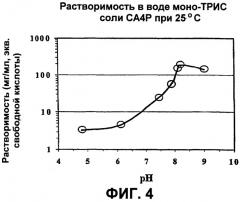
На Фиг.4 представлен график рН-растворимость моно-ТРИС соли СА4Р (полученной в примере 1) при 25°С. Значение рН устанавливают с помощью гидроксида натрия.
На Фиг.5 представлена термограмма дифференциальной сканирующей калориметрии (ДСК) моно-L-гистидиновой соли СА4Р (полученной в примере 3) (образец 2,0900 мг).
На Фиг.6 представлена термограмма дифференциальной сканирующей калориметрии (ДСК) моно-L-гистидиновой соли СА4Р (полученной в примере 3).
На Фиг.7 представлена термограмма дифференциальной сканирующей калориметрии (ДСК) моно-L-гистидиновой соли СА4Р (полученной в примере 3).
На Фиг.8 представлены спектры порошковой рентгенографии моно-L-гистидиновой соли СА4Р (полученной в примере 3).
На Фиг.9 представлены спектры порошковой рентгенографии моно-L-гистидиновой соли СА4Р (полученной в примере 3).
На Фиг.10 представлена термограмма дифференциальной сканирующей калориметрии (ДСК) безводной моно-L-гистидиновой соли СА4Р (полученной в примере 3).
На Фиг.11 представлены спектры порошковой рентгенографии безводной моно-L-гистидиновой соли СА4Р (полученной в примере 3).
На Фиг.12 представлена термограмма дифференциальной сканирующей калориметрии (ДСК) моно-соли метилового эфира глицина и СА4Р (полученной в примере 4).
На Фиг.13 представлены спектры порошковой рентгенографии моно-соли метилового эфира глицина и СА4Р (полученной в примере 4).
Подробное описание изобретения
Настоящее изобретение основано на удивительном и неожиданном открытии, что могут быть получены пролекарственные моно- и ди-соли органических аминов, моно- и ди-соли аминокислот и моно- и ди-соли эфиров аминокислот фосфата комбретастатина А-4, которые имеют повышенную растворимость in vivo по сравнению с растворимостью природного комбретастатина А-4, легко регенерируют комбретастатин А-4 в физиологических условиях, и при регенерации выделяют физиологически переносимые органические амины или физиологически переносимые аминокислоты или эфиры аминокислот, которые легко метаболизируют in vivo.
Если говорить более широко, то настоящее изобретение относится к соединению, имеющему общую структуру:
где:
один из заместителей -OR1 или -OR2 представляет собой -О-QH+, а другой представляет собой гидроксил или -О-QH+; и
Q представляет собой
(А) органический амин, содержащий, по меньшей мере, один атом азота, который вместе с протоном образует четвертичный аммониевый катион QH+;
(В) аминокислоту, содержащую, по меньшей мере, два атома азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+; или
(С) аминокислоту, содержащую один или несколько атомов азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+ и где, кроме того, все карбоксильные группы аминокислоты находятся в форме эфиров.
Все изомеры рассматриваемых соединений (например, изомеры, которые могут существовать из-за наличия асимметричных атомов углерода, например, на различных заместителях), в том числе энантиомерные формы и диастереомерные формы, входят в объем по настоящему изобретению. Отдельные стереоизомеры соединений изобретения могут, например, по существу не содержать другие изомеры (например, чистые или по существу чистые оптические изомеры, имеющие удельную активность) или могут быть смешаны, например, в виде рацематов или со всеми другими или другими выбранными стереоизомерами. Хиральные центры соединений по настоящему изобретению могут иметь S или R конфигурацию в соответствии с рекомендациями IUPAC 1974. Рацемические формы могут быть разделены физическими способами, такими как, например, дробная кристаллизация, разделение или кристаллизация диастереомерных производных, или путем разделения с помощью хиральной колоночной хроматографии. Индивидуальные оптические изомеры могут быть получены из рацематов любым подходящим способом. Олефиновая группа, связывающая мостиком фенильные остатки ядра комбретастатина А-4, находится в цисконфигурации, которая является предпочтительной конфигурацией соединений по настоящему изобретению. Использование определения "комбретастатина А-4" или "СА4" в качестве названия или части названия соединения в данном случае означает соединение в этой цисконфигурации. Также подразумеваются сольваты соединения формулы I, такие как гидраты.
По всему описанию группы и заместители могут быть выбраны так, чтобы были получены стабильные остатки и соединения.
Варианты осуществления изобретения, представленные в документе как примеры или в качестве предпочтительных вариантов, предназначены только для иллюстрации изобретения и не ограничивают его.
В другом варианте осуществления изобретения настоящее изобретение относится к фармацевтической композиции, содержащей соединение по настоящему изобретению и фармацевтически приемлемый носитель. Конечно, соединения по настоящему изобретению могут быть использованы в любой форме, такой как твердая форма или раствор (особенно водный раствор), которые также описаны ниже. Например, соединение по настоящему изобретению может быть получено и использовано в лиофилизированной форме отдельно или с подходящими вспомогательными веществами.
В еще одном варианте осуществления настоящее изобретение относится к способу модулирования роста опухоли или метастаза у животного, который включает введение ему эффективного количества соединения, имеющего общую структуру формулы I:
где:
один из заместителей -OR1 или -OR2 представляет собой
-О-QH+, а другой представляет собой гидроксил или -О-QH+; и
Q представляет собой
(А) органический амин, содержащий, по меньшей мере, один атом азота, который вместе с протоном образует четвертичный аммониевый катион QH+;
(В) аминокислоту, содержащую, по меньшей мере, два атома азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+; или
(С) аминокислоту, содержащую один или несколько атомов азота, где один из атомов азота вместе с протоном образует четвертичный аммониевый катион QH+ и где, кроме того, все карбоксильные группы аминокислоты находятся в форме эфиров.
Конечно, соединение по настоящему изобретению может быть введено отдельно или в фармацевтической композиции.
Термины и выражения, используемые в документе, определены ниже и имеют указанные значения, если не оговорено особо.
В описании термины "модулируют", "модулирование" или "модуляция" относятся к изменению скорости, при которой происходит конкретный процесс, к ингибированию конкретного процесса, к обращению конкретного процесса в другую сторону и/или предупреждению начала определенного процесса. Таким образом, когда конкретный процесс включает, например, рост опухоли или метастаз, "модуляция" процесса заключается в снижении скорости, при которой развивается опухоль и/или имеет место метастаз, в ингибировании роста опухоли и/или метастаза, в обращении в обратную сторону роста опухоли и/или метастаза (включая уменьшение и/или исчезновение) и/или предупреждении роста опухоли и/или метастаза, особенно у субъекта, который предрасположен к этому процессу.
Используемое в описании выражение "эффективное количество" или "эффективное для этого количество" соединения, введенного животному, означает количество, достаточное для модулирования роста опухоли или метастаза у животного. Специалист в данной области может легко определить, например, с помощью обычных методик, эффективное количество соединения по настоящему изобретению, которое должно быть введено животному. Примеры дозированных количеств для взрослого человека составляют приблизительно от 0,05 до 1000 мг/кг веса тела активного соединения в день, которые могут быть введены в виде единичной дозы (например, в виде ударной разовой дозы или в виде вливания в течение некоторого времени до предельно допустимой дозы или ниже) или в форме отдельных поделенных доз (например, путем последовательного введения доз ниже предельно допустимой дозы), например от 1 до 4 раз в день. Следует понимать, что конкретный уровень доз и частота введения дозы любому конкретному субъекту может меняться и зависит от ряда факторов, в том числе от активности конкретного используемого соединения, массы тела, общего состояния здоровья, пола и режима питания субъекта, способа и времени введения, скорости выделения, концентрации лекарства и серьезности конкретного состояния.
Как используется в данном описании, понятие "животное" предпочтительно включает таких субъектов, как домашние животные и, наиболее предпочтительно, людей.
Используемый в описании термин "пролекарство" относится к предшественнику соединения, который будет подвергаться метаболической активации in vivo с образованием активного лекарственного соединения. Таким образом, например, соединение по изобретению, введенное субъекту, будет подвергаться метаболической активации, и регенерировать комбретастатин А-4 вследствие диссоциации соединения по настоящему изобретению, например, под действием эндогенных неспецифических фосфатаз в плазме.
Используемое в описании понятие "органический амин" относится к органическому (то есть содержащему углерод) соединению, содержащему, по меньшей мере, одну первичную (то есть -NH2), вторичную (то есть -NH-) или третичную (то есть ) аминогруппу, способную образовывать фосфатную соль соединения формулы I по настоящему изобретению. Когда присутствует более одной первичной, вторичной и/или третичной аминогруппы в указанном органическом амине, то любая такая группа, обладающая указанным свойством, может образовывать четвертичную аммониевую группу QH+ формулы I. Настоящее определение "органический амин" не охватывает ни аминокислотные соединения (см. предыдущую заявку под названием "Combretastatin A-4 Phospate Mono- and Di-Amino Acid Salt Prodrugs", которая была подана Venit в виде заявки США с регистрационным номером №60/232568 14 сентября 2000, включенная в описание в качестве ссылки), ни некоторые соединения, описанные в публикации WO 99/35150 (глюкозамин, пиперазин, пиперидин, 6'-метоксицинхонан-9-ол, цинхонан-9-ол, пиразол, пиридин, тетрациклин, имидазол, аденозин, верапамил, морфолин), которые введены в описание в качестве ссылки. Используемый органический амин предпочтительно представляет собой физиологически переносимое соединение, выбранное из следующих групп:
(а) органические амины, имеющие значение рКа, больше или равное 7, более предпочтительно значение рКа, больше или равное 8;
(b) органические амины, где атом азота, образующий четвертичный аммониевый катион QH+ в формуле I, связан с необязательно замещенной алифатической группой или с необязательно замещенной гетероциклической неароматической группой (или двумя или тремя такими необязательно замещенными алифатическими и/или гетероциклическими неароматическими группами в случае вторичных или третичных аминов, соответственно). "Алифатическая группа" представляет собой линейный или разветвленный, насыщенный или ненасыщенный углеводород (например, алкан, алкен или алкин), содержащий от 1 до 20, предпочтительно от 1 до 12, более предпочтительно от 1 до 6 атомов углерода в цепи. "Гетероциклическая неароматическая группа" представляет собой насыщенное или частично ненасыщенное кольцо, содержащее атом азота, образующий четвертичный аммониевый катион QH+ в формуле I, а также необязательно другие гетероатомы в кольце, такие как О, S или дополнительные атомы N. "Необязательные заместители" предпочтительно представляют собой один или несколько заместителей, присутствующих в органическом амине, которые при использовании в формуле I по настоящему изобретению, приводят к фосфатным солям формулы I, которые являются кристаллическими и по существу негигроскопичными или негигроскопичными. Предпочтительными "необязательными заместителями" являются гидроксильная группа, аминогруппа (то есть -NH2) или алкокси-группа (то есть -О-алкил), наиболее предпочтительны одна или несколько гидроксильных групп; и/или
(с) органические амины, где атом азота, образующий четвертичный аммониевый катион QH+ в формуле I, представляет собой первичный амин, связанный с необязательно замещенной алифатической группой, или вторичный амин, связанный с двумя необязательно замещенными алифатическими группами, где предпочтительные необязательные заместители представляют собой одну или несколько гидроксильных или аминогрупп, наиболее предпочтительно, гидроксильные группы.
Конечно, любой данный органический амин, выбранный в качестве предпочтительного амина для использования в настоящем изобретении, может обладать свойствами двух или более групп (а)-(с), описанных выше (например, иметь значение рКа, больше или равное 7, и быть необязательно замещенным алифатическим амином, описанным в пункте (с)).
Любой органический амин, определенный таким образом, подходит для применения в соединениях формулы I по настоящему изобретению, а также в рассматриваемых фармацевтических композициях и способах. Понятие "органический амин" включает соединения в солевой форме с другими кислотными и/или основными фрагментами (где, например, одна аминогруппа образует фосфатную соль формулы I, а другая аминогруппа образует соль с кислотным остатком). Следовательно, остальная часть органического амина, входящая в соединение по настоящему изобретению, также может содержать солевые остатки.
Примерами органических аминов являются, но не ограничиваются только ими, трометамин, диэтаноламин, глюкамин, N-метилглюкамин, этилендиамин и 2-(4-имидазолил)этиламин.
"Моно-соль органического амина" фосфата комбретастатина А-4 формулы I содержит одну органическую аминогруппу Q как часть заместителей R1 или R2, как это определено выше; "ди-соль органического амина" фосфата комбретастатина А-4 формулы I содержит две органические аминогруппы Q, одну как часть заместителя R1 и одну как часть заместителя R2, как это определено выше. Предпочтительными являются "моно-соли органических аминов" формулы I. Соответствующие определения применяются к "моно-соли аминокислоты", "ди-соли аминоксилоты", "моно-соли эфира аминокислоты" и "ди-соли эфира аминокислоты".
Любая подходящая аминокислота находит применение в данном случае, включая множество природных и неприродных аминокислот, находящих применение в соединении по настоящему изобретению. Конкретными примерами являются, но, конечно, не ограничиваются только ими, орнитин, гистидин, лизин, аргинин и триптофан.
Как используется в данном описании, определение "аминокислота" относится к соединению, содержащему основную аминогруппу (NH2) и кислотную карбоксильную группу (СООН), в том числе такие соединения в форме цвиттер-иона (где амино- и карбоксильные группы вместе образуют цвиттер-ион или внутреннюю соль) или в солевой форме с другими кислотными и/или основными остатками (где, например, аминокислота содержит карбоксильную группу, помимо α-СООН-группы, и первая находится в солевой форме со щелочным металлом). Таким образом, остальная часть аминокислоты, находящаяся в соединении по настоящему изобретению, также может содержать солевые фрагменты. Определение включает неприродные, а также природные аминокислоты, такие как α-аминокислоты (в особенности L-аминокислоты), многие из которых являются строительными блоками белков. Определение "природные аминокислоты" относится к 20 аминокислотам, которые являются типичными для всех белков, то есть, глицин, аланин, валин, лейцин, изолейцин, пролин, серин, треонин, цистеин, метионин, аспарагин, глутамин, фенилаланин, тирозин, триптофан, лизин, аргинин, гистидин, аспартат и глютамат. Определение "неприродные аминокислоты" относится к аминокислотам, которые не являются обычными в белках, такие как 4-гидроксипролин, 5-гидроксилизин, N-метиллизин, γ-карбоксиглутамат, селеноцистеин, орнитин и цитруллин. Аминокислоты, содержащие два или несколько атомов азота, подходят для использования в соединениях формулы I по настоящему изобретению, когда Q имеет определение (В), а также в рассматриваемых фармацевтических композициях и способах.
Используемое в данном описании в связи с аминокислотой выражение "боковая цепь" означает такой остаток аминокислоты, который является разным для каждой аминокислоты, и особенно к группе, связанной с атомом углерода, соединяющим -NH2 и -СООН группы аминокислоты.
Используемое в описании определение "по существу негигроскопично", в отношении соединения, предпочтительно означает менее чем 1%-ное увеличение массы воды на массу соединения (более предпочтительно менее чем 0,5%-ное увеличение массы воды на массу соединения), измеренное при следующих условиях: температура приблизительно 25°С, относительная влажность от 20 до 95% и при равновесном состоянии (например, измеренная тогда, когда скорости сорбции и десорбции влаги выравниваются) относительно измерений, проведенных при 25°С и при относительной влажности 0%. Используемое в данном описании определение "негигроскопично", в отно