Способ получения ветеринарного альбумина
Иллюстрации
Показать всеИзобретение относится к ветеринарии и может быть использовано в научно-исследовательских биохимических лабораториях при получении альбумина по промышленной технологии. Способ включает четырехстадийное осаждение спиртовым раствором белковых фракций плазмы крови, при котором перед осаждением осуществляют определение связующей способности альбумина ССА плазмы крови флуоресцентным методом с использованием зондов-катионов, где за величину ССА принимают отношение ССА=ЭКА/ОКА·100%, где ЭКА - эффективная концентрация альбумина, ОКА - общая концентрация альбумина, после получения альбуминовой фракции снова проводят определение ССА плазмы крови флуоресцентным методом, полученную альбуминовую фракцию очищают на углеводных сорбентах, вновь осуществляют определение ССА плазмы крови флуоресцентным методом, очищенный альбумин стабилизируют хлоридом натрия до конечной концентрации 10-20%, подвергают осветляющей фильтрации, пастеризуют и окончательно стабилизируют. Технический результат: изобретение направлено на повышение детоксикационных свойств ветеринарного альбумина и увеличение его сорбционной емкости при обработке на углеводных сорбентах, кроме того снижается энерго- и трудоемкость процесса. 2 ил.
Реферат
Изобретение относится к ветеринарии и может быть использовано в научно-исследовательских биохимических лабораториях при получении альбумина по промышленной технологии.
Известен способ получения альбумина-глюкозата после извлечения из сыворотки крови здоровых животных гамма-глобулинов и удаления балластных фракций с помощью многостадийного осаждения этиловым спиртом при отрицательных температурах (Фром А.А., Скобелев Л.И., Русанов В.М., Никитенко А.А. "Белки плазмы и их фракционирование в производстве препаратов крови", М., Медицина 1974 г., с.251).
Недостатком данного способа является многостадийность и технологическая сложность процесса получения препарата, низкая стерильность и недостаточная апирогенность продукта, наличие специальных установок, обеспечивающих низкие температуры, дороговизна конечного продукта.
Технический результат заключается в повышении детоксикационных свойств ветеринарного альбумина и увеличении его сорбционной емкости при обработке на углеводных сорбентах. Кроме того, снижается энерго- и трудоемкость процесса за счет сокращения ряда стадий и времени получения препарата.
Сущность изобретения заключается в том, что в способе получения ветеринарного альбумина, включающем четырехстадийное растворение-осаждение спиртовым раствором белковых фракций плазмы крови, определяют связывающую способность альбумина плазмы крови флуоресцентным методом с использованием зондов-катионов с последующей обработкой альбумина в апирогенной среде при рН 6,5-7,0, температуре -5-0°С на углеродных сорбентах. Полученный раствор альбумина стабилизируют хлоридом натрия с последующей фильтрацией и пастеризацией.
Определение занятости активных центров связывания на молекуле альбумина производят на основе определения связывающей способности альбумина (ССА) по отношению к эффективной концентрации альбумина (ЭКА) к общей концентрации альбумина (ОКА) флуоресцентным методом, который основан на специфическом взаимодействии флуоресцентных органических соединений (зонд-катион К-35) с альбумином. Плазма крови, содержащая альбумин, у которого ССА=90-95%, является наиболее пригодной для приготовления альбумина с высокими детоксикацонными свойствами.
Способ осуществляют следующим образом.
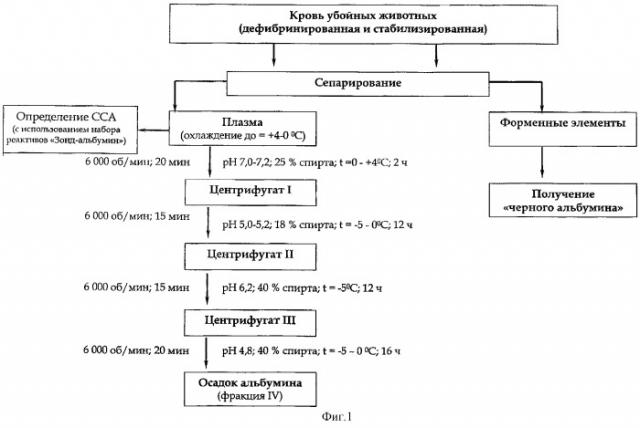
I. Фракционирование белков плазмы проводят спиртовым методом путем четырехэтапного отделения каждой фракции и получения альбуминовой фракции (фиг.1). Для этого 20 л стабилизированной и дефибринированной крови убойных животных помещают в сепаратор для разделения ее на плазму и форменные элементы. Полученную плазму охлаждают в холодильных камерах до температуры 0-4°С, форменные элементы можно использовать для получения "черного альбумина". Затем флуоресцентным методом определяют ЭКА и ОКА. К 0,025 мл плазмы добавляют 5 мл рабочего раствора реактива №1 (приготовлен путем разведения содержимого ампулы с реактивом №1 в 100 мл дистиллированной воды). Для определения показателя ЭКА к 2,0 мл полученного раствора добавляют 0,025 мл реактива №2. Перемешивают и измеряют интенсивность флуоресценции на флуориметре при λвозб=420±20 нм и λисп=515±20 нм. Для определения ОКА в исходный раствор вносят 0,025 мл реактива №3. Затем раствор вновь перемешивают и замеряют интенсивность флуоресценции на флуориметре при λвозб=420±20 нм и λисп=15±20 нм. За величину связывающей способности альбумина принимают отношение ЭКА/ОКА·100%.
После охлаждения к плазме прибавляют охлажденный 96% этиловый спирт до конечной концентрации 25% (рН 7,0-7,2). Смесь перемешивают и оставляют на 2 часа. На данном этапе в осадок выпадает фракция, содержащая в основном фибриноген, β- и γ-глобулины, протромбин, плазминоген, липоидные вещества. Раствор центрифугируют в рефрижераторной центрифуге при 6000 об/мин в течение 20 минут. Осадок отбрасывают.
Супернатант охлаждают до температуры (-5)-0°С. Доводят рН полученного раствора до значения, равного 5,8. Затем из расчета 389 мл центрифугата I доводят апирогенной дистилированной водой до 1 литра, охлажденной до минус 5°С. Добавлением ацетатного буфера доводят рН до 5,0-5,2 и оставляют смесь на 12 часов для более полного осаждения. Отделение «созревшего» осадка производится центрифугированием при 6000 об/мин в течение 15 минут и температуре (-5)-0°С. Осадок не используется.
К 1 л центрифугата II добавляют смесь, содержащую 1,14 г бикарбоната натрия, 7,9 мл 4 М раствора уксуснокислого натрия и воды до 77 мл. Доводят рН до 6,2. После коррекции рН к смеси добавляют холодный этиловый спирт до конечной концентрации 40%. Смесь оставляют для созревания осадка на 12 часов, затем отделяют осадок центрифугированием при 6000 об/мин в течение 15 минут и температуре -5°С. Осадок содержащий α- и β-глобулины отбрасывают.
Надосадочную жидкость (центрифугат III) фильтруют, рН снижают до 4,8, добавляя смесь, содержащую 10 н. раствор уксусной кислоты, 4 н. раствор ацетата натрия, 96% этилового спирта и воды в соотношениях 1:0,5:2,1:1.4. Раствор перемешивают и оставляют на 16 часов при температуре -5°С. Осадок отделяют центрифугированием при 6000 об/мин в течение 20 минут при -5°С. Надосадочная жидкость не используется. Осадок взвешивают, растворяют в минимальном количестве апирогенной воды при рН 6,5-7,0.
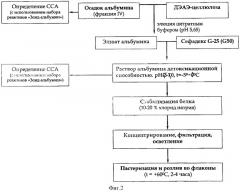
Затем флуоресцентным методом определяют ЭКА и ОКА (фиг.2). К 0,025 мл плазмы добавляют 5 мл рабочего раствора реактива №1 (приготовлен путем разведения содержимого ампулы с реактивом №1 в 100 мл дистиллированной воды). Для определения показателя ЭКА к 2,0 мл полученного раствора добавляют 0,025 мл реактива №2.
Затем перемешивают и измеряют интенсивность флуоресценции на флуориметре при λвозб=420±20 нм и λисп=515±20 нм. Для определения ОКА в исходный раствор вносят 0,025 мл реактива №3. Затем вновь перемешивают и измеряют интенсивность флуоресценции на флуориметре при λвозб=420±20 нм и λисп=515+20 нм.
За величину связывающей способности альбумина принимают отношение ЭКА/ОКА·100%.
II. Очистка альбуминовой фракции на ДЭАЭ-целлюлозе (диэтиламиноэтилцеллюлоза) (фиг.2). Для удаления средне- и высокомолекулярных соединений, адсорбированных на молекуле альбумина, производят очистку последнего на ДЭАЭ-целлюлозе (диэтиламиноэтилцеллюлоза). Для этого полученный на предыдущем этапе раствор альбумина вносят в колонку с ДЭАЭ-целлюлозой (диэтиламиноэтилцеллюлоза). Элюцию альбумина производят цитратным буфером (рН 5,65).
III. Очистка альбумина от низкомолекулярных лигандов на сефадексах G-25 (G-50). Элюат полученный на этапе II наносят на колонки сефадекса G-25 (G-50). Использование грубого или среднего сефадекса позволяет произвести удаление низкомолекулярных соединений (лигандов), обессоливание и концентрирование белка.
По окончании этапа очистки альбумина на сефадексах проводят заключительный отбор для определения ССА. Флуоресцентным методом определяют ЭКА и ОКА. К 0,025 мл плазмы крови добавляют 5 мл рабочего раствора реактива №1 (приготовлен путем разведения содержимого ампулы с реактивом №1 в дистиллированной воде). Для определения показателя ЭКА к 2,0 мл полученного раствора добавляют 0,025 мл реактива №2. Перемешивают и измеряют интенсивность флуоресценции на флуориметре при λвозб=420±20 нм и λисп=515±20 нм. Для определения ОКА в исходный раствор вносят 0,025 мл реактива №3. Затем раствор вновь перемешивают и измеряют интенсивность флуоресценции на флуориметре при λ=420±20 нм им λ=515±20 нм. За величину связывающей способности альбумина принимают отношение ЭКА/ОКА·100%.
IV. Полученный сывороточный альбумин с повышенной сорбционной (детоксикационной) способностью стабилизируют путем добавления в раствор хлорида натрия до конечной концентрации 10-20%, затем подвергают осветляющей фильтрации. На данном этапе проводят конечную коррекцию рН раствора (6,5-7,2).
V. Готовый раствор альбумина с повышенной детоксикационной способностью разливают во флаконы в стерильных условиях в ламинарном боксе с помощью фильтра с порами 0,45±0,2 мкм. Флаконы укупоривают резиновыми пробками и обкатывают аллюминиевыми колпачками. Флаконы пастеризуют в термостатах при температуре 60°С в течение 2-4 часов. После пастеризации препарат выдерживают при температуре 37°С в течение 2 недель для стабилизации белка.
Способ позволяет получить альбумин с высокими связывающими способностями, повышающими его функциональную загруженность. В процессе получения альбумина снижается трудоемкость процесса за счет сокращения ряда стадий (стадия осаждения антигемофильного фактора), сокращается время получения препарата. Полученный после очистки на сорбентах альбумин может быть использован в качестве лечебного препарата для внутривенного или париетального введения молодняку сельскохозяйственных животных.
Способ получения ветеринарного альбумина, включающий осаждение спиртовым раствором белковых фракций плазмы крови с получением альбуминовой фракции, отличающийся тем, проводят четырехстадийное осаждение спиртовым раствором белковых фракций плазмы крови, перед осаждением осуществляют определение связующей способности альбумина ССА плазмы крови флуоресцентным методом с использованием зондов-катионов, где за величину связующей способности альбумина ССА принимают отношение ССА=ЭКА/ОКА·100%, где ЭКА - эффективная концентрация альбумина, ОКА - общая концентрация альбумина, после получения альбуминовой фракции снова проводят определение связующей способности альбумина ССА плазмы крови флуоресцентным методом, полученную альбуминовую фракцию очищают на углеводных сорбентах, вновь осуществляют определение связующей способности альбумина ССА плазмы крови флуоресцентным методом, очищенный альбумин стабилизируют хлоридом натрия до конечной концентрации 10-20%, подвергают осветляющей фильтрации, пастеризуют при температуре 60°С в течение 2-4 ч и окончательно стабилизируют две недели при температуре 37°С.