Иммуномодулирующее средство в форме спрея
Иллюстрации
Показать всеИзобретение относится к области химико-фармацевтической промышленности и касается препарата природного иммунокорректора Тактивина в форме спрея. Изобретение заключается в том, что средство содержит Тактивин, витамин С и 0,14 М раствор натрия хлорида в качестве растворителя при определенном содержании компонентов. Изобретение обеспечивает повышение эффективности действия, стабильность при хранении и использовании. 1 з.п. ф-лы, 5 табл., 4 ил.
Реферат
Изобретение относится к области химико-фармацевтической промышленности и касается препарата природного иммунокорректора Тактивина в форме спрея.
Наибольшую актуальность проблема часто возникающих респираторных заболеваний приобретает в медицинской практике в связи с высоким риском развития осложнений и формирования хронических заболеваний. Развивающаяся при этом иммунологическая недостаточность является тем патогенетическим фактором, который и приводит к формированию контингента "часто болеющих людей".
В работах последних лет показано, что у часто болеющих людей имеется снижение количественных показателей Т-звена иммунитета и недостаточность их функциональной активности. У этого контингента больных обнаружен дисбаланс в показателях гуморального иммунитета и снижение функции клеток моноцитарного ряда. Это обусловливает необходимость включения иммунокорректоров в комплексное лечение.
Отметим, что иммунокоррекция и, особенно, иммунореабилитация - длительный процесс.
По данным Министерства здравоохранения РФ в целом по стране более 30% населения нуждаются в коррекции иммунной системы, а в крупных городах (с высокоразвитой промышленностью) - до 50%.
Таким образом, имеется значительная потребность в препаратах, влияющих на иммунную систему.
Первыми иммуностимуляторами были вакцины, применение которых позволило резко снизить заболеваемость многими инфекциями (оспа, полиомиелит, туберкулез, коклюш и др.). Вакцины стимулируют специфический иммунный ответ и применяются для профилактики определенных инфекционных заболеваний.
Следующим шагом стало создание препаратов, оказывающих стимулирующее влияние на различные показатели клеточного и гуморального иммунитета, которые могли бы быть использованы для лечения иммунодефицитых состояний, опухолей, вирусных и бактериальных инфекций, аутоиммунных заболеваний.
Среди иммунокорректирующих средств известны:
- продукты микроорганизмов (бронховаксом, крестин, лентинан, биостим, рибомунил);
- вещества известной химической структуры (левамизол, инозин пранобекс, импрег, бромипирин и др.);
- экстракты пептидов тимуса (тимостимулин, тактивин, тимомодулин).
К сожалению, многие из известных средств проявляют ряд значительных побочных эффектов. Например, при повышении активности некоторых субпопуляций (например Т-хелперов) в ряде случаев наблюдается клиническое ухудшение. Это требует осторожности при применении препаратов.
Исследователи продолжают поиск новых препаратов и новых лекарственных форм известных препаратов, проявляющих более высокую эффективность и более безопасных.
Наиболее перспективными, как представляется, являются препараты тимуса, которые обладают мягким иммуномодулирующим действием. Особое внимание привлекает препарат тимуса Тактивин. Многочисленными исследованиями доказана его функциональная гетерогенность. Очень важно то, что Тактивин является истинным иммунокорректором. Он приводит к норме все параметры иммунной системы независимо от того, были ли они снижены или повышены до начала иммунотерапии. Параметры, находящиеся в норме, препарат не изменяет.
Большинство препаратов этой группы вводится с помощью инъекций.
В последнее десятилетие устойчиво сохраняется тенденция к росту числа часто и длительно болеющих детей. Группу повышенного риска при острых респираторных заболеваниях составляют дети с иммунологической недостаточностью, у которых, несмотря на существование самых разнообразных антибиотиков, заметного снижения заболеваемости, в первую очередь связанной с бактериальными возбудителями, не отмечается. Обусловлено это, в частности, ростом резистентности основных возбудителей инфекций верхних дыхательных путей к антибактериальным препаратам, усилением роли условно-патогенной микробной флоры в этиологии различных заболеваний у детей. Использование препаратов мягкого воздействия на иммунную систему может облегчить решение проблемы снижения указанной тенденции.
В то же время для таких категорий пациентов существует настоятельная потребность в формах для неинвазивного введения.
Предпринимаются попытки по созданию таких форм, например, спреев, удобных для применения в амбулаторной практике. Однако реально на рынке число таких препаратов недостаточно, и в основном они имеют ограничения по срокам хранения.
В настоящее время выпускается препарат Тимоген 0,025% раствор в 0,9% NaCl в форме дозированного спрея, основное действующее вещество которого представляет собой дипептид глутамил-триптофан, идентичный природному соединению, выделенному хроматографическим методом из экстракта вилочковой железы (http://terramedica.spb.ru/1_2004/nacharova.htm). Его применяют у взрослых и детей в составе комплексной терапии при заболеваниях и состояниях, сопровождающихся угнетением иммунитета. Однако Тимоген действует только на конечный этап иммунного процесса - активацию лимфоцитов периферической крови, поэтому данный препарат недостаточно эффективен в случаях, когда необходима нормализация иммунологических процессов.
Кроме того недостаток спрея этого средства связан с общими для ингаляционных форм препаратов пептидной или белковой природы проблемами, связанными со склонностью к образованию конгламератов, затрудняющей распыление и доставку к участкам респираторного тракта, а также их физико-химической нестабильностью.
Для решения проблем при создании спреев пептидных препаратов, предлагались различные пути. Например, микронизирование частиц, однако мелкие частицы имеют повышенную адгезию к стенкам ингалятора, что затрудняет их перемещение. Предлагалось также использование носителей типа лактозы (GB 2240337 А1), добавление аминокислот, таких как лейцин, обладающих поверхностно-активными свойствами (US 6153224 А); использование вспомогательных носителей, таких как гидроксипропилметилцеллюлоза или крахмал, обеспечивающих целенаправленную доставку (US 5626871 А). Однако насколько в минимальных количествах не содержались бы вспомогательные компоненты, их присутствие нежелательно, особенно с учетом того, что больные с иммунными нарушениями более всего склонны к проявлению аллергических реакций.
Предпринимались также попытки стабилизации препаратов тимуса. В основном таким стабилизирующим агентом предпочтительно являлся фенол в определенных концентрациях (DE 19609261 А1). Однако введение подобных стабилизаторов при создании детских форм неприемлемо.
Задачей настоящего изобретения является создание новой лекарственной формы Тактивина, более эффективной, пригодной для длительного применения, стабильной.
Тактивин (Т-активин) - препарат полипептидной природы, получаемый из тимуса крупного рогатого скота, в медицинской практике используется как иммуномодулирующее средство. Тактивин - комплекс пептидов тимуса, который, как отмечалось, обладает функциональной гетерогенностью. Разные молекулы, входящие в его состав, выполняют различные строго определенные функции, что и позволяет обеспечивать регуляторную функцию. Совсем недавно было обнаружено, что процессы апоптоза лимфоцитов находятся под контролем тимуса. При ряде заболеваний (красная волчанка, часто болеющие дети и др.) наблюдается повышенный апоптоз лимфоцитов. Применение иммунокорректора Тактивина нормализует процесс естественной гибели (апоптоз) лимфоцитов.
При иммунодефицитных состояниях препарат нормализует количественные и функциональные показатели Т-системы иммунитета, стимулирует продукцию лимфокинов, в том числе альфа и гамма интерферона, восстанавливает активность Т-киллеров, нормализует соотношение субпопуляций хелперных Т-клеток, восстанавливает функциональную активность стволовых гемопоэтических клеток и нормализует ряд других показателей, характеризующих напряженность Т-клеточного иммунитета.
Тактивин применяют при иммунодефицитных состояниях с преимущественным поражением Т-системы иммунитета, возникающих при инфекционных, гнойных и септических процессах, лимфопролиферативных заболеваниях (лимфогранулематоз, лимфолейкоз), рассеянном склерозе, туберкулезе, рецидивирующем офтальмогерпесе, псориазе и других заболеваниях, протекающих на фоне иммунодефицита.
В настоящее время для лечения людей широко используется Тактивин, вводимый инвазивным (инъекционным) способом в виде 0,01% раствора, что создает неудобства в его использовании, особенно при необходимости длительного применения препарата как профилактического средства. Инъекции являются травмирующим фактором для пациентов, особенно детей, манипуляция требует присутствия среднего медицинского персонала. Инъекционный путь введения лекарственных препаратов полностью не исключают инвазию инфекций, в том числе, и особо опасных. Важно и то, что инвазивный метод не может быть использован при проведении профилактических мероприятий и в полевых условиях.
В результате поиска неинвазивных методов введения иммуноактивных пептидов тимуса была разработана новая форма - в форме спрея, содержащая Тактивин, витамин С и 0,14 М раствор натрия хлорида в качестве носителя при следующем содержании компонентов:
Тактивин 100-120 мкг
Витамин С 100-150 мкг
0,14 М раствор натрия хлорида - до 1 мл
Может быть также введен дополнительно диэтилпирокарбонат (ДЭП) - 0,5-1 мкг в 1 мл раствора препарата. Указанный интервал дозирования является безопасным и обеспечивает возможность полной стерилизации до стадии фильтрации.
В заявленных дозах Тактивин нормализует основные функции организма человека: улучшение показателей сердечно-сосудистой, эндокринной, иммунной и нервной системы, гомеостаз и метаболизм. Препарат не только восстанавливает параметры иммунной системы, но и снимает интоксикацию.
При хранении пептиды, составляющие комплекс, образующий Тактивин, распадаются на отдельные более низкомолекулярные цепочки, и это приводит к резкому снижению активности. При разработке состава раствора, пригодного к распылению в форме спрея, данная проблема была успешно решена введением в состав определенных количеств витамина С (аскорбиновой кислоты). Известно, что аскорбиновая кислота используется широко как антиоксидант. Но до сих пор не было известно, что она может выполнять роль стабилизатора пептидов за счет предотвращения их разрушения, не связанного с окислительными процессами.
В качестве растворителя используют 0,14 М раствор натрия хлорида. Его использование вместо воды является более оптимальным, поскольку натрия хлорид повышает всасываемость пептидов.
Еще одним немаловажным техническим результатом является длительное сохранение стерильности раствора. Как правило, для спреев также существует требование сохранения стерильности. После первого применения в дозатор попадает воздух и стерильность нарушается. Процесс лечения пациентов с нарушениями иммунной системы, как уже отмечалось выше, является длительным; дозаторы такие пациенты используют самостоятельно, и их было бы удобно носить с собой. Поэтому разработанная форма является перспективной и с этой точки зрения, поскольку при ее использовании стерильность сохраняется практически полностью в течение минимально 30 дней и более.
Способ получения препаративной формы включает следующие стадии:
- растворение сухого Тактивина в 0.14 М растворе натрия хлорида;
- добавление аскорбиновой кислоты;
- стерилизация полученного раствора через фильтры с размером предпочтительно 0,22 микрона;
- фасовка в стерильные флаконы-ингаляторы.
Изобретение может быть проиллюстрировано следующими примерами.
Пример 1.
Данные по часто болеющим пациентам (105 человек) с простым и обструктивным бронхитом.
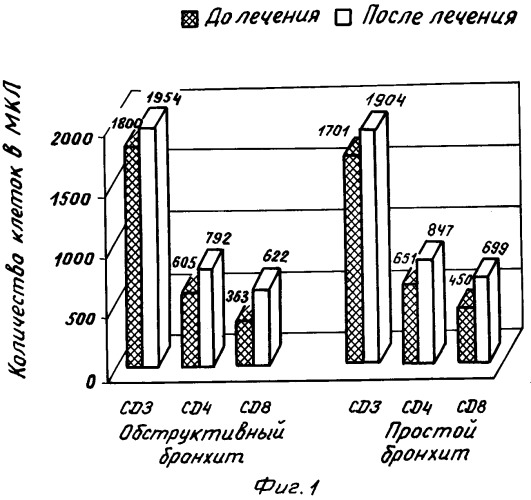
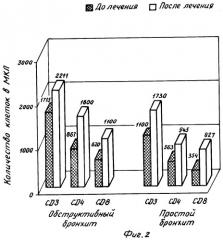
Больным (100 человек) вводили спрей Тактивина, содержащий 100 мкг активного вещества и 100 мкг витамина С в 1 мл 0.14 М раствора натрия хлорида, и (5 человек) спрей Тактивина, содержащий 100 мкг активного вещества, 100 мкг витамина С и 0,5 мкг ДЭП в 1 мл 0.14 М раствора натрия хлорида. Препарат вводили из расчета на активное вещество: 2-3 мкг/кг веса взрослого пациента и 1-2 мкг/кг веса ребенка.
Результаты представлены на фиг.1-4.
Пример 2.
Применение при онкологических заболеваниях.
Тактивин вводили в форме спрея, содержащего 110 мкг активного вещества и 150 мкг витамина С в 1 мл 0.14 М раствора натрия хлорида (табл.1).
| Таблица 1.Иммунограмма пациента В.М., 64 года (диагноз: опухоль молочной железы - онкология) Субпопуляции лимфоцитов крови | ||||
| Показатель | Ед. измерения | Норма | До лечения | После лечения |
| СD3+(Т-лимфоциты) | Процент | 60-75 | 47,0 | 68,0 |
| Кл/мл | 800-1800 | 719,1 | 1205 | |
| СD4+(Т-хелперы/индукторы) | Процент | 35-46 | 24,5 | 39,2 |
| Кл/мл | 500-1100 | 374,8 | 921 | |
| CD8+(T-супрессоры/ | Процент | 25-30 | 18,2 | 26,9 |
| цитотоксические) | Кл/мл | 400-800 | 278,6 | 608 |
| СD20+(В-лимфоциты) | Процент | 5-15 | 9,5 | 12,9 |
| Кл/мл | 100-400 | 145,3 | 312 | |
| HLA-DR+(В-лимфоциты, | Процент | 7-15 | 14,2 | 13,2 |
| активированные Т-лимф.) | Кл/мл | 120-400 | 217,2 | 298 |
| СD38+(активированные | Процент | 24-40 | 27,9 | 29,9 |
| лимфоциты) | Кл/мл | 300-1000 | 426,8 | 528 |
| СD25+(альфа-цепь | Процент | 0-5 | 1,7 | |
| рецептора интерлейкина-2) | Кл/мл | 0-100 | 26,0 | |
| CD16(NK-клетки) | Процент | 10-20 | 20,1 | 20,0 |
| Кл/мл | 120-500 | 307,5 | 319 | |
| CD11b+(C3bi рецептор С3 | Процент | 10-35 | 29,1 | |
| комп.комплемента) | Кл/мл | 120-800 | 445,2 | |
| CD50+(молекула адгезии) | Процент | 85-100 | 76,9 | |
| Кл/мл | 1100-2400 | 1176,0 | ||
| СD45RА+(В-лимф., Т-лимф., NK- | Процент | 45-65 | 49,6 | |
| клетки) | Кл/мкл | 600-1500 | 758,8 | |
| CD5+(Т-лимфоциты) | Процент | 60-80 | 45,1 | 65,2 |
| Кл/мл | 800-1900 | 690,0 | 812 | |
| СD7+(Т-лимфоциты, NK-клетки) | Процент | 60-80 | 54,3 | |
| Кл/мл | 800-1900 | 830,7 | ||
| CD71+) +(рецептор трансферрина) | Процент | 0-5 | 6,5 | |
| Кл/мл | 0-100 | 99,4 | ||
| CD95+ (FAS/APO-1антиген, | Процент | 23-60 | 21,7 | |
| опосредующий апоптоз) | Кл/мл | 300-1400 | 332,0 | |
| СD4+/СD8+(иммунорегуляторный | Процент | 1,2-2,4 | 1,34 | 1,46 |
| индекс) | Кл/мл | |||
| Показатели гуморального иммунитета | ||||
| Показатель | Ед.изм. | Норма | До лечения | После лечения |
| Иммуноглобулин G | г/л | 12,8±0,6 | 11,3 | 14,0 |
| Иммуноглобулин А | г/л | 2,05±0,11 | 1,53 | 1,98 |
| Иммуноглобулин М | г/л | 1,33±0,06 | 0,6 | 1,21 |
Пример 3. Применение при онкологических заболеваниях.
Тактивин вводили в виде спрея, содержащего 100 мкг активного вещества и 100 мкг витамина С в 1 мл 0.14 М раствора натрия хлорида (табл.2).
| Таблица 2Иммунограмма пациента Г.П., 60 лет (диагноз: опухоль яичников - онкология) Субпопуляции лимфоцитов крови | ||||
| Показатель | Ед. измерения | Норма | До лечения | После лечения |
| СD3+(Т-лимфоциты) | Процент | 60-75 | 70,8 | 71,9 |
| Кл/мл | 800-1800 | 390,8 | 1250 | |
| СD4+(Т-хелперы/индукторы0) | Процент | 35-46 | 52,8 | 39,1 |
| Кл/мл | 500-1100 | 291,4 | 890 | |
| СD8+(Т-супрессоры/ | Процент | 25-30 | 29,9 | 28,6 |
| цитотоксические) | Кл/мл | 400-800 | 165,0 | 620 |
| СD20++(В-лимфоциты) | Процент | 5-15 | 16,0 | 14,3 |
| Кл/мл | 100-400 | 88,3 | 258 | |
| HLA-DR+(В-лимфоциты, | Процент | 7-15 | 14,5 | 14,1 |
| активированные Т-лимф.) | Кл/мл | 120-400 | 80,0 | 139 |
| CD38+ (активированные | Процент | 24-40 | 41,5 | 39,3 |
| лимфоциты) | Кл/мл | 300-1000 | 229,0 | 590 |
| СD25+(альфа-цепь | Процент | 0-5 | 1,7 | 1,1 |
| рецептора интерлейкина-2) | Кл/мл | 0-100 | 9,38 | 10 |
| CD16(NK-клетки) | Процент | 10-20 | 11,4 | 15,2 |
| Кл/мл | 120-500 | 62,9 | 320 | |
| CD11b+(C3bi рецептор С3 | Процент | 10-35 | 16.4 | 21,1 |
| комп.комплемента) | Кл/мл | 120-800 | 90,5 | 402 |
| CD50 (молекула адгезии) | Процент | 85-100 | 96,4 | 95,2 |
| Кл/мл | 1100-2400 | 532,1 | 1650 | |
| СD45RА+(В-лимф., Т-лимф., | Процент | 45-65 | 66,1 | 60,0 |
| NK-клетки) | Кл/мл | 600-1500 | 364,8 | 791 |
| CD5+(Т-лимфоциты) | Процент | 60-80 | 79,0 | 78,5 |
| Кл/мл | 800-1900 | 436,0 | 1095 | |
| СD7+(Т-лимфоциты, NK-клетки) | Процент | 60-80 | 79,7 | |
| Кл/мл | 800-1900 | 439,9 | ||
| СD71+(рецептор трансферрина) | Процент | 0-5 | 18 | |
| Кл/мл | 0-100 | 9,9 | ||
| CD95+ (FAS/APO-1антиген, | Процент | 23-60 | 10,7 | |
| опосредующий апоптоз) | Кл/мл | 300-1400 | 59,0 | |
| СD4+/СD8+(иммунорегуляторный | Процент | 1,2-2,4 | 1,76 | 1,37 |
| индекс) | Кл/мл | |||
| Показатели гуморального иммунитета | ||||
| Показатель | Ед.изм. | Норма | До лечения | После лечения |
| Иммуноглобулин G | г/л | 12,8±0,6 | 13,5 | 13,0 |
| Иммуноглобулин А | г/л | 2,05±0,11 | 1,83 | 1,89 |
| Иммуноглобулин М | г/л | 1,33±0,06 | 7,78 | 1,22 |
Пример 4.
Результаты исследования стабильности препарата при хранении (табл.3 и 4). Определение активности препарата Тактивина проводили стандартным методом восстановления чувствительности фоновых розеткообразующих клеток (фРОК) селезенки тимэктомированных мышей к ингибирующему действию азатиоприна (Dardenne М., Bach J.-F., 1975). Метод был разработан специально для тестирования биологической активности пептидных препаратов, выделенных из тимуса. Согласно данному методу, активными считаются препараты, вызывающие восстановление чувствительности фРОК селезенки к азатиоприну на 50% и выше.
| Таблица 3.Стабильность препарата Тактивин (100 мкг в 1 мл) в растворе 0,14 М NaCl +0,01% аскорбиновой кислоты (100 мкг в 1 мл) | ||||
| № серии | дата анализа | Кол-во мкг Тактивина в пробе | Активность* | Условные обозначения |
| Л-16 | 11.02.2002 | 10 | 80% | +++ |
| 5 | 67% | + | ||
| Л-16 | 10.11.2003 | 10 | 82% | +++ |
| 5 | 65% | + | ||
| Л-16 | 22.12.2004 | 10 | 80% | +++ |
| 5 | 63% | + | ||
| Таблица 4.Стабильность препарата Тактивин в растворе 0,14 М NaCl | ||||
| № серии | дата анализа | Кол-во мкг Тактивина в пробе | Активность* | Условные обозначения |
| Л-16 | 11.02.2002 | 10 | 80% | +++ |
| 5 | 67% | + | ||
| Л-16 | 10.11.2003 | 10 | 76% | ++ |
| 5 | 55% | + | ||
| Л-16 | 22.12.2004 | 10 | 60% | + |
| 5 | 49% | ± |
При хранении препарата Тактивина в растворе 0,14 М NaCl в присутствии аскорбиновой кислоты стабильность препарата сохраняется практически неизменной в течение 3-х лет.
По данным клинических испытаний применение неинвазивного способа иммунокоррекции с помощью изобретения способствовало снижению частоты заболевания ОРЗ до 2-3 раз в год у 90% обследованных пациентов. При этом длительность заболевания и его тяжесть были существенно снижены. На фиг.1-4 приводятся сравнительные иммунограммы (105 детей) больных с обструктивным и простым бронхитом, которых лечили Тактивином - спреем (Тактивин - спрей содержал витамин С) и Тактивином в инъекциях. У всех детей до лечения наблюдали снижение всех параметров иммунной системы. После лечения все показатели Т- и В-систем иммунитета, а также макрофагальное звено (таблица 5) были приведены в пределы возрастной нормы.
Разработанная новая форма Тактивина может быть рекомендована для широкого использования в клинической практике.
| Таблица 5.Показатели фагоцитоза до и после иммунокоррекции (А - спрей, Б - инъекции) | |||||
| Маркеры | Норма | Результаты | Уровень значимости Р | ||
| До лечения | После лечения | ||||
| % фагоцитирующихнейтрофилов | 70-80 | А | 60±4,5 | 70,5±2,9 | >0,005 |
| Б | 58±5,0 | 76±3,2 | >0,005 | ||
| Фогоцитарный индекс | 4-7 | А | 3,8±1 | 5,0±0,2 | >0,005 |
| Б | 3,0±0,3 | 6,0±1,2 | >0,005 | ||
| НСТ-тест(спонтанный) | 80-99 | А | 174±25 | 180±36 | >0,005 |
| Б | 188±20 | 100±19 | >0,005 | ||
| НСТ-тест(индуцированный) | 130-153 | А | 164±12 | 163±14 | >0,005 |
| Б | 315±47 | 149±27 | <0,001 |
1. Иммуномодулирующее средство в форме спрея, характеризующееся тем, что оно содержит Тактивин, витамин С и 0,14 М раствор натрия хлорида в качестве растворителя, при следующем содержании компонентов:
| Тактивин | 100-120 мкг |
| Витамин С | 100-150 мкг |
| 0,14 М раствор натрия хлорида | До 1 мл |
2. Средство по п.1, характеризующееся тем, что оно содержит дополнительно диэтилпирокарбонат (ДЭП) - 0,5-1 мкг.