Компонент катализатора, предшественник катализатора и катализатор полимеризации олефинов на основе галогенида магния
Иллюстрации
Показать всеИзобретение относится к композициям на основе галогенида магния, катализаторам, приготовленным на их основе, способам получения композиций на основе галогенидов магния и катализаторам, а также к способам полимеризации. Описан компонент катализатора полимеризации олефинов на основе галогенида магния, полученный из а) галогенида магния, б) растворителя, подходящего в качестве донора электронов, в) электронно-донорного соединения, представляющего собой линейный или разветвленный, замещенный или незамещенный, алифатический или ароматический спирт, имеющий от 1 до 25 атомов углерода, где галогенид магния характеризуется растворимостью в растворителе, которая не снижается под влиянием температуры вплоть до температуры кипения растворителя, и растворимость галогенида магния в растворителе выше, чем 0,7 моль/л. Также описан предшественник катализатора полимеризации олефинов, включающий продукт взаимодействия компонента катализатора, описанного выше, и второго компонента, включающего переходный металл, выбранный из группы, включающей титан, цирконий, гафний и ванадий, и их комбинации, и описан катализатор полимеризации олефинов, включающий продукт взаимодействия предшественника катализатора и со-катализатора, представляющего собой алкильное соединение алюминия. Технический эффект - получение катализаторов с более высоким содержанием магния, имеющих более высокую растворимость или такую растворимость, которая не снижается с увеличением температуры, снижение затрат, связанных с приготовлением катализатора при маленьком размере загрузки. 3 н. и 11 з.п. ф-лы, 4 ил., 1 табл.
Реферат
Область применения изобретения
Настоящее изобретение относится к композициям на основе галогенидов магния, катализаторам, приготовленным на их основе, способам получения композиций на основе галогенидов магния и катализаторам, а также способам полимеризации.
Предпосылки создания изобретения
Растворы MgCl2 в различных электроно-донорных растворителях, как было установлено, используются в промышленности для получения катализаторов полимеризации. Часто в таких растворах используют простые эфиры, кетоны и сложные эфиры, чтобы получить Mg-Ti предшественники катализатора, которые нашли широкое применение в каталитических процессах полимеризации олефинов. Известные предшественники получаются путем растворения хлорида магния и хлорида титана в растворителе, с последующим выпариванием или отгонкой избытка растворителя. Тетрагидрофуран (ТГФ), как было показано, является особенно подходящим растворителем благодаря его способности координировать как MgCl2, так и TiClx, и его относительно низкой температуре кипения, что облегчает отгонку и рекуперацию растворителя. Образующийся высушенный предшественник катализатора обрабатывают со-катализатором, обычно соединением алкилалюминия, с целью получения композиции, которая активна при полимеризации олефинов.
Использование таких предшественников катализаторов в промышленных процессах полимеризации основано на растворимости MgCl2 в растворителе. Галогениды щелочноземельных металлов обычно нерастворимы в углеводородных растворителях. Однако растворимость в определенных координирующих электронно-донорных растворителях может быть достаточно высокой для промышленного применения. Например, растворимость MgCl2 в тетрагидрофуране (ТГФ) повышается от примерно 0,2 моль/л при -25°С до примерно 0,7 моль/л при 30°С. Количество предшественника, которое можно получить в один прием, ограничено растворимостью MgCl2.
Интересно, однако, что при более высоких температурах растворимость MgCl2 в таких растворителях понижается. Например, при температуре кипения ТГФ (65°С) растворимость MgCl2 составляет всего лишь примерно 0,4 моль/л при атмосферном давлении. Такое уменьшение растворимости осложняет процесс сушки предшественника, поскольку удаление растворителя при нагревании обычно осуществляется наиболее эффективно при температуре, близкой к температуре кипения растворителя. Чтобы избежать уменьшения концентрации MgCl2 в растворе предшественника до нежелательного уровня процесс сушки проводят при пониженных температурах и давлении. К сожалению, удаление растворителя при таких условиях требует большего времени и является менее эффективным, снижая, таким образом, производительность установки.
Пониженная растворимость MgCl2 при повышенных температурах также вызывает образование твердой корки осажденного MgCl2 на стенках реактора и трубках, когда пределы растворения при данной температуре превышены.
По этим причинам, система каталитического предшественника с улучшенной растворимостью найдет применение в процессах полимеризации. Также были бы полезными способы увеличения растворимости и изменения профиля растворимости MgCl2 как функции температуры. Следовательно, были бы полезными компоненты катализатора на основе галогенидов магния, имеющие более высокую растворимость, или такую растворимость, которая не снижается с увеличением температуры, и способы использования таких компонентов катализаторов, а также катализаторы, полученные на их основе.
Краткое изложение сущности изобретения
В некоторых предпочтительных вариантах изобретение предлагает способ повышения растворимости галогенидов магния, включающий: 1) обеспечение электроно-донорного растворителя; контактирование галогенида магния с электроне-донорным растворителем; и 2) обеспечение электронно-донорного соединения с целью получения композиции на основе галогенида магния, где композиция характеризуется растворимостью галогенида магния в растворителе, которая не понижается с увеличением температуры вплоть до температуры кипения растворителя.
В других предпочтительных вариантах предлагается компонент катализатора полимеризации, включающий галогенид магния, электронно-донорный растворитель и электронно-донорное вещество, причем композиция характеризуется растворимостью в электронно-донорном растворителе, которая не снижается с повышением температуры вплоть до температуры кипения растворителя.
В некоторых других предпочтительных вариантах предлагается способ получения катализатора. В таких предпочтительных вариантах способ включает получение содержащей магнии композиции, контактирование содержащей магний композиции с соединением переходного металла с целью получения предшественника катализатора и контактирование предшественника катализатора с со-катализатором. Содержащая магний композиция включает галогенид магния, электроно-донорный растворитель и электроно-донорное соединение, которое характеризуется растворимостью в электроно-донорном растворителе, которая не снижается с повышением температуры вплоть до температуры кипения электроно-донорного растворителя.
Еще некоторые предпочтительные варианты предлагают способы получения полимера, включающие взаимодействие не менее одного мономера олефинов в присутствии катализатора, включающего продукт реакции следующих компонентов: содержащей магний композиции, которая содержит галогенид магния, электроно-донорного растворителя и электроно-донорного соединения. Содержащая магний композиция характеризуется растворимостью в электроно-донорном растворителе, которая не снижается с повышением температуры вплоть до температуры кипения электроно-донорного растворителя. Каталитическая композиция также включает соединение переходного металла, где переходный металл выбирается из группы, включающей титан, цирконий, гафний, ванадий, ниобий, тантал и их комбинации, а также композицию со-катализатора.
В некоторых из описанных выше предпочтительных вариантах композиции по большей части не содержат электронно-донорных соединений, и молярное соотношение электронно-донорного соединения и галогенида магния меньше или равно 1,9. В некоторых предпочтительных вариантах отношение электронно-донорного соединения к галогениду магния меньше, чем примерно 1,75, в то время как в других предпочтительных вариантах отношение электронно-донорного соединения к галогениду магния изменяется от примерно 0,1 до менее, чем примерно 0,5.
В некоторых способах, предшественников катализатора, компонентах катализатора, и катализаторах, описанных в настоящем описании, галогенид магния представляет собой хлорид магния, бромид магния, иодид магния или их комбинации. Электронно-донорное соединение может быть линейным, разветвленным, замещенным или незамещенным алифатическим или ароматическим спиртом, содержащим от одного до 25 атомов углерода. Примеры спиртов включают метанол, этанол, пропанол, изопропанол, бутанол, 2-этилгексанол, 1-додеканол, циклогексанол, и ди-трет-бутилфенол.
Растворитель можно выбирать из группы, включающей алкиловые сложные эфиры алифатических или ароматических карбоновых кислот, алифатические простые эфиры циклические простые эфиры, и алифатические кетоны. В некоторых предпочтительных вариантах осуществления изобретения растворитель выбирают из группы, включающей алкиловые сложные эфиры алифатических и ароматических карбоновых кислот, простые эфиры и алифатические кетоны. Примеры алкиловых сложных эфиров, подходящих в качестве растворителей, включают метилацетат, этилацетат, этилпропионат, метилпропионат, этилбензоат и их комбинации. Простые эфиры, которые пригодны для использования в качестве растворителя, включают, но не ограничиваются ими, диэтиловый эфир, диизопропиловый эфир, ди-н-бутиловый эфир, этилизопропиловый эфир, метилбутиловый эфир, метилаллиловый эфир, этилвиниловый эфир, тетрагидрофуран, 2-метил-тетрагидрофуран и их комбинации. Подходящие кетоны включают ацетон, метилэтилкетон, циклогексанон, циклопентилметилкетон, 3-бром-4-гептанон, 2-хлорциклопентанон, аллилметилкетон и их комбинации. Конечно, смешанные растворители, содержащие второй электронно-донорный растворитель, который представляет собой алкиловый сложный эфир алифатической или ароматической карбоновой кислоты, алифатический или циклический простой эфир, или алифатический кетон, можно использовать в некоторых предпочтительных вариантах. В некоторых предпочтительных вариантах, описанных здесь, растворимость композиции на основе галогенида магния в растворителе выше, чем примерно 0,7 моль/л.
В отдельных примерах галогенид магния представляет собой хлорид магния, спирт представляет собой этанол или изопропанол, молярное отношение спирта к магнию составляет от примерно 0,1 до примерно 1,1, растворимость галогенида магния или композиции на основе галогенида магния в растворителе составляет от примерно 0,8 до 2,5 моль MgCl2/л.
Некоторые предпочтительные варианты предлагают компонент катализатора, включающий композицию формулы
Mg(ED)rCl2[S]q,
где r выше 0 и менее 1,9, q выше 0 и менее 4.
Некоторые предшественники катализаторов, описанные в настоящем описании, включают композиции, содержащие продукт реакции или смесь магнийсодержащего компонента катализатора, имеющего такую растворимость в растворителе, которая не снижается при повышении температуры вплоть до температуры кипения растворителя, и второй компонент, содержащий переходный металл, выбранный из группы, включающей титан, цирконий, гафний, ванадий, ниобий, тантал и их комбинации. Некоторые из типичных таких вторых компонентов включают по крайней мере одно соединение титана формулы Ti(OR†)аХb, где R†′ представляет собой R† или COR†, где R†′ представляет собой один из алифатических углеводородных радикалов от С1 до С14 или ароматических углеводородных радикалов от С6 до С14; каждый Х представляет собой отдельно Cl, Br или I; а имеет величину 0 или 1; b имеет величину от 2 до 4 включительно; и a+b составляет 3 или 4. В некоторых предпочтительных вариантах по меньшей мере одно соединение титана включает галогенид титана, такой как, но не ограничивающийся ими, TiCl4, TiCl3 или восстановленный алюминием TiCl3.
В определенных предпочтительных вариантах состав предшественника катализатора включает композицию формулы
[Mg(ED)r]mTi(OR)nXp[S]q,
где ED включает линейные или разветвленные спирты, содержащие от одного до примерно 25 атомов углерода; Х представляет собой отдельно Cl, Br или I; S выбирают из группы, включающей алкиловые сложные эфиры алифатических или ароматических карбоновых кислот, алифатические простые эфиры, циклические простые эфиры, и алифатические кетоны; m изменяется от 0,5 до 56; n составляет 0, 1, или 2; р изменяется от 4 до 116; q изменяется от 2 до 85 и r изменяется от 0,1 до 1,9.
Некоторые предпочтительные варианты предлагают катализатор, который представляет собой продукт взаимодействия предшественника катализатора и со-катализатора. Другие предпочтительные варианты дополнительно включают модифицирование катализатора кислотой Льюиса. Некоторые подходящие кислоты Льюиса имеют формулу
,
где R* представляет собой R*1 или OR*1; где R*1 представляет собой алифатический углеводород, имеющий от 1 до 14 атомов углерода, или ароматический углеводородный радикал, содержащий от 6 до 14 атомов углерода; М представляет собой Al или В; Х представляет собой Cl, Br или I; и g изменяется от 0 до 3. Отдельные примеры кислот Льюиса на основе хлоридов включают три-н-гексилалюминий, триэтилалюминий, диэтилалюминийхлорид, этилалюминийдихлорид, триметилалюминий, диметилалюминийхлорид, метилалюминийдихлорид, триизобутилалюминий, три-н-бутилалюминий, диизобутилалюминийхлорид, изобутилалюминийдихлорид, этокси дихлорид алюминия, фенилалюминийдихлорид и феноксидихлорид алюминия. Отдельные примеры бромсодержащих кислот Льюиса включают диэтилалюминийбромид, этилалюминийдибромид, диметилалюминийбромид, метилалюминий, дибромид, диизобутилалюминийбромид, изобутилалюминийдибромид, этоксиалюминийдибромид, фенилалюминийдибромид и феноксиалюминийдибромид. Кислоты Льюиса на основе иода включают диэтилалюминийиодид, этилалюминийдииодид, триметилалюминийиодид, метилалюминий, дииодид, диизобутилалюминийиодид, изобутилалюминийдииодид, этоксиалюминийдииодид, фенилалюминийдииодид и феноксиалюминийдииодид.
Другие подходящие кислоты Льюиса включают трихлорид бора, трибромид бора, этилбордихлорид, этоксибородихлорид, диэтоксибородихлорид, фенилбородихлорид, феноксибородихлорид, дифеноксиборохлорид, (С6Н13)BCl2 или (С6Н13О)BCl2.
Дополнительные подходящие кислоты Льюиса или со-катализаторы имеют формулу
AlX'd(R'')cHe
где X' представляет собой Cl или OR'''; R'' и R''' представляют собой по отдельности замещенные углеводородные радикалы от C1 до С14; d составляет от 0 до 1,5; е принимает значения 0 или 1; c+d+e составляет 3. Отдельные примеры таких активаторов включают Al(СН3)3, Al(C2H5)3, Al(С2Н5)2Cl, Al(i-С4Н9)3, Al(C2H5)1,5Cl1,5, Al(i-C4H9)2H, Al(С6Н13)3, Al(C8H17)3, Al(C2H5)2H, Al(С2Н5)2(ОС2Н5). В некоторых предпочтительных вариантах один или более активаторов присутствуют при соотношении активатор: соединение переходного металла, меняющемся от примерно 1 до примерно 400 молей активатора на моль соединения переходного металла. В некоторых предпочтительных вариантах отношение количества активатора к количеству соединения переходного металла составляет примерно 4, примерно 10, примерно 15 или примерно 60 молей активатора на моль соединения переходного металла.
Некоторые описанные в данном описании методы полимеризации обеспечивают полимеры, имеющие плотность в пределах от 0,88 до 0,98 г/см3. Некоторые полимеры содержат этилен в количествах, равных или выше примерно 90 мольных процентов, и один или более со-мономеров в количестве, равном или менее чем примерно 10 мольных процентов.
Краткое описание чертежей
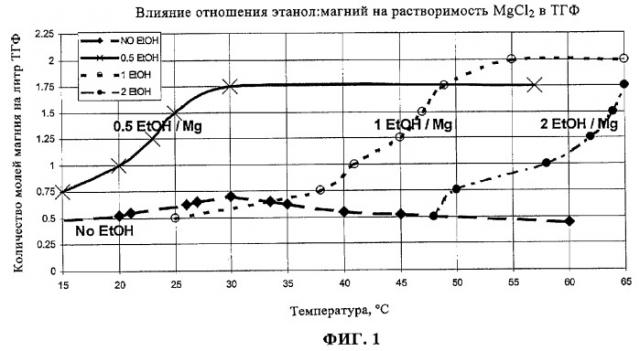
На фиг.1 показана зависимость растворимости MgCl2 для трех предпочтительных вариантов настоящего изобретения от содержания в растворе спирта и температуры раствора.
На фиг.2 показан профиль растворимости в нескольких предпочтительных вариантах настоящего изобретения в зависимости от температуры, концентрации MgCl2 и соотношения спирт : Mg в ТГФ.
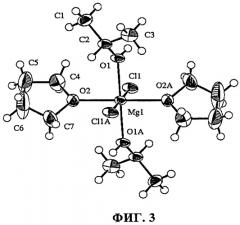
На фиг.3 показана структура одного из примеров компонента катализатора, содержащего галогенид магния.
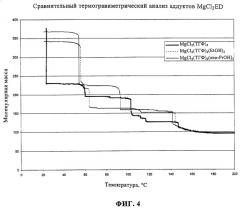
На фиг.4 показаны результаты термогравиметрического анализа (ТГА) для предпочтительных вариантов предложенного в настоящем изобретении компонента катализатора.
Описание предпочтительных вариантов осуществления изобретения
Предпочтительные варианты настоящего изобретения предлагают способы увеличения растворимости галогенида магния, которые предусматривают получение электроно-донорного растворителя, контактирование галогенида магния с растворителем и обеспечение электронно-донорного вещества, с целью получения композиции на основе галогенида магния, где композиция характеризуется такой растворимостью в растворителе, которая не снижается при повышении температуры вплоть до температуры кипения растворителя. Предлагаются компоненты катализатора, имеющие растворимость, которая не снижается при повышении температуры. Выявлены предпочтительные варианты данного изобретения, которые предлагают предшественники катализатора, включающие такие компоненты катализатора. Также выявлены способы приготовления таких соединений, так же, как и катализаторы полимеризации и способы полимеризации, использующие такие катализаторы.
В последующем описании все приведенные в нем числа имеют примерные величины, независимо от того, использованы перед ними или не использованы слова «примерно» или «приблизительно». Они могут изменяться в пределах 1, 2, 5% или иногда от 10 до 20%. Когда выявлен численный интервал с нижним пределом, RL, и с верхним пределом, RU, любое число R, выпадающее из интервала, поясняется отдельно. В частности, следующие числа R внутри интервала описывают отдельно: R=RL+k*(RU-RL), где k представляет собой переменную, изменяющуюся от 1 до 100% с инкрементом 1%, то есть k принимает значения 1, 2, 3, 4, 5, ... 50, 51, 52, ... 95, 96, 97, 98, 99 или 100%. Более того, любой численный интервал, определенный двумя числами, R, как описано выше, также описывают отдельно.
Любые ссылки в настоящем описании на «электронно-донорные соединения» означают соединения, которые изменяют растворимость галогенида магния в электронно-донорном растворителе так, что растворимость не снижается в температурном интервале вплоть до температуры кипения электронно-донорного растворителя. В настоящем описании термин «электронно-донорные соединения» не включает «растворители», как они определены ниже, даже когда такие растворители имеют электронно-донорные свойства. Отдельные примеры электронно-донорных соединений включают спирты, тиолы, слабодонорные амины и фосфины. В настоящем описании термин «практически не содержащий других электронно-донорных соединений» означает, что другие «электронно-донорные соединения», как они определены в настоящем описании, не присутствуют в концентрациях выше, чем уровни, которые обычно находят в качестве примесей в таких веществах, поставляемых в качестве растворителей и имеющих соответствующую степень чистоты. Так композиции, включающие растворитель, обладающий электронно-донорными свойствами, и «электронно-донорное вещество» считают «практически не содержащими других электронно-донорных соединений». В некоторых предпочтительных вариантах, «практически не содержащий» означает менее чем 1, 0,1, 0,01 или 0,001 мас.%.
Подходящие растворители включают любые простые эфиры, кетоны или сложные эфиры. Если такие растворители обладают электронно-донорными свойствами, любые ссылки в настоящем описании на «растворитель» или «растворители» не включают соединения, обозначенные как «электронно-донорные вещества». Так композиции, которые «практически не содержат электронно-донорных соединений», могут включать один или более «растворителей».
В настоящем описании термин «простой эфир» определяют как любое вещество формулы R-O-R', где R и R' представляют собой замещенные или незамещенные углеводородные группы. В некоторых случаях R и R' одинаковы. В качестве примеров, не ограничивающих данное изобретение, симметричные простые эфиры представляют собой диэтиловый эфир диизопропиловый эфир, и ди-н-бутиловый эфир. Примеры несимметричных простых эфиров включают этилизопропиловый эфир и метилбутиловый эфир. Примеры подходящих замещенных эфиров включают, например, метилаллиловый эфир и этилвиниловый эфир. Еще в других предпочтительных вариантах R и R' могут образовывать конденсированное кольцо, которое может быть насыщенным или ненасыщенным. Одним из примеров такого соединения служит тетрагидрофуран. Другой из таких подходящих циклических эфиров представляет собой 2-метилтетрагидрофуран. Еще раз следует подчеркнуть, что специально пронумерованные вещества приведены только в качестве примеров подходящих типов соединений; однако любое вещество, имеющее функциональную группу R-O-R', может быть на их месте.
В настоящем описании термин «кетон» обозначает любое вещество, имеющее формулу R(C=O)R'. R и R' могут представлять собой отдельно замещенные или незамещенные углеводородные группы, как описано выше при описании простых эфиров. Примерами кетонов служат ацетон, метилэтилкетон, циклогексанон и циклопентилметилкетон. Галогенированные кетоны, такие как 3-бромо-4-гептанон или 2-хлороциклопентанон, также могут быть использованы. Другие подходящие кетоны могут включать другие функциональные группы, в том числе ненасыщенные, как в аллилметилкетоне. Каждое из этих вещество удовлетворяет формуле R(C=O)R', где атом углерода карбонильной группы в молекуле образует связи с двумя другими атомами углерода.
Подходящие сложные эфиры включают любое соединение общей формулы R(C=O)OR'. В таких соединениях атом углерода карбонильной группы образует одну связь с углеродным атомом, а другую связь с атомом кислорода. R и R' по отдельности выбирают из замещенных или незамещенных углеводородных групп, они могут быть одинаковыми или разными. В некоторых предпочтительных вариантах сложные эфиры включают алкиловые эфиры алифатических и ароматических карбоновых кислот. Циклические сложные эфиры, насыщенные сложные эфиры и галогенированные сложные эфиры также включаются в данную группу. Не ограничивающие объем настоящего изобретения примеры включают метилацетат, этилацетат, этилпропионат, метилпропионат и этилбензоат. Еще раз следует подчеркнуть, что специально пронумерованные вещества приведены только в качестве примеров подходящих типов соединений; однако любое вещество, имеющее функциональную группу R(C=O)OR', может быть использовано вместо них.
Как правило, растворитель присутствует в большом избытке по отношению к первому координационному окружению магния. В некоторых предпочтительных вариантах отношение растворителя к магнию составляет примерно 100 к 1; в других предпочтительных вариантах отношение может быть даже выше. Еще в других предпочтительных вариантах растворитель присутствует в отношении от не менее примерно 1,0, не менее примерно 2,0, не менее примерно 5,0, не менее примерно 10 или не менее примерно 20 молей растворителя на моль магния. В некоторых предпочтительных вариантах можно использовать два или более растворителя.
Контактирование галогенида магния с любым подходящим растворителем осуществляется непосредственно смешиванием галогенида магния и растворителя. В некоторых предпочтительных вариантах галогенид магния представляет собой хлорид магния; однако, можно использовать также бромид магния и иодид магния. Подходящими источниками галогенидов являются галогениды магния, такие как MgBr2, MgCl2, MgI, или смешанные галогениды магния, такие как MgClI, MgClBr и MgBrI. В некоторых предпочтительных вариантах галогенид магния добавляют к растворителю в безводной форме. В других предпочтительных вариантах галогенид магния добавляют в гидратированной форме.
Электронно-донорное вещество добавляют к смеси растворителя и галогенида магния любым подходящим способом. Предпочтительно, электронно-донорное соединение добавляют непосредственно к смеси. В некоторых предпочтительных вариантах электронно-донорное вещество представляет собой спирт, тиол, слабодонорный амин или слабодонорный фосфин. Спирт может быть любым химическим соединением, имеющим общую формулу ROH. R может быть любой замещенной или незамещенной углеводородной группой. В некоторых предпочтительных вариантах спирт представляет собой алифатический спирт, включающий от примерно 1 до примерно 25 атомов углерода. В некоторых предпочтительных вариантах спирт представляет собой монодентатный спирт. В настоящем описании термин «монодентатный спирт» включает такие соединения, в которых R может быть получен таким образом, чтобы замещение не приводило к молекуле, содержащей более одной гидроксильной группы (ОН), которая координирует с атомом магния в растворе. Примеры таких спиртов могут включать метанол, этанол, пропанол, изопропанол и бутанол. Спирты, содержащие алифатические группы с более длинной цепью, такие как 2-этилгексанол или 1-додеканол, также образуют растворы, в которых растворимость галогенида магния повышается с температурой. Также можно использовать спирты, содержащие больше атомов углерода. Спирты могут также быть циклическими, такими как циклогенсанол, или ароматическими спиртами, такими как фенол.
В определенных предпочтительных вариантах отношение содержания электронно-донорного вещества к галогениду магния меньше или равно 1,9. В некоторых предпочтительных вариантах молярное отношение спирта к магнию меньше, чем примерно 1,75, меньше 1,5, меньше 1,0, меньше 0,75, меньше 0,5, меньше, чем примерно 0,4 или меньше, чем примерно 0,25. Еще в других предпочтительных вариантах молярное отношение донора электронов к магнию составляет примерно 0,1. В других предпочтительных вариантах молярное отношение может быть выше 1,9, например примерно 2,0, примерно 2,2, примерно 2,5 и примерно 3,0.
Добавление маленьких количеств одного электронно-донорного соединения, отличного от растворителя, к смеси, содержащей растворитель и галогенид магния, приводит к получению содержащей магний композиции, растворимость которой повышается с температурой и растворимость которой при температуре кипения растворителя относительно более высокая, чем растворимость аддуктов галогенид магния/донор электронов, в которых не присутствует электронно-донорное соединение. Растворимость также выше, чем растворимость сравнимых аддуктов галогенид магния/донор электронов, содержащих определенные виды электронно-донорных соединений. Высказано предположение, что добавление маленьких количеств одного донора электронов к растворителю в присутствии галогенидов магния подавляет конверсию растворимых частиц в полимерных аддуктах. В некоторых предпочтительных вариантах растворимые частицы имеют формулу
MgXx(ED)ySz,
где х обычно равно 2, что соответствует окислительному состоянию магния, у менее 4, и x+y+z меньше или равно 6. В некоторых предпочтительных вариантах у составляет примерно 0,5, 0,75, 1, 1,5, 1,75, 1,9 или менее. В некоторых других предпочтительных вариантах, у составляет примерно 0,1, 0,25, 0,3 или 0,4. Такие частицы обычно имеют растворимость в растворителе, которая повышается с температурой вплоть до температуры кипения растворителя. Если растворителем является ТГФ, концентрация галогенида магния в растворе может быть до пяти раз выше, чем в сравнимых растворах, не содержащих электронно-донорного соединения, особенно там, где электронно-донорным соединением является спирт.
На фиг.1 показан профиль растворимости растворов хлорида магния в тетрагидрофуране и спирте в зависимости от температуры. Как видно из фиг.1, композиции, не содержащие спирта, как правило, имеют растворимость галогенида магния, которая повышается от примерно 0,5 молей магния на литр до максимально менее чем примерно 0,65 молей магния на литр при 30°С. Выше 30°С растворимость постепенно снижается вплоть до достижения температуры кипения растворителя. Напротив, смеси, в которые был добавлен спирт, такой как этанол, имеют растворимость галогенида магния, которая не снижается при повышении температуры вплоть до температуры кипения растворителя. Например, в смесях, в которых отношение этанола к магнию составляет примерно 0,5, растворимость магния при 15°С составляет примерно 0,75 моль/л. Растворимость хлорида магния повышается с увеличением температуры до примерно 30°С, при которой концентрация магния в растворе составляет примерно 1,75 моль/л. При повышении температуры выше 30°С растворимость остается примерно постоянной вплоть до температуры кипения растворителя.
На фиг.1 также показана растворимость смесей, в которых отношение спирта к магнию составляет примерно 1. При 25°С концентрация магния, присутствующего в растворе, составляет примерно 0,5 моль/л. Однако концентрация повышается до примерно 2 моль/л к тому времени, когда температура достигает 55°С, и остается приблизительно постоянной вплоть до температуры кипения растворителя. В образцах, в которых молярное отношение спирта к магнию составляет два, растворимость магния также повышается с повышением температуры кипения вплоть до температуры кипения, при которой величина растворимости составляет 1,75 молей магния на литр.
На фиг.2 показан профиль растворимости нескольких смесей, содержащих различные количества добавленного спирта. Каждая точка в данных на фиг.2 была получена добавлением такого количества хлорида магния, которое необходимо для достижения желаемой концентрации, при которой весь хлорид магния растворен в ТГФ. Затем добавляли некоторое количество спирта, с тем чтобы получить требуемое соотношение спирт : магний, и смесь нагревали до растворения композиции. Затем раствор медленно охлаждали до начала образования осадка. Температуру, при которой начинал образовываться осадок, записывали на оси ординат на фиг.2. Таким образом, фиг.2 показывает температуру, необходимую для приготовления растворов хлорида магния различной концентрации в присутствии спирта. Например, ряд данных 210 представляет температуру, необходимую для получения раствора, содержащего 0,75 М хлорида магния, в котором растворителем является ТГФ, в присутствии различных концентраций этанола. В смесях, приготовленных при соотношении спирта и магния, составляющем 0,25, концентрация магния в растворе составляет примерно 0,75 М только при 5°С. Смеси, приготовленные при соотношении спирта к хлориду магния 0,5, достигают концентрации в 0,75 М по магнию при примерно 15°С, в то время как смеси с соотношением 1,0 достигают концентрации 0,75 М при примерно 33°С. Если смеси приготовлены так, что отношение спирта к хлориду магния составляет 1,5 или 2,0 молей, концентрация магния в растворе 0,75 М достигается при 47 и 53°С соответственно. Таким образом, ряд данных 210 показывает, что смеси с более высоким отношением спирт : магний становятся менее растворимыми.
Таким образом, на фиг.2 показано, что меньшие отношения спирта к хлориду магния дают растворы с большей концентрацией растворенного магния. Снижение растворимости с повышением отношения ROH/MgCl2 предполагает, что маленькие количества добавленного ROH предотвращают образование полимерного аддукта MgCl2(ТГФ)2, а добавление больших количеств ROH или дополнительного количества спиртов способствует образованию в растворе менее растворимых аддуктов, содержащих больше ROH. Используемое соотношение ROH/Mg определяет максимум растворимости, который можно достичь при нужной температуре. Ряды данных 220-260 на фиг.2 показывают, что для данного отношения спирт : магний повышение температуры увеличивает количество растворимого магния. Например, растворы, имеющие молярное отношение спирт : магний 0,5, содержат концентрацию магния примерно 0,75 М при примерно 15°С, в то время как при 20°С в растворе можно достичь концентрации магния 1,0 М. Линия 230 показывает, что при примерно 23°С тот же раствор может растворить примерно 1,25 моль/л хлорида магния. Фиг.2 также показывает, что растворимость хлорида магния в таких растворах также повышается до температуры примерно 30°С. Например, растворы, в которых молярное отношение спирта к магнию составляет 1, демонстрируют, что при температуре примерно 35°С растворимость хлорида магния составляет примерно 0,75 М, в то время как при примерно 41°С растворимость повышается до примерно 1М. Данные кривых 230-260 показывают, что растворимость продолжает повышаться по мере приближения к температуре кипения ТГФ. Растворы, имеющие более высокие отношения спирт:магний, проявляют сходное поведение.
Природа частиц, присутствующих в растворе, была выяснена с использованием разнообразных методов определения. Исследования методом ЯМР показывают, что доноры электронов, координированные с MgCl2 в растворе ТГФ, находятся в быстром равновесии, причем индивидуальные долгоживущие частицы отсутствуют. Газовая фаза над раствором ТГФ, содержащим MgCl2 и 2 эквивалента этанола (EtOH) на Mg, содержит существенно меньше спирта, чем газовая фаза над тем же раствором EtOH/ТГФ, не содержащим MgCl2. Это заставляет предположить, что этанол изолирован молекулой MgCl2 в растворе. Видимо, спиртовая группа координирована с центром MgCl2 в фазе раствора. Максимальная растворимость при средних соотношениях спирт : MgCl2 означает, что в растворе существуют различные частицы, концентрация которых зависит от природы спирта, удельного отношения спирта и от температуры раствора.
На фиг.3 показана рентгеновская структура изолированного кристалла одного из компонентов катализатора, выделенного в виде твердого вещества. Как показано на фиг.3, этот компонент включает молекулу с магнием в центре. В предпочтительном варианте осуществления изобретения предшественник содержит две молекулы растворителя - ТГФ, связанные с магнием, а также два галогена в виде хлора и два спиртовых лиганда. Таким образом, компонент имеет формулу MgCl2ROH2ТГФ2, где ROH представляет собой изопропиловый спирт. Также были выделены подобные соединения, в которых ROH представляет собой этанол. В этом конкретном примере представленную структуру обычно называют транс-октаэдрической магний-центрированной структурой, поскольку лиганды одного вида связаны через центр симметрии - атом магния. Однако такая структура не является обязательной для любого предпочтительного варианта компонента катализатора. В других предпочтительных вариантах компонент может включать смеси одного или более индивидуальных соединений. В других предпочтительных вариантах компонент может включать смеси MgCl2ROH1ТГФ3 и MgCl2ROH2ТГФ2. Любое число индивидуальных соединений может быть представлено так, чтобы смесь в целом удовлетворяла формуле MgXx(ED)ySz, где у меньше или равно 1,9.
В других предпочтительных вариантах компонент катализатора на основе галогенида магния имеет формулу MgX2(ED)ySz, где y+z меньше или равно 4, у меньше или равно 1,9. В таких предпочтительных вариантах, где y+z меньше 4, компонент катализатора может рассматриваться как дефицитный в отношении растворителя. Эти композиции можно также назвать нестехиометрическими композициями. Такие композиции можно получить в твердом виде из полностью координированного MgCl2(ROH)2(ТГФ)2 или другой композиции состава MgXx(ED)ySz путем нагревания, применения пониженного давления или комбинации обоих способов.
На фиг.4 показаны результаты термогравиметрического анализа (ТГА) для MgCl2(ROH)2(ТГФ)2. ТГА проводили при скорости нагрева 10°С/мин в тех областях, когда потери массы не отмечалось. В тех областях, когда образец терял массу, температуру поддерживали постоянной до тех пор, пока изменение массы прекращалось. На фиг.4 показано, что большая часть растворителя и спирта может быть удалена путем нагревания композиции до 50-200°С, причем сначала удаляется одна молекула ТГФ, затем как ROH, так и ТГФ. Таким образом можно получить разнообразные пористые содержащие MgCl2 композиции, пригодные для образования пористых компонентов катализаторов. Таким образом, в некоторых предпочтительных вариантах компонент катализатора может иметь координационно-ненасыщенную и полимерную, а не мономерную, структуру.
В другом аспекте применяется способ приготовления компонентов катализатора, описанный выше. Способы приготовления компонентов катализатора включают введение растворителя, контактирование галогенида магния с растворителем и добавление электронно-донорного соединения, с целью образования компонента катализатора полимеризации. В некоторых предпочтительных вариантах молярное отношение донора электронов к магнию меньше или равно 1,9. В других предпочтительных вариантах, особенно когда электронно-донорное соединение является спиртом, отношение спирта к магнию может быть выше 1,9, таким как примерно 2,0, примерно 2,1, примерно 2,2, примерно 2,5 или примерно 3,0. В некоторых предпочтительных вариантах способ может также включать выделение компонента катализатора полимеризации. Предпочтительные варианты способа могут также вкл