Средство на основе лигнина, обладающее антиоксидантной активностью
Иллюстрации
Показать всеИзобретение относится к фармацевтической промышленности и используется в качестве средства, обладающего антиоксидантной активностью. Средство, обладающее антиоксидантной активностью, содержит водорастворимый лигнин, полученный из природного растительного материала, причем водорастворимый лигнин выделяют посредством обработки лигнинсодержащего сырья водным диоксаном в присутствии HCl при температуре кипения с последующей обработкой диоксанлигнина раствором щелочи до полного растворения, настаиванием щелочного раствора с катионитом до определенного значения рН. Средство, полученное вышеописанным способом из лигнинсодержащего растительного сырья, обладает высокой антиоксидантой активностью. 2 ил., 2 табл.
Реферат
Изобретение относится к медицинской промышленности, биохимии и химии высокомолекулярных соединений, а именно к антиоксидантам на основе лигнина.
Известно применение мальтало - продукта переработки древесной зелени пихты в качестве антиоксидантного средства (патент РФ №2178303).
Известно антиоксидантное средство - дигидрокверцетин, полученный из измельченной древесины лиственницы (патент РФ 2014841).
Недостатком вышеуказанных аналогов является ограничение ореола обитания растительного сырья и как следствие ограничение сырьевой базы.
Известны способы получения медицинского лигнина (патенты РФ №1290583, №2131262, А.С. №919186), основное назначение которого - применение в качестве сорбента.
В настоящее время широкое распространение имеет препарат «Полифепан» (Polyphepanum) - неспецифический энтеросорбент (рег. №80/1211/3), который применяется при острых и хронических заболеваниях желудочно-кишечного тракта и экзогенных отравлениях.
Известен водорастворимый лигнин, описанный в заявке ЕР 94256 А2, 16.11.1983, выбранный за прототип. Выделение лигнина осуществляется посредством культивирования на лигноцеллюлозном материале микроорганизмов рода Streptomyces, обладающих лигнинолитической активностью, с последующей экстракцией культуральной среды с биодеградированным лигнином водным растворителем. Затем проводится осаждение деградированного лигнина кислотой. Лигнин модифицируется для придания ему антиоксидантных свойств за счет увеличения количества фенольных гидроксилов и уменьшения числа функциональных групп, снижающих антиоксидантную активность.
Недостатком наиболее близкого аналога является то, что выделенный лигнин представляет собой биодеградированный препарат, который относится к сильноизмененным лигнинам, отличающимся по строению и свойствам от природного лигнина. Такой водорастворимый лигнин может быть вреден для человека, т.к. получен с помощью микроорганизмов, которые неконтролируемо могут менять химическую природу лигнина.
Задачей, на решение которой направлено настоящее изобретение, заключается в расширении арсенала средств, обладающих высокой антиоксидантной активностью.
Технический результат состоит в том, что полученный препарат является малоизмененным природным препаратом и обладает 100% растворимостью в воде. Кроме того, процесс выделения водорастворимого лигнина по времени является быстрым в сравнении с прототипом.
Технический результат достигается тем, что средство, обладающее антиоксидантной активностью, содержит водорастворимый лигнин, полученный из природного растительного материала, согласно изобретению водорастворимый лигнин выделяют посредством обработки лигносодержащего сырья водным диоксаном в присутствии HCl при температуре кипения с последующей обработкой диоксанлигнина раствором щелочи до полного растворения, настаиванием щелочного раствора с катионитом до рН 7.
Лигнин является источником биологически активных веществ с весьма разнообразным набором полезных свойств для использования в медицине, ветеринарии, растениеводстве, косметологии (Опыт доклинического исследования на примере Олипифата / Под ред. В.А.Филова, А.М.Берковича. - СПб: НИКА, 2002. - 288 с.). Лигнин относится к природным полифенолам и является одним из основных компонентов растительной ткани практически всех наземных растений. Содержание лигнина в древесине хвойных пород составляет 25-30, лиственных - 19-24, травянистых - 17-23%. Лигнины наряду с целлюлозой, гемицеллюлозами и пектинами являются обязательной составной частью пищевых волокон и с продуктами питания растительного происхождения неизбежно попадают в желудочно-кишечный тракт человека. Содержание лигнина (%) в пищевых волокнах некоторых продуктов переработки зерновых составляет: темная мука - 10, непросеянная мука - 6, отруби обработанные - 7, овсяная крупа - 6; в овощах: капуста зимняя - 13, капуста белая - 11; в съедобной части фруктов и ягод: бананы - 15, грейпфрут - 13, апельсины - 15, груша - 19, слива - 19, клубника - 38 (Дудкин М.С., Казанская И.С., Базилевский А.С. Пищевые волокна (Обзор) // Химия древесины, 1984. - №2. - С.3-14).
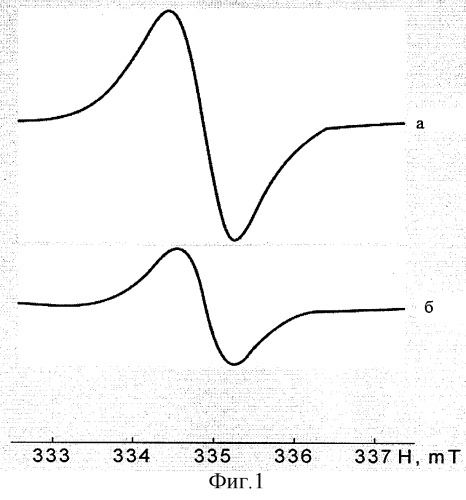
Характерной чертой макромолекул лигнинов является наличие феноксильных радикалов. Присутствие стабильных феноксильных радикалов обусловливает уникальную особенность лигнина как природного полимера проявлять парамагнитные свойства. Как показывают наши исследования, сигналы ЭПР лигнина, выделенного из овса и пшеницы, представляют собой практически изотропные синглеты с g-фактором ˜2 (фиг.1 и табл.1). Это дает основания нам утверждать, что лигнины - биополимеры растительного происхождения, структурной единицей и активным началом которого является фенилпропановая единица (ФПЕ):
обладают антиоксидантными свойствами, т.е. они способны тормозить или устранять свободнорадикальное окисление клеток организма, вступая в реакцию рекомбинации с продуктами превращения кислорода - свободными радикалами являющимися одной из основных причин возникновения и развития патологических заболеваний, в том числе онкологических.
Основной характеристикой антиоксидантов является величина суммарного показателя антиоксидантной активности (АОА). При этом необходимым условием для эффективного проявления препаратом антиоксидантных свойств является его водорастворимость. Все известные препараты медицинского лигнина в воде практически не растворимы.
Известен водорастворимый лигнин, способ получения которого (А.С. СССР 186468) заключается в том, что сульфатный лигнин, выделенный путем насыщения черного щелока углекислым газом и обессмоленный с помощью соляной кислоты, растворяют в водной щелочи при 80-100°С и выдерживают при этой температуре не менее 20-30 мин, затем разбавляют водой до концентрации 0,1-3,0% (по лигнину), фильтруют, пропускают через колонку с катионитом для удаления золы и катионов, а также для гидратации лигнинов и получают водный раствор лигнина с рН 3,0-3,5. Добавив щелочь, можно довести рН раствора до 5,5-6,0.
В качестве исходного сырья используют сульфатный лигнин - отход сульфатного производства целлюлозы, который по химической структуре и свойствам отличается от нативного лигнина.
Наиболее предпочтительным является получение водорастворимого лигнина (водного раствора лигнина) из природного растительного материала, не требующего предварительной стадии технологической переработки, связанной с применением высоких давлений, сложного оборудования и больших энергозатрат. Природный водорастворимый лигнин, наиболее близкий по химической структуре и свойствам к нативному лигнину, проявляет ярко выраженную антиоксидантную активность.
Способ получения антиоксидантного средства из природного лигносодержащего сырья осуществляется следующим образом.
Из измельченного и обессмоленного растительного лигносодержащего сырья выделяют препарат диоксанлигнин с помощью обработки водным диоксаном в присутствии HCl при температуре кипения. Затем получают водорастворимые формы диоксанлигаинов путем обработки их раствором щелочи с последующим взаимодействием с избытком катионообменной смолы для замещения катиона H+ на Na+ (перевод в Н-форму) при постоянном контроле рН до достижения значения рН 7. В результате получают водный раствор природного лигнина или водорастворимый препарат лигнина (т.е. лигнин с растворимостью в воде 100%).
Водные растворы лигнина характеризуются:
- прозрачностью раствора;
- отсутствием хлопьев, крупных взвешенных частиц и мути.
В качестве исходного лигнинсодержащего материала используются: зрелые стебли (солома) овса Avena saliva L.; овса Avena sativa L., модифицированного щелочью; пшеницы Triticum sp.; овсяницы луговой Festuca pratensis Huds.; биомасса травянистых растений (фуражное сено), модифицированное ферментным препаратом целловиридином ГЗх; зрелые стебли амаранта Amaranthus sp.; древесина рябины Sorbus aucuparia; акации Robmia pseudoacacia и лиственницы Larix sibirica. Для сравнения используется медицинский лигнин (Полифепан). По нашим данным содержание лигнина Комарова в среднем: солома овсяная - 22,5%; солома овса модифицированная - 15,0%; солома пшеницы - 22,0%; солома овсяницы луговой - 18,9%; сено модифицированное - 25,7% (содержание лигнина в исходном сене 19,2%); стебли амаранта - 21,4%; древесина рябины - 20,1; акации - 22,7; лиственницы - 31,2; медицинский лигнин - 95,6% (трудногидролизуемые полисахариды, зола - остальное). Содержание лигнина определяли по методу Комарова, применяемому в химии древесины в качестве стандартной методики для количественного извлечения лигнина и соединений фенольной природы (Оболенская А.В., Ельницкая З.П., Леонович А.А. Лабораторные работы по химии древесины и целлюлозы / Учебное пособие для вузов. - М.: Экология, 1991. - 320 с.).
Модификация щелочью проводилась для частичной делигнификации исходного растительного материала. Цель - установление влияния количественного содержания лигнина на величину АОА препарата.
Модификация ферментным препаратом целловиридином ГЗх, обладающего как целлюлазной, так и ксиланазной активностями, проводилась для увеличения содержания лигнина в исходном растительном материале за счет разрушения целлюлозы и гемицеллюлоз. Цель - установление влияния количественного содержания лигнина на величину АОА препарата.
Изобретение проиллюстрировано таблицами и графическими материалами, на которых:
- табл.1 - параметры спектров ЭПР и концентрация парамагнитных центров в различных образцах лигнина;
- табл.2 - антиоксидантная активность лигнина;
- на фиг.1 представлены спектры ЭПР препаратов овса и пшеницы (а) и (б);
- на фиг.2 представлена антиоксидантная активность образцов лигнина.
Ниже приведены примеры получения антиоксиданта на основе лигнина.
Пример 1. Навеску воздушно-сухой измельченной овсяной соломы массой 5 г с размерами частиц 0,5-2,0 мм заливают спирто-бензольной смесью в соотношении солома : спирто-бензольная смесь - 1:2 и экстрагируют в течение 6 часов. Затем проводят экстракцию холодной водой в объеме 500 мл в течение 48 часов, после чего обрабатывают горячей водой в объеме 250 мл в течение 3 часов. Проэкстрагированное сырье обрабатывают водным диоксаном 9:1 в присутствии HCl (0,7%) при температуре кипения. Очистку препарата проводят двукратным переосаждением из диоксана в диэтиловый эфир. Высушивают методом лиофильной сушки. Навеску полученного диоксанлигнина массой 1 г заливают 40 мл 0,1 н. щелочи NaOH и выдерживают в течение 1 ч, затем добавляют 40 мл воды и 4 г катионообменной смолы КУ-2. Процесс осуществляют при перемешивании на магнитной мешалке и при постоянном контроле величины рН с помощью рН-метра до достижения рН 7. При достижении рН 7 смолу отфильтровывают на бумажном фильтре «синяя лента». Раствор анализируют на АОА. Все стадии проводятся при атмосферном давлении. Данные приводятся в таблице 2 и на фиг.2.
Пример 2. Способ осуществляют аналогично примеру 1, но в качестве исходного сырья используют овсяную солому, модифицированную щелочью. Для этого к размолотой проэкстрагированной соломе массой 10 г добавляют 100 мл 7 н. NaOH и выдерживают в течение 24 час при комнатной температуре. Затем отфильтровывают на пористом стеклянном фильтре, промывают водой до нейтральной реакции промывных вод. Обработку оставшегося на фильтре вещества ведут по примеру 1. Данные в табл.2 и на фиг.2.
Пример 3. Способ осуществляют аналогично примеру 1, но в качестве исходного сырья используют пшеничную солому. Данные приводятся в табл.2 и на фиг.2.
Пример 4. Способ осуществляют аналогично примеру 1, но в качестве исходного сырья используют овсяницу луговую (стебель). Данные приводятся в табл.2 и на фиг.2.
Пример 5. Способ осуществляют аналогично примеру 1, но в качестве исходного сырья используют сено, модифицированное ферментным препаратом целловиридином ГЗх. Для этого к 190 мл дистиллированной воды добавляли 10 г размолотого до порошкообразного состояния сена, смесь перемешивали, затем добавляли 10 г порошка целловиридина, опять перемешивали. После 24 часов ферментативного гидролиза смесь фильтровали через бумажный фильтр под вакуумом. Осадок субстрата на фильтре промывали дистиллированной водой многокрартной декантацией для очистки от примеси ферментного препарата, затем высушивали при 60°С. Далее по примеру 1. Данные приводятся в табл.2 и на фиг.2.
Пример 6. Способ осуществляют аналогично примеру 1, но в качестве исходного сырья используют амарант (стебель). Данные приводятся в табл.2 и на фиг.2.
Пример 7. Способ осуществляют аналогично примеру 1, но в качестве исходного сырья используют рябину. Данные приводятся в табл.2 и на фиг.2.
Пример 8. Способ осуществляют аналогично примеру 1, но в качестве исходного сырья используют акцию. Данные приводятся в табл.2 и на фиг.2.
Пример 9. Способ осуществляют аналогично примеру 1, но в качестве исходного сырья используют лиственницу. Данные приводятся в табл.2 и на фиг.2.
Пример 10: Навеску воздушно-сухого медицинского лигнина (Полифепана) массой 1 г заливают 40 мл 0,1 н. щелочи NaOH и выдерживают в течение 1 ч, затем добавляют 40 мл воды и 4 г катионообменной смолы КУ-2. Процесс осуществляют при перемешивании на магнитной мешалке и при постоянном контроле величины рН с помощью рН-метра до достижения рН 7. При достижении рН 7 смолу вместе с нерастворившейся частью отфильтровывают на бумажном фильтре «синяя лента». Раствор анализируют на АОА. Все стадии проводятся при атмосферном давлении. Данные приводятся в табл.2 и на фиг.2.
Электронный парамагнитный резонанс соединений изучали на серийном радиоспектрометре SE/X-2547 (RadioPAN, Poland) в Х-частотном диапазоне с ВЧ модуляцией 100 кГц при комнатной температуре образцов, мощность СВЧ поля - 2,2 мВт. Применяли прямоугольный резонатор RX102 с модой ТЕ 102. Оценку концентрации свободных радикалов производили с помощью эталонных образцов дифенилпикрилгидразила с количеством спинов (7,0±0,7)×1016 спин/г и (2,7±0,3)×1018 спин/г. Погрешность определения концентрации радикалов - 15%.
Оценку антиоксидантной активности проводили методом кулонометрического титрования (Абдуллин И.О., Чернышева Н.Н., Зиятдинова Г.К., Лапин А.А. Способ определения интегральной антиоксидантной емкости продуктов питания и напитков // Заявка на патент РФ 2003132741/13 от 10.11.2003). Метод базируется на кулонометрическом титровании химических веществ электрогенерированными соединениями брома (Br3 -, Br2, Br•). Количество электричества в кулонах, затрачиваемое на 100 г продукта, рассчитывали по формуле: Q=(100I×t)/Vал, где I - сила тока; t - время достижения конечной точки титрования; Vал - объем аликвотны.
Полученные данные свидетельствуют о том, что водорастворимые препараты лигнина, выделенные из природного растительного сырья, обладают ярко выраженной антиоксидантной активностью. Выявлена зависимость между количественным содержанием лигнина в исходном сырье и антиоксидантной активностью препаратов на его основе. Так, частичная делигнификация растительного сырья ведет к снижению величины АОА (примеры 1 и 2). Модификация растительного сырья, приводящая к повышению содержания лигнина за счет ферментативной деструкции целлюлозы и гемицеллюлоз, позволяет получить препарат с высокими значениями АОА (пример 5). Использование в качестве сырьевого источника сильноизмененного технического лигнина не приводит к количественному переводу лигнина в растворимую форму, что выражается в низких значениях АОА (пример 10).
Поскольку структурной единицей всех лигнинов является фенилпропановая единица (ФПЕ), то согласно полученным результатам именно ФПЕ благодаря наличию свободных стабильных радикалов служит активным началом и сообщает препаратам на основе лигнина свойства антиоксидантов.
Природные лигнины могут быть рекомендованы для использования в медицине, фармакологии, ветеринарии, пищевой и парфюмерной промышленности с целью получения препаратов лечебного и профилактического назначения, обладающих высокой антиоксидантной активностью.
| Таблица 1.Параметры спектров ЭПР и концентрация парамагнитных центров в различных образцах лигнина | |||
| Образцы | g-фактора | ΔН, мТл | Концентрация,1017 спин/г* |
| ДЛ-О | 2,0044 | 0,78 | 2,2 |
| ДЛ-П | 2,0042 | 0,81 | 1,2 |
| Обозначения: ДЛ-О - диоксанлигнин овса; ДЛ-П - диоксанлигнин пшеницы. |
| Таблица 2.Антиоксидантная активность (АОА) лигнинов (n=5 р=0.95) | |||
| Сырьевой источник | № примера | АОЕ, кКл/100 г | |
| Х±S | Sr | ||
| Овес (солома) | Пример 1 | 69,4±2,8 | 0,04 |
| Овес (солома) модифицированный | Пример 2 | 23,6±0,2 | 0,01 |
| Пшеница (солома) | Пример 3 | 61,3±2,1 | 0,03 |
| Овсяница луговая (солома) | Пример 4 | 41,5±2,8 | 0,07 |
| Сено модифицированное | Пример 5 | 72,7±4,3 | 0,06 |
| Амарант (стебель) | Пример 6 | 57,0±2,8 | 0,05 |
| Рябина | Пример 7 | 50,6±4,3 | 0,08 |
| Акация | Пример 8 | 37,0±1,5 | 0,04 |
| Лиственница | Пример 9 | 45,8±2,4 | 0,05 |
| Лигнин медицинский (на основе технического гидролизного лигнина) | Пример 10 | 1,7±0,1 | 0,04 |
Средство, обладающее антиоксидантной активностью, содержащее водорастворимый лигнин, полученный из природного растительного материала, отличающееся тем, что водорастворимый лигнин выделяют посредством обработки лигнинсодержащего сырья водным диоксаном в присутствии HCl при температуре кипения, с последующей обработкой диоксанлигнина раствором щелочи до полного растворения, настаиванием щелочного раствора с катионитом до рН 7.