Геранильные соединения, фармацевтическая композиция на их основе и применение
Иллюстрации
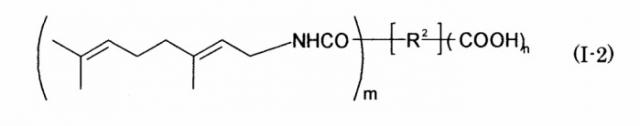
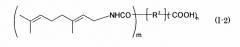
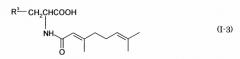
Показать всеИзобретение относится к геранильным соединениям, представленным следующими формулами (I-1), (I-2) или (I-3):
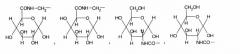
в которых R1 означает
R2 означает остаточную группу, остающуюся после удаления всех карбоксильных групп, присутствующих в карбоновой кислоте, выбранной из группы, состоящей из яблочной кислоты, лимонной кислоты, янтарной кислоты, фумаровой кислоты, и т.д., m равно 1, 2 или 3, n равно 0, 1 или 2, причем m+n представляет число карбоксильных групп, которые присутствуют в указанной карбоновой кислоте, и R3 обозначает п-гидроксифенил или меркаптогруппу. Изобретение относится к производным мевалоновой кислоты, представленным следующей формулой (1-4):
в которой R4 обозначает -СН2ОН или СН3. Изобретение относится к противоопухолевому средству, содержащему в качестве активного ингредиента геранильное соединение формулы (I-1), (I-2) или (I-3), или производное мевалоновой кислоты формулы (I-4), и необязательно фармацевтически приемлемый носитель или растворитель. Изобретение также относится к способу лечения рака печени за счет геранильного соединения формул (I-1), (I-2) или (I-3), или производного мевалоновой кислоты формулы (I-4) и применению данных соединений для производства противоопухолевого средства. Технический результат - геранильные соединения или производные мевалоновой кислоты, в качестве противоопухолевых средств. 6 н.п. ф-лы, 3 табл.
Реферат
Область техники
Данное изобретение относится к новым геранильным соединениям или производным мевалоновой кислоты, и их использованию в качестве противоопухолевых средств.
Предпосылки создания изобретения
Многие геранильные соединения, имеющие 1,5-диеновую структуру, присутствуют in vivo и, как известно, in vivo являются предшественниками веществ, имеющих полиеновую структуру и проявляющих различное физиологическое действие. Данные вещества, имеющие 1,5-диеновое строение, и производные от них полиены, неизменно происходят от мевалоновой кислоты и получаются путем биосинтеза.
Обращено внимание на такие геранильные соединения, имеющие 1,5-диеновое строение, гераниевую кислоту или гераниламин, и, кроме того, мевалоновую кислоту, которая является основой для биосинтеза полиенов, синтезированы различные производные гераниевой кислоты или гераниламина и мевалоновой кислоты, и исследована их физиологическая активность, в частности противоопухолевая активность, и токсичность, и совершено данное изобретение.
Описание изобретения
Данное изобретение представляет геранильные соединения, представляемые следующими формулами (I-1), (I-2) или (I-3):
в которых
R1 означает
R2 означает остаточную группу, остающуюся после удаления всех карбоксильных групп, присутствующих в карбоновой кислоте, выбранной из группы, состоящей из яблочной кислоты, лимонной кислоты, янтарной кислоты, фумаровой кислоты, 2-оксоглютаровой кислоты, пировиноградной кислоты, п-пирувоаминобензойной кислоты, ретиноевой кислоты, тирозина, цистеина, глютаминовой кислоты и серина, и когда гидроксильная(ые) или аминогруппы присутствуют в остаточной группе, они могут быть необязательно защищены ацилом (например, низшим алканоилом) или бензилоксикарбонильной(ыми) группой(ами),
m равно 1, 2 или 3,
n равно 0, 1 или 2,
m+n вместе показывают число карбоксильных групп, которые присутствуют в указанной карбоновой кислоте, и
R3 означает п-гидроксифенильную или меркаптогруппу.
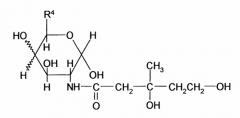
Данное изобретение представляет также производные мевалоновой кислоты, представляемые следующей формулой (I-4):
(I-4)
в которой R4 означает -СН2ОН или -СН3.
Эти геранилсахаридные производные вышеприведенной формулы (I-1) включают следующие пять соединений:
N-геранилглюкуронамид
N-геранилгалактуронамид
N-галактозилгеранамид
N-глюкозилгеранамид
и N-фукозогеранамид
Гераниламидные производные представленной выше формулы (I-2) включают, например, следующие соединения.
N,N'-дигераниляблочный диамид
О-ацетил-N-гераниляблочный моноамид
О-ацетил-N,N'-дигераниляблочный диамид
N,N',N''-тригераниллимонный триамид
N-геранилянтарный моноамид
N,N'-дигеранилянтарный диамид
N,N'-дигеранилфумаровый диамид
N-геранилфумаровый моноамид
N,N'-дигеранил-2-оксоглютаровый диамид
N-геранилпирувамид
N-геранил-п-пируваминобензамид
Тирозингераниламид
N-ацетилтирозингераниламид
Цистеингераниламид
Глютаминовый дигеранилдиамид
Серингераниламид
и N-геранилретинамид
А также гераниламидные производные вышеприведенной формулы (I-3) включают следующие два соединения:
N-гераноилтирозин
и N-гераноилцистеин
Производные мевалоновой кислоты приведенной выше формулы (I-4) включают, например, следующие:
N-глюкозилмевалонамид
N-галактозилмевалонамид
и N-фукозомевалонамид
(27)
Среди соединений формулы (I-1), соединения формул (1) и (2) можно получить, например, подвергая гераниламин реакции амидирования с реактивными производными (например, смешанным ангидридом кислоты, активным сложным эфиром, галогенангидридом или тому подобным) глюкуроновой кислоты или галактуроновой кислоты, гидроксильные группы которой защищены ацильными группами (например, ацетилом).
Из соединений формулы (I-1), соединения формул с (3) по (5) можно получить, например, подвергая реактивные производные гераниевой кислоты (например, смешанные ангидрид кислоты, активный сложный эфир, галогенангидрид или тому подобное) реакции амидирования с помощью галактозамина, глюкозамина или фукозамина.
Указанная реакция амидирования может быть проведена по обычной в области пептидной химии методике реакции амидирования, обычно в адекватном инертном органическом растворителе (например, тетрагидрофуране, хлороформе, N,N-диметилформамиде, дихлорметане или тому подобном) или в воде при охлаждении до примерно 0°С или нагревании до примерно 60°С, предпочтительно, при от примерно 0°С до комнатной температуры.
Используемое отношение гераниламина к реактивному производному глюкуроновой кислоты или галактуроновой кислоты, гидроксильные группы которой защищены, строго не ограничивается, но обычно предпочтительно использовать гераниламин в пределах 1-2 молей на моль реактивного производного.
Используемое отношение галактозамина, глюкозамина или фукозамина к реактивному производному гераниевой кислоты также строго не ограничено, но обычно предпочтительно использовать галактозамин, глюкозамин или фукозамин в пределах 1-2 молей на моль реактивного производного.
Когда присутствуют защищающие гидроксил группы, после реакции амидирования указанные защитные группы удаляют с помощью реакции удаления защиты, такой как гидролиз, с получением геранилсахаридных производных формулы (I-1).
Геранилсахаридные производные формулы (I-1), получаемые посредством вышеприведенных реакций, могут быть выделены из реакционных смесей и очищены обычными способами, например, экстрагированием, кристаллизацией, хроматографией и тому подобного.
Гераниламидные производные вышеприведенной формулы (I-2) можно получить, например, проведением реакции амидирования гераниламина с реактивными производными (например, смешанными ангидридом кислоты, активным сложным эфиром, галогенангидридом и тому подобным) карбоновой кислоты, представляемой формулой (II):
в которой R2, m и n имеют ранее представленные значения, у которых гидроксильная(ые) или аминогруппа(ы) защищена(ы) ацилом (например, низшим алканоилом, таким как ацетил), бензилоксикарбонилом и тому подобными группами.
Указанная реакция амидирования может быть проведена по обычной в области пептидной химии методике реакции амидирования, обычно в подходящем инертном органическом растворителе (например, тетрагидрофуране, простом эфире, дихлорметане, хлороформе, N,N-диметилформамиде и тому подобном) при охлаждении до примерно 0°С или нагревании до примерно 60°С, предпочтительно, при от примерно 0°С до комнатной температуры.
Используемое отношение гераниламина к реактивному производному карбоновой кислоты формулы (II) изменяется в зависимости от числа геранильных групп (m), которые нужно ввести в карбоновую кислоту, тогда как обычно предпочтительно использовать отношение в интервале от 1 моля до (m+2) молей на моль реактивного производного.
Когда присутствуют защищающие гидроксил или аминогруппы, после реакции амидирования их удаляют, когда необходимо, с помощью реакции удаления защиты, такой как гидролиз, с получением гераниламидных производных формулы (I-2).
Эти гераниламидные производные формулы (I-3) можно также получить, например, подвергая реактивные производные гераниевой кислоты (например, смешанные ангидридкислоты, активный сложный эфир, галогенангидрид и тому подобное) реакции амидирования с тирозином или цистеином.
Эту реакцию амидирования можно также проводить по обычной в области пептидной химии методике реакции амидирования, обычно в адекватном инертном органическом растворителе (например, тетрагидрофуране, простом эфире, дихлорметане, хлороформе, N,N-диметилформамиде и тому подобном) или в воде при охлаждении до примерно 0°С или нагревании до примерно 60°С, предпочтительно, при от примерно 0°С до комнатной температуры.
Используемое отношение тирозина или цистеина к реактивному производному гераниевой кислоты строго не ограничено, но обычно предпочтительно использовать одно из интервала в пределах 1-2 молей на моль реактивного производного.
Такие гераниламидные производные формулы (I-2) или (I-3), полученные при вышеприведенных реакциях, могут быть выделены из реакционных смесей и очищены обычными методами, например, экстрагированием, кристаллизацией, хроматографией и тому подобными.
Производные мевалоновой кислоты формулы (I-4) можно получить, например, по реакции аминосахара, представляемого следующей формулой:
в которой R4 имеет представленное ранее значение, или его соли с мевалолактоном или мевалоилгалогенидом.
Указанная реакция аминосахара формулы (III) или его соли с мевалолактоном или мевалоилгалогенидом (например, мевалоилхлоридом) может быть проведена в воде или подходящем инертном органическом растворителе (например, N,N-диметилформамиде, тетрагидрофуране, хлороформе или тому подобном) при температуре между комнатной температурой и температурой кипения растворителя, предпочтительно, от примерно 40°С до примерно 70°С.
Используемое отношение мевалолактона или мавалоилгалогенида к аминосахару формулы (III) строго не ограничено, но обычно предпочтительно использовать 1-2 моля мевалолактона или мевалоилгалогенида на моль аминосахара формулы (III).
Когда соль аминосахара формулы (III) или мевалоилгалогенид используют в качестве исходного вещества, обычно желательно проводить вышеприведенную реакцию с добавлением основания, например третичного амина, такого как N-метилпиперидин; или неорганического основания, такого как гидроксид натрия, гидроксид калия, карбонат калия и тому подобное.
Производные мевалоновой кислоты формулы (I-4), полученные по вышеприведенным реакциям, могут быть выделены из реакционных смесей и очищены обычными методами, такими как экстрагирование, кристаллизация, хроматография и тому подобное.
Соединения формул с (I-1) по (I-4), предложенные данным изобретением, обладают превосходной противоопухолевой активностью, что ясно из следующей оценки противоопухолевого эффекта.
Оценка противоопухолевого эффекта
Клетки карциномы HuH-7 (штамм дендриформных клеток человеческой гепатомы), имплантированные или субимплантированные под кожу на спине 5-недельным самкам "голых" мышей (BALB/с, Ninox), извлекали асептически и дробили на кусочки размером 5·5 мм в забуферном фосфатном растворе (PBS, ФСБ), часть из которых затем имплантировали под кожу на спине "голым" мышам.
Каждое испытуемое вещество растворяли в кукурузном масле и раствор вводили внутрибрюшинно "голой" мыши последовательно, один раз в день со скоростью 250 мкг/мышь в течение 3 недель, начиная со срока через неделю после имплантации. После прекращения введения карциномы извлекали и производили взвешивания для расчета противоопухолевого эффекта и потери веса мыши по следующим уравнениям. Для испытания использовали шесть мышей на группу; группа, которой вводили только растворитель (кукурузное масло), представляла собой контрольную группу:
Противоопухолевый эффект (%)
Средний вес опухоли испытуемой группы
=――――――――――――――――――――――――― · 100
Средний вес опухоли контрольной группы
Потеря веса (%)
Средний вес тела мышей испытуемой группы
=―――――――――――――――――――――――――― · 100
Средний вес тела мышей контрольной группы
Оценки противоопухолевого эффекта и потери веса проводили по следующему стандарту, где значения для контрольной группы принимали за 100%.
Противоопухолевый эффект
-: > 100%, +/-: 100˜75%, +:75˜50%, ++:50˜25%, +++:25˜0%
Потеря веса
-: > 110%, +/-: 110˜100%, +: 100˜95%, ++:95˜90%, +++:<90%
Степень гибели
(степень гибели во время периода испытания)
-: ни одной
+/-: гибель происходила при введении высокой концентрации
(500 мкг/мышь)
+: 1-3 мыши погибли
++: 3-5 мышей погибли
+++: все 6 мышей погибли
Синтетическая оценка
-: слабый противоопухолевый эффект и очень сильная токсичность в отношении мыши-хозяина
+/-: регистрируемый слабый противоопухолевый эффект и токсичность для мыши-хозяина тоже наблюдается
+: видимый фиксированный уровень противоопухолевого эффекта, но токсичность для мыши-хозяина также сильная
++: видимый сильный противоопухолевый эффект, а токсичность для мыши-хозяина слабая
+++: видимый сильный противоопухолевый эффект и нет токсичности для мыши-хозяина
Результаты показаны в следующих таблицах 1-3.
| Таблица 1 | ||||
| Испытуемое вещество | Противоопухолевый эффект | Токсичность | Синтетическая оценка | |
| Потеря веса | Степень гибели | |||
| N-геранилгулонамид | ++ | +/- | - | ++ |
| N-геранилгалактуронамид | +++ | +/- | +/- | |
| N-галактозилгеранамид | +++ | + | - | +++ |
| N-фукозогеранамид | ++ | +/- | - | +++ |
| Таблица 2 | ||||
| Испытуемое вещество | Противоопухолевый эффект | Токсичность | Синтетическая оценка | |
| Потеря веса | Степень гибели | |||
| N,N`-дигераниляблочный диамид | + | + | - | ++ |
| N,N`-дигеранилфумаровый диамид | ++ | +/- | - | ++ |
| N-геранил-4-пирувоаминобензамид | ++ | - | - | +++ |
| N-гераноилтирозин | ++ | +/- | - | ++ |
| Тирозингераниламид | + | +/- | - | + |
| N-ацетилтирозингераниламид | + | +/- | - | + |
| Таблица 3 | ||||
| Испытуемое вещество | Противоопухолевый эффект | Токсичность | Синтетическая оценка | |
| Потеря веса | Степень гибели | |||
| N-глюкозилмевалонамид | ++ | +/- | - | +++ |
Как видно из представленных результатов, соединения данного изобретения формул c (I-1) по (I-4) обладают превосходным противоопухолевым действием против клеток HuH-7 и, кроме того, почти не имеют токсичности, и, как ожидается, будут пригодны в качестве противоопухолевых средств для лечения и терапии различных солидных злокачественных опухолей, представляемых раком печени.
Когда соединение данного изобретения используется в качестве лекарственного средства, такого как противоопухолевое средство, его можно вводить перорально или парентерально (например, путем внутривенной инъекции, внутримышечной инъекции, подкожной инъекции и тому подобного). Эффективная доза меняется в широком интервале, в зависимости от индивидуальных симптомов пациента, тяжести заболевания, веса тела, возраста и диагноза врача и т.д. Обычно, однако, рассматривая случай введения путем инъекции, доза может быть равна от примерно 1 до примерно 50 мг/кг/сутки, которые можно вводить за один раз или за много раз, дробно за сутки.
Когда соединение данного изобретения используется в качестве лекарственного средства, эффективная доза соединения может быть изготовлена в рецептуре с фармацевтически приемлемым носителем или разбавителем (например, наполнитель, растворитель и другие вспомогательные вещества) в форме препарата, пригодного для введения в элементе дозировки, например, таблетки, порошка, гранулы, капсулы, пилюли с энтеросолюбильным покрытием, драже, сиропа, эликсира, жидкости, суспензии, эмульсии и тому подобного.
В качестве носителей или растворителей, пригодных для изготовления лекарственной формы, можно назвать, например, такие наполнители, как крахмал, лактоза, сахароза, маннит, карбоксиметилцеллюлоза и тому подобное; смазывающие вещества, такие как стеарат магния, лаурилсульфат натрия, тальк и тому подобное; связывающие вещества, такие как декстрин, микрокристаллическая целлюлоза, поливинилпирролидон, аравийская камедь, кукурузный крахмал, желатин и тому подобное; дезинтеграторы, такие как картофельный крахмал, карбоксиметилцеллюлоза и тому подобное; разбавляющие растворители, такие как вода для инъекций, физиологический раствор, водный раствор декстрозы, растительное масло для инъекций, пропиленгликоль, полиэтиленгликоль и тому подобное. Кроме того, когда необходимо, могут быть включены средства, корректирующие вкус и запах, краситель, средство для создания изотоничности, стабилизатор, антисептик, болеутоляющее (успокаивающее) средство и тому подобное.
В фармацевтические препараты по данному изобретению, кроме того, могут быть включены, когда необходимо, другие фармакологически активные вещества.
Далее данное изобретение объяснено более конкретно с обращением к рабочим примерам.
Примеры
Пример синтеза 1
Синтез N-геранилгалактуронамида
К тетрагидрофурановому раствору (ТГФ) (20 мл), содержащему О-тетраацетилгалактуроновую кислоту (3,62 г, 10 ммоль), добавляли триэтиламин (1,01 г, 10 ммоль) и раствор охлаждали до 0°С. В этот раствор каплями добавляли раствор изобутилхлорформиата (1,37 г, 10 ммоль) в ТГФ (5 мл) при 0°С с последующим 30-минутным перемешиванием. В полученный раствор каплями добавляли раствор гераниламина (1,53 г, 10 ммоль) в ТГФ (5 мл) с последующим одночасовым перемешиванием при 0°С и дополнительным 4-часовым перемешиванием при комнатной температуре. После окончания реакции добавляли 150 мл хлороформа и хлороформный слой три раза промывали, каждый раз 50 мл воды. Хлороформный слой сушили над сульфатом магния, хлороформ концентрировали и остаток очищали колоночной хроматографией на силикагеле. В результате получали 3,58 г (73,5%) N-геранил-О-тетраацетилгалактуронамида в виде вязкого маслянистого вещества из его гексан-ацетонового (3:1) дистиллята.
1Н ЯМР (CDCl3) δ = 1,58 (3Н, c), 1,65 (3H, c), 1,68 (3H, c), 2,01 (3H, c), 2,02 (3H, c), 2,05 (3H, c), 2,15 (3H, c), 2,02-2,11 (4H, м), 3,70-3,83 (1H, м), 3,83-3,96 (1H, м), 5,00-5,17 (2H, м), 5,29 (1H, д, J=10,8 Гц), 5,39 (1H, д, J=10,8 Гц), 6,29-6,46 (2H, м).
3,58 г (7 ммоль) вышеуказанного продукта растворяли в 30 мл этанола, добавляли 35 мл 1N водного раствора гидроксида натрия и перемешивали в течение 2 часов при комнатной температуре. Затем к реакционной смеси добавляли 35 мл 1N соляной кислоты и конденсировали при пониженном давлении. К остатку добавляли 150 мл этанола и осажденный хлорид натрия отфильтровывали. Фильтрат снова конденсировали и остаток разделяли колоночной хроматографией на силикагеле. Из гексан-этанольного (3:1) дистиллята получали 1,95 г N-геранилгалактуронамида в виде вязкого соединения. К этому продукту добавляли эфир, чтобы провести кристаллизацию и с помощью вакуум-фильтрования получали 1,03 г кристаллизованного соединения, названного в заголовке. Выход составил 45%.
1Н ЯМР (ДМСО-d6) δ = 1,50 (3H, c), 1,55 (3H, c), 1,56 (3H, c), 1,86-2,04 (4H, м), 3,48-3,76 (2H, м), 3,80-3,94 (2H, м), 4,07-4,84 (3H, м), 4,99 (1H, д, J=9,6 Гц), 5,06 (1H, д, J=9,6 Гц).
Пример синтеза 2
Синтез N-геранилглюкуронамида
Синтез из примера 1 повторяли, за исключением того, что О-тетраацетилглюкуроновую кислоту использовали вместо О-тетраацетилгалактуроновой кислоты с получением соединения, названного в заголовке.
1Н ЯМР (ДМСО-d6) δ = 1,60 (3H, c), 1,68 (3H, c), 1,73 (3H, c), 2,07-2,09 (4H, м), 3,58-3,62 (2H, м), 3,81-3,95 (2H, м), 4,07-4,86 (3H, м), 5,05-5,09 (1H, м), 5,36-5,40 (1H, м).
Пример синтеза 3
Синтез N-галактозилгеранамида
К ТГФ-раствору (20 мл), содержащему гераниевую кислоту (0,84 г, 5 ммоль), добавляли триэтиламин (0,51 г, 5 ммоль) и охлаждали до 0°С, куда затем каплями добавляли ТГФ-раствор (5 мл), содержащий изобутилхлорформиат (0,68 г, 5 ммоль), с последующим 30-минутным перемешиванием при 0°С. Затем гидрохлорид галактозамина (1,08 г, 5 ммоль) растворяли в 10 мл воды, куда затем добавляли 5 мл 1N гидроксида натрия, и данный раствор добавляли к реакционной смеси весь сразу. После последующего перемешивания в течение часа при 0°С и в течение еще 4 часов при комнатной температуре реакционную смесь конденсировали при пониженном давлении. К остатку добавляли 150 мл ацетона и осажденный хлорид натрия отфильтровывали. Фильтрат конденсировали еще раз и остаток разделяли колоночной хроматографией на силикагеле. В результате из гексан-этанольного (2:1) дистиллята получали продукт в виде вязкого маслянистого вещества, к которому добавляли минимальное количество эфира, чтобы кристаллизовать данный продукт. Посредством последующего вакуум-фильтрования получали 0,754 г соединения, названного в заголовке. Выход составил 46%, и температура плавления была в интервале 85-87°С.
1Н ЯМР (ДМСО-d6) δ = 1,53 (3H, c), 1,57 (3H, c), 1,59 (3H, c), 1,95-2,01 (4H, м), 3,63-3,79 (7H, м), 4,25-4,60 (3H, м), 4,85-4,92 (1H, м), 5,00-5,08 (1H, м), 6,25-6,31 (1H, м).
Пример синтеза 4
Синтез N-глюкозилгеранамида
Пример синтеза 3 повторяли, за исключением того, что гидрохлорид глюкозамина использовали вместо гидрохлорида галактозамина с получением соединения, названного в заголовке.
1Н ЯМР (ДМСО-d6) δ = 1,54 (3Н, c), 1,60 (3H, c), 2,03 (3H, c), 1,96-2,20 (4H, м), 3,38-3,61 (4H, м), 4,38-4,66 (3H, м), 5,75 (1H, c), 6,34-6,39 (1H, м).
Пример синтеза 5
Синтез N-фукозогеранамида
Пример синтеза 3 повторяли, за исключением того, что гидрохлорид фукозамина использовали вместо гидрохлорида галактозамина с получением соединения, названного в заголовке.
1Н ЯМР (ДМСО-d6) δ = 1,31 (3Н, д, J=5,4 Гц), 1,53 (3H, c), 1,60 (3H, c), 1,72 (3H, c), 1,97-2,05 (4H, м), 3,88-3,95 (2H, м), 4,21-4,24 (1H, м), 4,44-4,46 (1H, м), 4,82-4,87 (1H, м), 5,00-5,13 (1H, м).
Пример синтеза 6
Синтез N,N'-дигеранилфумарового диамида
К тетрагидрофурановому раствору (ТГФ) (20 мл), содержащему фумаровую кислоту (0,58 г, 5 ммоль), добавляли триэтиламин (1,01 г, 10 ммоль) и охлаждали раствор до 0°С, в который каплями добавляли ТГФ-раствор (5мл), содержащий изобутилхлорформиат (1,53 г, 10 ммоль). Когда продолжалось добавление, начинал образовываться белый осадок. После 30-минутного перемешивания при 0°С в данную систему каплями добавляли ТГФ-раствор (5 мл), содержащий гераниламин (1,53 г, 10 ммоль), с последующим одночасовым перемешиванием при 0°С и дополнительным 4-часовым перемешиванием при комнатной температуре. После окончания реакции добавляли 50 мл воды к реакционной смеси, которую затем экстрагировали хлороформом. Хлороформный слой промывали водой и сушили над сульфатом магния. Отфильтровав сульфат магния, хлороформный слой конденсировали с получением белого кристаллического вещества. Перекристаллизовывая данное вещество из этанола, получали 1,07 г соединения, названного в заголовке. Выход составил 55%.
1Н ЯМР (CDCl3) δ = 1,60 (6H, c), 1,62 (6H, c), 1,68 (6H, c), 2,01-2,10 (8H, м), 3,95 (4H, т, J=9,6 Гц), 5,04-5,09 (2H, м), 5,20-5,25 (2H, м), 5,94 (2H, шир.c), 6,90 (2H, c), 7,26 (2H, c).
Пример синтеза 7
Пример синтеза 6 повторяли, за исключением того, что фумаровую кислоту заменяли соответствующей карбоновой кислотой, ранее представленной формулы (II) в каждом цикле с получением следующих соединений:
N-геранилпирувамида
1Н ЯМР (CDCl3) δ = 1,55 (3Н, c), 1,64 (3H, c), 1,82 (3H, c), 2,00 (3Н, c), 1,92-2,12 (4Н, м), 3,84 (2H, д, J=7,2 Гц), 4,96-5,12 (1H, м), 5,22-5,35 (1H, м).
N,N'-дигераниляблочного диамида
1Н ЯМР (CDCl3) δ = 1,58 (6H, c), 1,64 (6H, c), 1,67 (6H, c), 1,94-2,14 (8H, м), 2,54 (1H, дд, J=4,8, 14,8 Гц), 2,79 (1H, дд, J=3,2, 14,4 Гц), 3,75-3,93 (4H, м), 4,32-4,40 (1H, м), 5,00-5,10 (2H, м), 5,10-5,22 (2H, м).
О-ацетил-N-гераниляблочного моноамида
1Н ЯМР (CDCl3) δ = 1,60 (3H, c), 1,68 (3H, c), 1,69 (3H, c), 1,96-2,11 (4H, м), 2,19 (3H, c), 2,65 (1H, дд, J=9,6, 22,8 Гц), 3,00 (1H, дд, J=2,4, 22,8 Гц) 3,79-3,89 (2H, м), 4,51-4,56 (1H, м), 5,08 (1H, т, J=7,2 Гц), 5,18 (1H, т, J=6,0 Гц).
О-ацетил-N,N'-дигераниляблочного диамида, который синтезировали подобным же способом, используя моноамид N-гераниляблочной кислоты в качестве исходного вещества.
1Н ЯМР (CDCl3) δ = 1,59 (6Н, c), 1,67 (6Н, c), 1,68 (6H, c), 1,94-2,01 (8H, м), 2,16 (3H, c), 2,55 (1H, дд, J=13,2, 22,8 Гц), 2,97 (1H, дд, J=2,4, 22,8 Гц), 3,79-3,89 (4H, м), 4,34-4,40 (1H, м), 5,02-5,10 (2H, м), 5,10-5,20 (2H, м).
N,N',N''-тригераниллимонного триамида
1Н ЯМР (CDCl3) δ = 1,60 (9Н, c), 1,66 (9Н, c), 1,68 (9H, c), 1,98-2,08 (12H, м), 3,76 (6H, т, J=6,3 Гц), 4,26 (4H, c), 5,07 (6H, т, J=6,0 Гц), 5,20 (6H, т, J=7,2 Гц).
N-геранилянтарного моноамида
1Н ЯМР (CDCl3) δ = 1,60 (3Н, c), 1,70 (3H, c), 1,72 (3H, c), 1,92-2,15 (4Н, м), 2,52 (2H, т, J=9,6 Гц), 2,70 (2H, т, J=9,6 Гц), 3,80-3,90 (2H, м), 5,08 (1H, т, J=9,6 Гц), 5,18 (1H, т, J=6,0 Гц), 5,61 (1H, шир.c).
N,N'-дигеранилянтарного диамида, который синтезировали подобным же способом, используя моноамид N-геранилянтарной кислоты в качестве исходного вещества.
1Н ЯМР (CDCl3) δ = 1,60 (6H, c), 1,66 (6H, c), 1,69 (6H, c), 1,97-2,11 (4H, м), 2,53 (4H, c), 3,84 (4H, т, J=5,5 Гц), 5,07 (2H, т, J=4,9 Гц), 5,17 (2H, т, J=5,5 Гц), 5,90 (2H, шир.c).
N-геранилфумарового моноамида
1Н ЯМР (CDCl3) δ = 1,59 (3H, c), 1,67 (3H, c), 1,70 (3H, c), 1,94-2,16 (4H, м), 3,88-4,04 (2H, м), 5,06 (1H, т, J=7,2 Гц), 5,21 (1H, т, J=4,8 Гц), 6,30 (1H, д, J=12,0 Гц), 6,46 (1H, д, J=12,0 Гц).
N,N'-дигеранил-2-оксоглютарового диамида
1Н ЯМР (CDCl3) δ = 1,60 (6H, c), 1,68 (12H, c), 1,94-2,13 (8H, м), 2,69 (2H, т, J=6,3 Гц), 3,26 (2H, т, J=6,3 Гц), 3,81-4,04 (4H, м), 5,02-5,10 (2H, м), 5,15-5,22 (2H, м).
N-геранил-п-пирувоаминобензамида
1Н ЯМР (CDCl3) δ = 1,60 (3Н, c), 1,68 (3H, c), 1,70 (3H, c), 2,03-2,11 (4Н, м), 2,17 (3H, c), 3,95-4,04 (2H, м), 4,83 (1H, шир.c), 5,09 (1H, т, J=6,6 Гц), 5,28 (1H, т, J=6,9 Гц),5,94 (1H, шир.c), 6,64 (2H, д, J=8,7 Гц), 7,60 (2H, д, J-8,7 Гц).
N-геранилретинамида
1Н ЯМР (CDCl3) δ = 1,03 (6Н, c), 1,12-1,63 (6H, м), 1,60 (3Н, c), 1,66 (3H, c), 1,68 (3H, c), 1,72 (3H, c), 1,87-1,93 (4H, м), 2,01 (3H, c), 2,37 (3H, c), 3,82-3,92 (2H, м), 5,03-5,24 (2H, м), 5,80 (1H, c), 6,12-6,40 (3H, м), 7,02 (1H, д, J=12,0 Гц), 7,07 (1H, д, J=12,0 Гц).
Пример синтеза 8
Синтез N-гераноилцистеина
К ТГФ-раствору (20 мл), содержащему гераниевую кислоту (1,68 г, 10 ммоль), добавляли триэтиламин (1,01 г, 10 ммоль) и охлаждали его до 0°С, и туда каплями добавляли ТГФ-раствор (5 мл) изобутилхлорформиата (1,37 г, 10 ммоль) с последующим 30-минутным перемешиванием при 0°С. К реакционной смеси добавляли раствор цистеина (1,35 г, 10 ммоль), который растворяли в 1N гидроксиде натрия (10мл), с последующим одночасовым перемешиванием при 0°С и дополнительным 4-часовым перемешиванием при комнатной температуре. После окончания реакции к реакционной смеси добавляли 10 мл 1N соляной кислоты и перемешивали в течение 10 минут при комнатной температуре. Затем реакционную смесь конденсировали с помощью роторного испарителя. К остатку добавляли этанол, после чего осажденный хлорид натрия удаляли фильтрованием. Этанольный раствор еще раз конденсировали при пониженном давлении с помощью испарителя и остаток разделяли колоночной хроматографией на силикагеле. Таким образом получали 0,556 г соединения, названного в заголовке, из гексан-ацетонового (2:1) дистиллята. Выход составил 19,5%:
1Н ЯМР (CDCl3) δ = 1,59 (6H, c), 1,68 (3H, c), 2,00-2,24 (4H, м), 2,60-2,77 (1H, м), 3,00-3,30 (2H, м), 4,48-4,58 (1H, м), 5,00-5,13 (1H, м), 8,96 (1H, c).
Пример синтеза 9
N-гераноилтирозин
Пример синтеза 8 повторяли, за исключением того, что цистеин заменяли тирозином, с получением соединения, названного в заголовке:
1Н ЯМР (CDCl3) δ = 1,55 (6H, c), 1,64 (3H, c), 1,96-2,00 (4H, м), 2,90-3,17 (2H, м), 4,81-5,06 (3Н, м), 6,40-7,21 (4H, м), 7,25 (1H, c).
Примера синтеза 10
Синтез глютаминового дигеранилдиамида
К ТГФ-раствору (20мл) N-бензилоксикарбонилглютаминовой кислоты (2,634 г, 9,4 ммоль) добавляли триэтиламин (1,899 г, 18,8 ммоль) и охлаждали до 0°С. В эту смесь каплями добавляли ТГФ-раствор (10 мл) изобутилхлорформиата (2,566 г, 18,8 ммоль) с последующим 30-минутным перемешиванием при 0°С. Затем каплями добавляли ТГФ-раствор (10 мл) гераниламина (2,880 г, 18,8 ммоль) с последующим одночасовым перемешиванием при 0°С и дополнительным 4-часовым перемешиванием при комнатной температуре. После завершения реакции к системе добавляли 150 мл хлороформа и хлороформный раствор промывали водой и сушили над сульфатом магния. Органический раствор удаляли с помощью испарителя и остаток разделяли колоночной хроматографией на силикагеле. Таким образом получали 3,034г N-бензилоксикарбонилглютаминового дигеранилдиамида из гексан-ацетонового (2:1) дистиллята. Выход составил 58,6%.
Затем N-бензилоксикарбонилглютаминовый дигеранилдиамид (3,034 г, 5,5 ммоль) растворяли в метаноле (20 мл) и к этому же раствору добавляли 20 мл 1N раствора гидроксида натрия с последующим 5-часовым перемешиванием при комнатной температуре. Реакционную смесь конденсировали с помощью испарителя и остаток разделяли колоночной хроматографией на силикагеле с получением целевого соединения из гексан-этанольного (3:1) дистиллята. Так как полученный таким образом продукт был вязким и аморфным, к данному продукту добавляли эфир для кристаллизации. После вакуум-фильтрования системы получали 852 мг целевого соединения. Выход составил 37,2%.
1Н ЯМР (CDCl3) δ = 1,58 (12H, c), 1,61 (6Н, c), 1,75-2,12 (8H, м), 2,32-2,53 (2H, м), 3,54-3,88 (7H, м), 4,88-5,21 (4H, м).
Пример синтеза 11
При повторении примера синтеза 10, за исключением того, что N-бензилоксикарбонилглютаминовую кислоту заменяли тирозином, N-ацетилтирозином, цистеином или серином, получали следующие соединения. Когда использовали N-ацетилтирозин, последующую операцию удаления защиты не проводили.
Тирозингераниламид
1Н ЯМР (CDCl3) δ = 1,59 (3H, c), 1,67 (6H, c), 1,82-2,18 (4H, м), 2,99-3,09 (2H, м), 3,74-3,78 (2H, м), 4,99-5,26 (3H, м), 7,17-7,43 (5H, м).
N-ацетилтирозингераниламид
1Н ЯМР (CDCl3) δ = 1,60 (3H, c), 1,68 (3H, c), 1,98 (3H, c), 2,00-2,11 (4H, м), 2,18 (3H, c), 2,90-3,00 (2H, м), 3,69-3,79 (2H, м), 4,59 (1H, дд, J=15,6, 9,6 Гц), 5,00-5,10 (2H, м), 6,70 (2H, д, J=7,8 Гц), 7,01 (2H, д, J=7,8 Гц), 7,27 (1H, c).
Цистеингераниламид
1Н ЯМР (CDCl3) δ = 1,58 (3H, c), 1,66 (3H, c), 1,67 (3H, c), 1,93-2,10 (4H, м), 2,83-3,16 (2H, м), 3,83-4,08 (3H, м), 5,03-5,19 (2H, м), 7,33 (1H, c).
Серингераниламид
1Н ЯМР (CDCl3) δ = 1,59 (3H, c), 1,68 (6H, c), 1,95-2,14 (4H, м), 3,80-3,95 (2H, м), 4,34-4,47 (2H, м), 4,67 (1H, т, J=10,8 Гц), 5,06 (1H, т, J=6,0 Гц), 5,17 (1H, т, J=6,0 Гц), 6,77 (2H, шир.c).
Пример синтеза 12
Синтез N-глюкозилмевалонамида
Гидрохлорид глюкозамина (2,16 г, 10 ммоль) растворяли в 20 мл воды и к водному раствору добавляли 10 мл 1N раствора гидроксида натрия и мевалолактон (1,30 г, 10 ммоль) с последующим 5-часовым нагреванием при перемешивании при 55°С. После окончания реакции реакционную смесь конденсировали при пониженном давлении. К остатку добавляли 100 мл метанола, после чего выделившийся осадок отфильтровывали. Фильтрат снова конденсировали с помощью испарителя и остаток разделяли колоночной хроматографией на силикагеле с получением 1,45 г целевого продукта из этанольного дистиллята. Выход составил 47%. Так как полученный продукт был вязким маслянистым веществом, к нему добавляли минимальное количество дихлорметана, чтобы осуществить кристаллизацию. После вакуум-фильтрования получали 1,10 г соединения, названного в заголовке, которое было сильно гигроскопичным и его температуру плавления можно было определить:
1Н ЯМР (ДМСО-d6) δ = 1,00 (3H, c), 1,44-1,59 (2H, м), 2,47 (2H, c), 2,96-3,74 (10H, м), 4,04-5,08 (3H, м).
Пример синтеза 13
Синтез N-галактозилмевалонамида
Пример синтеза 12 повторяли, за исключением того, что гидрохлорид глюкозамина заменяли гидрохлоридом галактозамина с получением соединения, названного в заголовке:
1Н ЯМР (ДМСО-d6) δ = 1,08 (3H, c), 1,51-1,61 (2H, м), 2,44 (2Н, c), 2,74-5,16 (13Н, м).
Пример синтеза 14
Синтез N-фукозомевалонамида
Пример синтеза 12 повторяли, за исключением того, что гидрохлорид глюкозамина заменяли гидрохлоридом фукозамина с получением соединения, названного в заголовке:
1Н ЯМР (ДМСО-d6) δ = 1,06 (3H, c), 1,20 (3H, д, J=24,0 Гц), 1,54-1,62 (2H, м), 2,44 (2H, c), 2,74-5,15 (12H, м).
Пример препарата 1
Два (2) г N-галактозилгеранамида растворяли в 1 литре воды для инъекций при комнатной температуре, изотонировали хлоридом натрия, разливали в ампулы и запаивали. Один (1) мл данного препарата для инъекций содержит 2 мг активного ингредиента.
Пример препарата 2
Два (2) г N,N'-дигераниляблочного диамида растворяли в 1 литре воды для инъекций при комнатной температуре, изотонировали хлоридом натрия, разливали в ампулы и запаивали. Один (1) мл данного препарата для инъекций содержит 2 мг активного ингредиента.
Пример препарата 3
Два (2) г N-глюкозилмевалонамида растворяли в 1 литре воды для инъекций при комнатной температуре, изотонировали хлоридом натрия, разливали в ампулы и запаивали. Один (1) мл данного препарата для инъекций содержит 2 мг активного ингредиента.
1. Геранильные соединения, представляемые следующими формулами (I-1), (I-2) или (I-3):
в которых
R1 означает
R2 означает остаточную группу, остающуюся после удаления всех карбоксильных групп, присутствующих в карбоновой кислоте, выбранной из группы, состоящей из яблочной кислоты, лимонной кислоты, янтарной кислоты, фумаровой кислоты, 2-оксоглютаровой кислоты, пировиноградной кислоты, п-пирувоаминобензойной кислоты, ретиноевой кислоты, тирозина, цистеина, глютаминовой кислоты и серина, и, когда в остаточной группе присутствуют гидроксильные или аминогруппы(а), они могут быть необязательно защищены ацилом (например, низшим алканоилом) или бензилоксикарбонильной(ыми)группой(ами),
m равно 1, 2 или 3,
n равно 0, 1 или 2, причем
m+n представляет число карбоксильных групп, которые присутствуют в указанной карбоновой кислоте, и
R3 обозначает п-гидроксифенил или меркаптогруппу.
2. Производные мевалоновой кислоты, представляемые следующей формулой (1-4):
в которой R4 обозначает -СН2Н или СН3.
3. Противоопухолевое средство, содержащее в качестве активного ингредиента геранильное соединение формулы (I-1), (I-2) или (I-3), которое представлено в п.1, или производное мевалоновой кислоты формулы (I-4), которое представлено в п.2, и необязательно фармацевтически приемлемый носитель или растворитель.
4. Способ лечения рака печени, включающий введение пациенту эффективного для противоопухолевого действия количества геранильного соединения формул (I-1), (I-2) или (I-3), которое представлено в п.1, или производного мевалоновой кислоты формулы (I-4), которое представлено в п.2.
5. Использование геранильного соединения формулы (I-1), (I-2) или (I-3), которое представлено в п.1, или производного мевалоновой кислоты формулы (I-4), которое представлено в п.2, для лечения рака печени.
6. Использование геранильного соединения формулы (I-1), (I-2) или (I-3), которое представлено в п.1, или производного мевалоновой кислоты формулы (I-4), которое представлено в п.2, для производства противоопухолевого средства.