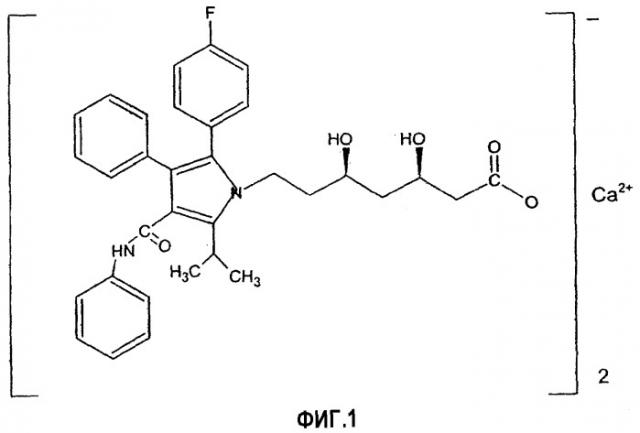
Форма vi аторвастатина кальция или ее гидраты
Иллюстрации
Показать всеИзобретение относится к новой кристаллической форме VI аторвастатина кальция или ее гидратов с картиной рентгеновской порошковой дифракции по значениям 2Θ, определенным с использованием Shimadzu XRD-6000 с К излучением меди с λ 1,5406 Å и с относительной интенсивностью >15%, 3,7365; 7,7200; 8,6985; 10,2185; 12,5933; 17,9103; 18,3600; 19,4031; 20,2800; 20,8200; 22,5122 и 25,5848. А также описываются способы их получения. Технический результат: преимуществом данной формы является высокая чистота, стабильность и растворимость. 3 н. и 19 з.п. ф-лы, 2 табл., 3 ил.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к форме VI аторвастатина кальция или ее гидратам и способу их получения. В частности, данное изобретение относится к новой кристаллической форме аторвастатина кальция.
УРОВЕНЬ ТЕХНИКИ
Аторвастатин является представителем класса лекарственных веществ, называемых статинами. Статиновые лекарственные вещества в настоящее время являются наиболее терапевтически эффективными из доступных лекарственных средств для снижения концентрации частиц липопротеинов низкой плотности (ЛНП) в кровотоке пациентов с риском сердечно-сосудистых заболеваний. Он также, по-видимому, снижает общее содержание глицеридов и общее содержание холестерина. Высокий уровень ЛНП в кровотоке связан с образованием коронарных повреждений, которые препятствуют кровотоку и могут вызвать разрыв и способствовать тромбозу. Goodman and Gilman. The Pharmacological Basis of Therapeutics 879 (9th ed. 1996). Снижение уровней ЛНП в плазме, как было показано, снижает риск клинических случаев у пациентов с сердечно-сосудистыми заболеваниями и пациентов, у которых нет сердечно-сосудистого заболевания, но у которых есть гиперхолестеринемия [Scandinavian Simvastatin Survival Study Group, 1994; Lipid Research Clinics Program, 1984a, 1984b].
Были изучены некоторые подробности механизма действия статиновых лекарственных веществ. Они препятствуют синтезу холестерина и других стеринов в печени путем конкурентного ингибирования фермента 3-гидрокси-3-метилглутарилкофермент-А-редуктазы («ГМГ-КоА-редуктазы»). ГМГ-КоА-редуктаза катализирует превращение ГМГ-КоА в мевалонат, которое является определяющей скорость стадией в биосинтезе холестерина, и поэтому ее ингибирование приводит к снижению концентрации холестерина в печени. Липопротеин с очень низкой плотностью (ЛОНП) является биологическим носителем для переноса холестерина и триглицеридов из печени к периферическим клеткам. ЛОНП катаболизируется в периферических клетках, которые выделяют жирные кислоты, которые могут храниться в адипоцитах или окисляться в мышцах. ЛОНП превращается в липопротеин средней плотности (ЛСП), который или удаляется рецепторами ЛНП, или превращается в ЛНП. Снижение продукции холестерина приводит к повышению числа рецепторов ЛНП и соответствующему снижению продукции частиц ЛНП путем метаболизма ЛСП.
Аторвастатин является общепринятым названием вещества с химическим наименованием [R-(R*,R*)]-2-(4-фторфенил)-β,δ-дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1Н-пиррол-1-гептановая кислота. Свободная кислота подвержена лактонизации. Молекулярная структура лактона представлена формулой (1).
Аторвастатин поставляется на рынок в виде тригидрата полу-кальциевой соли под названием липитор (LIPITOR) Warner-Lambert Co. Он является синтетическим ингибитором ГМГ-КоА-редуктазы и используется для лечения гиперлипидемии и гиперхолестеринемии. Эмпирическая формула аторвастатина кальция представляет собой (С33Н34FN2О5)2Са, и его молекулярный вес равен 1155,42.
Его структурная формула представляет собой:
Фигура 1
Аторвастатин кальций представляет собой белый, до не совсем белого, аморфный или кристаллический порошок, который нерастворим в водных растворах с рН 4 и ниже. Он очень слабо растворим в дистиллированной воде, фосфатном буфере с рН 7,4 и ацетонитриле, слабо растворим в этаноле и свободно растворяется в метаноле.
Лактон аторвастатина впервые был представлен общественности и заявлен в патенте США № 4681893. Полу-кальциевая соль, представленная формулой (II) (здесь далее «аторвастатин кальций»), энантиомер, имеющий R-форму кислоты с разомкнутым кольцом, описана в патенте США № 5273995. В этом патенте указано, что эту кальциевую соль получают кристаллизацией из насыщенного раствора соли, получающегося при преобразовании натриевой соли с помощью CaCl2, и далее очищают кристаллизацией из смеси 5:3 этилацетата и гексана. Оба этих патента США включены сюда в виде ссылки.
В патентах США с номерами 5003080, 5097045, 5103024, 5124482, 5149837, 5155251, 5216174, 5248793, 5280132, 5342952, 5007080, 6274740, которые включены сюда в виде ссылки, описаны различные способы и ключевые промежуточные соединения для получения аторвастатина кальция. Все эти способы дают смесь кристаллической и аморфной форм.
Аторвастатин получают в виде его кальциевой соли. Кальциевая соль является желательной, так как она дает возможность приготовить подходящие препараты с аторвастатином в соответствии с целями введения. Кроме того, существует необходимость получения аторвастатина в чистой и кристаллической форме, чтобы сделать его способным соответствовать строгим фармацевтическим требованиям и техническим условиям.
Кроме того, необходимо, чтобы способ, которым получают аторвастатин, был пригоден для крупномасштабного производства. К тому же, желательно, чтобы продукт находился в форме, которую легко выделить. И, наконец, экономически желательно, чтобы продукт имел длительный срок хранения без необходимости соблюдения особых условий хранения.
В способах представленных выше патентов США описан аморфный аторвастатин, который имеет свойства, неподходящие для фильтрования и сушки в условиях крупномасштабного производства, и должен быть защищен от нагревания, света, кислорода и влаги.
В патенте США № 5969156 описаны три полиморфа аторвастатина, обозначенные авторами, открывшими их, как формы I, II и IV. Хотя авторы заявляют об определенных преимуществах переработки и терапевтических преимуществах этих форм над аморфным аторвастатином кальцием, преимущества могут быть реализованы еще и с помощью других не открытых ранее форм аторвастатина кальция.
В заявке РСТ WO 97/03960 и заявке РСТ WO 00/71116 описан способ производства аморфного аторвастатина кальция.
В заявке РСТ WO 97/03958 и патенте США № 6121461 описан способ получения формы III кристаллического аторвастатина кальция, и в то же время в заявке РСТ WO97/03959 сообщается о способе получения форм I, II и IV кристаллического аторвастатина кальция.
В заявке РСТ WO 01/36384 описана форма V аторвастатина кальция. Во всех этих патентах заявлено о преимуществах над существующими патентами тем или иным образом.
Данное изобретение включает новую кристаллическую форму аторвастатина кальция как в виде гидрата, так и безводном состоянии. Полиморфизм является свойством некоторых молекул и молекулярных комплексов принимать более чем одну кристаллическую или аморфную форму в твердом состоянии. Единственная молекула, подобная аторвастатину формулы (I) или солевому комплексу формулы (II), может образовать ряд твердых веществ, имеющих особые физические свойства, такие как растворимость, стабильность, чистота, картина дифракции рентгеновских лучей и 13С ЯМР спектр в твердом состоянии. Различия физических свойств полиморфов является результатом ориентации и межмолекулярных взаимодействий соседних молекул (комплексов) в массе твердого вещества. Соответственно, полиморфы являются отдельными твердыми веществами, имеющими одну и ту же молекулярную формулу, которую можно представить как аналогичную элементарной ячейке в металлургии, еще обладающей ясными благоприятными и/или неблагоприятными физическими свойствами по сравнению с другими формами в семействе полиморфов. Одним из наиболее важных физических свойств фармацевтических полиморфов является их растворимость в водном растворе, особенно их растворимость в желудочном соке пациента. Например, когда всасывание из желудочно-кишечного тракта является медленным, часто для лекарственного вещества, которое нестабильно в условиях в желудке или кишечнике пациента, желательно, чтобы оно растворялось медленно, так чтобы оно не скапливалось во враждебном окружении. С другой стороны, когда эффективность лекарственного вещества коррелирует с пиковыми уровнями в кровотоке, что характерно для статиновых лекарственных веществ, и при условии, что лекарственное вещество быстро всасывается из ЖК системы, тогда более быстро растворяющаяся форма, вероятно, проявит повышенную эффективность по отношению со сравнимым количеством более медленно растворяющейся формы.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
ФИГ. 1 представляет структурную формулу новой кристаллической полиморфной формы VI аторвастатина кальция данного изобретения.
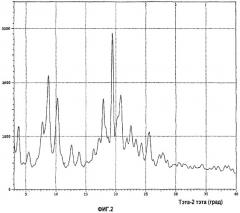
ФИГ. 2 представляет рентгеновскую дифрактограмму порошка аторвастатина кальция формы VI.
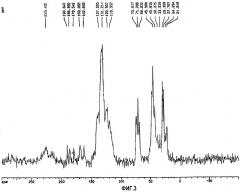
ФИГ. 3 представляет 13С ЯМР спектр в твердом состоянии аторвастатина кальция формы VI.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение представляет новую кристаллическую полиморфную форму аторвастатина кальция, обозначенную как форма VI, как в безводном состоянии, так и в виде гидрата, преимуществом которой является высокая чистота, стабильность и растворимость.
Данное изобретение, кроме того, представляет простой недорогой способ получения новой формы VI аторвастатина кальция, который обладает достоинствами легкого и быстрого выделения и кристаллизации, не считая чистоты, выхода и стабильности. Число входящих в него стадий очень невелико.
Данное изобретение также обеспечивает высокий выход и очень низкий объем остаточных растворителей.
Соответственно, данное изобретение относится к кристаллической полиморфной форме VI аторвастатина кальция как в безводном состоянии, так и в виде гидрата.
Новая полиморфная кристаллическая форма VI аторвастатина кальция отличается следующей картиной порошковой рентгеновской дифракции, выраженной в виде 2 тета, d-интервалов и относительных интенсивностей с относительной интенсивностью >15%, определенной на Shimadzu XRD-6000 c К излучением меди с лямда 1,5406 Å:
| 2Θ | D | Относительная интенсивность (>15%) |
| 3,7365 | 23,4584 | 23,0 |
| 7,7200 | 11,4425 | 36,0 |
| 8,6985 | 10,1574 | 74,0 |
| 10,2185 | 8,6497 | 57,0 |
| 12,5933 | 7,0234 | 19,0 |
| 17,9103 | 4,9485 | 47,0 |
| 18,3600 | 4,8283 | 20,0 |
| 19,4031 | 4,5710 | 100,0 |
| 20,2800 | 4,3753 | 29,0 |
| 20,8200 | 4,2630 | 48,0 |
| 22,5122 | 3,9463 | 24,0 |
| 25,5848 | 3,4923 | 25,0 |
Кроме того, кристаллическая форма VI аторвастатина кальция или ее гидраты по пункту I имеют пики порошковой рентгеновской дифракции при 2Θ 3,7; 8,6; 10,2 и 20,9 градусов и широкий пик при 2Θ 19,5 градусов.
Кроме того, данное изобретение относится к кристаллической форме VI аторвастатина и ее гидратам, отличающейся следующим спектром 13С ядерного магнитного резонанса (ЯМР) в твердом состоянии, где химический сдвиг выражен в миллионных долях (м.д.), определенным на спектрофотометре Varian.
| δ (м.д.) |
| 21,898 |
| 24,294 |
| 27,767 |
| 29,368 |
| 33,939 |
| 38,275 |
| 42,836 |
| 45,980 |
| 68,932 |
| 71,266 |
| 73,617 |
| 119,357 |
| 122,987 |
| 131,214 |
| 137,515 |
| 162,696 |
| 169,066 |
| 179,540 |
| 186,890 |
| 190,640 |
Кристаллическая форма VI аторвастатина кальция или ее гидраты по пункту 1 имеют сигналы 13С ЯМР в твердом состоянии при примерно 162,689 м.д., 169,066 м.д., 179,54 м.д., 186,89 м.д. и 190,64 м.д.
В предпочтительном варианте осуществления данного изобретения кристаллическая форма VI аторвастатина кальция содержит до 8 моль воды на моль аторвастатина кальция.
В еще одном предпочтительном варианте осуществления данного изобретения кристаллическая форма VI аторвастатина кальция является тригидратом.
Данное изобретение, кроме того, представляет способ получения новой кристаллической полиморфной формы VI аторвастатина кальция как в виде гидрата, так и в безводном состоянии, [R-(R*,R*)]-2-(4-фторфенил)-бета,дельта-дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1Н-пиррол-1-гептановой кислоты полу-кальциевой соли (2:1), имеющей формулу, которая представлена на фигуре 1:
а) растворение кальциевой соли любой формы аторвастатина в органическом растворителе, таком как алифатический кетон, с получением прозрачного раствора соли аторвастатина,
b) по желанию, удаление примесей,
с) добавление деминерализованной воды,
d) выделение кристаллической полиморфной формы VI аторвастатина кальция и сушку, по желанию, с захватом необходимой кристаллизационной воды.
Кроме того, данное изобретение представляет также способ получения новой кристаллической полиморфной формы VI аторвастатина кальция, [R-(R*,R*)]-2-(4-фторфенил)-бета,дельта-дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1Н-пиррол-1-гептановой кислоты полу-кальциевой соли (2:1), имеющей формулу фиг.1, который включает:
а) растворение лактонной формы аторвастатина в органическом растворителе, предпочтительно в алифатическом кетоне, с получением прозрачного раствора,
b) добавление водного раствора гидроксида щелочно-земельного металла и деминерализованной воды при перемешивании,
с) выделение кристаллической полиморфной формы VI аторвастатина кальция и сушку, по желанию, с захватом необходимой кристаллизационной воды.
В одном из воплощений данного изобретения используемый аторвастатин кальция может быть аморфным или в виде кристаллической формы I, II, III, IV и V аторвастатина кальция или их смесью.
В дополнительном воплощении используемый аторвастатин кальция может быть в безводном состоянии или в виде гидрата, содержащего до 9 молекул воды.
В еще одном дополнительном воплощении используемый органический растворитель может быть выбран из алифатических кетонов, содержащих от 1 до 3 атомов углерода. Используемые алифатические кетоны могут быть ацетоном, метилэтилкетоном, диэтилкетоном, метилпропилкетоном, предпочтительно, ацетоном.
В еще одном воплощении используемый органический растворитель может быть в 100-кратномм, предпочтительно 15-кратном, более предпочтительно, 10-кратном количестве от исходного соединения.
В соответствии с еще одним аспектом данного изобретения растворение может быть проведено посредством нагревания суспензии аторвастатина кальция в органическом растворителе до температуры кипения используемого растворителя, предпочтительно, до температуры выше 40°С и ниже 80°С, более предпочтительно, от 40°С до 50°С.
При одном из добавочных воплощений примеси удаляют фильтрованием.
В еще одном добавочном воплощении количество используемой ДМ воды может быть в 100 раз, предпочтительно, в 10 раз больше количества исходного соединения.
В другом воплощении ДМ вода может быть добавлена каплями при сохранении температуры.
Кроме того, используемый гидроксид щелочно-земельного металла может быть гидроксидом кальция. Водный раствор гидроксида щелочно-земельного металла может быть, предпочтительно, добавлен при повышенной температуре, предпочтительно при температуре выше 40°С и ниже 80°С, более предпочтительно при температуре от 40°С до 50°С.
Гидроксид щелочно-земельного металла может быть добавлен в 50-кратном, предпочтительно в 10-кратном количестве от исходного соединения, более предпочтительно, в соотношении 1:1.
В еще одном воплощении раствор может быть медленно охлажден до температуры в интервале от -20°С до 20°С (комнатная температура), предпочтительно, в интервале от 15°С до 20°С, для осуществления кристаллизации. Охлаждение может быть произведено со скоростью 2-3°С в минуту.
Выделение может быть осуществлено любыми общепринятыми методами, такими как фильтрование, вакуум-фильтрование, декантация, центрифугирование.
Сушка может быть осуществлена с помощью известных средств, подобных вакуумной лотковой сушилке, барабанной вакуум-сушилке, и при температуре выше 50°С и ниже 80°С, предпочтительно при 55°С, в течение от 12 до 30 часов для регуляции количества воды в молекулах. Специалист в данной области поймет, что путем регулировки температуры и времени этих стадий можно оптимизировать выход желаемого продукта.
Новая кристаллическая форма VI аторвастатина кальция имеет потенциальное применение для лечения гиперлипидемии, гиперхолестеринемии, гипохолестеринемии, болезни Альцгеймера, атеросклероза, ксантомы и, в синергизме с другими лекарственными средствами, для лечения дефицита липазы при фитостеринемии, и тому подобного.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Порошковая рентгеновская дифрактограмма новой полиморфной кристаллической формы VI (фиг. 2) имеет средние пики при 2Θ 3,7±0,2; 8,6±0,2; 10,2±0,2 и 20,9±0,2 градусов и один большой пик при 2Θ 19,5±0,2 градусов.
Эта картина рентгеновского излучения сильно отличается от картины для известных кристаллических форм I, II, III, IV, V, а также от картины рентгеновской дифракции аморфной формы, которая отличается двумя широкими максимумами в интервале 2Θ 8-14 градусов и 2Θ 15-26 градусов.
Рентгеновская дифрактограмма фиг.2 была получена известными методами, с использованием Schimadzu XRD-6000, применяли излучение меди с λ=1,5406 Å. Интервал измерения 2Θ 3-40 градусов. В таблице 1 перечислены 2Θ, d-интевалы и относительные интенсивности со сравнительной интенсивностью >15%.
| ТАБЛИЦА 1 | ||
| 2Θ | D | Относительная интенсивность (>15%) |
| 3,7635 | 23,4584 | 23,0 |
| 7,7200 | 11,4425 | 36,0 |
| 8,6985 | 10,1574 | 74,0 |
| 10,2185 | 8,6497 | 57,0 |
| 12,5933 | 7,0234 | 19,0 |
| 17,9103 | 4,9485 | 47,0 |
| 18,3600 | 4,8283 | 20,0 |
| 19,4031 | 4,5710 | 100,0 |
| 20,2800 | 4,3753 | 29,0 |
| 20,8200 | 4,2630 | 48,0 |
| 22,5122 | 3,9463 | 24,0 |
| 25,5848 | 3,4923 | 25,0 |
Спектр 13С ЯМР в твердом состоянии новой полиморфной формы характеризуется следующими химическими сдвигами.
| δ (м.д.) |
| 21,898 |
| 24,294 |
| 27,767 |
| 29,368 |
| 33,939 |
| 38,275 |
| 42,836 (сильный) |
| 45,980 |
| 68,932 |
| 71,266 |
| 73,617 |
| 119,357 |
| 122,987 |
| 131,214 (сильный) |
| 137,515 |
| 162,696 |
| 169,066 |
| 179,540 |
| 186,890 |
| 190,640 |
Спектр 13С ЯМР в твердом состоянии сильно отличается от спектров известных форм I, II, III, IV, V, а также аморфной формы, которая дает другую картину со сдвигами, значительно отличающимися от картины новой полиморфной формы VI, проявляющимися при 162,698 м.д., 169,066 м.д., 179,54 м.д., 186,89 м.д. и 190,64 м.д., что соответствует С12 или С25 углеродным атомам соединения формулы с фиг. 1. Спектр с фиг. 3 был получен на спектрометре Varian при 300 МГц (мегагерц). Прибор оборудован 13С сп головкой для пробы массы, и образец подавался при скорости вращения 7,0 кГц. Магический угол и эффективность развязки протонов были оптимизированы перед регистрацией данных.
РД и ЯМР выполняли на неразмолотых образцах.
Новая полиморфная форма существует в безводном состоянии, а также в виде гидрата. Она содержит до 9 молекул воды. Однако предпочтительна тригидратная форма.
Изобретение далее иллюстрируется следующими примерами, которые не ограничивают фактический объем формулы изобретения.
ПРИМЕР 1:
Аторвастатин кальция (100,0 г) добавляли к ацетону (1 л) при комнатной температуре. Смесь нагревали до 50°С в течение 30 минут до получения прозрачного раствора. К этому раствору по каплям добавляли ДМ воду (500 мл) при 50°С. Раствор медленно охлаждали до комнатной температуры со скоростью 2°С/мин, при этом выкристаллизовывалась новая полиморфная форма аторвастатина кальция. Продукт отфильтровывали вакуум-фильтрованием и затем сушили в лотковой вакуум-сушилке при 50-55°С в течение 24 часов.
Выход: 90,0 г (90,0%)
Относительная чистота (ВЭЖХ): 99,63%
Остаточный растворитель:
Ацетон: не более 0,2%
ПРИМЕР 2:
Аторвастатин кальция (100,0 г) добавляли в ацетон (100,0 мл) при комнатной температуре. Смесь нагревали до 50°С в течение 30 минут до получения прозрачного раствора. К этому раствору по каплям добавляли ДМ воду (100 мл) при 50°С. Раствор медленно охлаждали до комнатной температуры со скоростью 2°С/мин, при этом выкристаллизовывалась новая полиморфная форма аторвастатина кальция. Продукт отфильтровывали вакуум-фильтрованием и затем сушили в лотковой вакуум-сушилке при 55-60°С в течение 28 часов.
Выход: 92,0 г (92,0%)
Относительная чистота (ВЭЖХ): 99,68%
Остаточный растворитель:
Ацетон: не более 0,2%
ПРИМЕР 3:
Аторвастатин кальция (10,0 г) добавляли к ацетону (1 л) при комнатной температуре. Смесь нагревали до 45°С в течение 20 минут до получения прозрачного раствора. К этому раствору по каплям добавляли ДМ воду (1,0 л) при 45°С. Раствор медленно охлаждали до комнатной температуры со скоростью 2°С/мин, при этом выкристаллизовывалась новая полиморфная форма аторвастатина кальция. Продукт отфильтровывали вакуум-фильтрованием и затем сушили в лотковой вакуум-сушилке при 55-60°С в течение 24 часов.
Выход: 90,0 г (90,0%)
Относительная чистота (ВЭЖХ): 99,61%
Остаточный растворитель:
Ацетон: не более 0,2%
ПРИМЕР 4:
Лактонную форму аторвастатина кальция (100,0 г) добавляли в ацетон (1 л) при комнатной температуре. К этому раствору добавляли гидроксид кальция (10,0 г), суспендированный в ДМ воде (100 мл), одной порцией. Реакционную массу перемешивали при 45-46°С до исчезновения лактонной формы аторвастатина кальция (ТСХ, 2,0 часа). По каплями добавляли ДМ воду (400 мл) при 45°С. Раствор медленно охлаждали до комнатной температуры со скоростью 2°С/мин, при этом выкристаллизовывалась новая полиморфная форма аторвастатина кальция. Продукт отфильтровывали вакуум-фильтрованием и затем сушили в лотковой вакуум-сушилке при 50-55°С в течение 20 часов.
Выход: 100,0 г (90,0%)
Относительная чистота (ВЭЖХ): 99,31%
Остаточный растворитель:
Ацетон: не более 0,2%
ПРИМЕР 5:
Лактонную форму аторвастатина кальция (10,0 г) добавляли в ацетон (10,0 мл) при комнатной температуре. К этому раствору добавляли гидроксид кальция (1,0 г), суспендированный в ДМ воде (5,0 мл), одной порцией. Реакционную массу перемешивали при 50°С до исчезновения лактонной формы аторвастатина кальция (ТСХ, 2,0 часа). По каплям добавляли ДМ воду (5 мл) при 50°С. Раствор медленно охлаждали до комнатной температуры со скоростью 2°С/мин, при этом выкристаллизовывалась новая полиморфная форма аторвастатина кальция. Продукт отфильтровывали вакуум-фильтрованием и затем сушили в лотковой вакуум-сушилке при 55-60°С в течение 24 часов.
Выход: 10,0 г (90,0%)
Относительная чистота (ВЭЖХ): 99,20%
Остаточный растворитель:
Ацетон: не более 0,2%
ПРИМЕР 6:
Лактонную форму аторвастатина кальция (10,0 г) добавляли в ацетон (1,0 л) при комнатной температуре. К этому раствору добавляли гидроксид кальция (1,0 г), суспендированный в ДМ воде (100,0 мл), одной порцией. Реакционную массу перемешивали при 45-46°С до исчезновения лактонной формы аторвастатина кальция (ТСХ, 2,0 часа). По каплям добавляли ДМ воду (900 мл) при 45-46°С. Раствор медленно охлаждали до комнатной температуры со скоростью 2°С/мин, при этом выкристаллизовывалась новая полиморфная форма аторвастатина кальция. Продукт отфильтровывали вакуум-фильтрованием и затем сушили в лотковой вакуум-сушилке при 55-60°С в течение 24 часов.
Выход: 10,2 г (92,0%)
Относительная чистота (ВЭЖХ): 99,22%
Остаточный растворитель:
Ацетон: не более 0,2%
Несмотря на то что данное изобретение было описано на основе его конкретных воплощений, некоторые модификации и эквиваленты будут очевидны специалистам в данной области, и, подразумевается, что они включены в объем данного изобретения.
1. Кристаллическая форма VI аторвастатина кальция или ее гидраты, отличающиеся картиной рентгеновской порошковой диффракции по значениям 2Θ, определенным с использованием Shimadzu XRD-6000 с К излучением меди с λ 1,5406Å и с относительной интенсивностью >15%
3,7365; 7,7200; 8,6985; 10,2185; 12,5933; 17,9103; 18,3600; 19,4031; 20,2800; 20,8200; 22,5122 и 25,5848.
2. Кристаллическая форма VI аторвастатина кальция или ее гидраты по п.1, имеющие пики рентгеновской порошковой диффракции при 2Θ 3,7; 18,0 и 20,9° и большие пики при 2Θ 8,6; 10,2 и 19,5°.
3. Кристаллическая форма VI аторвастатина кальция или ее гидраты по п.1, отличающиеся следующим спектром 13С ядерного магнитного резонанса (ЯМР) в твердом состоянии, причем химический сдвиг выражен в миллионных долях (м.д.):
| δ (м.д.) |
| 21,898 |
| 24,294 |
| 27,767 |
| 29,368 |
| 33,939 |
| 38,275 |
| 42,836 |
| 45,980 |
| 68,932 |
| 71,266 |
| 73,617 |
| 119,357 |
| 122,987 |
| 131,214 |
| 137,515 |
| 162,696 |
| 169,066 |
| 179,540 |
| 186,890 |
| 190,640 |
4. Кристаллическая форма VI аторвастатина кальция или ее гидраты по п.1, имеющие сигналы 13С ЯМР в твердом состоянии при примерно 162,689 м.д., 169,066 м.д., 179,54 м.д., 186,89 м.д. и 190,64 м.д.
5. Кристаллическая форма VI аторвастатина кальция по п.1, которая содержит до 8 моль воды на моль аторвастатина кальция.
6. Кристаллическая форма VI аторвастатина кальция по п.1, которая содержит до 3 моль воды на моль аторвастатина кальция.
7. Кристаллическая форма VI аторвастатина кальция по п.1, которая имеет температуру плавления в интервале от 177 до 182°С.
8. Способ получения кристаллической формы VI аторвастатина кальция по п.1 как в виде гидрата, так и в безводном состоянии, [R-(R*,R*)]-2-(4-фторфенил)-бета, дельта-дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1Н-пиррол-1-гептановой кислоты полукальциевой соли (2:1), имеющей формулу
который включает
a) растворение кальциевой соли любой формы аторвастатина в органическом растворителе, таком как алифатический кетон, предпочтительно при температуре в интервале от комнатной до температуры кипения с получением прозрачного раствора соли аторвастатина,
b) по желанию, удаление примесей,
c) добавление деминерализованной воды при сохранении той же температуры,
d) выделение кристаллической полиморфной формы VI аторвастатина кальция и сушку, при желании, с захватом необходимой кристаллизационной воды.
9. Способ получения новой полиморфной кристаллической формы VI аторвастатина кальция, [R-(R*,R*)]-2-(4-фторфенил)-бета,дельта-дигидрокси-5-(1-метилэтил)-фенил-4-[(фениламино)-карбонил]-1Н-пиррол-1-гептановой кислоты кальциевой соли (2:1), имеющей формулу
который включает
a) растворение лактонной формы аторвастатина в органическом растворителе, предпочтительно алифатическом кетоне, при температуре в интервале от комнатной до температуры кипения с получением прозрачного раствора,
b) добавление водного раствора гидроксида щелочноземельного металла и деминерализованной воды при перемешивании при сохранении той же температуры,
c) выделение кристаллической полиморфной формы VI аторвастатина кальция и сушку, при желании, с захватом необходимой кристаллизационной воды.
10. Способ по п.8, где используемый аторвастатин кальций является аморфным или в виде кристаллической формы I, II, III, IV и V аторвастатина кальция или их смесью.
11. Способ по п.8, где используемый аторвастатин кальций находится в безводном состоянии или в виде гидрата с содержанием до 9 молекул воды.
12. Способ по пп.8 и 9, где используемый органический растворитель выбран из алифатических кетонов, содержащих от 1 до 3 атомов углерода.
13. Способ по п.12, где используемые алифатические кетоны представлены ацетоном, метилэтилкетоном, диэтилкетоном, метилпропилкетоном, предпочтительно ацетоном.
14. Способ по пп.8 и 9, где органический растворитель используют в 100-кратном, предпочтительно 15-кратном, более предпочтительно 10-кратном количестве от исходного соединения.
15. Способ по п.8, где растворение осуществляют нагреванием суспензии аторвастатина кальция в органическом растворителе до температуры выше 40°С и ниже 80°С, более предпочтительно, от 40 до 50°С.
16. Способ по пп.8 и 9, где примеси удаляют фильтрованием.
17. Способ по пп.8 и 9, где используют деминерализованную (ДМ) воду в 100-кратном, предпочтительно 10-кратном, более предпочтительно 5-кратном количестве от исходного соединения.
18. Способ по п.9, где используемый гидроксид щелочноземельного металла является гидроксидом кальция.
19. Способ по п.9, где добавляют гидроксид щелочноземельного металла в 50-кратном, предпочтительно 10-кратном количестве от исходного соединения, более предпочтительно в соотношении 1:1.
20. Способ по пп.8 и 9, где охлаждение осуществляют медленно до температуры от -20 до 20°С (комнатная температура), предпочтительно от 15 до 20°С для осуществления кристаллизации, причем указанное охлаждение может быть осуществлено со скоростью 2-3°С в минуту.
21. Способ по пп.8 и 9, где выделение осуществляют обычными методами, такими как фильтрование, вакуум-фильтрование, декантация, центрифугирование.
22. Способ по пп.8 и 9, где сушку выполняют с помощью обычных средств, таких как вакуумная лотковая сушилка, барабанная вакуумная сушилка и при температуре выше 50 и ниже 80°С, предпочтительно при 55°С в течение от 12 до 30 ч.