Композиции на основе белка вируса гепатита в и стрессового белка и их применение
Иллюстрации
Показать всеИзобретение относится к области иммунотерапии. Предложен белок слияния, включающий стрессовый белок и белок вируса гепатита В (HBV). Белок при введении индивидууму индуцирует или усиливает иммунный ответ против белка HBV. Предложены также нуклеиновые кислоты, кодирующие такой белок, фармацевтическая композиция, векторы и способы получения такого белка. Кроме того, предложены способы индукции или усиления иммунного ответа против белка HBV. Изобретение может быть использовано в медицине. 14 н. и 32 з.п. ф-лы, 17 ил.
Реферат
Настоящая заявка притязает на приоритет по дате подачи заявки США № 60/266733 (февраль 5, 2001). Содержание заявки № 60/266733 полностью включено в настоящую заявку в качестве ссылки.
Область изобретения
Изобретение относится к области иммунотерапии вируса гепатита B.
Предпосылки изобретения
Вирус гепатита B (HBV) представляет собой нецитопатический ДНК-содержащий вирус, который заражает людей и может привести к двум клиническим исходам. В большинстве случаев клинического инфицирования взрослых (90-95%) вирус исчезает после нескольких недель или месяцев, а у пациента развивается пожизненный иммунитет против повторного инфицирования. Однако в остальных случаях не происходит удаление вируса из тканей, и пациент остается хронически инфицированным. Последствия хронической инфекции являются серьезными: у таких субъектов с высокой вероятностью развивается рубцевание ткани печени (цирроз), а со временем может развиться гепатоцеллюлярная карцинома.
Существует профилактическая вакцина против HBV, и многие развитые страны внедрили программы детской вакцинации для уменьшения общего риска инфицирования. К сожалению, так как заболеваемость и смертность в результате инфицирования HBV происходят в течение десятилетий, воздействие вакцинации не будет, как следует, реализовано до наступления будущего. Действительно, ожидают, что ежегодный процент инфицирования HBV у взрослых снизится менее чем до 5% в течение следующих восьми лет. К 2008 году в Соединенных Штатах ежегодно будет происходить более 150000 новых случаев инфицирования и ожидают даже более в Европе и Японии. Данные субъекты составят огромный резервуар вируса, из которого возникнут от 20000 до 40000 случаев хронического инфицирования в год. Очевидно, что, несмотря на доступность вакцины, хроническая инфекция HBV продолжит оставаться серьезной проблемой для здоровья многих последующих лет.
Современные способы лечения хронического HBV включают альфа, интерферон (IFN-α) и ламивудин. Данные способы лечения оценивают по их способности уменьшать вирусную нагрузку и вызывать сероконверсию или потерю Hbe-антигена, маркера репликации HBV, и вирусемии высокого титра. IFN-α способен элиминировать Hbe, но только примерно у одной трети пациентов, у тех, у которых низка вирусная нагрузка. Лечение является дорогим и связано со значительными нежелательными побочными эффектами. Ламивудин представляет собой противовирусное средство с малой молекулой, которое хорошо переносится при оральном введении. Данное соединение эффективно в уменьшении вирусной нагрузки у пациентов, но относительно мало пациентов отвечают потерей Hbe, а прекращение лечения обычно приводит к увеличению вирусной нагрузки. С другой стороны, непрерывная терапия может привести к селекции устойчивых к ламивудину мутантных вариантов. Совместное лечение IFN-α и ламивудином не показало повышенной эффективности. Очевидно, что успешная иммунотерапия для лечения инфекций HBV является крайне желательной.
Сущность изобретения
В настоящем изобретении представлены композиции, включающие стрессовый белок или его часть и антиген HBV. Данные композиции детально обсуждают ниже. Мы отмечаем здесь, что их компоненты можно получить из различных источников, а их длина и содержание могут варьировать. Например, стрессовый белок может представлять собой белок, который экспрессируется в естественных условиях у любого млекопитающего (например, у человека или других приматов) или у любого другого класса организмов, экспрессирующих стрессовый белок (например, у бактерий или микобактерий); стрессовый белок или антиген HBV может являться полноразмерным, укороченным или удлиненным посредством добавления одного или нескольких аминокислотных остатков; и, в дополнение, содержание стрессового белка или антигена HBV может варьировать (например, стрессовый белок или его часть и антиген HBV могут содержать один или несколько аминокислотных замен). Результатом любого изменения, однако, должна являться композиция, которая может индуцировать или усилить иммунный ответ против HBV у млекопитающих. Предпочтительно, иммунный ответ является по существу достаточным, чтобы пациент, инфицированный HBV, почувствовал улучшение в признаке или симптоме инфекции. Таким образом, антиген включает встречающиеся в природе антигены, а также его фрагменты и другие варианты, которые при введении субъекту (например, посредством описанных здесь способов) индуцируют иммунный ответ на один или несколько эпитопов, представленных во фрагменте или варианте.
Также, в дополнение к полноразмерным или встречающимся в природе стрессовым белкам, композиции по изобретению могут включать фрагменты стрессовых белков, которые представляют собой иммуностимуляторы (например, фрагменты, которые способствуют иммунному ответу на антиген). Стрессовый белок или его фрагмент способствует иммунному ответу тогда, когда иммунный ответ является более значительным или в любом отношении лучшим, чем иммунный ответ, который обычно происходит при введении одного антигена HBV.
Иммунный ответ может представлять собой или гуморальный или клеточный ответ. Например, антигенный фрагмент может содержать один или несколько пептидных антигенов для HLA класса I, как описано здесь. Клеточный иммунный ответ включает в себя антиген-специфические клетки, такие как цитотоксические T-лимфоциты (CTL), а также, возможно, T-хелперные лимфоциты (Th) и клетки врожденной иммунной системы, такие как моноциты, макрофаги, дендритные клетки, натуральные киллерные клетки и γδ-T-клетки. Специалист в данной области легко способен обнаружить или иным образом оценить иммунный ответ, который выражается, например, посредством индукции цитотоксических T-лимфоцитов (см. примеры ниже), клеточным пролиферативным ответом, индукцией цитокинов или комбинацией этих событий.
В конкретном осуществлении, антиген HBV может представлять собой коровый антиген, или его фрагмент, или производное. Производные антигена HBV включают варианты антигена HBV, такие как варианты, содержащие одну или несколько аминокислотных замен (например, консервативные замены аминокислот). Например, вариант антигена HBV может содержать 1-2, 2-5, 5-10, 10-25 или более замещенных аминокислотных остатков. Альтернативно, замены или другие мутации, такие как делеции или укорочения (трункации), могут составлять 1-2, 2-5, 5-10 или 10-25% последовательности полноразмерного антигена HBV. Подобно антигенной части композиции, вариант стрессового белка может содержать одну или несколько аминокислотных замен (например, консервативные замены аминокислот). Например, вариант стрессового белка может содержать 1-2, 2-5, 5-10, 10-25 или более консервативных замен аминокислот. Здесь замены или другие мутации, такие как делеции или укорочения, опять могут составлять 1-2, 2-5, 5-10 или 10-25% последовательности полноразмерного стрессового белка.
Различные комбинации стрессовых белков и антигенов HBV также находятся в объеме изобретения. Например, композиции по изобретению включают композиции, в которых полноразмерный антиген HBV подвергнут слиянию с полноразмерным стрессовым белком; антиген, состоящий из фрагмента или другого варианта антигена HBV, объединен с полноразмерным стрессовым белком; полноразмерный антиген HBV объединен с фрагментом или другим вариантом стрессового белка, и в которых фрагмент или другой вариант антигена HBV объединен с фрагментом или другим вариантом стрессового белка. Конечно, как описано здесь, может присутствовать более чем один каждого из этих компонентов (например, более чем один антиген HBV и более чем один стрессовый белок), а каждый из компонентов может присутствовать в виде полноразмерного белка или его иммунологически активного фрагмента или варианта.
Более того, в любом из описанных здесь воплощений, антиген HBV и стрессовый белок можно объединять любым образом. Например, стрессовый белок и антиген HBV можно представить в форме полипептида слияния (где стрессовый белок и антиген HBV ковалентно связывают во время трансляции слитой открытой рамки считывания). Альтернативно, стрессовый белок и антиген HBV можно связать посредством химической конъюгации после индивидуальной трансляции или синтеза каждого из них. Компоненты можно объединять нековалентно (например, в смеси или более упорядоченной композиции). Термины "полипептид" или "белок" применяют попеременно для описания цепи аминокислотных остатков, исключая случаи, когда из контекста ясно, что подразумевают определенный смысл.
Несмотря на то, что стрессовый белок обсуждается ниже, здесь авторы настоящего изобретения замечают, что стрессовый белок может представлять собой белок теплового шока (Hsp). Более того, Hsp может представлять собой микобактериальный Hsp, такой как Hsp65 (например, Hsp65 из Mycobacterium bovis) или любой представитель семейства белков Hsp из любых видов.
Можно составить композиции по изобретению для введения субъекту различными путями и, необязательно, содержащие адъювант. Дополнительные необязательные компоненты композиции включают фармацевтически приемлемые разбавители, наполнители и носители.
Также изобретение содержит в себе способы лечения инфекций HBV у субъекта (например, у млекопитающего, такого как человек) посредством введения композиции по изобретению субъекту, инфицированному HBV, и способы предотвращения (или уменьшения вероятности) инфицирования субъекта (например, млекопитающего, такого как человек) HBV посредством введения субъекту композиции по изобретению до инфицирования HBV.
Компоненты композиции не обязательно вводить субъекту непосредственно в виде полипептидов. Вместо этого можно вводить нуклеиновую кислоту, кодирующую стрессовый белок, антиген HBV или белок слияния, содержащий один или несколько каждого из них, и белок, антиген или белок слияния будут экспрессироваться у субъекта in vivo. Нуклеиновая кислота может представлять собой часть вирусного вектора, например часть генома вирусного вектора, или ее можно инкапсулировать, например, в липосомы. Альтернативно, нуклеиновую кислоту можно доставлять как голую нуклеиновую кислоту, такую как плазмидная ДНК, находящуюся под контролем регуляторных последовательностей, специфичных для эукариотических клеток или клеток млекопитающих. Способы введения молекул нуклеиновой кислоты хорошо известны в данной области.
Кроме того, изобретение включает применение композиций по изобретению (например, белков слияния, содержащих HBV, кодирующих их молекул нуклеиновой кислоты и содержащих их фармацевтических композиций) для производства лекарственного средства для лечения инфекций вируса гепатита B в соответствии с описанными здесь способами.
Другие возможности или преимущества настоящего изобретения станут ясны из детального описания, чертежей и формулы изобретения. Все цитированные здесь заявки на выдачу патента, патенты и публикации включены полностью посредством ссылки.
Краткое описание чертежей
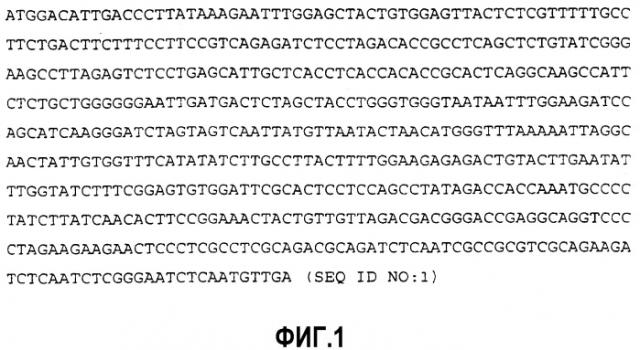
Фигура 1 представляет собой последовательность ДНК, кодирующую коровый антиген (HBc) (SEQ ID NO:1) у HBV (подтип adw).
Фигура 2 представляет собой аминокислотную последовательность корового антигена (SEQ ID NO:2) у HBV (подтип adw).
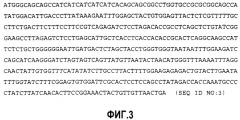
Фигура 3 представляет собой последовательность ДНК конструкции hisHepCorT(149/87S97F), которая кодирует меченный гистидином укороченный коровый антиген HBV (аминокислоты 1-149; SEQ ID NO:3).
Фигура 4 представляет собой аминокислотную последовательность, кодируемую последовательностью ДНК, указанной на фигуре 3 (SEQ ID NO:4).
Фигура 5 представляет собой последовательность ДНК конструкции hisHepCor(97F)Hsp65, которая кодирует меченный гистидином белок слияния, включающий полноразмерный коровый антиген HBV и белок Hsp65 (SEQ ID NO:5)
Фигура 6 представляет собой аминокислотную последовательность, кодируемую последовательностью ДНК, указанной на фигуре 5 (SEQ ID NO:6).
Фигура 7 представляет собой последовательность ДНК конструкции hisHepCorT(149/87S97F)Hsp65, которая кодирует меченный гистидином белок слияния, включающий укороченный (аминокислоты 1-149) коровый антиген HBV, слитый с белком Hsp65 (SEQ ID NO:7).
Фигура 8 представляет собой аминокислотную последовательность, кодируемую последовательностью ДНК, указанной на фигуре 7 (SEQ ID NO:8).
Фигура 9 представляет собой последовательность ДНК конструкции HepCorT(151/97F)Hsp65, которая кодирует белок слияния, включающий укороченный (аминокислоты 1-151) коровый антиген HBV, слитый с белком Hsp65 (SEQ ID NO:9).
Фигура 10 представляет собой аминокислотную последовательность, кодируемую последовательностью ДНК фигуры 9 (SEQ ID NO:10).
Фигура 11 представляет собой последовательность ДНК конструкции HepCor(97F)Hsp65, которая кодирует белок слияния, включающий полноразмерный коровый антиген HBV, слитый с белком Hsp65 (SEQ ID NO:11).
Фигура 12 представляет собой аминокислотную последовательность, кодируемую последовательностью ДНК, указанной на фигуре 11 (SEQ ID NO:12).
Фигура 13 представляет собой график, отображающий активность примирования CTL (корректированный % лизиса в зависимости от соотношения эффектор:цель) у мышей C57BL/6, иммунизированных различными иммуногенами (HepCorT(151/97F)Hsp65, HepCor(97F)Hsp65, HepCorT(151/97F), HepCor(97F) и hisHepCorT(149/87S97F)Hsp65). Результирующую активность CTL оценивали по сравнению с клетками EL4, предварительно импульсно активированных контрольным пептидом MUT-1.52-59.Kb. Контрольным мышам инъецировали плацебо (буфер).Фигура 14 представляет собой график, отображающий активность примирования CTL (корректированный % лизиса в зависимости от соотношения эффектор:цель) у мышей C57BL/6, иммунизированных различными иммуногенами (как на фигуре 13). Результирующую активность CTL оценивали по сравнению с клетками EL4, предварительно импульсно активированных специфичным для антигена HBV пептидом HBc.93-100.Kb. Контрольным мышам инъецировали плацебо (буфер).
Фигура 15 представляет собой график, отображающий активность примирования CTL (корректированный % лизиса в зависимости от соотношения эффектор:цель) у мышей C57BL/6, иммунизированных различными иммуногенами (как на фигуре 13). Результирующую активность CTL оценивали по сравнению с клетками EL4.HBc.1D7, экспрессирующими коровый антиген гепатита B. Контрольным мышам инъецировали плацебо (буфер).
Фигура 16 представляет собой график, отображающий активность примирования CTL (IFN-γ (пкг/мл) в зависимости от соотношения эффектор:цель) у мышей C57BL/6, иммунизированных различными иммуногенами (как на фигуре 13). Способность получающихся в результате CTL секретировать гамма интерферон (IFN-γ) оценивали по сравнению с клетками EL4, культивированными совместно со специфичным для антигена HBV пептидом HBc.93-100.Kb. Контрольным мышам инъецировали плацебо (буфер).
Фигура 17 представляет собой график, отображающий активность примирования CTL (TNF-α (OD410)) у мышей C57BL/6, иммунизированных различными иммуногенами (как на фигуре 13). Способность образовавшихся CTL секретировать фактор некроза опухоли альфа (TNF-α) оценивали по сравнению с клетками EL4, культивированными совместно со специфичным для антигена HBV пептидом HBc.93-100.Kb. Контрольным мышам инъецировали плацебо (буфер).
Детальное описание
Изобретение относится к композициям, содержащим антиген HBV, подходящим для лечения или предотвращения инфекции HBV. Состав композиций может варьировать, как описано здесь, но композиции включают стрессовый белок или его часть (например, фрагмент) или его производное и антиген HBV. Ниже обсуждают различные материалы и процедуры, подходящие для применения в способах по изобретению.
Так как последовательности нуклеиновой кислоты, кодирующие стрессовый белок и белки HBV известны и доступны, конструкции нуклеиновой кислоты, кодирующие их (по одному или как продукт слияния) можно легко получить с использованием способов, регулярно применяемых в данной области. Например, нуклеиновые кислоты, кодирующие стрессовый белок (Hsp), факультативно связанные с антигеном, смотри в WO 89/12455, WO 94/29459, WO 98/23735, WO 99/07860 и ссылках, цитированных в них. Белки слияния можно получать не только посредством рекомбинантных способов, но также посредством конъюгации стрессового белка (например, Hsp) и антигена HBV после трансляции. Способы конъюгации описаны, например, у Hermanson (Bioconjugate Techniques, Academic Press, San Diego, CA, 1996), Lussow et al. (Eur. J. Immun. 21:2297-2302, 1991) и у Barrios et al. (Eur J. Immun. 22:1365-1372, 1992). Такие способы конъюгации включают применение связывающих средств, таких как глютаральдегида, карбодиимидов и бисдиазобензидина; применение гетеробифункциональных веществ, образующих поперечные связи, таких как сложного эфира M-малеимидобензоил-N-гидроксисукцинимида или использование цистеиновых остатков (которые присутствуют в естественных условиях и/или которые включили рекомбинантным способом) стрессового белка и антигена для содействия формированию межмолекулярных дисульфидных связей.
Для включения в белок слияния или композицию по изобретению подходит любой антиген HBV. Предпочтительный антиген HBV представляет собой коровый антиген HBV или его фрагмент или производное. Для облегчения тестирования антиген HBV необязательно можно модифицировать так, чтобы включать известные рестрицированные по MHC мышиные эпитопы CTL, например, такие как рестрицированные по H-2Kb мышиные эпитопы CTL. Пример такой модификации описан в примерах (например, в штамме HBV adw, остаток 97 представляет собой изолейцин, его замена на фенилаланин приводит к получению рестрицированного по H-2Kb эпитопа CTL). Кроме того, антиген можно модифицировать, так чтобы он включал эпитопы HLA человека более чем из одного подтипа HBV (например, adw, ayw, adr или ayr). Например, единичная замена треонина на валин в позиции 91 корового антигена HBV, показанного на фигуре 2, воспроизведет последовательность известного рестрицированного по HLA-A11 эпитопа CTL, обнаруженного и в подтипе HBV adw и в подтипе HBV adr. Другие производные корового антигена HBV включают укорочения. Такие укорочения включают в качестве неограничивающих примеров укорочения, при которых удаляется весь богатый аргинином C-концевой домен или его часть (аминокислоты HBc от 150 до 185). Подходящие укороченные фрагменты HBc включают фрагменты, состоящие только из первых N-концевых 149 аминокислот или из первых N-концевых 151 аминокислот HBc. В любом случае, подходящий фрагмент антигена HBc (или любого подходящего антигена HBV) в идеале могли бы включать один или несколько B-клеточных или T-клеточных эпитопов (один или несколько B-клеточных эпитопов или один или несколько T-клеточных эпитопов), предпочтительно один или несколько эпитопов CTL. Дополнительно, концевой цистеин корового антигена HBV можно удалить или заменить другой аминокислотой. Можно произвести другие модификации аминокислотной последовательности. Другой пример представляет собой замену якорного остатка известного рестрицированного по HLA эпитопа CTL для усиления активности связывания пептида с молекулой MHC класса I. Хотя данные модифицированные коровые антигены HBV подходят для включения в белки слияния, для получения иммунного ответа на HBV их также можно применять самостоятельно (факультативно сформулированных с адъювантом).
Дополнительные антигены HBV, подходящие для применения по настоящему изобретению, включают коровый антиген HBV, антиген HBV e (HBeAg), белок x (HBx), полипептид полимеразы и белки оболочки HBV S, M и L (Seeger and Mason, Microbiol. Mol. Biol. Rev. 64:51-68, 2000; Ganem and Schneider, Hepadnavirdae: The viruses and their replication. In: Knipe, DM and Howley, PM, eds. Fields Virology, Philadelphia: Lippincott Williams & Wilkins, 2001:2923-2969).
Как описано выше, антиген HBV, стрессовый белок или оба вместе могут содержать одну или несколько аминокислотных замен (например, консервативные замены аминокислот). Данные замены можно, хотя и не обязательно, произвести вместо одного или нескольких предсказанных одного или нескольких несущественных аминокислотных остатков. Термин "консервативная замена аминокислоты" представляет собой замену, в которой один аминокислотный остаток заменяют другим аминокислотным остатком, обладающим схожей боковой цепью. В данной области установлены семейства аминокислотных остатков, обладающие схожими боковыми цепями. Данные семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислотными боковыми цепями (например, аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин), неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Независимо от того, рассчитывают ли произвести замену в предсказанном несущественном участке или вносят случайно во всю кодирующую последовательность антигена HBV или стрессового белка (например, посредством насыщающего мутагенеза) или ее часть, получающиеся в результате мутанты можно скринировать на антигенную и иммуностимулирующую активности, соответственно, для определения мутантов, сохраняющих биологическую активность. Вслед за мутагенезом кодируемые белки можно рекомбинантно экспрессировать и определить активность белков.
Антиген HBV можно подвергнуть слиянию или с N-концом или с C-концом стрессового белка, с линкером или промежуточной экзогенной последовательностью или без них. В альтернативном осуществлении два антигена HBV (встречающиеся в естественных условиях или вариант, как описано здесь) можно присоединить к стрессовому белку (один к N-концу, а другой к C-концу стрессового белка; оба к N-концу или оба к C-концу). Дополнительно, один или несколько антигенов HBV (опять, встречающиеся в естественных условиях или их фрагменты, или другие варианты, или из того же или другого белков HBV) можно присоединить или к N-концу или к C-концу стрессового белка или к обоим. Для специалистов в данной области ясно, что можно произвести дополнительные альтернативные расположения, если включить более чем один стрессовый белок.
Стрессовый белок и антиген HBV (или их комбинации, например стрессовый белок и два или несколько антигенов HBV) можно связать посредством химической конъюгации после того, как каждый транслируется и синтезируется индивидуально. Как отмечено выше, компоненты можно также объединять нековалентно (например, в смеси или более упорядоченной композиции). Композиции, содержащие стрессовый белок или его иммуностимуляторные фрагменты, нековалентно объединенные с антигеном HBV, можно получить, как описано в патентах США №№ 6048530, 6017544, 6017540, 6007821, 5985270, 5948646, 5935576, 5837251, 5830464 или 5750119. Также см. патенты США №№ 5997873, 5961979, 6030618, 6139841, 6156302, 6168793 и Международную публикацию № WO 97/06821.
Кроме того, в композицию можно включать более чем один тип вирусного антигена. Например, в дополнение к антигену HBV, композиции по изобретению могут включать (или кодировать; любые описанные здесь белки можно вводить непосредственно или посредством нуклеиновых кислот) антиген другого патогенного организма. Таким образом, в дополнение к антигену HBV, композиции могут включать (или кодировать) антиген гепатита C, антиген вируса простого герпеса (HSV), антиген вируса иммунодефицита человека (HIV), антиген цитомегаловируса (CMV), антиген вируса Эпштейна-Барр (EBV), антиген респираторно-синцитиального вируса (RSV), антиген вируса папилломы человека (HPV), антиген вируса герпеса или их комбинации. Такие же альтернативы, какие были описаны для осуществлений, в которых композиции содержали только HBV в качестве вирусного антигена (например, способ объединения со стрессовым белком, включение полноразмерных, фрагментированных белков или их вариантов; различное количество компонентов и их расположение), подходят для осуществлений, в которых в композиции присутствуют (или ею кодируются), по меньшей мере, один антиген HBV и, по меньшей мере, один другой вирусный антиген.
Неожиданно также обнаружили, что удаление С-концевого богатого аргинином домена из корового антигена приводит к получению полипептида, способного индуцировать иммунный ответ к коровому антигену, конкретно клеточный и/или иммунный ответ посредством CTL. Богатый аргинином домен корового антигена расположен между 150 и 183 аминокислотами корового антигена (Nassal, J. Virol. 66:4107-4116, 1992). Походящие фрагменты корового антигена включают, но не ограничиваются ими, фрагменты без всего данного региона или его части. Например, подходящие фрагменты корового антигена могут содержать первые 149 или 151 аминокислота (или менее чем 149 или 151 аминокислота).
Композиции по изобретению могут факультативно включать адъювант. Пример адъювантов, которые могут быть эффективны, включают в качестве неограничивающих примеров полный адъювант Фрейнда (FCA), неполный адъювант Фрейнда (FIA), SAF, мурамил дипептид (MDP), липополисахарид (LPS), липид A, монофосфорил липид A (MPL), токсин коклюша (PT), стеарилтирозин, γ-инулин, RIBI (содержащий три компонента, выделенных из бактерий), Quil-A, сапонины (QS21), квасцы (гидрохлорид алюминия, фосфат алюминия), фосфат кальция, MF-59, иммуностимуляторные комплексы (ISCOMS), олигонуклеотиды CpG и цитокины (Gupta and Siber, Vaccine 13:1263-1276, 1995; Singh and O'Hagan, Nature Biotechnology 17:1075-1081, 1999).
Подходящий фрагмент или производное антигена HBV в идеале должен содержать, по меньшей мере, один B-клеточный или T-клеточный эпитоп (или оба). В предпочтительном осуществлении, фрагмент или производное должны содержать, по меньшей мере, один эпитоп для CTL.
Изолированы, клонированы и охарактеризованы множество стрессовых белков из разнообразного множества организмов (Mizzen, Biotherapy 10:173-189, 1998). Любой иммуностимулирующий Hsp или его иммуностимулирующий фрагмент подходят для применения в полипептидах слияния и композициях. Например, среди главных детерминант, узнаваемых посредством иммунных ответов хозяев в ответ на инфекцию Mycobacterium tuberculosis и Mycobacterium leprae находятся Hsp70, Hsp60, Hsp20-30 (Hsp с низкой молекулярной массой) и Hsp10 (гомолог GroES). В дополнение обнаружено, что Hsp65 из Bacille Calmette Guerin (BCG), штамма Mycobacterium bovis представляет собой эффективный иммуностимулирующий агент, как описано в примере ниже.
Семейства стрессовых генов и белков для применения по настоящему изобретению хорошо известны в данной области и включают, например, Hsp100-200, Hsp100, Hsp90, Lon, Hsp70, Hsp60, TF55, Hsp40, FKBP, циклофилины, Hsp20-30, ClpP, GrpE, Hsp10, убиквитин, калнексин и дисульфидизомеразы белка. См., например, Macario, Cold Spring Harbor Laboratory Res. 25:59-70, 1995; Parsell et al., Rev. Genet. 27:437-496, 1993 и патент США № 5232833.
Примеры белков Hsp100-200 включают Grp170 (белок регулируемый глюкозой). Grp170 находится в просвете ER и в компартменте, предшествующем аппарату Гольджи, и может играть роль в укладке и сборке иммуноглобулинов.
Примеры белков Hsp100 включают Hsp100 млекопитающих, Hsp104 дрожжей и ClpA, ClpB, ClpC, ClpX и ClpY E. coli.
Примеры белков Hsp90 включают HtpG E. coli, Hsp83 и Hsc83 дрожжей и Hsp90alpha, Hsp90beta и Grp94 (малый gp96) человека. Hsp90 связывает группы белков, которые представляют собой типичные регуляторные молекулы, такие как рецепторы стероидных гормонов (например, рецепторы глюкокортикоидов, эстрогенов, прогестерона и тестостерона), транскрипционные факторы и протеинкиназы, которые играют роль в механизмах передачи сигналов. Белки Hsp90 также участвуют в формировании больших, часто встречающихся комплексов белков, включающих другие стрессовые белки.
Lon представляет собой тетрамерную АТФ-зависимую протеазу, которая разрушает несобственные белки E. coli.
Примеры белков Hsp70 включают Hsp72 и Hsc73 клеток млекопитающих, DnaK бактерий или микобактерий, таких как Mycobacterium leprae, Mycobacterium tuberculosis, and Mycobacterium bovis (такие как Bacille Calmette Guerin; указанный здесь выше как Hsp71), DnaK E. coli, дрожжей и других прокариот и BiP и Grp78. Hsp70 способен специфически связывать АТФ, а также развернутые полипептиды и пептиды и принимать участие в укладке и разворачивании, а также в сборке и разрушении комплексов белков.
Примеры белков Hsp60 включают Hsp65 микобактерий. Бактериальный Hsp60 также широко известен как GroEL. Hsp60 формирует большие гомоолигомерные комплексы и, кажется, играет ключевую роль в укладке белка. Гомологи Hsp60 присутствуют в митохондриях и хлоропластах эукариот.
Примеры белков TF55 включают Tcp1, TRiC и термосому. Данные белки обычно встречаются в цитоплазме эукариот и некоторых архебактерий и формируют многочленные кольца, способствующие укладке белка. Также они слабо гомологичны с Hsp60.
Примеры белков Hsp40 включают DnaJ прокариот, таких как E. coli и микобактерии и HSJ1, HDJ1 и Hsp40. В числе других активных веществ клетки Hsp40 играет роль в качестве молекулярного шаперона в укладке белка, обеспечении термоустойчивости и репликации ДНК.
Примеры FKBP включают FKBP12, FKBP13, FKBP25 и FKBP59, Fprl и Nepl. Обычно белки обладают пептидилпропилизомеразной активностью и взаимодействуют с иммуносупрессорами, такими как FK506 и рапамицин. Белки обычно обнаруживают в цитоплазме и эндоплазматическом ретикулуме.
Пример циклофилина включают циклофилины A, B и C. Белки обладают пептидилпропилизомеразной активностью и взаимодействуют с иммуносупрессором циклоспорином A.
Hsp20-30 также называют малый Hsp. Hsp20-30 обычно обнаруживают в больших гомоолигомерных комплексах или, возможно, гетероолигомерных комплексах. Организм или тип клеток может экспрессировать несколько различных типов малых Hsp. Hsp20-30 взаимодействует со структурами цитоскелета и может играть роль в регуляции полимеризации/деполимеризации актина. Hsp20-30 быстро фосфорилируется при стрессе или воздействии на покоящиеся клетки ростовых факторов. Гомологи Hsp20-30 включают альфа-кристаллин.
ClpP представляет собой протеазу E. coli, вовлеченную в деградацию аномальных белков. Гомологи ClpP обнаружены в хлоропластах. ClpP формирует гетероолигомерные комплексы с ClpA.
GrpE представляет собой белок E. coli массой примерно 20 кДа, который вовлечен в поиск поврежденных стрессом белков, а также деградацию поврежденных белков. GrpE играет роль в регуляции экспрессии стрессовых генов у E. coli.Примеры Hsp10 включают GroES and Cpn10. Hsp10 обнаружен у E. coli и в митохондриях и хлоропластах эукариотических клеток. Hsp10 формирует семичленное кольцо, ассоциированное с олигомерами Hsp60. Hsp10 также вовлечен в укладку белков.
Обнаружено, что убиквитин связывает белки в координации с протеолитическим удалением белков посредством АТФ-зависимой цитозольной протеазы.
В дополнение к полноразмерным стрессовым белкам, любые иммуностимулирующие фрагменты или производные могли бы являться пригодными по настоящему изобретению. Иммуностимулирующий фрагмент или производное (например, иммуностимулирующий фрагмент Hsp) представляет собой фрагмент или производное, которые способствуют иммунному ответу на антиген. Фрагмент или производное могут способствовать иммунному ответу рядом способов. Например, фрагмент может индуцировать иммунный ответ, который не мог бы возникнуть иначе, или усиливать иммунный ответ, который мог бы. Описан ряд иммуностимулирующих фрагментов. Подходящие фрагменты включают в качестве неограничивающих примеров (a) 161-370 аминокислоты Hsp70 микобактерий (конкретно, Hsp70 M. tuberculosis) (Huang et al., J. Exp. Med. 191:403-408; 2000, заявка на патент США 09/761534, поданная 16 января 2001 года); (b) АТФазный домен или связывающий пептиды домен Hsp70 микобактерий (конкретно, Hsp70 M. tuberculosis) (Young, заявка США № 09/025178, поданная 25 ноября 1997 года); (c) 280-385 аминокислоты мышиного Hsc70 (основного представителя семейства Hsc70) (Udono et al., Int. Immunol. 13:1233-1242, 2001); (d) 359-610 аминокислоты Hsp70 M. tuberculosis (Wand et al., Immunity 15:971-983, 2001); (e) соответствующие с (a) по (d) регионы гомологов Hsp70 других видов и (f) с 1 по 200 аминокислоты Hsp65 микобактерий (конкретно, Hsp65 M. bovis) (Chu et al., заявка США № 09/613303, поданная 10 июля 2000 года).
Стрессовые белки, пригодные по настоящему изобретению, можно получить из любого подходящего организма, включая в качестве неограниченных примеров грамположительные бактерии, грамотрицательные бактерии, энтеробактерии (например, E. coli), микобактерии (конкретно, M. leprae, M. tuberculosis, M. vaccae, M. smegmatis и M. bovis), дрожжи, дрозофилу и позвоночных (например, птиц, таких как цыплята, или млекопитающих, таких как крысы, мыши или приматы, включая людей).
Для получения терапевтической (например, иммунотерапевтической) композиции, содержащей белок слияния, полипептид можно получать рекомбинантным способом в бактериях, дрожжах, растениях или клетках растений или животных или клетках животных. Например, полипептиды слияния по изобретению можно получать посредством трансформации (трансфекции, трансдукции или инфекции) клеток-хозяев фрагментом ДНК, кодирующим полипептид, в подходящем экспрессирующем носителе. Подходящие экспрессирующие носители включают плазмиды, вирусные частицы и фаги. Для клеток насекомых подходят бакуловирусные экспрессирующие векторы. Целый экспрессирующий носитель или его часть может интегрироваться в геном клетки-хозяина. В некоторых обстоятельствах это желательно для использования индуцибельного экспрессирующего вектора, например, для LACSWITCH® Inducible Expression System (Stratagene; La Jolla, CA).
Специалистам в области молекулярной биологии понятно, что можно применять любую из обширного множества экспрессирующих систем для доставки рекомбинантных полипептидов слияния. Определенная клетка-хозяин и вектор не критичны для изобретения.
Белки и полипептиды можно получать с помощью клеток растений. Для клеток растений подходят вирусные экспрессирующие векторы (например, вирус мозаики цветной капусты и вирус табачной мозаики) и плазмидные экспрессирующие векторы (например, плазмида Ti). Такие клетки и векторы доступны из широкого диапазона источников (например, the American Type Culture Collection, Manassas, VA; также см., например, Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, New York, 1994). Способы трансформации и трансфекции и выбор экспрессирующего носителя зависит от избранной системы-хозяина. Способы трансформации и трансфекции ранее описаны, например, у Ausubel et al. Экспрессирующие носители можно выбрать из экспрессирующих носителей, описанных, например, в Pouwels et al., Cloning Vectors: A Laboratory Manual, 1985, Supp. 1987. Клетки-хозяева, содержащие экспрессирующий носитель, можно культивировать в обычной питательной среде, адаптированной как необходимо для активации или репрессии выбранных генов, отбора трансформированных клеток или амплификации выбранных генов.
Когда уместно и выгодно, нуклеиновая кислота, кодирующая полипептид слияния, может включать сигнальную последовательность для выделения полипептида слияния, например, для облегчения выделения полипептида из культуры клеток. Для эффективной трансляции вставленных последовательностей нуклеиновой кислоты также могут являться необходимыми специфические сигналы инициации. Данные сигналы включают инициирующий кодон ATG и расположенные рядом последовательности. В некоторых случаях необходимо предоставить внешние сигналы контроля трансляции, включая, возможно, инициирующий кодон ATG. Более того, для обеспечения трансляции целой вставки, инициирующий кодон должен находиться в фазе с рамкой считывания желательной кодирующей последовательности. Данные внешние сигналы контроля трансляции и инициирующие кодоны могут быть различного происхождения: и естественного, и синтетического. Эффективность экспрессии можно увеличить посредством включения соответствующих усиливающих транскрипцию или трансляцию элементов (например, которые описаны в Bittner et al., Methods in Enzymol. 153:516, 1987). Дополнительно генную последовательность можно модифицировать для оптимального использования кодонов в соответствующей экспрессирующей системе или, альтернативно, экспрессирующего хозяина можно модифицировать для экспрессии специфических молекул тРНК для содействия экспрессии желательного гена.
Могло бы оказаться полезным, если бы полипептиды слияния растворялись при нормальных физиологических условиях. Также в изобретении представлены способы применения белков слияния (или других конфигураций белков, включая ковалентные и нековалентные комплексы и микстуры), в которых стрессовый белок (или его иммуностимулирующий фрагмент) и антиген HBV подвергнут слиянию (или иначе объединены) с не имеющим к ним отношения третьим белком или полипептидом для создания, по меньшей мере, белка, состоящего из трех частей, или смеси белков. Третий белок может облегчить очистку, обнаружение или растворение белка слияния или другого комплекса или он может обеспечивать некоторые другие функции. Например, для создания белков слияния с lacZ, можно применять экспрессирующий вектор pUR278 (Ruther et al., EMBO J. 2:1791, 1983). Для экспрессии чужеродных полипептидов как белков слияния, содержащих глутатион-S-трансферазу (GST), можно применять ве