Композиции на основе белков матрикса зубной эмали для модуляции иммунного ответа
Иллюстрации
Показать всеПредложено применение препарата из активного вещества матрикса зубной эмали, выбранного из белков, представляющих собой энамелины, амелогенины, неамелогенины, обогащенные пролином неамелогенины, тафтелины и их смеси для производства фармацевтической композиции для профилактики или лечения системного воспаления и/или инфекции и соответствующий способ. Композиция защищает от тяжелого септического шока и полиорганной недостаточности, вызванной токсином или тяжелой системной инфекцией, а снижение уровней TNF и IL-6 свидетельствует об общей ремиссии. 2 н. и 50 з.п. ф-лы, 3 ил.
Реферат
Область изобретения
Настоящее изобретение относится к применению препарата активного вещества матрикса зубной эмали, такого как амелогенин, процессированный продукт амелогенина или его метаболит, для производства фармацевтической композиции для модуляции иммунного ответа. Композицию можно использовать для профилактики и/или лечения состояния или заболевания у млекопитающего, характеризующегося наличием у млекопитающего дисбаланса его естественного иммунного ответа на внутренние и/или внешние стимулы. Как правило, указанное состояние может быть системным или местным, таким как системное и/или посттравматическое общее воспаление или аутоиммунное заболевание.
Предпосылки изобретения
Нормальной функцией иммунной системы является защита организма посредством атаки и разрушения чужеродных микроорганизмов таких, как бактерии и вирусы. В нормальных условиях они распознаются в качестве инвазивных агентов и таким образом обезвреживаются.
Ответственной за иммунный ответ индивидуума является лимфоидная система, которая представляет собой совокупность лимфоцитов, их предшественников и производных и всех поддерживающих клеток. При аномальных состояниях или дисбалансе иммунной системы она не способна реагировать и разрушать чужеродные микроорганизмы, ошибочно принимает собственные клетки и ткани за чужеродные и атакует их или неадекватно активируется по типу гиперчувствительности.
Иммунный ответ на антигенный агент, является ли он чужеродным антигеном или аутоантигеном, обычно характеризуется продукцией антител В-лимфоцитами и разрушением любых клеток, несущих данные антигены, Т-лимфоцитами или природными клетками-киллерами (NK). Однако дефекты лимфоидных В- или Т-клеток могут привести к развитию иммунодефицитных заболеваний или нарушению функции иммунного ответа. Дефицит или дефект иммунной системы может быть врожденным, т.е. возникнуть в результате мутации гена, или может быть приобретенным, например, в результате вирусной инфекции или в результате старения. Возникший таким образом дефект может приводить или не приводить к летальному исходу в зависимости от стадии дифференцировки стволовых клеток или лимфоцитов, на которой он происходит.
Помимо антигена для полной активации лимфоцитам необходимы лимфокины. Например, Т-хелперные клетки не пролифирируют, пока не получат сигналы от макрофагов, а Т-цитотоксические клетки, равно как и В-клетки, зависят от сигналов от Т-хелперных клеток и, возможно, также от макрофагов, для их полного развития. Для адекватного иммунного ответа необходимы скоординированные активности нескольких типов клеток, что означает, что модуляция экспрессии или активности лимфокинов потенциально оказывает положительное воздействие на побочные иммунные ответы.
После шоков, ожогов, обширных хирургических вмешательств или травматических повреждений функции иммунной системы могут быть гиперстимулированы, что выражается в системном, неизбирательном, интенсивном общем воспалении организма, в то время как другие функции резко угнетены. В случае, когда иммунный ответ хозяина является таким образом неконтролируемым, то разбалансированные состояния клеточной активации, которые наблюдаются, в последующем приводят к проявлению клинических состояний. Подобные состояния могут быть ответной реакцией острой фазы, общим воспалением, анергией, сепсисом, инфекцией или недостаточностью отдельных органов, и в конечном итоге могут привести к полиорганной недостаточности. Полиорганная недостаточность, или дисфункция, является наиболее распространенной причиной смерти в отделениях интенсивной терапии. В настоящее время терапия, направленная на профилактику или лечение неконтролируемого иммунного ответа, неспособна значительно изменить исход таких состояний.
Другими примерами разбалансированных состояний являются случаи, когда иммунная система атакует свой собственный организм. Данные ситуации различаются по природе антигена, который «запускает» атаку, а также механизмам и проявлению атаки. Часто данные реакции относят соответственно к аллергии, гиперчувствительности замедленного типа, аллотрансплантату и аутоиммунным реакциям.
Анергия представляет собой другое разбалансированное состояние, при котором организм не способен реагировать на введенный аллерген или антиген. Полагают, что анергия является результатом межклеточной передачи сигналов после взаимодействия Т-клеточного рецептора (TCR) и антигена пептидпредставляющего главного комплекса гистосовместимости (МНС) при отсутствии «костимулирующего» сигнала. Данный костимулирующий сигнал в норме присутствует на клеточной поверхности антигенпрезентирующих клеток (АРС).
Иммунная система модулирует свою функцию локально и системно. Например, гиперчувствительность замедленного типа может проявляться либо локально в характерной кожной реакции, либо в системной реакции, когда большие количества антигена поступают в кровяное русло, и которая характеризуется лихорадкой, недомоганием, болями в суставах и снижением числа циркулирующих лимфоцитов. В общем, воспаление определяется как локальная ответная реакция на повреждение клеток, в то время как общее воспаление или полиорганная недостаточность представляет системное воспаление.
После травмы моноциты и макрофаги немедленно гиперактивируются с очень интенсивным высвобождением провоспалительных цитокинов. Данное интенсивное высвобождение приводит к развитию общего воспаления с последующим существенным параличом функции клеток у большинства пациентов. Через 3-5 суток данное состояние преодолевается с помощью вновь поступивших моноцитов/макрофагов, у которых, возможно, отсутствует полный спектр активности, вследствие того, что они являются незрелыми. Кроме того, у пациентов также может протекать противовоспалительная стадия (синдром компенсаторной противовоспалительной ответной реакции) и иногда наблюдается смешанная реакция с наличием как про-, так и противовоспалительных компонентов (синдром смешанной антагонистической ответной реакции).
Таким образом, посттравматическое нарушение баланса опосредуемой клетками иммунной регуляции в основном возникает в результате одновременной атаки на направление дифференцировки моноцитов/макрофагов и Т-клетки, вызывая разобщение взаимодействия интактных клеток. Травматический стресс оказывает влияние не только на способность к адекватной и специфической деятельности каждого типа клеток, но также влияет на способность к регуляции и модулирующему контролю, которыми в норме обладают моноциты/макрофаги и Т-клетки по отношению друг к другу в ряде регуляторных путей. Данная потеря регуляторной функции происходит моментально в момент повреждения.
Известными цитокинами воспаления, которые вызывают вышеописанное первоначальное системное гипервоспаление, являются, например, фактор некроза опухолей α (TNF-альфа), интерлейкин-1 (IL-1), IL-6 и гамма-интерферон, которые могут взаимодействовать синергически с TNF-альфа. Результаты клинических испытаний, направленных на даун-регуляцию данных медиаторов, с использованием, например, антител против эндотоксина, TNF-альфа, антагонистов IL-1 или активирующего фактора тромбоцитов, оказались в равной степени разочаровывающими. Было установлено, что данные средства не только не проявляли регулирующего действия, но даже повышали смертность.
Кроме того, в стрессовых условиях легко запускается продукция и высвобождение моноцитами/макрофагами простагландина Е2(PGE2), который, возможно, является наиболее сильным эндогенным иммунным супрессором. PGE2 представляет ингибитор митогенеза Т-клеток, экспрессии рецептора IL-2 и синтеза IgM-антител В-клетками. Посредством внутриклеточного повышения уровня цАМФ, PGE2 также отрицательно регулирует синтез TNFα и IL-1 моноцитами/макрофагами. PGE2 может также ингибировать синтез ТН1-цитокинов (IL-2, IFNγ), но не синтез IL-4 ТН2-клетками. Таким образом, секреция PGE2 может изменить баланс в пользу ответа ТН2-типа, приводя к «запуску» продукции от IgM к IgG1 и IgE В-клетками. Изменение баланса таким образом оказывает влияние на развитие ТН1- или ТН2-доминирующего ответа.
Традиционные средства и способы, используемые для регуляции иммунного ответа у пациента, часто приводят к проявлению нежелательных побочных реакций. Например, иммуносупрессоры, такие как циклоспорин А, азатиоприн и преднизон, используются для подавления иммунной системы пациента с аутоиммунным заболеванием или у пациентов, которым были пересажены трансплантаты. Однако подобные препараты подавляют общий иммунный ответ у пациентов, тем самым подавляя способность у пациента к проявлению иммунного ответа против возбудителей инфекционных заболеваний, не являющихся причиной возникновения первоначального заболевания. Вследствие подобных вредных побочных эффектов и значения в медицине регуляции иммунной системы средства и способы регуляции специфических компонентов иммунной системы были предметом изучения в течение многих лет.
Белки матрикса зубной эмали, присутствующие в матриксе зубной эмали, представляют наиболее хорошо известные предшественники зубной эмали. Перед образованием цемента белки матрикса зубной эмали откладываются на поверхности корней в апикальном конце развивающегося корня зуба. Отложенный матрикс зубной эмали является инициирующим фактором образования цемента. Кроме того, образование цемента само по себе связано с развитием периодонтальной связки и альвеолярной кости. Как было показано заявителями настоящей заявки, перед осуществлением настоящего изобретения белки матрикса зубной эмали могут, следовательно, способствовать периодонтальной регенерации посредством имитации естественному прикреплению в зубе (Gestrelius S., Lyngstadaas SP, Hammarströцm L. Emdogain - periodontal regeneration based on biomimicry. Clin. Oral Invest 4:120-125 (2000)).
Матрикс зубной эмали состоит из ряда белков, таких как амелогенин, энамелин, тафт-белок, протеазы и альбумин. Амелогенины, основные составляющие компоненты матрикса зубной эмали, представляют семейство гидрофобных белков, происходящих из одного гена посредством последующего альтернативного сплайсинга и контролируемого постсекреторного процессинга. Они остались высококонсервативными в ходе эволюции позвоночных и проявляют высокий общий уровень гомологии последовательностей среди исследованных высших позвоночных (> 80%). Фактически транскрипт гена амелогенина свиньи и человека различается только на 4% оснований. Так, белки матрикса зубной эмали, несмотря на происхождение от свиней, являются «своими» при попадании в организм человека и могут способствовать регенерации зубов у людей без «запуска» аллергических ответных реакций или других нежелательных реакций.
Белки матрикса зубной эмали и производные матрикса зубной эмали (EMD) были описаны ранее в патентной литературе, как способные к образованию твердой ткани (т.е. образованию эмали, патент США № 4672032 (Slavkin)), связыванию твердых тканей (EP-B-0337967 и EP-B-0263086) и заживлению ран, например, на коже и слизистой (заявка WO 99/43344).
Сущность изобретения
Настоящее изобретение основано на неожиданной находке, что активные вещества зубной эмали обладают способностью модулировать иммунные механизмы у млекопитающих. В данном случае иммуномодуляция определяется как повышение или снижение уровня иммунного ответа посредством различных специфических и неспецифических средств.
Таким образом, предпочтительное воплощение настоящего изобретения представляет собой применение активного вещества зубной эмали для производства фармацевтической композиции для профилактики и/или лечения состояния у млекопитающего, где указанное состояние характеризуется дисбалансом иммунного ответа у указанного млекопитающего на иммуноген такой, как внешний или внутренний стимулирующий фактор.
«Дисбаланс иммунного ответа» может иметь место после шоков, ожогов, обширных хирургических вмешательств и/или травматического повреждения. Термин относится к ситуации/состоянию, при котором одна или более функций иммунной системы могут быть либо гиперстимулированы, что выражается в системном, неизбирательном, обширном воспалении, в то время как другие функции могут быть одновременно или независимо подавлены. Термин «дисбаланс иммунного ответа» относится к ситуации/состоянию, при котором иммунологический ответ хозяина не контролируется, и когда небалансированные состояния активации клеток, которые при этом наблюдаются, приводят к последующему проявлению клинических состояний. Подобные состояния могут быть реакцией в острой фазе, общим воспалением, анергией, шоком, сепсисом, инфекцией и/или недостаточностью органа, и в конечном итоге могут привести к полиорганной недостаточности.
Другими примерами «дисбаланса иммунного ответа» являются ситуации/состояния, при которых инертная иммунная система субъекта атакует свой собственный организм. Подобные ситуации различаются по природе антигена, который «запускает» атаку, и механизмам и проявлениям атаки. Часто данные реакции относят соответственно к аллергии, гиперчувствительности замедленного типа, аллотрансплантату и аутоиммунным реакциям.
Термин «дисбаланс иммунного ответа» может относиться как к местным, так и к системным ситуациям, описанным выше. Например, в общем воспаление определяется, как местный ответ на повреждение клеток, в то время как общее воспаление или полиорганная недостаточность представляют примеры системного воспаления.
В настоящем контексте термин «иммуноген» используется для описания любого фактора, который способен вызывать иммунный ответ. Он может представлять собой, например, токсин, грибок, паразит, вирус, бактерию, пыльцу, пыль, загрязняющую частицу, цитокин, гормон, стресс, хирургическую операцию, ожог, трансплантированный орган или кровь, тканевый трансплантат, шок, травму или чужеродный или собственный антиген.
Иммунологические реакции по типу гиперчувствительности представляют иммунные ответы, которые приводят к повреждению тканей или нарушению функции органов. Они подразделяются на пять типов (I-V) согласно механизму повреждения тканей, они принимают участие в развитии многих серьезных заболеваний и нарушений у людей, таких как анафилаксия, астма, пищевая аллергия, тяжелая псевдопаралитическая миастения и системная красная волчанка.
В одном воплощении настоящего изобретения активное вещество зубной эмали используется для производства фармацевтической композиции для профилактики и/или лечения состоянии у млекопитающего, при котором, по меньшей мере, часть иммунной системы реагирует по типу гиперчувствительности на указанный иммуноген. В предпочтительном воплощении, по меньшей мере, часть иммунной системы указанного млекопитающего таким образом неизбирательно стимулирована.
Состояния, для которых выгодно изобретение, включают состояния, при которых дисбаланс иммунного ответа у указанного млекопитающего является локальным и/или системным. В настоящем контексте "системный" определяется как относящийся к или общий для системы, т.е. поражающий организм в целом, в противоположность местной реакции. Указанное состояние может представлять собой, например, аутоиммунное заболевание, выбранное из группы, состоящей из ревматоидного артрита, заболеваний кожи, аллергии, склероза, артериосклероза, рассеянного склероза, астмы, псориаза, волчанки, системной красной волчанки, сахарного диабета, тяжелой псевдопаралитической миастении, синдрома хронической усталости, фибромиалгии, болезни Крона, тиреоидита Хашимото, болезни Грейвса, болезни Аддисона, синдрома Гиллиана-Барре и склеродермы.
В настоящем контексте термин «аутоиммунное заболевание» относится к широкому ряду более чем 80 различных тяжелых хронических заболеваний. Аутоиммунные заболевания являются третьей основной категорией заболеваний в США после злокачественных опухолей и заболеваний сердца. 75-90% всех аутоиммунных заболеваний имеют место у женщин и, как правило, в детородном возрасте. Помимо органов аутоиммунные заболевания поражают также нервы, мышцы, кровь, соединительные ткани, желудочно-кишечную систему и все системы организма.
Причина аутоиммунных заболеваний полностью не известна или не понятна, однако полагается, что гормоны, наследственность и факторы окружающей среды играют основную роль в их причине и начале развития. Причины большинства данных заболеваний являются чисто индивидуальными и практически непредсказуемыми. Аутоиммунные заболевания не представляют полное нарушение механизма толерантности, а в большей степени отражают возникновение специфической ответной реакции на определенный собственный антиген.
Другие состояния, в равной степени предусмотренные для настоящего изобретения, характеризуются как системные воспаления и/или инфекции, и они могут быть связаны с травмой, ожогами, хирургической операцией, диализом, шоком и/или бактериальной или вирусной инфекцией. В предпочтительном воплощении изобретения системное состояние связано с заболеванием, выбранным из группы, состоящей из экстракорпоральной мембранной оксигенации (ЕСМО), шока, синдрома системной воспалительной реакции (SIRS) сепсиса, полиорганной недостаточности, отторжения имплантата, такого как орган и/или протез, хирургической операции по поводу шунтирования сердца и легких, хронического воспаления, астмы и/или стресса, связанного с заболеванием легких, бактериальной инфекции, гангрены, инфекции мягких тканей и инфекции ран.
Некоторые тяжелые травмы, такие как обширная хирургическая операция, системное воспаление, ожоги или шок, могут привести к тяжелому нарушению иммунологической реактивности у пациента, клиническим последствием которого является высокая чувствительность индивидуума с травмой к возникновению тяжелой системной инфекции, которая может привести к обширному разрушению тканей и недостаточности органов.
В одном воплощении настоящего изобретения активные вещества зубной эмали используются таким образом для производства фармацевтической композиции для профилактики и/или лечения состояния у млекопитающего, где, по меньшей мере, часть иммунной системы атакует молекулы, клетки или ткани организма, продуцировавшего их. В данном случае активные вещества зубной эмали используются для производства фармацевтической композиции для профилактики и/или лечения состояния у млекопитающего, где состояние характеризуется как системное воспаление и/или инфекция.
При системном, неизбирательном, обширном воспалении части иммунной системы стимулированы, в то время как другие функции в комплексе опосредованного клетками иммунитета (CMI) в значительной степени подавлены. Нарушения иммунной системы как последствия травмы происходят в виде последовательности состояний активации клеток и внутри сложной очередности событий, которые еще не совсем хорошо понятны. Одним известным фактом является то, что травматический стресс вызывает разобщение взаимодействия интактных моноцитов с Т-клетками, которое связано с существенными изменениями в регуляции моноцитов и значительным подавлением функции Т-клеток. В предпочтительном воплощении настоящего изобретения активные вещества зубной эмали используются таким образом для производства фармацевтической композиции для восстановления баланса во взаимодействии моноцитов с Т-клетками у пациента, т.е. для восстановления нормальной регуляции моноцитов и функции Т-клеток.
В настоящем контексте воспаление определяется как местная ответная реакция на повреждение клеток, для которого характерно расширение капилляров, инфильтрация лейкоцитов, краснота, жар, боль, отечность и/или потеря функции, и что в норме служит в качестве механизма начала элиминации вредных агентов и отторжения поврежденной ткани.
Активные вещества зубной эмали в настоящем изобретении используются для производства фармацевтической композиции для модуляции концепции активации Т-хелперных клеток у млекопитающих. Активное вещество зубной эмали, входящее в фармацевтическую композицию, в данном случае может модулировать уровень экспрессии, высвобождения и/или функцию меж- и/или внутриклеточных сигнальных соединений. Активное вещество зубной эмали, входящее в состав фармацевтической композиции, может альтернативно модулировать уровень экспрессии, высвобождения и/или функцию, по меньшей мере, одного цитокина, принимающего участие в механизме иммунитета у указанного млекопитающего или модулировать клеточный сигнальный путь, участвующий в механизме иммунитета у того же указанного млекопитающего.
Многие распространенные и клинически важные болезненные состояния, такие как ревматоидный артрит, астма, туберкулез, лепра, шистосомоз, хронический гепатит, тиреоидит и рассеянный склероз, представляют примеры хронического воспаления и его последствия. Хроническое воспаление может возникнуть в результате неспособности элиминировать возбудитель острого воспаления, от аутоиммунного ответа до собственного антигена, или может быть вызвано врожденным хроническим раздражителем низкой интенсивности, который присутствует. Оно характеризуется одновременным протеканием воспаления и восстановления, с притоком и активацией макрофагов, лимфоцитов и других клеток, «запущенных» скоординированным действием цитокинов и факторов роста. Предпочтительное воплощение настоящего изобретения включает применение активного вещества зубной эмали для производства фармацевтической композиции для лечения и/или профилактики хронического воспаления.
Хроническое воспаление наиболее подходящим образом определяется как процесс, при котором практически не прекращающееся воспаление и пытающееся реализоваться заживление ткани восстановлением происходят одновременно. Несмотря на то, что часто оно просто определяется по времени протекания, например, при наличии очагов поражения в течение более 6 недель, его традиционно по продолжительности относят к хроническому, любое подобное определение в целом является произвольным. В некоторых случаях на микроскопическом уровне хроническое воспаление определяют по клеточной ответной реакции, хотя этот критерий бывает различным и вместе с тем не совсем надежным.
Характерные признаки данного процесса наилучшим образом оцениваются при его сравнении с острой воспалительной реакцией. В противоположность острому воспалению, при котором ответная реакция хозяина приводит к элиминации раздражителя, с последующей регенерацией или восстановлением затронутых тканей, хроническое воспаление в большей мере характеризуется одновременным проявлением воспаления и восстановления, чем последовательным протеканием этих процессов. Восстановление всегда является признаком хронического воспаления, поскольку оно связано с раздражителями, которые вызывают разрушение структуры тканей. Как правило, восстановление достигается врастанием грануляционной ткани, которая включает макрофаги, фибробласты и новые кровеносные сосуды.
Другие важные отличия между острым и хроническим воспалением относятся к относительному балансу между экссудацией и притоком клеток, а также типам клеток, которые преобладают в воспалительной ответной реакции. При хроническом воспалении, как правило, имеется менее выраженная экссудативная реакция и повышенный приток воспалительных клеток, что может сопровождаться местной клеточной пролиферацией. В противоположность острому воспалению, которое обычно характеризуется притоком большого количества нейтрофилов, при всех формах хронического воспаления преобладающими инфильтрующими клетками являются макрофаги. В зависимости от природы раздражителя в месте воспаления продуцируются различные профили медиаторов воспаления и факторов роста (в общем называемых цитокинами), приводя к развитию различных морфологических типов хронического воспаления.
Системные эффекты воспаления более выражены при хронических воспалительных заболеваниях, и они могут вносить существенный вклад в клинические последствия. Данные системные эффекты в значительной степени опосредуются цитокинами. В то время как наиболее типичными системными эффектами острого воспаления являются жар и лейкоцитоз, для хронического воспаления, как правило, характерны усталость, сонливость, потеря массы тела и истощение.
Когда состояние и/или заболевание, относящееся к настоящему изобретению, характеризуется как инфекция, то указанное состояние может быть вызвано обсеменением бактерией, выбранной, но не ограничиваясь этим, из группы, состоящей из грамотрицательных бактерий и грамположительных бактерий 1) G+: например, стафилококки и стрептококки, которые способны высвобождать эндотоксин пептидогликан (PepG), который является специфическим компонентом клеточной оболочки G+ бактерий. 2) G-: например, колиформы и другие бактерии, высвобождающие липополисахариды (LPS) из их внешней клеточной оболочки во время заражения. В данном случае иммунологическое состояние вызывается эндотоксином и/или экзотоксином, продуцированным инфицирующей бактерией.
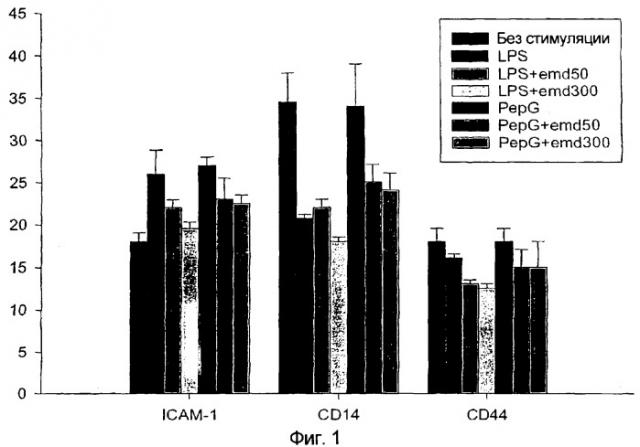
В настоящем изобретении клеточные ответные реакции в крови человека, вызванные эндотоксинами из Staphylococcus aureus (PepG) и Escherichia coli (LPS), эффективно модулируются введением амелогенинов, как представлено в примере 1. Данные результаты четко показывают потенциальное модулирующее действие активных веществ зубной эмали на иммунный механизм у млекопитающих.
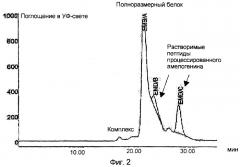
В другом опыте, проведенном заявителями и документально представленном в настоящей заявке в примере 2, при использовании модели сепсиса на свиньях, потенциальное терапевтическое действие производных матрикса зубной эмали исследуется в условиях in vivo.
EMD, даже при доставке в больших болюсах-инъекциях, как это показано в опыте 2, являются безопасными при системном введении в высоких дозах. Кроме того, в данном случае доказано, что системные инъекции производных матрикса зубной эмали нейтрализуют действие эндоксина (LPS) у свиней. В целом можно придти к заключению, что начало септического шока у обработанных свиней замедляется по сравнению с контрольными свиньями. Задержка зависит от дозы, доза 1 мг/кг массы тела приводит к непродолжительной задержке (примерно на 30 мин), в то время как доза 5 мг/кг защищает, или, по меньшей мере, достоверно замедляет (> 5 час), начало септического шока и связанную с ним полиорганную недостаточность.
Одним возможным механизмом, с помощью которого можно объяснить положительное действие производных матрикса зубной эмали в отношении индуцированного LPS шока, является то, что производные матрикса зубной эмали связывают LPS и таким образом инактивируют его токсическое действие. Другой, в равной степени предполагаемой возможностью, является то, что производные матрикса зубной эмали конкурируют с LPS за один и тот же рецептор(ы), например, на лейкоцитах, макрофагах, остеокластах и/или тучных клетках. Таким образом, предпочтительное воплощение изобретения относится к применению активного вещества зубной эмали для получения фармацевтической композиции, где указанное активное вещество зубной эмали инактивирует токсическое действие эндотоксина и/или экзотоксина, продуцированного микроорганизмом, непосредственным связыванием с указанным эндотоксином и/или экзотоксином, и/или связыванием с клеточным рецептором указанного эндотоксина и/или экзотоксина.
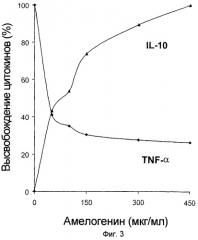
Третьим и, с большей долей вероятности, возможным механизмом является то, что производные матрикса зубной эмали модулируют иммунный ответ непосредственно регуляцией, положительным образом, экспрессии каскада цитокинов и сигнальных молекул, которые играют важную роль в развитии индуцированного LPS септического шока. Основываясь на ранее проведенных опытах ex vivo, не описанных в настоящей заявке, представляется разумным отнести, по меньшей мере, частично действие производных матрикса зубной эмали к последнему механизму. Кроме того, на основании проведенного анализа крови также можно предположить, что производные матрикса зубной эмали оказывают прямое действие на экспрессию цитокинов в лейкоцитах. Действие является специфическим, имеющим сильное влияние на TNF и IL-6, но не на IL-1β. Наконец, вполне возможно, что принимают участие все предложенные механизмы и что это является комбинацией данных эффектов, которые и приводят к положительному действию производных матрикса зубной эмали на данной модели.
Задержка начала развития септического шока, о которой сообщается в примере 2, имеет большое клиническое значение. В одном предполагаемом воплощении изобретения задержка непосредственно связана с количеством «свободного» LPS в крови, и производные матрикса зубной эмали будут, таким образом, доставляться в качестве вспомогательного средства для антибиотиков при тяжелой бактериемии и инфекциях, подобных менингиту, для задержки и/или снижения действия токсинов. Подобное лечение будет решающим для выживания пациента в критические часы с последующим началом лечения антибиотиками.
В другом в равной степени предпочтительным воплощении действие производных матрикса зубной эмали вызвано непосредственной модуляцией воспалительной ответной реакции, и таким образом производные матрикса зубной эмали можно использовать в широком ряду клинических ситуаций, когда шок является возможным осложнением. Сюда входят все обширные хирургические операции, трансплантации, травмы, ЕСМО, острый диализ, тяжелые инфекции, тяжелые аллергии и многое другое.
Не намереваясь ограничить объем настоящего изобретения, одним теоретическим объяснением механизма, с помощью которого описанное здесь активное вещество зубной эмали может модулировать иммунную систему млекопитающего, является его взаимодействие с клеточным поверхностным рецептором и/или клеточной поверхностной структурой, выбранной из группы, состоящей из ICAM, HLA-антигена, рецептора интерлейкина 1, рецептора интерлейкина 2, рецептора интерлейкина 3, рецептора интерлейкина 4, рецептора интерлейкина 5, рецептора интерлейкина 6, рецептора интерлейкина 7, рецептора интерлейкина 8, рецептора интерлейкина 9, рецептора интерлейкина 10, рецептора интерлейкина 11, рецептора интерлейкина 12, рецептора интерлейкина 13, рецептора интерлейкина 14, рецептора интерлейкина 15, рецептора интерлейкина 16, рецептора интерлейкина 17, рецептора интерлейкина 18, рецептора IFNα, рецептора IFNβ, рецептора IFN▵, рецептора IFNγ, рецептора IFN Ω, рецепторов PDGF, рецепторов TGF, рецептора TNF, рецептора EGF, вариантов CD44 и семейства рецепторов интегрина.
Клеточные поверхностные рецепторы являются хорошо известными медиаторами коммуникации клеток, когда они активируются их соответствующей сигнальной молекулой, лигандом. Клеточный поверхностный рецептор связывается с лигандом с высокой или низкой аффинностью и превращает данное внеклеточное событие в один и более внутриклеточных сигналов, которые изменяют поведение клетки-мишени. Таким образом, активные вещества зубной эмали могут быть способны модулировать иммунную систему изменением поведения клетки-мишени аналогичным образом. Таким образом, в одном воплощении настоящего изобретения активные вещества зубной эмали активируют клеточный поверхностный рецептор, тем самым индуцируя специфический межклеточный путь передачи сигналов рецепторами и изменяя экспрессию одного или более генов, что в конечном итоге приводит к изменению поведения указанной клетки.
В другом воплощении настоящего изобретения активное вещество зубной эмали может активировать клеточный поверхностный рецептор, который непосредственно функционирует в качестве фермента, так называемого каталитического рецептора, примером является трансмембранный белок с цитоплазматическим доменом, который функционирует в качестве тирозинкиназы.
В еще одном предпочтительном воплощении настоящего изобретения активное вещество зубной эмали активирует G-белок-связанный поверхностный рецептор, который непосредственно активирует или инактивирует определенный, связанный с мембраной фермент плазмы или ионный канал. Взаимодействие между рецептором и ферментом и/или ионным каналом, как правило, опосредуется третьим белком, таким как G-белок (GTP-связывающий регуляторный белок), который активирует внутриклеточные медиаторы такие как, но не ограничиваясь этим, циклический АМР, InsP3 и Ca2+.
Все цитокины, такие как интерлейкины, IFNγ и TNFα, играют решающую роль в регуляции иммунного ответа. Особый интерес вызывает регуляция гена цитокина, как часть дифференциации Т-клеток в подгруппы ТН1 и ТН2. Действие цитокина может, например, опосредоваться через его специфический рецептор, который инициирует путь трансдукции сигнала, который сам по себе может привести к высвобождению цитокинов по принципу обратной связи.
Как показано в примере 1, амелогенин обладает модулирующим действием на высвобождение цитокинов и регуляцию поверхностных рецепторов воспаления в ответ на продукты клеточной оболочки бактерий. Таким образом, воплощение настоящего изобретения включает применение активного вещества зубной эмали для производства фармацевтической композиции для модуляции иммунного ответа опосредованием сигнала через рецептор цитокина, такой как IL-2R, IL-4R, IL-10R, IFNγR и TNFαR. Альтернативно, поскольку высвобождение цитокинов регулируется уровнем их экспрессии, активное вещество зубной эмали также может модулировать иммунный ответ инициацией повышающей и/или понижающей регуляцией уровня экспрессии одного или более цитокина(ов) у млекопитающего, тем самым модулируя высвобождение и/или функцию одного или более цитокина(ов).
В особо предпочтительном воплощении настоящего изобретения активное вещество зубной эмали опосредует регуляцию иммунного ответа через TNFαR. Рецепторы TNFα экспрессируются на всех типах соматических клеток за исключением эритроцитов. Описано два рецептора массой 55 кДа (TNF-R1; также обозначаемый CD120а, также относящийся к члену 1А надсемейства рецепторов TNF (TNF-RSF1A) и массой 75 кДа (TNF-R2; также обозначаемый CD120b, также относящийся к члену 1В надсемейства рецепторов TNF (TNF-RSF1B). TNFαR имеет отношение к рецептору NGF с низкой аффинностью и к человеческому клеточному поверхностному антигену CD40 и эффективно экспрессируется на стимулированных Т-клетках и В-лимфоцитах. Третий подтип рецепторов экспрессируется в печени здорового человека. Он связывается с TNFα, но не с TNFβ.
Были установлены различные эффекты двух подтипов рецепторов. Оказалось, что участие р55-рецептора специфически приводит к индукции молекул клеточной адгезии ICAV-1, E-селектина, V-CAM-1 и CD44, в то время как участие р55- и р75-рецепторов индуцирует экспрессию α-2-интегрина. Помимо связанных с мембраной рецепторов описано несколько растворимых белков, которые связываются с TNF. Данные белки массой примерно 30 кДа, называемые Т-ВР-1 и Т-ВР-2 (белки, связывающиеся с фактором некроза опухолей), происходят из TNF-связывающего домена мембранного рецептора. Возможно, они функционируют в качестве физиологических регуляторов активности TNF посредством ингибирования связывания TNF с его рецептором.
Биологическая активность IL-2 опосредуется мембранным рецептором, который экспрессируется практически исключительно на активированных, но не находящихся в покое, Т-клетках. IL-5 и IL-6 модулируют экспрессию рецептора IL-2. В другом предпочтительном воплощении настоящего изобретения представляется, что активное вещество зубной эмали опосредует регуляцию иммунного ответа через IL-2R.
Выделяют три различных типа рецепторов IL-2, которые экспрессируются различно и независимо. Рецептор IL-2 с высокой аффинностью составляет примерно 10% всех рецепторов IL-2, экспрессируемых клетками. Данный рецептор является мембранным рецепторным комплексом, состоящим из двух субъединиц IL-2R-альфа (антиген ТАС = антиген активации Т-клеток; р55) и IL-2R-бета (р75; новое обозначение CD122). р75 экспрессируется конститутивно на находящихся в покое Т-лимфоцитах, NK-клетках и ряде других типах клеток, в то время как экспрессия р55, как правило, наблюд