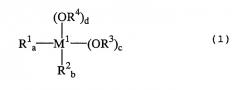Способ получения эфира угольной кислоты
Иллюстрации
Показать всеИзобретение относится к усовершенствованному способу производства диалкилкарбоната, включающий стадии: (1) проведения реакции между первой смесью металлорганического соединения и диоксидом углерода, необязательно в присутствии алкилового спирта, содержащего линейную или разветвленную С1-С12-алкильную группу, причем указанная первая смесь металлорганического соединения содержит смесь реакционноспособного металлорганического соединения, имеющего в своей молекуле две связи металл-кислород-углерод, и нерегенерируемого инертного соединения, которое образовано из указанного реакционноспособного металлорганического соединения и которое имеет в своей молекуле три связи металл-углерод, где указанное реакционноспособное металлорганическое соединение выбрано из группы, которую составляют: металлорганическое соединение, представленное формулой (1):
где: М1 представляет собой атом олова или титана; каждый из заместителей R1 и R2 независимо друг от друга представляет собой линейную или разветвленную С1-С12-алкильную группу, каждый из заместителей R3 и R4 независимо друг от друга представляет собой линейную или разветвленную C1-С12-алкильную группу, и каждый из индексов а и b представляет собой целое число от 0 до 2, а+b=2, каждый из индексов c и d представляет собой целое число от 0 до 2, и a+b+c+d=4; и металлорганическое соединение, представленное формулой (2):
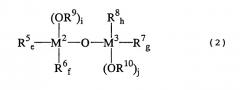
где: каждый из М2 и М3 независимо друг от друга представляет собой атом олова или титана; каждый из заместителей R5, R6, R7 и R8 независимо друг от друга представляет собой линейную или разветвленную С1-С12-алкильную группу; каждый из заместителей R9 и R10 независимо друг от друга представляет собой линейную или разветвленную С1-С12-алкильную группу; и каждый из индексов е, f, g и h представляет собой целое число от 0 до 2, e+f=2, g+h=2, каждый из индексов i и j представляет собой 1, е+f+i=3 и g+h+j=3, и где нерегенерируемое инертное соединение включает, по меньшей мере, одно соединение, представленное следующей формулой (6):
где: M представляет собой атом олова или титана; каждый из заместителей R11, R12 и R13 независимо друг от друга представляет собой линейную или разветвленную С1-С12-алкильную группу; заместитель R14 представляет собой линейную или разветвленную С1-С12-алкильную группу; и каждый из индексов k, l и m представляет собой целое число от 0 до 4, k+l+m=3 или 4, n представляет собой целое число 0 или 1, и k+l+m+n=4, с получением в результате реакционной смеси, содержащей диалкилкарбонат, образованный в ходе реакции, указанное негенерируемое инертное соединение и регенерируемое метаморфное металлорганическое соединение, образованное из указанного реакционноспособного металлорганического соединения; (2) разделения указанной реакционной смеси, необязательно в присутствии алкилового спирта, содержащего линейную или разветвленную С1-С12-алкильную группу, на первую часть, содержащую диалкилкарбонат и указанное нерегенерируемое инертное соединение, и вторую часть, содержащую указанное регенерируемое метаморфное металлорганическое соединение; и (3) взаимодействия указанной второй части указанной реакционной смеси с алкиловым спиртом, содержащим линейную или разветвленную C1-C12-алкильную группу, с образованием второй смеси металлорганического соединения и воды и удаления указанной воды из указанной второй смеси металлорганического соединения, причем указанная вторая смесь металлорганического соединения содержит смесь реакционноспособного металлорганического соединения, имеющего в своей молекуле две связи металл-кислород-углерод, и нерегенерируемого инертного соединения, которое образуется из указанного реакционноспособного металлорганического соединения и которое имеет в своей молекуле три связи металл-углерод, где указанное реакционноспособное металлоорганическое соединение включает, по меньшей мере, одно соединение, выбранное из группы, состоящей из металлорганического соединения, представленного формулой (1) и металлорганического соединения, представленного формулой (2), и указанное нерегенерируемое инертное соединение включает, по меньшей мере, одно соединение, представленное формулой (6). 13 з.п. ф-лы, 2 табл., 2 ил.
Реферат
Область техники
Настоящее изобретение относится к способу получения эфира угольной кислоты из металлорганического соединения и диоксида углерода. Более конкретно настоящее изобретение относится к способу получения эфира угольной кислоты, включающему стадии: (1) проведения реакции между первой смесью металлорганического соединения и диоксидом углерода, где первая смесь металлорганического соединения содержит смесь реакционноспособного металлорганического соединения, имеющего в своей молекуле, по меньшей мере, две связи металл-кислород-углерод, и нерегенерируемого инертного соединения, которое образовано из реакционноспособного металлорганического соединения, с получением в результате реакционной смеси, содержащей эфир угольной кислоты, полученный в результате реакции, нерегенерируемое инертное соединение и регенерируемое метаморфное металлорганическое соединение, образованное из реакционноспособного металлорганического соединения; (2) разделения реакционной смеси на первую часть, содержащую сложный эфир угольной кислоты и нерегенерируемое инертное соединение, и вторую часть, содержащую регенерируемое металлорганическое соединение; и (3) взаимодействия второй части реакционной смеси со спиртом с образованием второй смеси металлорганического соединения и воды и удаления воды из второй смеси металлорганического соединения, где вторая смесь металлорганического соединения содержит смесь реакционноспособного металлорганического соединения, имеющего в своей молекуле, по меньшей мере, две связи металл-кислород-углерод, и нерегенерируемого инертного соединения, которое образовано из реакционноспособного металлорганического соединения.
С помощью способа настоящего изобретения эфир угольной кислоты может быть получен с высоким выходом из металлорганического соединения, имеющего в своей молекуле, по меньшей мере, две связи металл-кислород-углерод, и диоксида углерода. Одним из преимуществ указанного способа является то, что диоксид углерода не обладает ни токсичностью, ни коррозионной активностью и является недорогим. Кроме того, способ настоящего изобретения обладает преимуществом не только в том, что металлорганическое соединение после применения в этом способе может быть регенерировано и рециркулировано для повторного применения, но также и в том, что нерегенерируемое инертное металлорганическое соединение, образованное в этом способе, может быть удалено из реакционной системы, посредством чего реализуется эффективное и стабильное производство эфира угольной кислоты. Более того, отсутствует необходимость в использовании большого количества дегидратирующего агента, в результате чего предотвращается образование отходов, образующихся из дегидратирующего агента. Таким образом, способ настоящего изобретения является коммерчески весьма полезным и имеет высокое промышленное значение.
Предшествующий уровень техники
Эфир угольной кислоты является полезным соединением. Например, эфир угольной кислоты используют в качестве добавок в различных целях, таких как присадка к бензину для повышения октанового числа и присадка к дизельному топливу для снижения количества частиц в выхлопном газе, генерируемом при сгорании дизельного топлива. Эфир угольной кислоты также используют в качестве алкилирующего агента, карбонилирующего агента, растворителя и т.д. в области синтеза органических соединений, таких как поликарбонат, уретан, фармацевтические средства и агрохимикаты. Эфир угольной кислоты также может быть использован в качестве электролита для литиевого аккумулятора, исходного вещества для получения смазочного масла и исходного вещества для получения раскислителя, который может быть использован для защиты бойлерных труб от ржавления.
В качестве обычного способа получения эфира угольной кислоты можно упомянуть способ, в котором фосген, используемый в качестве источника карбонила, вводят в реакцию со спиртом, в результате чего образуется эфир угольной кислоты. Так как фосген, используемый в этом способе, является исключительно вредным и высококоррозионным, этот способ невыгоден из-за того, что транспортировка и хранение фосгена требует особой осторожности, и, кроме того, необходимы большие затраты на эксплуатацию технологического оборудования и обеспечение безопасности. Кроме того, этот способ вызывает проблему необходимости утилизации соляной кислоты, образующейся в качестве загрязняющего побочного продукта.
Другой обычный способ получения эфира угольной кислоты представляет собой способ окислительного карбонилирования, при котором монооксид углерода, используемый в качестве источника карбонила, вводят в реакцию со спиртом и кислородом в присутствии катализатора, такого как хлорид меди, в результате чего получают эфир угольной кислоты. В указанном способе монооксид углерода (который является исключительно вредным) используют под высоким давлением; следовательно, указанный способ невыгоден из-за того, что имеют место большие затраты на эксплуатацию технологического оборудования и обеспечение безопасности. Кроме того, проблема названного способа заключается в том, что имеет место побочная реакция, такая как окисление монооксида углерода с образованием диоксида углерода. По этой причине желательно разработать безопасный и более эффективный способ производства эфира угольной кислоты.
В таких обычных способах, в которых фосген или монооксид углерода используются в качестве исходного вещества, галоген, такой как хлор, присутствует в исходном веществе сам по себе или в составе катализатора. Следовательно, в случае указанных способов полученный эфир угольный кислоты содержит следовое количество галогена, который не может быть полностью удален с помощью простой стадии очистки. Когда такой эфир угольной кислоты используют в качестве присадки к бензину, присадки к светлым нефтепродуктам или в качестве материала для производства электронного оборудования, существует опасность, что галоген, содержащийся в эфире угольной кислоты, будет вызывать коррозию оборудования. Для снижения количества галогена в эфире угольной кислоты только до следовых количеств необходимо проводить тщательную очистку эфира угольной кислоты. По этой причине желательно разработать способ производства эфира угольной кислоты, в котором не используют какое-либо галогенсодержащее исходное вещество и галогенсодержащий катализатор.
С другой стороны, на практике реализован способ, в котором диоксид углерода вводят в реакцию с этиленоксидом или подобным соединением с получением циклического угольного эфира и полученный циклический эфир угольной кислоты вводят в реакцию с метанолом, получая в результате диметилкарбонат. Преимущество указанного способа заключается в том, что диоксид углерода как исходное вещество является безвредным, и коррозионные вещества, такие как соляная кислота, по существу не используются и не образуются. Однако этот способ отличается следующими проблемами. В этом способе побочным продуктом является этиленгликоль; следовательно, с точки зрения стоимости производства необходимо искать пути эффективной утилизации побочного этиленгликоля. Кроме того, трудно осуществить безопасную транспортировку этилена (который является исходным веществом для производства этиленоксида) и этиленоксида. Следовательно, для исключения потребности в транспортировке необходимо, чтобы завод по производству эфира угольной кислоты этим способом был построен в месте, которое находится рядом с заводом по производству этилена и этиленоксида.
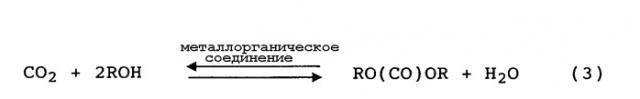
Также известен способ, по которому диоксид углерода, используемый в качестве источника карбонила, вступает в равновесную реакцию со спиртом в присутствии катализатора, содержащего металлорганическое соединение, имеющее связь металл-кислород-углерод, в результате чего образуется эфир угольной кислоты и вода. Такая равновесная реакция представлена следующим уравнением (3):
(R представляет собой ненасыщенную или насыщенную углеводородную группу)
Преимущество указанного способа состоит в том, что диоксид углерода и спирт как исходные вещества являются безвредными. Однако этот способ основан на равновесной реакции, в которой эфир угольной кислоты и вода как продукты реакции образуются одновременно. Как и в случае названного выше способа окислительного карбонилирования с использованием монооксида углерода образуется вода. Однако в способе окислительного карбонилирования не используется равновесная реакция. Равновесие равновесной реакции с использованием диоксида углерода в качестве исходного вещества термодинамически смещено в сторону исходной системы. Следовательно, проблема способа на основе равновесной реакции заключается в том, что для получения эфира угольной кислоты с высоким выходом необходимо, чтобы эфир угольной кислоты и вода как продукты реакции удалялись из реакционной системы. Кроме того, также существует проблема в том, что образующаяся вода разлагает катализатор, что не только препятствует реакции, но также приводит к тому, что число рециклов катализатора (то есть число циклов регенерации и повторного использования) составляет только 2 или 3. Для решения этой проблемы предложены различные способы удаления воды (которая является продуктом реакции) с использованием дегидратирующего агента.
Например, предложен способ, в котором спирт и диоксид углерода вводят в реакцию друг с другом, в результате чего образуется эфир угольной кислоты и вода, где большое количество дициклогексилкарбодиимида (DCC) (который является дорогим органическим дегидратирующим агентом) или подобного соединения используется в качестве дегидратирующего агента (см. Collect. Czech. Chem. Commun., Vol. 60, 687-692 (1995)). Проблема указанного способа состоит в том, что дегидратирующий агент после использования не может быть регенерирован, в результате чего существует большое количество отходов, полученных из дегидратирующего агента.
В других способах получения эфира угольной кислоты используют ортоэфир карбоновой кислоты в качестве органического дегидратирующего агента (см. нерассмотренную выложенную патентную заявку Японии N. Hei 11-35521) (В этом патентном документе есть следующие слова: «ортоэфир карбоновой кислоты вводят в реакцию с диоксидом углерода» и «ацеталь реагирует с диоксидом углерода». Однако в результате последних исследований в данной области в общем случае высказано предположение, что настоящий реакционный путь состоит в следующем. «Спирт и диоксид углерода реагируют друг с другом с получением эфира угольной кислоты и воды. Воду вводят в реакцию с ортоэфиром карбоновой кислоты»). Этот способ имеет проблему в том, что ортоэфир карбоновой кислоты (который является дорогим соединением) используется в качестве дегидратирующего агента, а метилацетат является побочным продуктом (см. "Kagaku Sochi (Chemical Equipment)", Vol. 41, № 2, 52-54 (1999)). Следовательно, указанный способ также неудачен, как и упомянутые выше способы.
Кроме того, еще в одном способе используют большое количество ацеталя в качестве органического дегидратирующего агента (см. патент Германии № 4310109). Также существует патентный документ, в котором описывается, что ацеталь и диоксид углерода реагируют друг с другом при использовании в качестве катализатора алкоксида металла или оксида дибутилолова (см. нерассмотренную выложенную патентную заявку Японии № 2001-31629). (Что касается реакции, описанной в последней, то в результате недавних исследований в данной области сделано общее предположение, что действительный ход реакции заключается в следующем. «Спирт и диоксид углерода реагируют друг с другом с получением эфира угольной кислоты и воды. Вода затем вступает в реакцию с ацеталем»). Однако эти патентные документы не указывают на способ или не предлагают способа достаточно эффективного производства ацеталя без образования отходов. Кроме того, способы, описанные в указанных патентных документах, имеют проблему в том, что когда в качестве дегидратирующего агента используют ацеталь, образуются большие количества побочных продуктов, таких как кетон и альдегид, в качестве отходов.
Результаты, достигаемые с помощью способов, в которых используют органический дегидратирующий агент, должны улучшить число рециклов катализатора. Однако органический дегидратирующий агент расходуется в стехиометрическом количестве в соответствии с образованием эфира угольной кислоты (и воды в качестве побочного продукта), так что расходуется большое количество органического дегидратирующего агента, приводя в результате к образованию большого количества продукта разложения органического дегидратирующего агента. Таким образом, необходимо проводить дополнительную стадию регенерации большого количества органического дегидратирующего агента. Кроме того, несмотря на использование органического дегидратирующего агента в большом количестве, все еще остается вероятность дезактивации катализатора. Причина состоит в следующем. В обычном способе получения эфира угольной кислоты при использовании равновесной реакции приведенного выше уравнения (3) диоксид углерода находится в сверхкритическом состоянии. В общем случае в сверхкритическом диоксиде углерода катализатор имеет плохую растворимость, и частицы катализатора, по-видимому, связаны вместе. Следовательно, проблема состоит в том, что когда оловоорганическое соединение (которое чувствительно к полимеризации) используют в качестве катализатора в сверхкритическом диоксиде углерода, оловоорганическое соединение как катализатор, вероятно, дезактивируется вследствие полимеризации.
Также предложен способ, в котором используется твердый дегидратирующий агент (см. Applied Catalysis, Vol. 142, L1-L3 (1996)). Однако проблема указанного способа состоит в том, что твердый дегидратирующий агент не может быть регенерирован, следовательно, образуется большое количество отходов.
Также известен способ, в котором спирт (метанол) и диоксид углерода реагируют друг с другом в присутствии оксида металла (оксида дибутилолова) с получением в результате реакционной смеси, и полученную реакционную смесь охлаждают и вводят в насадочную колонну, содержащую твердый дегидратирующий агент, в результате чего постепенно смещают равновесие в сторону эфира угольной кислоты, воздействуя при этом на дегидратацию, чтобы получить эфир угольной кислоты (см. нерассмотренную выложенную патентную заявку Японии № 2001-247519). Указанный способ основан на методике, в которой обычная методика использования дегидратирующего агента объединена с известным явлением, что способность адсорбировать воду обычного дегидратирующего агента (такого как молекулярные сита) имеет температурную зависимость. Дегидратирующий агент (такой как молекулярные сита) имеет более низкую способность адсорбировать воду при высоких температурах, чем при низких температурах. Следовательно, для удаления следового количества воды (побочного продукта) из реакционной смеси, которая содержит значительный избыток низкомолекулярного спирта, используемого в качестве растворителя, необходимо охлаждать реакционную смесь, в которой равновесие достигается при высокой температуре и в условиях высокого давления, до введения реакционной смеси в насадочную колонну, содержащую твердый дегидратирующий агент. Кроме того, для повышения конверсии спирта как исходного вещества, необходимо, чтобы реакционная смесь, которая охлаждена и дегидратирована в насадочной колонне, была возвращена в условия с высокой температурой и высоким давлением, которые необходимы для реакции. Следовательно, проблема способа состоит в том, что необходимо расходовать исключительно большое количество энергии для охлаждения и нагревания и требуется большое количество твердого дегидратирующего агента. Указанный способ очень широко используется для производства алифатических сложных эфиров, имеющих относительно большую константу равновесия. Однако при производстве эфира угольной кислоты из диоксида углерода и спирта, когда равновесие реакции сильно смещено в сторону исходной системы, это способ неприемлем, так как такой способ имеет проблему, заключающуюся в том, что необходимо повторять упомянутую выше операцию, которая требует очень большого расхода энергии для охлаждения и нагревания. Кроме того, для регенерации использованного дегидратирующего агента, который абсорбирует воду до насыщения, обычно необходимо прокаливать использованный дегидратирующий агент при нескольких сотнях °С, что делает этот способ коммерчески неприемлемым. Кроме того, в этом способе только один (вода) из двух продуктов равновесной реакции удаляется и, следовательно, существует проблема в том, что, когда равновесная реакция развивается с повышением концентрации эфира угольной кислоты в реакционной системе, становится невозможным дальнейшее протекание реакции, то есть способ все еще находится под ограничением равновесной реакции. Кроме того, оксид дибутилолова, который используется в качестве катализатора в этом способе, имеет исключительно низкую растворимость в метаноле и, следовательно, почти весь оксид дибутилолова как катализатор остается в реакционной системе в твердой форме. Таким образом, когда реакционную смесь охлаждают до комнатной температуры на стадии охлаждения, реакционная смесь превращается в белую суспензию, вызывая такую проблему, что на последующей стадии дегидратации, проводимой с использованием насадочной колонны, содержащей дегидратирующий агент, суспензия вызывает забивку насадочной колонны.
В целом в данной области реакций органического синтеза известен способ дегидратации, в котором воду удаляют отгонкой. Однако в области производства эфира угольной кислоты из диоксида углерода и спирта, хотя в публикации «Study Report of Asahi Glass Association for Promotion of Industrial Technology (Asahi Garasu Kogyogijutsu Shoreikai Kenkyu Hokoku)», Vol. 33, 31-45 (1978) утверждается, что «дегидратация отгонкой в настоящее время изучается», отсутствуют сообщения и подобные публикации, в которых утверждается, что способ дегидратации с использование отгонки осуществлен.
Есть статья, в которой упоминается отделение отгонкой эфира угольной кислоты из реакционной смеси, содержащей алкоксид металла, где реакционная смесь получена при взаимодействии диоксида углерода и спирта друг с другом в присутствии катализатора алкоксида металла; однако в данной области известно, что когда используется в качестве катализатора алкоксид металла, разделение отгонкой вызывает обратную реакцию, что делает трудным выделение эфира угольной кислоты отгонкой (см. «Journal of the Chemical Society of Japan (Nippon Kagaku Kaishi)», № 10, 1789-1794 (1975)). В частности, не известен способ, по которому эфир угольной кислоты, имеющий высокую температуру кипения, мог бы быть отделен с высоким выходом от реакционной смеси, содержащей алкоксид металла.
С другой стороны, алкоксид металла является настолько нестабильным, что чувствителен к дезактивации под действием влаги воздуха. Следовательно, в приведенном выше способе работа с алкоксидом металла требует большой осторожности. По этой причине обычная методика использования в качестве катализатора алкоксида металла не применяется при промышленном производстве эфира угольной кислоты. Катализатор на основе алкоксида металла является дорогим соединением, и не известна методика регенерации дезактивированного алкоксида металла как катализатора.
Предложен способ производства эфира угольной кислоты с использованием диалкоксида дибутилолова в качестве катализатора, в котором при проведении реакции катализатор образуется из оксида дибутилолова (который устойчив к воздействию влаги), добавленного в реакционную систему (см. патент Японии № 3128576). Проблема указанного способа состоит в том, что, хотя оксид дибутилолова, который загружен в реакционную систему, является стабильным, оксид дибутилолова превращается в ходе реакции в диалкоксид дибутилолова, который нестабилен. Следовательно, указанный способ не решает названную выше проблему нестабильности катализатора алкоксида металла. То есть недостаток названного способа состоит в том, что при удалении реакционной смеси из реакционной системы для выделения эфира угольной кислоты, полученного в качестве продукта реакции, нестабильный диалкоксид дибутилолова дезактивируется и не может быть регенерирован по обычной методике. Следовательно, в этом способе нет другого выбора, как выбрасывать катализатор диалкоксид дибутилолова (который является дорогим соединением) в виде отхода после реакции.
С другой стороны, известно, что когда алкоксид металла (например, диалкоксид диалкилолова) нагревают приблизительно до 180°С, алкоксид металла подвергается термическому разложению с образованием алкоксида триалкилолова и т.д. (см. «Kougyoukagakuzasshi (Journal of the Society of Chemical Industry)», Vol. 72, № 7, рр. 1543-1549 (1969)). Также известно, что алкоксид триалкилолова, образовавшийся при термическом разрушении, имеет очень низкую способность к образованию эфира угольной кислоты (см. «J. Org. Chem.», Vol. 64, pp. 4506-4508 (1999)). Трудно (или по существу невозможно) регенерировать диалкоксид диалкилолова, имеющий прекрасную активность, из алкоксида триалкилолова. Кроме того, образование такого непригодного соединения (то есть нерегенерируемого инертного соединения) вызывают проблему в том, что когда алкоксид металла используется в качестве катализатора повторно, содержание активного катализатора в алкоксиде металла уменьшается и, следовательно, скорость реакции и выход эфира угольной кислоты понижаются, что делает стабильное производство эфира угольной кислоты трудным. В этом случае для стабилизации скорости реакции и выхода эфира угольной кислоты используют обычный способ, в котором в реакционную систему добавляют небольшое количество свежего алкоксида металла. Однако проблема указанного способа состоит в том, что, когда проводят добавление свежего алкоксида металла, оставляя продукт деградации, образовавшийся в ходе реакции, поскольку он присутствует в реакционной системе, продукт деградации, который имеет низкую каталитическую активность, в большом количестве накапливается в реакционной системе. Как очевидно из вышесказанного, не существует обычного способа, при котором алкоксид металла эффективно используется повторно в качестве катализатора; в любом из обычных способов получения эфира угольной кислоты по окончании реакции нет другого выбора, как выбрасывать алкоксид металла в качестве отхода, что делает производство эфира угольной кислоты неприемлемо дорогим.
Таким образом, в обычных способах производства эфира угольной кислоты с использованием алкоксида металла, диоксида углерода и спирта, когда алкоксид металла (который является дорогим продуктом) теряет свою каталитическую активность из-за гидролиза и т.д., нет путей легкой и эффективной регенерации и повторного использования алкоксида металла. Следовательно, недостаток обычных способов получения эфира угольной кислоты состоит в том, что необходимо использование большого количества органического дегидратирующего агента или твердого дегидратирующего агента в комбинации с небольшим количеством алкоксида металла.
Как описывалось выше, методики получения эфира угольной кислоты предшествующего уровня техники имеют много проблем и, следовательно, не могут быть введены в практику.
Для решения проблем, сопровождающих предшествующий уровень техники, заявители настоящего изобретения в публикации WO 03/055840 предложили новый способ получения эфира угольной кислоты. Существенным признаком нового способа является то, что в указанном способе используют реакционный путь, в котором органическое соединение, имеющее связь металл-кислород-углерод, используется в большом количестве в качестве предшественника эфира угольной кислоты, а не в качестве катализатора, и металлорганическое соединение вступает в реакцию присоединения с диоксидом углерода с образованием аддукта, после чего следует реакция термического разложения аддукта с получением в результате реакционной смеси, содержащей эфир угольной кислоты. Заявители настоящего изобретения установили, что этим способом эфир угольной кислоты может быть получен с высоким выходом. Большинство из приведенных выше проблем предшествующего уровня техники решено с помощью названного способа. Однако даже этот способ имеет проблему в том, что во время реакции образуется и накапливается в реакционной системе нерегенерируемое инертное металлорганическое соединение.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
С учетом сложившейся ситуации авторы настоящего изобретения провели дополнительные широкие и интенсивные исследования для решения названных выше проблем. В этих исследованиях авторы настоящего изобретения использовали методики своего предшествующего открытия, описанного в публикации WO 03/055840. В результате неожиданно было установлено, что проблема может быть решена с помощью способа получения эфира угольной кислоты, включающего стадии: (1) проведения реакции между первой смесью металлорганического соединения и диоксидом углерода, где первая смесь металлорганического соединения содержит смесь реакционноспособного металлорганического соединения, имеющего в своей молекуле, по меньшей мере, две связи металл-кислород-углерод, и нерегенерируемого инертного соединения, которое образовано из реакционноспособного металлорганического соединения, с получением в результате реакционной смеси, содержащей эфир угольной кислоты, полученный в результате реакции, нерегенерируемое инертное соединение и регенерируемое метаморфное металлорганическое соединение, образованное из реакционноспособного металлорганического соединения; (2) разделения реакционной смеси на первую часть, содержащую эфир угольной кислоты и нерегенерируемое инертное соединение, и вторую часть, содержащую регенерируемое метаморфное металлорганическое соединение; и (3) взаимодействия второй части реакционной смеси со спиртом с образованием второй смеси металлорганического соединения и воды и удаления воды из второй смеси металлорганического соединения, где вторая смесь металлорганического соединения содержит смесь реакционноспособного металлорганического соединения, имеющего в своей молекуле, по меньшей мере, две связи металл-кислород-углерод, и нерегенерируемого инертного соединения, которое образовано из реакционноспособного металлорганического соединения. Эфир угольной кислоты может быть легко выделен из первой части реакционной смеси обычным способом, таким как отгонка. Вторая смесь металлорганического соединения, полученная на стадии (3), может быть выделена и рециркулирована на стадию (1), где вторая смесь металлорганического соединения используется в упомянутой выше реакции получения эфира угольной кислоты. Настоящее изобретение осуществлено на основе этого открытия.
Таким образом, главной целью настоящего изобретения является разработка способа, в котором реакционноспособное металлорганическое соединение, используемое в реакции, может быть повторно использовано без необходимости большого количества дегидратирующего агента и с помощью которого промышленное производство эфира угольной кислоты с высоким выходом может быть осуществлено непрерывно и неоднократно любое число раз при удалении нерегенерируемого инертного металлорганического соединения из реакционной системы.
Перечисленные выше и другие объекты, признаки и преимущества настоящего изобретения будут очевидны из следующего подробного описания, рассматриваемого в сопровождении чертежей и прилагаемой формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На чертежах:
Фиг.1 представляет собой спектр 119Sn-ЯМР реакционноспособного металлорганического соединения, содержащего 2-этилгексилоксигруппу, используемого на стадии (1) в примере 1; и
Фиг.2 представляет собой спектр 119Sn-ЯМР нерегенерируемого инертного соединения, которое отгоняется на стадии (2) в примере 1.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение предлагает способ производства эфира угольной кислоты, который включает стадии:
(1) проведения реакции между первой смесью металлорганического соединения и диоксидом углерода, где первая смесь металлорганического соединения содержит смесь реакционноспособного металлорганического соединения, имеющего в своей молекуле, по меньшей мере, две связи металл-кислород-углерод, и нерегенерируемого инертного соединения, которое образовано из реакционноспособного металлорганического соединения и которое имеет в своей молекуле, по меньшей мере, три связи металл-углерод, с получением в результате реакционной смеси, содержащей эфир угольной кислоты, образовавшийся в ходе реакции, нерегенерируемое инертное соединение и регенерируемое метаморфное металлорганическое соединение, образованное из реакционноспособного металлорганического соединения;
(2) разделения реакционной смеси на первую часть, содержащую эфир угольной кислоты и нерегенерируемое инертное соединение, и вторую часть, содержащую регенерируемое метаморфное металлорганическое соединение; и
(3) взаимодействия второй части реакционной смеси с первым спиртом с образованием второй смеси металлорганического соединения и воды и удаления воды из второй смеси металлорганического соединения, причем вторая смесь металлорганического соединения содержит смесь реакционноспособного металлорганического соединения, имеющего в своей молекуле, по меньшей мере, две связи металл-кислород-углерод, и нерегенерируемого инертного соединения, которое образуется из реакционноспособного металлорганического соединения и которое имеет в своей молекуле, по меньшей мере, три связи металл-углерод.
Для простоты понимания настоящего изобретения ниже перечислены существенные признаки и различные предпочтительные варианты осуществления настоящего изобретения.
1. Способ производства эфира угольной кислоты, включающий стадии:
(1) проведения реакции между первой смесью металлорганического соединения и диоксидом углерода, причем первая смесь металлорганического соединения содержит смесь реакционноспособного металлорганического соединения, имеющего в своей молекуле, по меньшей мере, две связи металл-кислород-углерод, и нерегенерируемого инертного соединения, которое образовано из реакционноспособного металлорганического соединения и которое имеет в своей молекуле, по меньшей мере, три связи металл-углерод, с получением в результате реакционной смеси, содержащей эфир угольной кислоты, образовавшийся в ходе реакции, нерегенерируемое инертное соединение и регенерируемое метаморфное металлорганическое соединение, образованное из реакционноспособного металлорганического соединения;
(2) разделения реакционной смеси на первую часть, содержащую эфир угольной кислоты и нерегенерируемое инертное соединение, и вторую часть, содержащую регенерируемое метаморфное металлорганическое соединение; и
(3) взаимодействия второй части реакционной смеси с первым спиртом с образованием второй смеси металлорганического соединения и воды и удаления воды из второй смеси металлорганического соединения, причем вторая смесь металлорганического соединения содержит смесь реакционноспособного металлорганического соединения, имеющего в своей молекуле, по меньшей мере, две связи металл-кислород-углерод, и нерегенерируемого инертного соединения, которое образуется из реакционноспособного металлорганического соединения и которое имеет в своей молекуле, по меньшей мере, три связи металл-углерод.
2. Способ по пункту 1, который также включает после стадии (3) стадию (4), на которой вторую смесь металлорганического соединения, полученную на стадии (3), выделяют и рециркулируют на стадию (1).
3. Способ по пункту 1 или 2, где реакционноспособное металлорганическое соединение, используемое на стадии (1), содержит, по меньшей мере, одно соединение, выбранное из группы, включающей:
металлорганическое соединение, представленное формулой (1):
где:
М1 представляет собой атом металла, выбранный из группы, включающей элементы, принадлежащие к группам 4 и 14 Периодической таблицы, за исключением кремния;
каждый из заместителей R1 и R2 независимо друг от друга представляет собой линейную или разветвленную С1-С12-алкильную группу, С5-С12-циклоалкильную группу, линейную или разветвленную С2-С12-алкенильную группу, С7-С20-аралкильную группу, состоящую из незамещенного или замещенного С6-С19-арила и алкила, выбранного из группы, включающей линейный или разветвленный С1-С14-алкил и С5-С14-циклоалкил, или незамещенную или замещенную С6-С20-арильную группу;
каждый из заместителей R3 и R4 независимо друг от друга представляет собой линейную или разветвленную С1-С12-алкильную группу, С5-С12-циклоалкильную группу, линейную или разветвленную С2-С12-алкенильную группу или С7-С20-аралкильную группу, состоящую их незамещенного или замещенного С6-С19-арила и алкила, выбранного из группы, включающей линейный или разветвленный С1-С14-алкил и С5-С14-циклоалкил;
каждый из индексов a и b представляет собой целое число от 0 до 2, а + b = от 0 до 2, каждый из индексов с и d представляет собой целое число от 0 до 4, и а + b + c + d = 4; и
металлорганическое соединение, представленное формулой (2):
где:
каждый из М2 и М3 независимо друг от друга представляет собой атом металла, выбранный из группы, включающей элементы, принадлежащие к группам 4 и 14 Периодической таблицы, за исключением кремния;
каждый из заместителей R5, R6, R7 и R8 независимо друг от друга представляет собой линейную или разветвленную С1-С12-алкильную группу, С5-С12-циклоалкильную группу, линейную или разветвленную С2-С12-алкенильную группу, С7-С20-аралкильную группу, состоящую из незамещенного или замещенного С6-С19-арила и алкила, выбранного из группы, включающей линейный или разветвленный С1-С14-алкил и С5-С14-циклоалкил, или незамещенную или замещенную С6-С20-арильную группу;
каждый из заместителей R9 и R10 независимо друг от друга представляет собой линейную или разветвленную С1-С12-алкильную группу, С5-С12-циклоалкильную группу, линейную или разветвленную С2-С12-алкенильную группу или С7-С20-аралкильную группу, состоящую из незамещенного или замещенного С6-С19-арила и алкила, выбранного из группы, включающей линейный или разветвленный С1-С14-алкил и С5-С14-циклоалкил;
каждый из индексов e, f, g и h представляет собой целое число от 0 до 2, e + f = от 0 до 2, g + h = от 0 до 2, каждый из индексов i и j представляет собой целое число от 1 до 3, e + f + i = 3 и g + h + j = 3.
4. Способ по пункту 3, где каждый из заместителей R3 и R4 в формуле (1) и R9 и R10 в формуле (2) независимо друг от друга представляет собой н-бутильную группу, изобутильную группу, линейную или разветвленную С5-С12-алкильную группу или линейную или разветвленную С4-С12-алкенильную группу.
5. Способ по пункту 3, где каждый из М1 в формуле (1) и М2 и М3 в формуле (2) представляет собой атом олова.
6. Способ по пункту 3, где реакционноспособное металлорганическое соединение, используемое на стадии (1), получено из оловоорганического оксида и спирта.
7. Способ по пункту 1 или 2, где на стадии (1) реакционноспособное металлорганическое соединение используют, по меньшей мере, в одной из форм, выбранных из группы, включающей мономерную форму, олигомерную форму, полимерную форму и ассоциированную форму.
8. Способ по пункту 1 или 2, где на стадии (1) реакционноспособное металлорганическое соединение используют в количестве, которое сос