Улучшенные хелатные конъюгаты
Иллюстрации
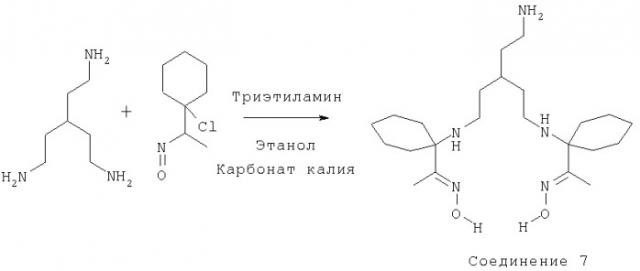
Показать всеНастоящее изобретение относится к улучшенным хелатным конъюгатам формулы
где каждый R1, R2 и R3 независимо представляет собой группу R; Y представляет собой -(A)n-X-Z, где Х представляет собой -NH-, -CO2-, -N(C=O)-; Z представляет собой биологическую группировку для направленной доставки, которая выбрана из 3-20-членного пептида, субстрата фермента, ингибитора фермента или синтетического связывающегося с рецептором соединения; -(А)n- представляет собой линкер, где каждый А независимо представляет собой -CR2-, -NRCO-, -CONR-, -CR2OCR2- или группировку полиалкиленгликоля; n представляет собой целое число, имеющее значение от 2 до 10; каждая группа R независимо представляет собой Н или С1-10алкил, или 2 группы R вместе с атомами, к которым они присоединены, образуют C3-6карбоциклическое насыщенное кольцо. Комплексы с радиоактивными металлами пригодны в качестве радиоактивных фармацевтических препаратов, в особенности с 99mTc. 7 н. и 21 з.п. ф-лы, 4 табл., 4 ил.
Реферат
Область изобретения
Настоящее изобретение относится к улучшенным хелатным конъюгатам с биологическими молекулами для направленной доставки, пригодными для образования комплексов с радиоактивными металлами. Комплексы с радиоактивными металлами пригодны в качестве радиоактивных фармацевтических препаратов, в особенности с 99mТс.
Предшествующий уровень техники
Диаминдиоксимы представляют собой известный класс хелатообразователей, которые, как было показано, образуют
Q=-(СН2)3 -, т.е. пропиленаминоксим или PnAO;
Q=-(СН2)4 -, т.е. бутиленаминоксим или BnAO;
Q=-(СН2)5 -, т.е. пентиленаминоксим или PentAO;
комплексы с радиоактивным металлом 99mТс.
Лиганд PentAO был впервые описан S.Jurisson et al [Inorg. Chem., 26, 3576-82 (1987)], который показал, что его комплекс с долгоживущим радиоактивным металлом 99Tc является нейтральным, имеющим ядро диоксо Tc(V) (т.е. TcO2 +). J-M Lo et al [Appl. Rad. Inst, 44, 1139-46 (1993)] описал синтез PentAO и образование его комплекса с 99mTc.
US 5688487 описывает хелатные конъюгаты диаминдиоксимов, имеющие С2-5 алкиленовый мостик с нитроимидазольными биологическими молекулами для направленной доставки для визуализации гипоксии. Описана конъюгация нитроимидазола в положении С1 (метил оксима).
WO 95/04552 описывает конъюгаты нитроимидазола с BnAO и PentAO. Пример демонстрирует конъюгацию в положении С1 (метил оксима).
WO 95/19187 описывает конъюгаты линейных или циклических 3-50-членных синтетических пептидов с полидентатными хелатообразователями, присоединяемыми на карбоксильном конце пептида, для применения в качестве радиоактивных фармацевтических препаратов. Диаминдиоксимы, такие как PnAO, BnAO и PentAO, описаны в качестве пригодных хелатообразователей.
WO 99/60018 описывает диаминдиоксимовые хелатные конъюгаты диаминдиоксимовых лигандов с пептидами для визуализации тромба. Как утверждалось, таким предпочтительным хелатообразователем является диаминдиоксим с Q=-(CH2)2NR(CH2)2-.
Настоящее изобретение
Диаминдиоксим-пептидные хелатные конъюгаты по WO 99/60018 формулы I
где Т=N и Y=-СН2СН2NH-[пептид],
тем не менее обладают существенными недостатками. Таким образом, при хелатировании с 99mТс этот аза-диаминдиоксим образует несколько частиц с технецием, которые могут быть разделены и обнаружены с помощью хроматографии. При температуре окружающей среды исходные радиоактивные частицы (промежуточные соединения) превращаются в течение времени (2-3 часа) в устойчивый продукт. Этому превращению промежуточное соединение - продукт может способствовать применение более высоких значений рН (рН>8) и нагревание. Эти условия не являются идеальными для госпитальной радиофармации, поэтому желателен хелатообразователь с меньшим количеством промежуточных соединений и/или более быстрым превращением промежуточное соединение - продукт. Очевидно, что необходимость в нагревании и возможно сравнительно высоком рН для достижения достаточной радиохимической чистоты (РХЧ) желаемых частиц 99mTc является нежелательной, поскольку такое нагревание может разрушить присоединенную биологическую молекулу для направленной доставки или пептид. Еще одна проблема с азадиаминдиоксимовыми хелатообразователями формулы I заключается в том, что атом азота третичного амина в основании мостика является сравнительно основным. Это означает, что при образовании соответствующего комплекса 99mТс в водном растворе третичный амин по меньшей мере частично протонируется, что приводит в результате к тому, что конъюгат является заряженным. Этот заряд может ограничивать применения меченой биологической группировки для направленной доставки, поскольку заряд может усложнять радиоактивно меченному конъюгату переход через клеточные мембраны.
Настоящее изобретение предлагает альтернативную хелатную систему (формула I, где Т=С), которая позволяет преодолеть эти проблемы предшествующего уровня техники, и предлагает конъюгаты, которые могут быть радиоактивно мечены с получением хорошей РХЧ при комнатной температуре в водной среде при почти нейтральном значении рН. Комплексы с радиоактивным металлом имеют хорошую стабильность. N2S2 и N3S тиолсодержащие бифункциональные хелатообразователи по предшествующему уровню техники имеют недостатки в том, что тиолы чувствительны к воздуху, быстро окисляются на воздухе до соответствующих дисульфидов при условиях от нейтральных до основных. Поэтому их следует держать в инертной атмосфере перед применением или в защитной матрице. В качестве альтернативы они могут применяться в виде защищенных частиц, таких как тиоацетат или тетрагидропиранила гемитиокеталь, но это требует обязательного удаления защитных групп перед применением с использованием кислоты или основания и нагревания. Все эти свойства уменьшают удобство этих хелатообразователей по сравнению с хелатообразователями по настоящему изобретению. Следовательно, хелатообразователи по настоящему изобретению полезны для конъюгации и радиоактивного мечения широкого диапазона биологических группировок для направленной доставки.
Подробное описание изобретения
В первом аспекте настоящего изобретения предложен хелатный конъюгат диаминдиоксимового лиганда с биологической группировкой для направленной доставки. Термин "хелатный конъюгат" означает соединение, где агент, образующий с металлом хелат, ковалентно связан ("конъюгирован") с биологической группировкой для направленной доставки. Хелатный конъюгат имеет формулу II
где каждый R1, R2 и R3 независимо представляет собой группу R;
Y представляет собой -(A)n-X-Z,
где Х представляет собой -NH-, -CO2-, -N(С=O)-;
Z представляет собой биологическую группировку для направленной доставки, которая выбрана из 3-20-членного пептида, субстрата фермента, ингибитора фермента или синтетического связывающегося с рецептором соединения;
-(A)n- представляет собой линкер, где каждый А независимо представляет собой
-CR2-, -NRCO-, -CONR-, -CR2OCR2- или группировку полиалкиленгликоля;
n представляет собой целое число, имеющее значение от 2 до 10;
каждая группа R независимо представляет собой Н или C1-10алкил, или 2 группы R вместе с атомами, к которым они присоединены, образуют С3-6карбоциклическое насыщенное кольцо.
Под термином "биологическая группировка для направленной доставки" понимают 3-100-членные пептиды или пептидные аналоги, которые могут представлять собой линейные пептиды или циклические пептиды или их комбинации; моноклональные антитела или их фрагменты; субстраты или ингибиторы ферментов; синтетические связывающиеся с рецептором соединения; олигонуклеотиды или фрагменты олиго-ДНК или олиго-РНК. Биологическая группировка для направленной доставки может иметь синтетическое или природное происхождение, но предпочтительно синтетическое. Предпочтительные биологические группировки для направленной доставки представляют собой 3-20-членные пептиды, которые могут иметь синтетическое или природное происхождение, но предпочтительно синтетическое. Под термином "циклический пептид" понимают последовательность, состоящую из 5-15 аминокислот, где две концевые аминокислоты связаны вместе ковалентной связью, которая может представлять собой пептидную или дисульфидную связь, или синтетическую непептидную связь, такую как тиоэфирная, фосфодиэфирная, дисилоксановая или уретановая связь.
Под термином "аминокислота" понимают L- или D-аминокислоту, аминокислотный аналог или аминокислотный миметик, который может встречаться в природе или иметь чисто синтетическое происхождение, и может быть оптически чистым, т.е. единственный энантиомер, и, следовательно, хиральный, или смесь энантиомеров. Предпочтительно аминокислоты по настоящему изобретению являются оптически чистыми. Под термином "аминокислотный миметик" понимают синтетические аналоги встречающихся в природе аминокислот, которые представляют собой изостеры, т.е. разработанны для того, чтобы имитировать стерическую и электронную структуру природного соединения. Такие изостеры хорошо известны специалистам в данной области техники и включают депсипептиды, ретро-инверзопептиды, тиоамиды, циклоалканы или 1,5-дизамещенные тетразолы, но не ограничиваются ими [описано в М.Goodman, Biopolymers, 24, 137, (1985)].
Подходящие пептиды для применения по настоящему изобретению включают в себя следующие:
- соматостатин, октреотид и аналоги,
- пептиды, которые связываются с рецептором ST, где ST относится к теплостабильному токсину, продуцируемому E.coli и другими микроорганизмами;
- фрагменты ламинина, например YIGSR, PDSGR, IKVAV, LRE и KCQAGTFALRGDPQG,
- N-формилпептиды, имеющие в качестве мишеней сайты аккумулирования лейкоцитов,
- тромбоцитарный фактор 4 (PF4) и его фрагменты,
- пептиды, содержащие RGD,
- фрагменты пептида α2-антиплазмина, фибронектина или бета-казеина, фибриногена или тромбоспондина. Последовательности аминокислот α2-антиплазмина, фибронектина, бета-казеина, фибриногена или тромбоспондина можно найти в следующих ссылках: предшественник α2-антиплазмина [М.Tone et al., J. Biochem, 102, 1033 (1987)]; бета-казеин [L.Hansson et al., Gene, 139, 193 (1994)]; фибронектин [A.Gutman et al., FEBS Lett., 207, 145, (1996)]; предшественник тромбоспондина-1 [V.Dixit et al., Proc. Natl. Acad. Sci., USA, 83, 5449 (1986)]; R.F.Doolittle, Ann. Rev. Biochem., 53, 195 (1984).
Предпочтительно пептиды по настоящему изобретению включают в себя последовательность аминокислот, взятую из N-конца:
(1) α2-антиплазмина,
т.е. NH2-Asn-Gln-Glu-Gln-Val-Ser-Pro-Leu-Thr-Leu-Thr-Leu-Leu-Lys-OH
или ее варианты, где замещена, добавлена или удалена одна или более чем одна аминокислота, такие как
NH2-Asn-Gln-Glu-Gln-Val-Ser-Pro-Leu-Thr-Leu-Thr-Leu-Leu-Lys-Gly-OH,
NH2-Asn-Gln-Glu-Ala-Val-Ser-Pro-Leu-Thr-Leu-Thr-Leu-Leu-Lys-Gly-OH,
NH2-Asn-Gln-Glu-Gln-Val-Gly-OH, или
(2) казеина,
т.е. Ac-Leu-Gly-Pro-Gly-Gln-Ser-Lys-Val-Ile-Gly.
Синтетические пептиды по настоящему изобретению могут быть получены путем обычного твердофазного синтеза, в соответствии с тем, как описано в Р.Lloyd-Williams, F.Albericio and E.Girald; Chemical Approaches to the Synthesis of Peptides and Proteins, CRC Press, 1997.
Подходящие моноклональные антитела или их фрагменты для применения по настоящему изобретению включают антитела к антигену CD-20, экспрессируемому на поверхности В-клеток; антилейкоцитарные или антигранулоцитарные антитела; антимиозиновые антитела или антитела в отношении карциноэмбрионального антигена (КЭА).
Подходящие субстраты или ингибиторы для ферментов включают в себя глюкозу и аналоги глюкозы, такие как фтордезоксиглюкоза; жирные кислоты или ингибиторы эластазы.
Подходящие синтетические связывающиеся с рецептором соединения включают в себя эстрадиол, эстроген, прогестин, прогестерон и другие стероидные гормоны; лиганды дофаминового рецептора D-1 или D-2, или переносчик дофамина, такой как тропаны; лиганды рецептора серотонина.
Под термином "фторалкил" понимают алкильную группу с по меньшей мере одним заместителем фтором, т.е. этот термин охватывает группы от монофторалкила (например, -CH2F) до перфторалкила (например, CF3).
В диаминдиоксимовых хелатообразователях по настоящему изобретению R3 предпочтительно представляет собой Н. Также предпочтительно, чтобы по меньшей мере одна группа R2 представляла собой Н, более предпочтительно, все группы R2 представляли собой Н. Каждый R1 предпочтительно представляет собой C1-3алкил. Особенно предпочтительно, чтобы все группы R1 представляли собой CH3.
Предпочтительные хелатные конъюгаты формулы II, где 2 группы R, которые вместе с атомами, к которым они присоединены, образуют карбоциклическое насыщенное кольцо, включают в себя такие кольца, которые имеют от 3 до 6 членов, в частности 5 или 6 членов. Предпочтительные карбоциклические кольца представляют собой кольца, где 2 группы R1, присоединенные либо к одному и тому же атому углерода, либо к соседним атомам углерода, соединены с образованием 3-6-членных, в частности 5 или 6-членных насыщенных колец.
Предусмотрено, что роль связывающей группы -(A)n- заключается в том, чтобы дистанционно отдалить относительно громоздкий комплекс с радиоактивным металлом, который получается в результате координации металла, от активного сайта биологической группировки для направленной доставки, таким образом, что, например, связывание с рецептором не нарушается. Этого можно достигнуть путем комбинации гибкости (например, обычные алкильные цепи), так что громоздкая группа обладает свободой располагаться дальше от активного сайта, и/или жесткости, так как при циклоалкильном или арильном разделителе, который ориентирует комплекс металла на расстоянии от активного сайта. Природа линкерной группы может также быть использована для модификации биологического распределения полученного комплекса конъюгата с радиоактивным металлом. Таким образом, например, введение эфирных групп в линкер, будет способствовать минимизации связывания с белками плазмы крови. Предпочтительные связывающие группы -(A)n- имеют основную цепь молекулы, состоящую из связанных атомов, которые образуют группировку -(A)n-, содержащую от 2 до 10 атомов, наиболее предпочтительно от 2 до 5 атомов, причем 2 или 3 атома являются особенно предпочтительными. Минимальная основная цепь молекулы линкерной группы, состоящая из 2 атомов, предоставляет преимущество, заключающееся в том, что хелатообразователь хорошо отделен от биологической группировки для направленной доставки, так что любое взаимодействие минимизировано. Еще одно преимущество заключается в том, что размер потенциального хелатного кольца групп Х и Z так велик (по меньшей мере 8 для 2-атомноой основной цепи), что эти группы вряд ли эффективно конкурируют с координацией хелатообразователя с радиоактивным металлом. Таким образом, в конъюгатах этого типа сохраняются как характеристики биологического нацеливания биологической группировки для направленной доставки, так и способность диаминдиоксимового хелатообразователя образовывать комплекс с металлом.
Непептидные линкерные группы, такие как алкиленовые группы, обладают тем преимуществом, что отсутствуют значительные взаимодействия между углеводородной связью и конъюгированной биологической группировкой для направленной доставки, так что линкер не обвивается вокруг биологической группировки для направленной доставки. Предпочтительные алкиленовые разделяющие группы представляют собой -(CH2)n-, где n представляет собой от 2 до 5.
Предпочтительная группа Y представляет собой, таким образом, -CH2CH2-X-Z, наиболее предпочтительно -CH2CH2-NR4-Z, причем особенно предпочтительно Y=-CH2CH2-NH-Z. Эти группы обладают дополнительным преимуществом, заключающемся в том, что происходят от промежуточного соединения R3C(CH2CH2NH2)3, предпочтительно от промежуточного соединения НС(СН2СН2NH2)3, которое, поскольку оно является симметричным, гораздо проще синтезировать, так как для триаминов с различной длиной цепи необходимо применение стратегий синтеза, чтобы химически различать различные амины (например, за счет использования защитных групп).
Группа Х представляет собой функциональную группу, которая обеспечивает легкую конъюгацию хелатирующего агента с биологической группировкой для направленной доставки Z. Так как большинство пептидов и белков имеют доступные карбоксильные или аминосайты для образования функциональной группы, то предпочтительными группами X, когда Z представляет собой пептид или белок, являются -NR4- и -CO2-, так как это обеспечивает легкую конъюгацию посредством амидных связей. Содержащие цистеин пептиды и белки могут обладать свободными тиоловыми группами, предпочтительными группами X, когда Z представляет собой содержащий цистеин пептид или белок, являются тиолфильные группы, такие как малеимид и акриламид, так как они обеспечивают легкую конъюгацию посредством тиоэфирных связей.
Предпочтительные диаминдиоксимовые хелатообразователи по настоящему изобретению являются симметричными, т.е. два заместителя -CR2 2R2 2NHCR1 2C(=N-OH)R1 на группировке -CY(R3)- выбраны таким образом, чтобы они были одинаковыми. Это обеспечивает преимущество, заключающееся в том, что хелатообразователь не содержит хирального центра, поскольку такие центры могут образовывать диастереоизомерные комплексы с радиоактивным металлом, и возможно для них требуется очистка конкретных изомеров.
Хелатные конъюгаты формулы II возможно могут применяться в форме соли кислоты, т.е. когда один или более чем один амин либо из набора диаминдиоксимовых доноров, либо из группы Y протонирован биосовместимой кислотой. Такие соли могут быть получены непосредственно, например, путем очистки с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ), использующей такие кислоты в подвижной фазе (например, уксусная или трифторуксусная кислота), или путем добавления биосовместимой кислоты к раствору хелатного конъюгата. Форма соли может быть пригодной для облегчения очистки (например, путем осаждения или перекристаллизации), или может облегчать растворение в водных средах (после чего рН при необходимости можно легко отрегулировать).
Хелатные конъюгаты по настоящему изобретению могут быть получены путем взаимодействия бифункционального хелатообразователя формулы III с биологической группировкой для направленной доставки
где каждый R1, R2 и R3 независимо представляет собой группу R;
Е представляет собой -(A)n-J,
где J представляет собой -NR5R6 или -CO2M, где R5 и R6 независимо представляют собой группу R или РG, и М представляет собой Н, катион, РG или активный сложный эфир;
-(A)n- представляет собой линкер, где А независимо представляет собой -CR2-, -NRCO-, -CONR-, -CR2OCR2- или группировку полиалкиленгликоля;
n представляет собой целое число, имеющее значение от 2 до 10;
каждая группа R независимо представляет собой Н или C1-10алкил, или 2 группы R вместе с атомами, к которым они присоединены, образуют C3-6 карбоциклическое насыщенное кольцо;
PG представляет собой защитную группу.
В соединениях формулы III J представляет собой функциональную группу, пригодную для конъюгации. Под термином "функциональная группа, пригодная для конъюгации" понимают функциональную группу, которая вступает в реакцию с соответствующей функциональной группой Z (как правило, аминогруппой, карбоксильной группой или тиоловой группой) для химического связывания диаминдиоксимового хелатообразователя с Z. Предпочтительные такие функциональные группы, пригодные для конъюгации, т.е. группы J, представляют собой -NR5R6 или -CO2M, где R5 и R6 независимо представляют собой группу R или PG; М представляет собой H, катион, PG или активный сложный эфир; РG представляет собой защитную группу. Катион в подходящем случае представляет собой положительно заряженный противоион, такой как ион металла, ион аммония (NH4 +) или четвертичный аммониевый или фосфониевый ион. Предпочтительно катион представляет собой биосовместимый катион. Термины "биосовместимый катион", "активный сложный эфир" и "защитная группа" определены ниже. Когда функциональная группа представляет собой -NR5R6, тогда по меньшей мере один и предпочтительно оба R5, так и R6 представляют собой Н.
Под термином "защитная группа" понимают группу, которая ингибирует или подавляет нежелательные химические реакции, но которая разработана таким образом, что является достаточно реакционноспособной для того, чтобы она могла отщепляться от рассматриваемой функциональной группы при достаточно мягких условиях, которые изменяют оставшуюся часть молекулы. После удаления защиты рассматриваемая группа может использоваться для конъюгации бифункционального хелата формулы III с биологической группировкой для направленной доставки.
Защитные группы хорошо известны специалистам в данной области техники и, когда J представляет собой -NR5R6, подходящим образом выбраны из Вос (где Вос представляет собой трет-бутилоксикарбонил), Fmoc (где Fmoc представляет собой флуоренилметоксикарбонил), трифторацетила, аллилоксикарбонила, Dde (т.е. 1-(4,4-диметил-2,6-диоксоциклогексилиден)этила) или Npys (т.е. 3-нитро-2-пиридинсульфенила), и когда J представляет собой -CO2PG: метилового эфира, трет-бутилового эфира, бензилового эфира. Применение дополнительных защитных групп описано в "Protective Groups in Organic Synthesis", Theorodora W.Greene and Peter G.M.Wuts (John Wiley & Sons, 1991).
Под термином "биосовместимый катион" понимают положительно заряженный противоион, который образует соль с ионизированной отрицательно заряженной группой, где указанный положительно заряженный противоион также не является токсичным и, следовательно, пригоден для введения в организм млекопитающего, в частности в организм человека. Примеры пригодных биосовместимых ионов включают щелочные металлы (например, натрий или калий), щелочноземельные металлы (например, кальций или магний) и ион аммония. Предпочтительный биосовместимый катион представляет собой ион натрия (Na+).
Под термином "активный сложный эфир" понимают эфирное производное карбоновой кислоты, которое разработано для того, чтобы служить в качестве более хорошей уходящей группы и, следовательно, обеспечивать более легкую реакцию с нуклеофилами, присутствующими на биологической группировке для направленной доставки, например аминами. Примеры пригодных активных сложных эфиров представляют собой N-гидроксисукцинимид (NHS), пентафторфенол, пентафтортиофенол, пара-нитрофенол и гидроксибензотриазол.
Функционализированные амином хелатообразователи формулы III (т.е. J=-NR5R6), таким образом, могут быть конъюгированы с карбоксильной группой(ми) биологической группировки для направленной доставки посредством амидных связей. Это связывание может осуществляться непосредственно (например, путем применения твердофазного пептидного синтеза) или в присутствии пригодного активирующего агента, такого как ВОР (т.е. бензотриазол-1-илокситрис(диметиламино)фосфоний) или N,N'-дициклогексилкарбодиимид (DCCI). Связывание может также осуществляться через образование подходящих промежуточных соединений, как известно из уровня техники, таких как активированные сложные эфиры карбоксильной группы биологической группировки для направленной доставки. В качестве альтернативы дополнительная аминогруппа бифункционального хелатообразователя сначала может быть преобразована в изотиоцианатную (-NCS) или изоцианатную группы (-NCO), которые допускают конъюгацию с содержащими амин биологическими группировками для направленной доставки посредством образования связывающих групп тиомочевины и мочевины соответственно. В качестве альтернативы дополнительная аминогруппа бифункционального хелатообразователя может вступать в реакцию с двухосновной кислотой для введения концевой карбоксильной группы посредством связывающей группы. Бифункциональный хелатообразователь, несущий карбоксильную функциональную группу (т.е. J=-CO2M), может быть использован подобным образом для связывания непосредственно с содержащими амин биологическими группировками для направленной доставки посредством амидной связи. Бифункциональный хелат может также нести группу, разработанную для того, чтобы вступать в реакцию с тиоловыми группами на биологической группировке для направленной доставки с образованием устойчивых тиоэфирных связывающих групп. Примеры таких групп представляют собой малеимиды (которые могут быть получены путем реакции малеинового ангидрида с соответствующим амином с последующим нагреванием с уксусным ангидридом) и акриламиды (которые могут быть получены путем реакции акрилилхлорида с амином).
Во втором аспекте настоящего изобретения предложены комплексы хелатного конъюгата, описанного выше, с радиоактивным металлом. Пригодные радиоактивные металлы могут представлять собой либо источники излучения позитронов, такие как 64Cu, 48V, 52Fe, 55Co, 94mТс или 68Ga, либо гамма-излучатели, такие как 94mТс, 111In, 113mIn или 67Ga. Наиболее предпочтительные радиоактивные металлы для диагностической визуализации представляют собой гамма-излучатели, в частности 94mТс. Металлические комплексы с некоторыми радионуклидами могут быть полезны в качестве радиоактивных фармацевтических препаратов для радиоактивного лечения различных заболеваний, таких как рак, или лечения тромбоза или рестеноза. Пригодные радиоизотопы для таких радиотерапевтических применений включают 90Y, 89Sr, 67Cu, 103Pd, 186Re, 188Re, 169Er, 153Sm и 198Au. Весьма предпочтительно, чтобы биологическая группировка для направленной доставки Z была связана с хелатообразователем таким образом, чтобы связывающая группа не претерпевала легкого метаболизма в крови, который приводил бы в результате к расщеплению комплекса металла перед тем, как меченая биологическая группировка для направленной доставки достигала желаемого сайта-мишени in vivo. Поэтому биологическая группировка для направленной доставки предпочтительно ковалентно связана с комплексами металлов по настоящему изобретению посредством связывающих групп, которые не подвергаются легкому метаболизму (как, например, эфирные связывающие группы).
Предпочтительные комплексы с радиоактивным металлом по настоящему изобретению являются симметричными, т.е. два заместителя -CR2 2R2 2NHCR1 2C(=N-OH)R1 на группировке -CY(R3)- выбирают таким образом, чтобы они были одинаковыми. Это обеспечивает преимущество, заключающееся в том, что хелатообразователь не содержит хирального центра, поскольку такие центры могут образовывать диастереоизомерные комплексы с радиоактивным металлом и возможно для них требуется очистка конкретных изомеров. Также предпочтительно, чтобы комплексы хелатного конъюгата были электрически нейтральными.
Полагают, что комплексы хелатообразователей с 99mTc по настоящему изобретению представляют собой
нейтральные диоксокомплексы с Tc(V) в соответствии с тем, как изображено выше.
В 99mTc-диаминдиоксимовых комплексах по настоящему изобретению R3 предпочтительно представляет собой Н. Также предпочтительно, чтобы по меньшей мере одна группа R2 представляла собой Н, более предпочтительно все группы R2 представляли собой Н. Каждая R1 предпочтительно представляет собой C1-3алкил. Особенно предпочтительно, чтобы все группы R1 представляли собой CH3. Предпочтительные группы Y для комплекса 99mTc являются такими, как было описано выше для хелатного конъюгата.
Предпочтительные комплексы с радиоактивным металлом по настоящему изобретению, где 2 группы R, которые вместе с атомами, к которым они присоединены, образуют карбоциклическое насыщенное кольцо, включают в себя такие кольца, которые имеют от 3 до 6 членов, в частности 5 или 6 членов. Предпочтительные карбоциклические кольца представляют собой кольца, где 2 группы R1, присоединенные либо к одному и тому же атому углерода, либо к соседним атомам углерода, соединены с образованием 3-6-членных, в частности 5 или 6-членных насыщенных колец.
Комплексы с радиактивным металлом по настоящему изобретению могут быть получены путем взаимодействия раствора радиоактивного металла в подходящем состоянии окисления с хелатным конъюгатом при подходящем значении рН. Раствор может предпочтительно содержать лиганд, который слабо вступает в комплекс с металлом (таким как глюконат или цитрат), т.е. получают комплекс с радиоактивным металлом путем обмена лигандами или трансхелатообразования. Такие условия пригодны для подавления нежелательных побочных реакций, таких как гидролиз иона металла. Когда ион радиоактивного металла представляет собой 99mTc, обычный исходный материал представляет собой пертехнетат натрия из генератора 99Mo. Технеций представлен в 99mTc-пертехнетате в состоянии окисления Tc(VII), которое является относительно нереакционноспособным. При получении комплексов технеция с более низким состоянием окисления от Tc(I) до Tc(V), таким образом, обычно для облегчения комплексообразования требуется добавление пригодного фармацевтически приемлемого восстановителя, такого как дитионит натрия, бисульфит натрия, аскорбиновая кислота, формамидинсульфиновая кислота, ион двухвалентного олова, Fe(II) или Cu(I). Фармацевтически приемлемый восстановитель предпочтительно представляет собой соль двухвалентного олова, наиболее предпочтительно хлорид двухвалентного олова, фторид двухвалентного олова или тартрат двухвалентного олова.
В третьем аспекте настоящего изобретения предложены радиоактивные фармацевтические препараты, которые включают в себя вышеупомянутые комплексы хелатных конъюгатов с радиоактивным металлом в стерильной форме, пригодной для введения человеку. Такие радиоактивные фармацевтические препараты удобным образом поставляются в контейнере, который оборудован крышкой, которая пригодна для разового или многократного укола шприцем для подкожных инъекций (например, изолирующая крышка с обжатой мембраной) при сохранении стерильности. Такие контейнеры могут содержать однократные или иногократные дозы для пациентов. Предпочтительные контейнеры для многократных доз включают одиночный объемный флакон (например, объемом от 10 до 30 см3), который содержит многократные дозы для пациентов, из которого в соответствии с клинической ситуацией в медицинские шприцы с различными интервалами времени в течение срока годности препарата могут быть отобраны однократные дозы для пациентов. Предварительно заполненные шприцы предназначены для содержания однократной дозы для человека и поэтому предпочтительно представляют собой одноразовые или другие шприцы, пригодные для клинического использования. Предварительно заполненный шприц возможно может быть снабжен защитным кожухом для защиты оператора от радиоактивной дозы. Такие пригодные защитные кожухи для шприца с радиоактивным фармацевтическим препаратом известны из уровня техники и предпочтительно включают в себя или свинец, или вольфрам.
Радиоактивность содержимого 99mТс, пригодная для диагностического радиоактивного фармацевтического препарата для визуализации, находится в диапазоне от 180 до 1500 мБк в зависимости от сайта визуализации in vivo, поглощения и соотношения мишень/фон. Для визуализации сердца с применением радиоактивного фармацевтического препарата, содержащего 99mTc, может применяться приблизительно 1110 мБк (30 мКи) для исследования в состоянии стресса и приблизительно 250 мБк (10 мКи) для исследования в состоянии покоя.
В четвертом аспекте настоящее изобретение предлагает нерадиоактивные наборы для приготовления радиоактивной фармацевтической композиции, содержащей 99mТс. Такие наборы предназначены для получения стерильных радиоактивных фармацевтических продуктов, пригодных для введения человеку, например, посредством прямой инъекции в кровоток. Для 99mТс набор предпочтительно лиофилизирован и предназначен для разведения стерильным 99mТс-пертехнетатом (TcO4 -) из генератора радиоизотопа 99mTc с получением раствора, пригодного для введения человеку без какой-либо дополнительной обработки. Пригодные наборы включают в себя контейнер (например, закрытый диафрагмой флакон), содержащий хелатный конъюгат формулы II или в форме свободного основания или соли кислоты, вместе с фармацевтически приемлемым восстановителем, таким как дитионит натрия, бисульфит натрия, аскорбиновая кислота, формамидинсульфиновая кислота, ион двухвалентного олова, Fe(II) или Cu(I). Фармацевтически приемлемый восстановитель предпочтительно представляет собой соль двухвалентного олова, такую как хлорид двухвалентного олова или тартрат двухвалентного олова. Альтернативно набор может возможно содержать комплекс металла, который при добавлении радиоактивного металла претерпевает переметаллирование (т.е. обмен металлом) с получением желаемого продукта.
Нерадиоактивные наборы могут возможно дополнительно включать в себя дополнительные компоненты, такие как трансхелатообразователь, радиопротектор, антимикробный консервант, агент, регулирующий рН, или наполнитель. "Трансхелатообразователь" представляет собой соединение, которое быстро вступает в реакцию с образованием слабого комплекса с технецием, затем замещается диаминдиоксимом. Это минимизирует риск образования восстановленного гидролизованного технеция (ВГТ) вследствие быстрого восстановления пертехнетата, конкурирующего с образованием комплекса с технецием. Такие пригодные трансхелатообразователи представляют собой соли слабой органической кислоты, т.е. органической кислоты, обладающие значением рКа, находящимся в диапазоне от 3 до 7, с биосовместимым катионом. Такие пригодные слабые органические кислоты представляют собой уксусную кислоту, лимонную кислоту, винную кислоту, глюконовую кислоту, глюкогептоновую кислоту, бензойную кислоту, фенолы или фосфоновые кислоты. Следовательно, пригодные соли представляют собой ацетаты, цитраты, тартраты, глюконаты, глюкогептонаты, бензоаты, феноляты или фосфонаты. Такие предпочтительные соли представляют собой тартраты, глюконаты, глюкогептонаты, бензоаты или фосфонаты, наиболее предпочтительно фосфонаты, в особенности дифосфонаты. Такой предпочтительный трансхелатообразователь представляет собой соль МДФ, т.е. метилендифосфоновой кислоты, с биосовместимым катионом.
Под термином "радиопротектор" понимают соединение, которое ингибирует реакции разрушения, такие как процессы окисления, путем захвата высокореакционных свободных радикалов, таких как кислородсодержащие свободные радикалы, возникающие в результате радиолиза воды. Радиопротекторы по настоящему изобретению удобным образом выбраны из аскорбиновой кислоты, пара-аминобензойной кислоты (т.е. 4-аминобензойной кислоты), гентизиновой кислоты (т.е. 2,5-дигидроксибензойной кислоты) и их солей с биосовместимым катионом в соответствии с тем, как было описано выше.
Под термином "антимикробный консервант" понимают агент, который ингибирует рост потенциально вредных микроорганизмов, таких как бактерии, дрожжи или плесневые грибы. Антимикробный консервант может также проявлять некоторые бактерицидные свойства в зависимости от дозы. Основная роль антимикробного консерванта(ов) по настоящему изобретению заключается в том, чтобы ингибировать рост любого микроорганизма в радиоактивной фармацевтической композиции после ее разведения, т.е. в самом радиоактивном диагностическом продукте. Тем не менее антимикробный консервант также возможно может использоваться для ингибирования роста потенциально вредных микроорганизмов в одном или более чем одном компоненте нерадиоактивного набора по настоящему изобретению перед разведением. Приемлемый(е) антимикробный(е) консервант(ы) включает(ют) в себя парабены, т.е. метил-, этил-, пропил- или бутилпарабен или их смеси; бензиловый спирт; фенол; крезол; цетавлон и тиомерсал. Предпочтительный(е) антимикробный(е) консервант(ы) представляет(ют) собой парабены.
Термин "агент, регулирующий рН" обозначает соединение или смесь соединений, пригодную для обеспечения того, что рН разведенного набора окажется в допустимых пределах (приблизительно рН от 4,0 до 10,5) для введения человеку и млекопитающим. Такие пригодные агенты, регулирующие рН, включают в себя фармацевтически приемлемые буферы, такие как трицин, фосфат или трис (т.е. трис(гидроксиметил)аминометан), и фармацевтически приемлемые основания, такие как карбонат натрия, бикарбонат натрия или их смеси. Когда конъюгат формулы II применяют в форм