Фармацевтическая композиция, содержащая полипептиды фактора vii и полипептиды фактора xi
Иллюстрации
Показать всеГруппа изобретений относится к композиции, содержащей фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактор XI полипептид, к наборам, содержащим указанные соединения, и к применению композиции для лечения кровотечений. Фармацевтическая композиция содержит эффективное количество фактор VII или родственный фактор VII полипептид и фактор XI или родственный фактору XI полипептид. Изобретение обеспечивает: 1. создание композиций, которые могут эффективно использованы для лечения или профилактики кровотечений и нарушений свертывания крови, предпочтительно пероральных композиций; 2. создание композиций в виде разовой дозированной формы, которая может быть эффективно использована для лечения или профилактики кровотечений или в качестве прокоагулянта; 3. создание композиций, обладающих синергическим действием, создание способов лечения или комплектов, применение которых способствует проявлению синергического эффекта; 4. создание композиций, способов лечения и комплектов, не имеющих существенных побочных эффектов, таких как высокий уровень системной активации системы свертывания крови. 3 н. и 40 з.п. ф-лы, 1 табл., 4 ил.
Реферат
Область изобретения
Настоящее изобретение относится к фармацевтической композиции, содержащей фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид. Изобретение также относится к применению комбинации фактора VII или полипептида, родственного фактору VII, и фактора XI или полипептида, родственного фактору XI, для производства лекарственного средства с целью лечения субъектов, страдающих кровотечениями, или профилактики кровотечений. Изобретение также относится к способу лечения кровотечений у субъектов и к способу ускорения образования сгустка у субъекта. Настоящее изобретение также относится к наборам, содержащим указанные соединения.
Предпосылки к созданию изобретения
Гемостаз инициируется посредством образования комплекса между тканевым фактором (TF), который экспонируется в кровотоке после повреждения стенки сосуда, и фактором FVIIa, который находится в кровотоке в количестве, соответствующем приблизительно 1% от общей массы белка FVII. Указанный комплекс прочно прикрепляется к TF-несущей клетке и активирует FX (фактор X) в FXa (фактор Xa) и активирует FIX (фактор IX) в FIXa (фактор IXa) на поверхности клетки. FXa активирует протромбин и превращает его в тромбин, который в свою очередь активирует FVIII, FV, FXI FXIII. Кроме того, ограниченное количество тромбина, образованного на этой первоначальной стадии гемостаза, также активирует тромбоциты. После воздействия тромбина на тромбоциты, последние изменяют форму и «выставляют» на поверхность заряженные фосфолипиды. Активированная поверхность тромбоцита образует матрицу для дальнейшей активации FX и полного образования тромбина. Дальнейшая активация FX на активированной поверхности тромбоцита происходит посредством комплекса FIXa-FVIIIa, образованного на поверхности активированного тромбоцита, и FXa затем превращает протромбин в тромбин, все еще оставаясь на поверхности. Затем тромбин превращает фибриноген в фибрин, который является нерастворимым и который стабилизирует первоначальную «пробку» из тромбоцитов. Этот процесс является обособленным, т.е. локализуется на участке экспрессии или местоположения TF, тем самым снижается риск системной активации свертывающей системы крови. Нерастворимый фибрин, образующий «пробку», кроме того, стабилизируется посредством поперечного связывания фибриновых волокон, катализируемого фактором FXIII.
Фактор FVII существует в плазме, главным образом, в виде одноцепочечного зимогена, который расщепляется посредством фактора FXa на двухцепочечную, активированную форму, FVIIa. Рекомбинантный активированный фактор VIIa (rFVIIa) был разработан в качестве прогемостатического агента. Введение rFVIIa приводит к быстрому и высокоэффективному прогемостатическому ответу у больных гемофилией с кровотечениями, которых нельзя лечить факторами свертывания вследствие образования антител. Кроме того, субъектов, которые страдают от кровотечений, с недостаточностью фактора VII или субъектов, у которых свертывающая система крови находится в норме, страдающих чрезмерным кровотечением, можно успешно лечить с помощью фактора FVIIa. При изучении данной проблемы исследователи не сталкивались с неблагоприятными побочными эффектами, обусловленными введением rFVIIa (в частности, возможность развития тромбоэмболии).
Дополнительно введенный фактор FVIIa улучшает образование тромбина на активированной поверхности тромбоцита. Такое явление имеет место у больных гемофилией, у которых отсутствует фактор FIX или FVIII и поэтому не осуществляется самый эффективный путь полного образования тромбина. Также в присутствии пониженного количества тромбоцитов или тромбоцитов с нарушением функции добавочный фактор FVIIa увеличивает образование тромбина.
Коммерческие препараты рекомбинантного человеческого фактора FVIIa продаются как NovoSeven®(Novo Nordisk A/S, Denmark). Novoseven® показан для лечения случаев кровотечений у больных гемофилией А и В. Novoseven® является единственным рекомбинантным фактором FVIIa, доступным на рынке, для эффективного и надежного лечения кровотечений.
Фактор FXI является одним из компонентов пути свертывания крови. Недостаточность FXI связана с кровотечениями, от слабых до умеренных, особенно из тканей с высокой локальной фибринолитической активностью. Исследователи полагают, что в сравнении с недостаточностью FXI, высокое содержание FXI являются фактором риска венозного тромбоза. Фактор FXI является зимогеном трипсиноподобной сериновой протеазы, который активируется посредством фактора FXIIa, тромбина и фактора FXIa. Активированный фактор FXI (FXIa) участвует в активации FIX, который в свою очередь (в комбинации с FVIII) также активирует FX и, таким образом, приводит к образованию тромбина.
Хорошо известно, что у субъектов, у которых наблюдается чрезмерное кровотечение в связи с операцией или обширной травмой и которые нуждаются в переливании крови, развивается больше осложнений, чем у субъектов, не страдающих кровотечениями. Однако, умеренные кровотечения у субъектов, нуждающихся во введении крови человека или элементов крови (тромбоциты, лейкоциты, произведенные из плазмы концентраты для лечения нарушений свертывания крови и т.д.), могут привести к осложнениям, связанным с риском передачи с кровью вирусов человека (вируса гепатита, ВИЧ, парвовируса и других, до сих пор неизвестных вирусов). Массивные кровотечения у субъектов, нуждающихся в значительных переливаниях крови, могут привести к развитию полиорганной недостаточности, включая нарушение функции легких и почек. Как только у субъекта начинают развиваться указанные серьезные осложнения, то запускается каскад реакций, в которые вовлекается ряд цитокинов, а также воспалительные реакции, делая любое лечение крайне затруднительным и, к сожалению, часто неэффективным. Поэтому основной задачей в хирургии, а также в лечении обширных повреждений ткани является предупреждение кровотечений или сведение их к минимуму. Для того, чтобы избежать кровотечений или свести их к минимуму, важно добиться образования стабильных и плотных гемостатических «пробок», которые плохо растворяются под действием фибринолитических ферментов. Кроме того, важно достичь быстрого и эффективного образования таких «пробок» или сгустков.
На сегодняшний день, в случаях кровотечений у субъектов, включая жертв различных травм и тех, у кого кровотечения связаны с хирургической операцией, лечение часто осуществляют посредством нескольких инъекций или инфузий фактора FVIIa, поскольку из-за короткого полупериода существования FVIIa (2,5 часа) может потребоваться более одного введения для поддержания определенного уровня гемостатической способности. Более быстрая остановка кровотечений принесет больше пользы таким субъектам. Поэтому в таких случаях следует снизить количество введений, чтобы остановить кровотечение и поддержать гемостаз.
Заявка на выдачу патента Японии No. 59-116213A касается аэрозольной композиции для использования ее как тканевого клея, содержащей в качестве активного компонента реагент, способствующий коагуляции крови. Реагент, способствующий коагуляции крови, может быть выбран из факторов свертывания крови I, II, III, IV, V, VII, VIII, IX, X, XI, XII и XIII, прекалликреина, высокополимерного кининогена и тромбина. Предпочтительной является комбинация фактора FXIII и тромбина.
Европейский патент No. 225160 (Novo Nordisk) касается композиций FVIIa и способов лечения нарушений, сопровождающихся кровотечением, которые не вызваны дефектами факторов свертывания крови или ингибиторами факторов свертывания крови.
Европейский патент No. 82182 (Baxter Travenol Lab.) касается композиции фактора VIIa, которую используют для восполнения недостаточности факторов свертывания крови или противодействия ингибиторам факторов свертывания крови у субъекта.
Международная патентная публикация No. WO 93/06855 (Novo Nordisk) касается местного применения FVIIa.
Патент США No. 5252217 касается способа получения концентрата фактора XI человека для терапевтических целей.
До сих пор в данной области существует потребность в усовершенствованном лечении субъектов, страдающих кровотечением, включая субъектов, у которых случаи кровотечения вызваны операцией, травмой или другими видами повреждений ткани; коагулопатией, включая коагулопатию у субъектов, претерпевших многократные переливания крови; обусловлены врожденными или приобретенными нарушениями в системе свертывания крови или нарушениями, сопровождающимися кровотечением, включая гипофункцию печени («заболевание печени»); обусловлены нарушением функции тромбоцитов или снижением количества тромбоцитов; отсутствием существенных «соединений» свертывания крови или наличием аномальных «соединений» свертывания крови (например, тромбоциты или белковый фактор Виллебранда); связаны с повышенным фибринолизом; обусловлены терапией антикоагулянтными средствами или терапией тромболитическими средствами; или трансплантацией стволовой клетки.
В данной области также сохраняется потребность в улучшенном, надежном и широко применяемом способе, повышающем свертывающую способность крови, улучшающем или обеспечивающем образование стабильных гемостатических «пробок», или увеличивающем возможности для благотворного лечения субъекта, или приводящем к достижению полного гемостаза у субъектов, в частности, у субъектов со сниженным образованием тромбина. Также имеется потребность в способах, в которых количество FVIIa, необходимое для достижения полного гемостаза, снижается, и способах, где время остановки кровотечения сокращается.
Краткое описание сущности изобретения
Одной целью настоящего изобретения является создание композиций, которые могут быть эффективно использованы для лечения или профилактики кровотечений и нарушений свертывания крови.
Второй целью настоящего изобретения является создание композиций в виде разовой дозированной формы, которая может быть эффективно использована для лечения или профилактики кровотечений или в качестве прокоагулянта. Другой целью настоящего изобретения является создание композиций, обладающих синергическим действием, создание способов лечения или комплектов, применение которых способствует проявлению синергического эффекта.
Другой целью настоящего изобретения является создание композиций, способов лечения и комплектов, не имеющих существенных побочных эффектов, таких как высокий уровень системной активации системы свертывания крови.
Другие цели настоящего изобретения будут очевидны при прочтении настоящего описания.
В первом аспекте, изобретение относится к фармацевтической композиции, содержащей фактор VII или родственный фактору VII полипептид, и фактор XI или родственный фактору XI полипептид.
Во втором аспекте, изобретение относится к набору компонентов, предназначенному для лечения кровотечений, содержащему
a) эффективное количество препарата фактора VII или родственного фактору VII полипептида и фармацевтически приемлемый носитель в первой разовой дозированной форме;
b) эффективное количество препарата фактора XI или родственного фактору XI полипептида и фармацевтически приемлемый носитель во второй разовой дозированной форме; и
с) контейнер, вмещающий указанные первую и вторую лекарственную формы.
В различных аспектах изобретения, набор также содержит эффективное количество TFPI-ингибитора и/или фактора VIII; TFPI-ингибитор или фактор VIII (или комбинация из них) могут находиться в отдельных стандартных лекарственных формах или могут находиться в одной из стандартных лекарственных форм, содержащей либо фактор VII или родственный фактору VII полипептид, либо фактор XI или родственный фактору XI полипептид.
В третьем аспекте, изобретение относится к применению фактора VII или родственного фактору VII полипептида в комбинации с фактором XI или родственным фактору XI полипептидом для производства лекарственного средства с целью лечения кровотечений у субъекта. В другом аспекте, изобретение относится к применению композиции, как описано в любом из пунктов формулы изобретения 1-18, для производства лекарственного средства с целью лечения кровотечений у субъекта.
В разных аспектах изобретения, лекарственные средства предназначены для снижения времени свертывания крови, увеличения времени фибринолиза и повышения прочности сгустка.
В другом аспекте, лекарственное средство получают для внутривенного введения, предпочтительно в виде инъекции или инфузии, в частности, в виде инъекции.
В одном аспекте, лекарственное средство получают в виде разовой дозированной формы; в другом аспекте, лекарственное средство получают в виде первой разовой дозированной формы, содержащей препарат фактора VII или родственного фактору VII полипептида, и в виде второй разовой дозированной формы, содержащей препарат фактора XI или родственного фактору XI полипептида.
В различных аспектах, лекарственные средства предназначены для лечения субъектов в случаях кровотечений вследствие операции, травмы или других типов повреждения ткани; коагулопатии, включающей коагулопатию у субъектов, претерпевших многократные переливания крови; врожденных или приобретенных нарушений в системе свертывания крови или нарушений, сопровождающихся кровотечением, включающих гипофункцию печени («заболевание печени»); нарушения функции тромбоцитов или снижения количества тромбоцитов; отсутствия существенных «соединений» системы свертывания крови или наличия аномальных «соединений» системы свертывания крови (например, тромбоциты или белковый фактор Виллебранда); повышенного фибринолиза; терапии антикоагулянтными средствами и терапии тромболитическими средствами; трансплантации стволовой клетки. В одной серии аспектов, кровотечения происходят в органах, таких как головной мозг, область внутреннего уха, глаз, печень, легкое, опухолевая ткань, желудочно-кишечный тракт; в другой серии аспектов, кровотечение является диффузным кровотечением, таким как при геморрагическом гастрите и профузное маточное кровотечение. В другой серии аспектов, случаи кровотечения связаны с операцией или травмой у субъектов, у которых наблюдаются острые гемартрозы (кровоизлияния в суставы), хроническая гемофилическая артропатия, гематомы (например, мышечные, забрюшинные, подъязычные и заглоточные), кровотечения в другой ткани, гематурия (кровотечение из мочевыводящих путей), кровоизлияние в мозг, которые подверглись хирургической операции (например, гепатэктомии), удаление зуба и желудочно-кишечные кровоизлияния (например, кровотечения при UGI). В одном аспекте, лекарственное средство предназначено для лечения кровотечений вследствие травмы, операции или пониженного числа тромбоцитов или сниженной активности тромбоцитов у субъекта.
В другом аспекте, изобретение относится к способу лечения кровотечений у субъекта, предусматривающему введение субъекту при необходимости количества первого препарата фактора VII или родственного фактору VII полипептида и количества второго препарата фактора XI или родственного фактору XI полипептида, где количества первого и второго препарата вместе взятые являются эффективными при лечении кровотечений.
В другом аспекте, изобретение относится к способу снижения времени свертывания крови у субъекта, предусматривающему введение субъекту при необходимости количества первого препарата фактора VII или родственного фактору VII полипептида и количества второго препарата фактора XI или родственного фактору XI полипептида, где количества первого и второго препарата, вместе взятые, являются эффективными для снижения времени свертывания крови.
В другом аспекте, изобретение относится к способу, способствующему повышению гемостаза, предусматривающему введение субъекту при необходимости количества первого препарата фактора VII или родственного фактору VII полипептида и количества второго препарата фактора XI или родственного фактору XI полипептида, где количества первого и второго препарата, вместе взятые, являются эффективными для повышения гемостаза.
В другом аспекте, изобретение относится к способу, позволяющему увеличить период времени фибринолиза у субъекта, предусматривающему введение субъекту при необходимости количества первого препарата фактора VII или родственного фактору VII полипептида и количества второго препарата фактора XI или родственного фактору XI полипептида, где количества первого и второго препарата, вместе взятые, являются эффективными для увеличения времени фибринолиза.
В другом аспекте, изобретение относится к способу повышения прочности сгустка у субъекта, предусматривающему введение субъекту при необходимости количества первого препарата фактора VII или родственного фактору VII полипептида и количества второго препарата фактора XI или родственного фактору XI полипептида, где количества первого и второго препарата, вместе взятые, являются эффективными для повышения прочности сгустка.
В одной серии аспектов способов, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид вводят в виде разовой дозированной формы.
В другой серии аспектов, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид вводят в виде первой разовой дозированной формы, содержащей препарат фактора VII или родственного фактору VII полипептида, и второй разовой дозированной формы, содержащей препарат фактора XI или родственного фактору XI полипептида. В серии аспектов изобретения, первую стандартную лекарственную форму и вторую стандартную лекарственную форму вводят раздельно с интервалом времени не более чем 15 минут.
В другом аспекте, изобретение относится к набору, предназначенному для лечения кровотечений, включающему в себя
d) эффективное количество фактора VII или родственного фактору VII полипептида и эффективное количество фактора XI или родственного фактору XI полипептида и фармацевтически приемлемый носитель в одной, разовой дозированной форме; и
е) контейнер, вмещающий указанную одну, стандартную лекарственную форму.
В одной серии аспектов изобретения, фактором VII или родственным фактору VII полипептидом является родственный фактору VII полипептид. В одной серии аспектов изобретения, родственный фактору VII полипептид представляет собой вариант аминокислотной последовательности фактора VII. В одном аспекте, отношение активности родственного фактору VII полипептида к активности нативного фактора VIIa человека (FVIIa дикого типа) составляет, по крайней мере, приблизительно 1,25, причем приведенные данные получены в результате исследований с помощью «анализа посредством гидролиза in vitro», как описано в настоящем описании.
В одной серии аспектов изобретения, фактором VII или родственным фактору VII полипептидом является фактор VII. В одном аспекте, указанным фактором VII является фактор VII человека. В одном аспекте, фактор VII является фактором VII крупного рогатого скота, свиньи, собаки, лошади, мыши или лосося. В другом аспекте, фактор VII является рекомбинантным фактором. В другом аспекте, фактор VII получен из плазмы. В предпочтительном аспекте, фактор VII является рекомбинантным фактором VII человека. В одной серии аспектов изобретения, фактор VII или родственный фактору VII полипептид находится в его активированной форме. В одном предпочтительном аспекте изобретения, фактор VII является рекомбинантным фактором VIIa человека.
В одной серии аспектов изобретения, фактором XI или родственным фактору XI полипептидом является родственный фактору XI полипептид. В одной серии аспектов изобретения, родственный фактору XI полипептид представляет собой вариант аминокислотной последовательности фактора XI. В одном аспекте, отношение активности указанного родственного фактору XI полипептида к активности нативного фактора XI плазмы человека (FXI дикого типа) составляет, по крайней мере, приблизительно 1,25, причем приведенные данные получены в результате исследований с помощью «FXI хромогенного анализа», как описано в настоящем описании. В одном аспекте, фактором XI или родственным фактору XI полипептидом является родственный фактору XI полипептид. В одном аспекте, фактором XI является фактор XI человека. В одном аспекте, фактор XI является фактором XI крупного рогатого скота, свиньи, собаки, лошади, мыши или лосося. В предпочтительном аспекте, фактор XI является рекомбинантным фактором. В другом аспекте, фактор XI получен из плазмы. В другом аспекте, фактор XI является полученным из тромбоцитов фактором XI. В предпочтительном аспекте, фактор XI является рекомбинантным фактором XI плазмы человека. В одной серии аспектов изобретения, фактор XI или родственный фактору XI полипептид находится в его активированной форме. В одном аспекте, родственный фактору XI полипептид является фрагментом фактора XI. В одном аспекте, родственный фактору XI полипептид является гибридным полипептидом фактора XI, например, гибридный полипептид свиньи/человека. В одном аспекте, фактор XI является активированным фактором XI плазмы человека (FXIa).
В одном аспекте, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид присутствуют в соотношении по массе приблизительно между 100:1 и 1:100 (мас./мас. фактор VII:фактор XI).
В одном аспекте, родственные фактору VII полипептиды представляют собой варианты аминокислотной последовательности, в которой не более чем 20 аминокислот замещены, удалены или вставлены по сравнению с фактором VII дикого типа (т.е., полипептид с аминокислотной последовательностью, описанной в патенте США No. 4784950). В другом аспекте, варианты фактора VII имеют не более чем 15 аминокислот, которые замещены, удалены или вставлены; в других аспектах, варианты фактора VII имеют не более чем 10 аминокислот, таких как 8, 6, 5 или 3 аминокислоты, которые замещены, удалены или вставлены по сравнению с фактором VII дикого типа. В одном аспекте, варианты фактора VII выбирают из перечня L305V-FVIIa, L305V/M306D/D309S-FVIIa, L305I-FVIIa, L305T-FVIIa, F374P-FVIIa, V158T/M298Q-FVIIa, V158D/E296V/M298Q-FVIIa, K337A-FVIIa, M298Q-FVIIa, V158D/M298Q-FVIIa, L305V/K337A-FVIIa, V158D/E296V/M298Q/L305V-FVIIa, V158D/E296V/M298Q/K337A-FVIIa, V158D/E296V/M298Q/L305V/K337A-FVIIa, K157A-FVII, E296V-FVII, E296V/M298Q-FVII, V158D/E296V-FVII, V158D/M298K-FVII и S336G-FVII.
В другом аспекте, родственные фактору VII полипептиды обладают повышенной активностью, независимой от тканевого фактора, по сравнению с активностью нативного фактора VIIa свертывания крови человека. В другом аспекте, повышенная активность не сопровождается изменениями в субстратной специфичности. В другом аспекте изобретения, связывание родственных фактору VII полипептидов с тканевым фактором не ухудшается, и родственные фактору VII полипептиды проявляют, по крайней мере, активность фактора VIIa дикого типа при связывании с тканевым фактором.
В предпочтительном аспекте, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид представляют собой рекомбинантный фактор VIIa человека и рекомбинантный фактор XI плазмы человека или рекомбинантный фактор VIIa человека и рекомбинантный фактор XIa плазмы человека.
В одном аспекте, время свертывания крови млекопитающих снижается. В другом аспекте, гемостаз в крови млекопитающих усиливается. В другом аспекте, время фибринолиза в крови млекопитающих увеличивается. В другом аспекте, прочность сгустка в крови млекопитающих повышается. В одном аспекте, кровью млекопитающих является кровь человека. В другом аспекте, кровью млекопитающих является кровь человека в норме; в одном аспекте, кровь представляет собой кровь субъекта, у которого образование тромбина снижено. В одном аспекте, кровь представляет собой кровь субъекта с недостаточностью одного или более факторов свертывающей системы; в другом аспекте, кровь представляет собой кровь субъекта, содержащую ингибиторы одного или более факторов свертывающей системы; в одном аспекте, кровь представляет собой кровь субъекта, содержащую сниженную концентрацию фибриногена; в одном аспекте, кровь представляет собой кровь человека с недостаточностью фактора XI. В одной серии аспектов, кровью является плазма.
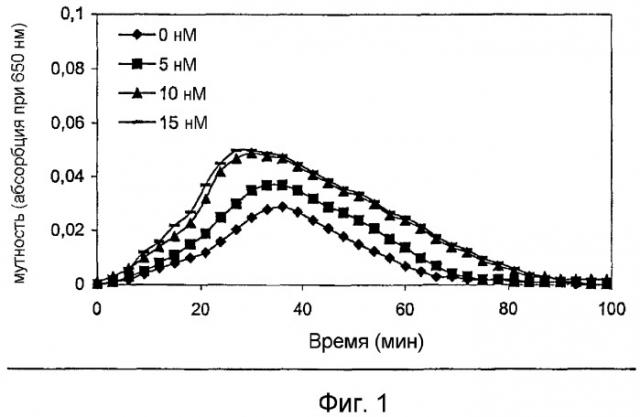
В одном аспекте, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид способствуют увеличению времени фибринолиза в плазме человека в норме. В другом аспекте, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид повышают до максимального уровня прочность сгустка и время фибринолиза в нормальной плазме человека in vitro. В другом аспекте, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид способствуют уменьшению времени свертывания в нормальной плазме человека in vitro.
В одном аспекте изобретения, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид являются единственными гемостатическими агентами в композиции. В другом аспекте, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид являются единственными, активными гемостатическими агентами в композиции. В другом аспекте, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид являются единственными факторами свертывания, вводимыми субъекту. В одном аспекте изобретения, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид являются единственными, активными агентами, вводимыми больному. В одном аспекте, композиция, по существу, не содержит протромбина; в другом аспекте, композиция, по существу, не содержит FX; в другом аспекте, композиция, по существу, не содержит FXa.
В другом аспекте, фармацевтическую композицию получают для внутривенного введения, предпочтительно в виде инъекции или инфузии, в частности, инъекции. В одном аспекте, композиция содержит, по крайней мере, один фармацевтически приемлемый наполнитель или носитель.
В одном аспекте изобретения, композиция находится в виде разовой дозированной формы, где однократная, стандартная лекарственная форма содержит оба фактора свертывания. В одном аспекте изобретения, композиция находится в виде набора компонентов, содержащего препарат фактора VII или родственного фактору VII полипептида как первую стандартную лекарственную форму и препарат фактора XI или родственного фактору XI полипептида как вторую стандартную лекарственную форму, и содержащего контейнер, вмещающий указанную первую и вторую стандартную лекарственную форму. В одном аспекте композиция или набор, по необходимости, также содержит инструкции для введения композиции или отдельных компонентов, соответственно.
В одном аспекте изобретения, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид вводят в виде разовой дозированной формы. В одном аспекте изобретения, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид вводят в виде первой разовой дозированной формы, содержащей препарат фактора VII или родственного фактору VII полипептида, и второй разовой дозированной формы, содержащей препарат фактора XI или родственного фактору XI полипептида.
В одном аспекте изобретения, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид вводят одновременно. В другом аспекте, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид вводят последовательно. В одном аспекте, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид вводят раздельно с интервалом времени не более чем 15 минут, предпочтительно 10, более предпочтительно 5, наиболее предпочтительно 2 минуты. В одном аспекте, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид вводят раздельно с интервалом времени вплоть до 2 часов, предпочтительно от 1 до 2 часов, более предпочтительно вплоть до 1 часа, более предпочтительно от 30 минут до 1 часа, более предпочтительно вплоть до 30 минут, наиболее предпочтительно от 15 до 30 минут.
В одном аспекте, эффективное количество фактора VII или родственного фактору VII полипептида составляет количество от приблизительно 0,05 мг/сутки до приблизительно 500 мг/сутки (субъект весом 70 кг). В одном аспекте, эффективное количество препарата фактора XI или родственного фактору XI полипептида составляет приблизительно от 0,01 мг/сутки до 500 мг/сутки (субъект весом 70 кг).
В одном аспекте, фактор VII или родственный фактору VII полипептид и фактор XI или родственный фактору XI полипептид присутствуют в соотношении по массе приблизительно между 100:1 и 1:100 (мас./мас. фактор VII: фактор XI).
В одном аспекте настоящего изобретения, фармацевтическая композиция представлена в виде однократной лекарственной формы и состоит, в основном, из препарата фактора VII или родственного фактору VII полипептида и препарата фактора XI или родственного фактору XI полипептида и одного или более компонентов, выбранных из перечня фармацевтически приемлемых наполнителей или носителей, стабилизаторов, детергентов, нейтральных солей, антиоксидантов, консервантов и протеазных ингибиторов. В следующем аспекте, субъектом является человек; в другом аспекте, у субъекта отмечается снижение образования тромбина; в одном аспекте, у субъекта наблюдается пониженная концентрация фибриногена в плазме (например, у субъекта, претерпевшего многократные переливания крови); в одном аспекте, у субъекта наблюдается пониженная концентрация фактора VIII в плазме.
В другом аспекте, изобретение касается способа, разработанного для повышения гемостаза у субъекта, страдающего синдромом, связанным с фактором VII, способа, сравненного со способом лечения субъекта посредством фактора VII как единственного свертывающего белка, способа, включающего в себя введение субъекту при необходимости количества первого препарата фактора VII или родственного фактору VII полипептида и количества второго препарата фактора XI или родственного фактору XI полипептида, где количества первого и второго препарата, вместе взятые, способствуют эффективному повышению гемостаза.
В другом аспекте, изобретение касается способа, разработанного для повышения образования тромбина у субъекта, способа, включающего в себя введение субъекту при необходимости количества первого препарата фактора VII или родственного фактору VII препарата и количества второго препарата фактора XI или родственного фактору XI полипептида, где количества первого и второго препарата, вместе взятые, способствуют эффективному повышению образования тромбина.
В другом аспекте, изобретение касается способа, разработанного для повышения образования тромбина у субъекта, страдающего синдромом, связанным с фактором VII, способа, сравненного со способом лечения субъекта посредством фактора VII как единственного свертывающего белка, способа, включающего в себя введение субъекту при необходимости количества первого препарата фактора VII или родственного фактору VII полипептида и количества второго препарата фактора XI или родственного фактору XI полипептида, где количества первого и второго препарата, вместе взятые, способствуют эффективному повышению образования тромбина.
В другом аспекте, изобретение касается способа, разработанного с целью уменьшения числа введений белкового фактора свертывания, требуемого для достижения гемостаза у субъекта, страдающего синдромом, связанным с фактором VII, по сравнению с количеством введений, требуемых в тех случаях, когда фактор VII вводят субъекту в качестве единственного белкового фактора свертывания, способа, включающего в себя введение субъекту при необходимости первого количества препарата фактора VII или родственного фактору VII полипептида и второго количества препарата фактора XI или родственного фактору XI полипептида, где первое и второе количество вместе способствуют эффективному снижению числа введений белкового фактора свертывания.
В другом аспекте, изобретение касается способа лечения кровотечений у субъекта, стадающего синдромом, связанным с фактором VII, способа, включающего в себя введение субъекту при необходимости количества первого препарата фактора VII или родственного фактору VII полипептида и количества второго препарата фактора XI или родственного фактору XI полипептида, где количества первого и второго препарата, вместе взятые, проявляют эффективность в лечении кровотечений.
В одном аспекте, фактор VII является рекомбинантным фактором VIIa человека (rFVIIa). В другом аспекте, rFVIIa является NovoSeven® (Novo Nordisk A/S, Bagsvaerd, Denmark).
В одном аспекте, фармацевтическую композицию получают для внутривенного введения. В одном аспекте, композиция также содержит ингибитор фибринолитической системы, включая, без ограничения, апротинин, ε-аминокапроновую кислоту или транексамовую кислоту. В одном аспекте, композиция также содержит TFPI ингибитор и/или FVIII.
В одном аспекте, композиция также содержит фактор VIII. В одном аспекте, фактор VIII является активированным фактором VIII (фактор VIIIa). В следующем аспекте фактором VIII является рекомбинантный фактор VIIIa. В следующем аспекте фактором VIII является рекомбинантный фактор VIIIa человека.
В другом аспекте, изобретение относится к применению фактора VIIa в комбинации с фактором XI для производства лекарственного средства, способствующего повышению образования фибринового сгустка в плазме млекопитающих.
В другом аспекте, изобретение относится к способу, направленному на повышение образования фибринового сгустка у субъекта, способу, который включает в себя введение субъекту при необходимости количества первого препарата фактора VII или родственного фактору VII полипептида и количества второго препарата фактора XI или родственного фактору XI полипептида, где количества первого и второго препарата, вместе взятые, проявляют эффективность в лечении кровотечений.
В одном аспекте настоящего изобретения, фармацевтическая композиция (в виде однократной формы) состоит, в основном, из фактора VIIa и фактора XI и, возможно, фармацевтически приемлемого наполнителя или носителя и, возможно, стабилизатора и, возможно, детергента и, возможно, нейтральной соли и, возможно, антиоксиданта и, возможно, консерванта и, возможно, протеазного ингибитора.
В другом аспекте настоящего изобретения, фармацевтическая композиция (в виде однократной формы) состоит, в основном, из фактора VIIa и фактора XI и, возможно, фармацевтически приемлемого наполнителя или носителя и, возможно, стабилизатора и, возможно, детергента и, возможно, нейтральной соли и, возможно, антиоксиданта и, возможно, консерванта и, возможно, протеазного ингибитора и TFPI-ингибитора.
В другом аспекте настоящего изобретения, фармацевтическая композиция (в виде однократной формы) состоит, в основном, из фактора VIIa и фактора XI и, возможно, фармацевтически приемлемого наполнителя или носителя, и, возможно, стабилизатора и, возможно, детергента и, возможно, нейтральной соли и, возможно, антиоксиданта, и, возможно, консерванта, и, возможно, протеазного ингибитора и фактора VIII и, возможно, TFPI-ингибитора.
В другом аспекте, фармацевтическая композиция (в виде набора) состоит из первой разовой дозированной формы, содержащей, в основном, фактор VIIa и, возможно, фармацевтически приемлемый наполнитель или носитель и, возможно, стабилизатор и, возможно, детергент и, возможно, нейтральную соль и, возможно, антиоксидант и, возможно, консервант и, возможно, протеазный ингибитор; и второй разовой дозированной формы, содержащей, в основном, фактор XI и, возможно, фармацевтически приемлемый наполнитель или носитель и, возможно, стабилизатор и, возможно, детергент и, возможно, нейтральную соль и, возможно, антиоксидант и, возможно, консервант и, возможно, протеазный ингибитор.
В другом аспекте, фармацевтическая композиция (в виде набора) состоит из первой разовой дозированной формы, содержащей, в основном, фактор VIIa и, возможно, фармацевтически приемлемый наполнитель или носитель и, возможно, стабилизатор и, возможно, детергент и, возможно, нейтральную соль и, возможно, антиоксидант и, возможно, консервант и, возможно, протеазный ингибитор; и второй разовой дозированной формы, содержащей, в основном, фактор XI и, возможно, фармацевтически приемлемый наполнитель или носит