Способ определения и разделения жирных кислот
Иллюстрации
Показать всеИзобретение относится к медицине и предназначено для определения состава жирных кислот (ЖК) в биологических тканях организма. Способ включает обработку крови хлороформметанольной смесью в соотношении 2:1, гидролиз и метилирование липидов в растворе серной кислоты и метанола при 80°С в течение 3 часов, охлаждение, обработку метилированной пробы гексансодержащим раствором, высушивание в токе азота и проведение газохроматографического определения и разделения жирных кислот на полярной жидкой фазе диэтиленгликольсукцината (ДЭГС), нанесенного на колонку с внешним диаметром 0,32 мм и длиной 50 м при температуре термостата колонки 140°С. Колонку перед нанесением на нее ДЭГС многократно промывают хлороформом, метанолом, ацетоном и гексаном, ДЭГС наносят на внутреннюю стенку капиллярной колонки динамическим методом так, что толщина слоя ДЭГС составляет 0,5 мкм, затем проводят продувку колонки азотом 5-6 часов на протяжении 3 суток при температуре термостата капиллярной колонки 200°С. Способ позволяет повысить чувствительность определения и разделения ЖК в биологических тканях организма в среднем в 34,95 раз. 2 ил., 3 табл.
Реферат
Изобретение относится к медицине и предназначено для определения состава жирных кислот (ЖК) в биологических тканях организма.
Известен способ оценки спектра ЖК (патент РФ №2237245, G 01 N 33/48, бюл. №27, 27.09.2004 г.), включающий экстрагирование липидов хлороформ-метанольной смесью, гидролиз и метилирование липидов во влажной камере в течение 6 часов с разделением ЖК с помощью полярной жидкой фазы 20% диэтиленгликольсукцината (ДЭГС) на хроматоне N-AW-DMCS при температуре термостата стеклянной колонки 180°С. Однако этот способ имеет недостаточную чувствительность регистрации жирных кислот при их низком содержании в тканях организма.
Задача изобретения: повышение чувствительности определения и разделения ЖК.
Поставленную задачу осуществляют за счет того, что используют капиллярную колонку с внешним диаметром 0,32 мм и длиной 50 м, перед нанесением ДЭГС на внутреннюю стенку капиллярной трубки последнюю многократно промывают органическими растворителями: хлороформом, метанолом, ацетоном и гексаном, для лучшего закрепления пленки ДЭГС, после промывки используют динамический метод нанесения ДЭГС: жидкую фазу ДЭГС прокачивают через капиллярную трубку с помощью сухого азота, растворитель испаряют и удаляют при продувке колонки азотом, толщина слоя ДЭГС составляет 0,5 мкм, после этого проводят продувку колонки азотом в течение 5-6 часов на протяжении 3 суток при температуре термостата капиллярной колонки 200°С, гидролиз и метилирование проводят в течение 3 часов с разделением жирных кислот на полярной жидкой фазе диэтиленгликольсукцината, нанесенного на капиллярную колонку, при температуре колонки термостата 140°С.
Способ осуществляют следующим образом.
Для анализа используют 0,5 мл плазмы крови, эритроцитов, тромбоцитов. Выделение общих липидов плазмы крови осуществляют так же, как и в способе оценки жирных кислот (патент РФ №2237245, G 01 N 33/48, бюл. №27, 27.09.2004 г.), хлороформметанольной смесью в соотношении 2:1, объемом 10 мл по методу Folch J., Lees M., Sloane Stanley G.H. (A simple method for the isolation and purification of total lipids from animal tissues // J. Biol. Chem, - 1957. - V.226. - P.497-509). После выпаривания нижнего слоя, содержащего экстрагированные липиды в хлороформе, в токе газообразного азота проводят этап метилирования с одновременным гидролизом липидов с целью получения летучих продуктов, анализируемых на газовом хроматографе. Для этого сухой липидный экстракт, разведенный в 0,5 мл хлороформа, переносят в виалы, снабженные герметически закрывающимися крышками, куда добавляют 2 мл метанола и 0,1 мл серной кислоты (особо чистой) и перемешивают. Пробы плотно закрывают крышками, помещают во влажную камеру и переносят в сушильный шкаф на 3 часа при температуре 80°С. Через 3 часа в охлажденную метилированную пробу добавляют 2 мл гексана и 1 мл дистиллированной воды. Пробу отстаивают в течение 30 мин, затем собирают верхний слой, содержащий метилированные эфиры жирных кислот в гексане, переносят в остроконечную колбу и высушивают досуха в токе газообразного азота на водяной бане при температуре 37°С.
Приготовление капиллярной колонки с полярной жидкой фазой диэтиленгликольсукцинат (ДЭГС): используют капиллярную колонку с внешним диаметром 0,32 мм и длиной 50 м. Перед нанесением ДЭГС на внутреннюю стенку капиллярной трубки последнюю многократно промывают органическими растворителями: хлороформом, метанолом, ацетоном и гексаном, для лучшего закрепления пленки ДЭГС. После промывки используют динамический метод нанесения ДЭГС. При этом жидкую фазу ДЭГС прокачивают через капиллярную трубку с помощью сухого азота. Затем растворитель испаряют и удаляют при продувке колонки азотом, толщина слоя ДЭГС составляет 0,5 мкм. После этого проводят продувку азотом в течение 5-6 часов на протяжении 3 суток при температуре термостата капиллярной колонки 200°С.
Для анализа метиловых эфиров жирных кислот общих липидов плазмы крови используют газовый хроматограф «Кристалл 2000 М». Для этого в образец добавляют 0,05 мл гексана, из полученного объема в инжектор хроматографа вносят 1 мкл пробы. Использовали режимы термостата колонки 140, 180 и 200°С. Идентификацию жирных кислот проводят с использованием стандартной смеси жирных кислот в концентрации 1 мкг/мл гексана по времени удерживания каждой жирной кислоты (производство стандартов метиловых эфиров жирных кислот фирмы «Serva», Германия).
В таблице 1 показана зависимость уровня регистрации ЖК от температуры колонки.
| Таблица 1Зависимость уровня регистрации ЖК плазмы крови человека от температуры термостата колонки в предлагаемом способе. | |||
| Название ЖК | Содержание ЖК выражено площадью, мм2 | ||
| температура 180°C. | температура 140°C. | температура 200°С. | |
| Лауриновая | 0,801±0,215 | 11,93±5,62* | Не определяется |
| Миристиновая | 2,263±0,492 | 0,001±0,0004** | Не определяется |
| Пальмитиновая | 53,126±11,159 | 69,68±14,31** | 40,68 |
| Пальмитолеиновая | 0,016±0,005 | 12,97±3,34* | 5,56 |
| Стеариновая | 6,851±1,353 | 14,21±0,92*** | 1,34 |
| Олеиновая | 9,177±1,978 | 34,84±2,26*** | 36,92 |
| Линолевая | 16,61±2,873 | 26,94±1,56*** | Не определяется |
| Линоленовая | 0,627±0,333 | 1,03±0,88 | Не определяется |
| Эйкозеновая | 0,991±0,368 | 4,99±1,32* | Не определяется |
| Эйкозотриеновая | 1,165±0,246 | 18,71±4,41** | 14,67 |
| Арахидоновая | 0,801±0,349 | 4,62±1,54* | 1,62 |
| Эйкозопентаеновая | 6,511±2,075 | 46,14±12,47* | 7,14 |
| Докозогексаеновая | 1,055±0,413 | 0,86±0,29 | 5,9 |
| Общая площадь | 99,995 | 246,92 | 113,83 |
Примечание:
Как показывают результаты таблицы 1, температура 140°С термостата колонки наиболее оптимальна по сравнению с 200°С и 180°С для разделения и регистрации ЖК. Общий уровень при температуре 140°С, по сравнению с другими температурными режимами, в 2,2-2,5 раз соответственно выше (Табл.1, общая площадь)
На фиг.1. отображена хроматограмма ЖК на стеклянной колонке с диэтиленгликольсукцинатом на хроматоне N-AW-DMCS. При разделении и регистрации ЖК в количестве, эквивалентном их содержанию в 10 мкл плазмы или при разведении в 100 раз, показана идентификация 5 жирных кислот: лауриновой, миристиновой, пальмитиновой, олеиновой и линолевой. Совсем не идентифицируются при данном разведении эйкозеновая, эйкозотриеновая, арахидоновая, эйкозопентаеновая и докозогексаеновая ЖК.
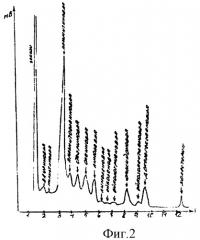
На фиг.2. отображена хроматограмма ЖК на капиллярной колонке с диэтиленгликольсукцинатом. При определении той же концентрации ЖК показана идентификация 10 жирных кислот: лауриновой, миристиновой, пальмитиновой, пальмитолеиновой, стеариновой, олеиновой, линолевой, арахидоновой, эйкозопентаеновой и докозогексаеновой. То есть по предлагаемому способу при данном разведении идентифицируется в 2 раза больше ЖК.
В таблице 2 представлена сравнительная характеристика определения эквивалентных количеств жирных кислот в прототипе и предлагаемом способах, выраженная в площади каждого пика (мм2). Из таблицы видно, что количественный уровень регистрации ЖК, в сравнении с прототипом, возрос от 5,33 до 615,22 раз. В целом чувствительность предлагаемого нами способа возрастает в среднем в 34,95 раза.
| Таблица 2Сравнительная характеристика определения жирных кислот плазмы в существующем и предлагаемом способах (мм2) | |||
| Название ЖК | Прототип | Предлагаемый способ | Соотношение уровня регистрации жирных кислот |
| Лауриновая | 0,012±0,003 | 0,801±0,215* | 66,75 |
| Миристиновая | 0,012±0,002 | 2,263±0,492** | 188,58 |
| Пальмитиновая | 2,198±0,957 | 53,126±11,15** | 24,17 |
| Пальмитолеиновая | 0,003±0,001 | 0,016±0,005* | 5,33 |
| Стеариновая | 0,015±0,005 | 6,851±1,353** | 456,66 |
| Олеиновая | 0,250±0,106 | 9,177±1,978** | 36,7 |
| Линолевая | 0,027±0,017 | 16,611±2,873* | 615,22 |
| Линоленовая | 0,003±0,002 | 0,627±0,333** | 209 |
| Эйкозеновая | 0,143±0,142 | 0,991±0,318** | 6,93 |
| Эйкозотриеновая | 0,064±0,027 | 1,165±0,246* | 18,2 |
| Арахидоновая | 0,080±0,035 | 0,801±0,349* | 10,1 |
| Эйкозопентаеновая | 0,035±0,010 | 6,511±2,075* | 186,02 |
| Докозогексаеновая | 0,019±0,006 | 1,055±0,413* | 55,52 |
| Общая сумма | 2,861 | 99,99 | 34,95 |
| Примечание:В таблице приведены средние данные по ЖК плазмы, взятой от 5 человек. Достоверность отличий предлагаемого способа от существующего р<0,05 - *; р<0,01 - **. |
В таблице 3 показана возможность определения спектра ЖК предлагаемым способом в других тканях организма: эритроцитах, тромбоцитах.
| Таблица 3Возможность определения жирных кислот предлагаемым способом в других тканях организма. | ||
| Название ЖК | Регистрируемый уровень ЖК в площади, мм2 | |
| Эритроциты | Тромбоциты | |
| Лауриновая | 26,405 | 16,45 |
| Миристиновая | 33,99 | 27,13 |
| Пальмитиновая | 19,08 | 10,8 |
| Пальмитолеиновая | 0,98 | 0,01 |
| Стеариновая | 3,51 | 2,53 |
| Олеиновая | 3,58 | 3,15 |
| Линолевая | 4,24 | 1,67 |
| Линоленовая | 1,70 | 1,4 |
| Эйкозотриеновая | 7,70 | 1,63 |
| Арахидоновая | 0,01 | 0,01 |
| Эйкозопентаеновая | 2,24 | 1,69 |
| Докозогексаеновая | 4,17 | 1,23 |
| Общая площадь | 107,605 | 67,7 |
| Примечание: Уровень ЖК определяется в пробах, содержащих 9,42·107 эритроцитов, 75,2·105 тромбоцитов, при температуре термостата колонки 140°С. |
Таким образом, предлагаемый способ позволяет повысить чувствительность определения и разделения ЖК в биологических тканях организма в среднем в 34,95 раз.
Способ определения и разделения жирных кислот в биологических тканях крови организма, включающий обработку крови хлороформметанольной смесью в соотношении 2:1, гидролиз и метилирование липидов в растворе серной кислоты и метанола при 80°С, охлаждение, обработку метилированной пробы гексансодержащим раствором, высушивание в токе азота и проведение газохроматографического определения и разделения жирных кислот на полярной жидкой фазе диэтиленгликольсукцината (ДЭГС), нанесенного на колонку, отличающийся тем, что гидролиз и метилирование липидов проводят в течение 3 ч, для газохроматографического определения и разделения жирных кислот используют капиллярную колонку с внешним диаметром 0,32 мм и длиной 50 м, которую перед нанесением на нее ДЭГС многократно промывают органическими растворителями хлороформом, метанолом, ацетоном и гексаном, ДЭГС наносят на внутреннюю стенку капиллярной колонки динамическим методом, при котором жидкую фазу ДЭГС прокачивают через капиллярную колонку с помощью сухого азота, растворитель испаряют и удаляют при продувке колонки азотом, где толщина слоя ДЭГС составляет 0,5 мкм, затем проводят продувку колонки азотом 5-6 ч на протяжении 3 суток при температуре термостата капиллярной колонки 200°С, а газохроматографическое определение и разделение жирных кислот осуществляют при температуре термостата колонки 140°С.