Аналоги витамина d
Иллюстрации
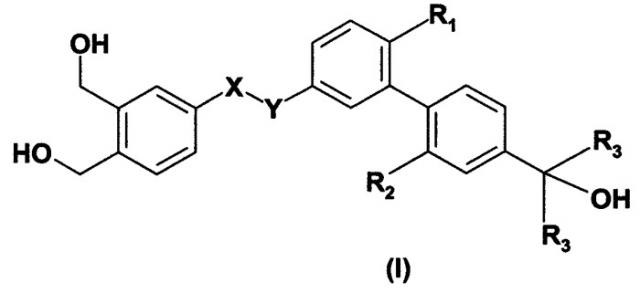
Показать всеИзобретение относится к новым триароматическим соединениям, аналогам витамина D, общей формулы (I):
в которой значения для R1, R2, R3, X, Y определены в п.1 формулы. Изобретение относится также к применению этих соединений в фармацевтических композициях, предназначенных для лечения: 1) дерматологических заболеваний, связанных с нарушением дифференциации или пролиферации кератиноцитов или себоцитов; 2) нарушений кератинизации; 3) дерматологических заболеваний, связанных с нарушением кератинизации с воспалительным и/или иммуноаллергическим компонентом; 4) воспалительных заболеваний, не являющихся нарушением кератинизации; 5) кожных или эпидермических разрастании; 6) дерматологических нарушений, таких как пузырчатые дерматозы и коллагенозы; 7) старения кожи, фотоиндуцированного или возрастного, или для уменьшения пигментации и кератозов, возникающих под действием света, или любых кожных патологий, связанных с возрастным или фотоиндуцированным старением; 8) нарушений заживления и рубцов на коже; 9) нарушений жировой функции, таких как угревой гиперстеатоз или простая себорея или себорейная экзема; 10) дерматологических заболеваний с иммунологическим компонентом; и кроме того, относится к косметическому применению косметической композиции для гигиены тела или волос. 6 н. и 10 з.п. ф-лы, 3 табл. 7 ил.
Реферат
Изобретение относится к триароматическим соединениям, аналогам витамина D, в качестве новых и полезных промышленных продуктов.
Изобретение относится также к способу их получения и их применению в фармацевтических композициях, предназначенных для использования в терапии человека или в ветеринарии, или, кроме того, в косметических композициях.
Соединения согласно изобретению обладают заметной активностью в областях клеточной пролиферации и дифференциации и, более конкретно, находят применения при местном и системном лечении дерматологических (или других) заболеваний, связанных с нарушением кератинизации, заболеваний с воспалительным и/или иммуноаллергическим компонентом и гиперпролиферации тканей эктодермальной природы (кожа, эпителий...), будь то доброкачественной или злокачественной. Кроме того, данные соединения могут быть использованы для борьбы со старением кожи, фотоиндуцированным или возрастным, и для лечения нарушений заживления.
Соединения согласно изобретению можно также использовать в косметических композициях для гигиены тела и волос.
Витамин D является витамином, существенным для профилактики и лечения нарушений минерализации хряща (рахит) и костей (остеомаляция), и даже некоторых форм остеопороза у больных пожилого возраста. Но теперь признают, что его функции распространяются намного шире, чем регулирование костного метаболизма и кальциевого гомеостаза. Среди упомянутых функций можно назвать его воздействие на клеточную пролиферацию и дифференциацию и регулирование реакций иммунной защиты. Их открытие открыло путь к новым терапевтическим подходам в дерматологии, онкологии, а также в области аутоиммунных заболеваний и в области трансплантации органов и тканей.
Эффективная терапевтическая поддержка длительное время сталкивалась с токсичностью данного витамина (гиперкальцемия, иногда со смертельным исходом). В настоящее время синтезированы структурные аналоги витамина D, некоторое из которых сохраняют только дифференцирующую способность и не оказывают влияния на кальциевый метаболизм.
Заявитель уже предложил в международной заявке на патент WO 01/38303 новые соединения - аналоги витамина D, которые обнаруживают селективное воздействие на клеточную пролиферацию и дифференциацию, не проявляя при этом свойств, приводящих к повышению содержания кальция в крови.
В данном изобретении неожиданно обнаружено, что некоторые соединения, конкретно не описанные в заявке WO 01/38303, проявляют биологическую активность, которая намного выше, чем биологическая активность специфически описанных соединений. Упомянутая активность настолько высока, что она больше или равна активности 1,25-дигидроксивитамина D3.
Таким образом, настоящее изобретение касается соединений следующей общей формулы (I):
в которой:
- X-Y обозначает связь, выбранную среди следующих структур:
-CH2-CH2-
-CH2-O-
-O-CH2-
-CH2-N(R4)-
при этом R4 имеет значения, приведенные ниже,
- R1 обозначает метил или этил,
- R2 обозначает этил, пропил или изопропил,
- R3 обозначает этил или трифторметил,
- R4 обозначает атом водорода, метил, этил или пропил,
а также их оптических и геометрических изомеров и их солей.
Настоящее изобретение относится также к соединениям, описанным выше, когда они находятся в форме солей неорганической или органической кислоты, в частности, соляной, серной, уксусной, фумаровой, гемиянтарной, малеиновой и миндальной кислоты.
Среди соединений формулы (I), входящих в объем охраны настоящего изобретения, можно, в частности, назвать следующие:
1. {5-[4'-(1-этил-1-гидроксипропил)-6-метил-2'-пропилбифенил-3-илоксиметил]-2-гидроксиметилфенил}метанол;
2. {5-[6,2'-диэтил-4'-(1-этил-1-гидроксипропил)бифенил-3-илоксиметил]-2-гидроксиметилфенил}метанол;
3. {4-[6-этил-4'-(1-этил-1-гидроксипропил)-2'-пропилбифенил-3-илоксиметил]-2-гидроксиметилфенил}метанол;
4. {4-[6-этил-4'-(1-этил-1-гидроксипропил)-2'-изопропилбифенил-3-илоксиметил]-2-гидроксиметилфенил}метанол;
5. (4-{2-[4'-(1-этил-1-гидроксипропил)-6-метил-2'-пропилбифенил-3-ил]этил}-2-гидроксиметилфенил)метанол;
6. {4-[4'-(1-этил-1-гидроксипропил)-6-метил-2'-пропилбифенил-3-илметокси]-2-гидроксиметилфенил}метанол;
7. (4-{[4'-(1-этил-1-гидроксипропил)-6-метил-2'-пропилбифенил-3-иламино]метил}-2-гидроксиметилфенил)метанол;
8. [4-({[4'-(1-этил-1-гидроксипропил)-6-метил-2'-пропилбифенил-3-ил]метиламино}метил)-2-гидроксиметилфенил]метанол;
9. [4-({этил-[4'-(1-этил-1-гидроксипропил)-6-метил-2'-пропилбифенил-3-ил]амино}метил)-2-гидроксиметилфенил]метанол;
10. [4-({[4'-(1-этил-1-гидроксипропил)-6-метил-2'-пропилбифенил-3-ил]пропиламино}метил)-2-гидроксиметилфенил]метанол;
11. (2-гидроксиметил-4-{2-[6-метил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-ил]этил}фенил)метанол;
12. {2-гидроксиметил-4-[6-метил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-илоксиметил]фенил}метанол;
13. {2-гидроксиметил-4-[6-метил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-илметокси]фенил}метанол;
14. (2-гидроксиметил-4-{[6-метил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-иламино]метил}фенил)метанол;
15. [2-гидроксиметил-4-({N-метил-[6-метил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-ил]амино}метил)фенил]метанол;
16. [4-({N-этил-[6-метил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-ил]амино}метил)-2-гидроксиметилфенил]метанол;
17. [2-гидроксиметил-4-({[6-метил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-ил]-N-пропиламино}метил)фенил]метанол;
18. (4-{2-[6-этил-4'-(1-этил-1-гидроксипропил)-2'-пропилбифенил-3-ил]этил}-2-гидроксиметилфенил)метанол;
19. {4-[6-этил-4'-(1-этил-1-гидроксипропил)-2'-пропилбифенил-3-илметокси]-2-гидроксиметилфенил}метанол;
20. (4-{[6-этил-4'-(1-этил-1-гидроксипропил)-2'-пропилбифенил-3-иламино]метил}-2-гидроксиметилфенил)метанол;
21. [4-({[6-этил-4'-(1-этил-1-гидроксипропил)-2'-пропилбифенил-3-ил]метиламино}метил)-2-гидроксиметилфенил]метанол;
22. [4-({этил-[6-этил-4'-(1-этил-1-гидроксипропил)-2'-пропилбифенил-3-ил]амино}метил)-2-гидроксиметилфенил]метанол;
23. [4-({[6-этил-4'-(1-этил-1-гидроксипропил)-2'-пропилбифенил-3-ил]пропиламино}метил)-2-гидроксиметилфенил]метанол;
24. (4-{2-[6-этил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-ил]этил}-2-гидроксиметилфенил)метанол;
25. {4-[6-этил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-илоксиметил]-2-гидроксиметилфенил}метанол;
26. {4-[6-этил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-илметокси]-2-гидроксиметилфенил}метанол;
27. (4-{[6-этил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-иламино]метил}-2-гидроксиметилфенил)метанол;
28. [4-({[6-этил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-ил]метиламино}метил)-2-гидроксиметилфенил]метанол;
29. [4-({[N-этил-[6-этил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-ил]амино}метил)-2-гидроксиметилфенил]метанол;
30. [4-({[6-этил-2'-пропил-4'-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)бифенил-3-ил]-N-пропиламино}метил)-2-гидроксиметилфенил]метанол;
31. (4-{[4'-(1-этил-1-гидроксипропил)-6,2'-диметилбифенил-3-иламино]метил}-2-гидроксиметилфенил)метанол.
Согласно настоящему изобретению наиболее предпочтительными соединениями формулы (I) являются соединения, для которых выполняется по меньшей мере одно, предпочтительно, все условия, следующие ниже:
(i) -X-Y- обозначает -CH2-CH2-;
(ii) R1 представляет собой этил;
(iii) R2 представляет собой пропил;
(iv) R3 представляет собой этил.
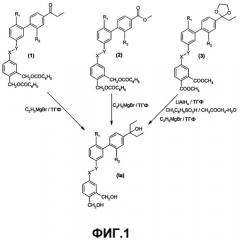
Предметом настоящего изобретения являются также способы получения соединений формулы (I) согласно схемам реакции, представленным на фиг.1.
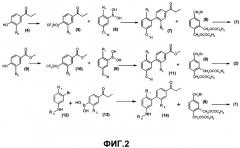
Когда -X-Y- представляет собой связь структуры -CH2-O- или -CH2-N(R4)-, соединения формулы (Ia) получают, предпочтительно, исходя из соединений (1) и (2), полученных согласно схемам реакции фиг.2.
Соединения (1) (в случае, когда Y = O) и (2) могут быть получены, соответственно, исходя из соединений (4) и (9), сначала получением производных трифторметансульфоната (соответственно (5) и (10)) в присутствии трифторметансульфонового ангидрида и основания, такого как триэтиламин, в дихлорметане. Затем реакцией сочетания типа Сузуки (Suzuki) с производными бороновой кислоты (6) в присутствии катализатора, такого как тетракис(трифенилфосфин)палладий(0), получают, соответственно, производные (7) и (11), и затем реакцией сочетания с бромпроизводными (8) в присутствии карбоната калия в метилэтилкетоне. В случае, когда Y=NR4, соединение (1) может быть получено, исходя из соединения (12), сначала реакцией сочетания типа Сузуки с производным бороновой кислоты (13) в присутствии катализатора, такого как тетракис(трифенилфосфин)палладий(0), получают производное (14) и затем реакцией сочетания с бромпроизводными (8) в присутствии гидрида натрия в диметилформамиде.
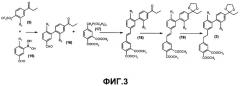
Когда -X-Y- представляет собой связь структуры -CH2-CH2-, соединения формулы (1а), представленные на фиг.1, получают, исходя из соединений (3), полученных согласно схеме реакции, представленной на фиг.3.
Реакцией типа Сузуки производных трифторметансульфоната (5) с производными бороновой кислоты (15) в присутствии катализатора, такого как тетракис(трифенилфосфин)палладий(0), и основания, такого как карбонат калия, в растворителе, таком как 1,2-диметоксиэтан, получают соединения (16). Эти последние превращают в соединения (18) реакцией типа Хорнера-Эммонса (Horner-Emmons) c соединением (17), затем в соединения (19) защитой кетоновой группы в форме диоксолана (этиленгликоль, п-толуолсульфокислота, толуол). Восстановлением двойной связи в присутствии палладия на угле в растворителе, таком как метанол, получают соединения (3).
Соединение (6) может быть получено согласно схеме реакции фиг.4.
Соединения (8) и (17) могут быть получены согласно схеме реакции фиг.5.
Соединения (12) и (13) могут быть получены согласно схеме реакции фиг.6.
Соединение (15) может быть получено согласно схеме реакции фиг.7.
Когда R3 представляет собой трифторметил, соединение (1) может быть получено, исходя из соответствующего бромсодержащего производного, образованием магнийсодержащего или литийсодержащего производного, затем реакцией с гексафторацетоном.
Соединения согласно изобретению обладают биологическими свойствами, аналогичными свойствам витамина D, в частности свойствами трансактивацииэлементов, отвечающих витамину D (ЭОВD) (VDRE),такими как агонистическая или антагонистическая активность по отношению к рецепторам витамина D или его производным. Под витамином D или его производными подразумевают, например, производные витамина D2 или D3 и, в частности, 1,25-дигидроксивитамин-D3 (кальцитриол).
Упомянутая агонистическая активность по отношению к рецепторам витамина D или его производных может быть выявлена "in vitro" методами, признанными в областиизучения генной транскрипции (Hansen et al., The Society For Investigative Dermatologie, vol.1, № 1, April 1996).
Биологические свойства, аналогичные свойствам витамина D, могут быть также измерены способностью продукта индуцировать дифференциацию промиелоцитарных клеток лейкемии HL60. Протокол, а также результаты, полученные с соединениями согласно изобретению, описаны в примере 8 настоящей заявки.
В качестве примера, агонистическая активностьPBD (VDR) может быть исследована на клеточной линии HeLa сотрансфекцией вектора экспрессиирецептора PBD(VDR) человека и информационной плазмиды р240Hase-CAT. Агонистическая активностьможет быть также охарактеризована в упомянутой системе сотрансфекцииопределением дозы, необходимой для достижения 50% от максимальной активности продукта (АК50) (АС50). Детали протокола данного теста, а также результаты, полученные с соединениями согласно изобретению, описаны в примере 9 настоящей заявки.
Биологические свойства, аналогичные свойствам витамина D, могут быть также измереныспособностью продукта ингибировать пролиферацию нормальных человеческих кератиноцитов (НЧК в культуре) (KHN). Продукт добавляют к НЧК, культивируемым в условиях, благоприятствующих пролиферативному состоянию.Продукт оставляют в контакте с клетками в течение пяти дней. Число пролиферативныхклеток измеряют при помощи включениябромдезоксиуридина (БДУ) (BRdU) в ДНК. Протокол данного испытания, а также результаты, полученные с соединениями согласно изобретению, описаны в примере 10 настоящей заявки.
Предметом настоящего изобретения являются также соединения, описанные выше, в качестве лекарства.
Соединения согласно изобретению особенно хорошо подходят для лечения в следующих областях:
1) для лечения дерматологических заболеваний, связанных с нарушением дифференциации или пролиферации кератиноцитов или себоцитов, в частности для лечения юношеских, обыкновенных, полиморфных, розовых угрей, узелково-кистозных, шаровидных угрей, старческих угрей, вторичных угрей, таких как солнечные, медикаментозные или профессиональные угри;
2) для лечения нарушений кератинизации, в частности ихтиозов, ихтиозоподобных состояний, болезни Дарье (Darier), ладонно-подошвенных кератодермий, лейкоплакий и лейкоплакиоподобных состояний, кожного лишая или лишая слизистой оболочки (слизистой оболочки рта);
3) для лечения других дерматологических заболеваний, связанных с нарушением кератинизации с воспалительным и/или иммуноаллергическим компонентом, в частности всех форм псориаза, будь то псориаз кожи, слизистой оболочки или ногтей, и даже псориатического ревматизма, а также кожной атопии, такой как экзема или респираторная атопия или десневая гипертрофия;
4) для лечения некоторых воспалительных заболеваний, не являющихся нарушением кератинизации, таких как атопическая экзема и контактные аллергии;
5) для лечения любых кожных или эпидермических пролифераций, доброкачественных или злокачественных, невирусной природы или вирусной природы, такими как обыкновенные простые бородавки, плоские бородавки и эпидермодисплазия, напоминающая бородавку, оральные или кровоточащие папилломатозы, и пролифераций, которые могут быть вызваны ультрафиолетовым излучением, в частности, в случае базалиомы и спиноцеллюлярной эпителиомы.
6) для лечения других дерматологических нарушений, таких как пузырчатые дерматозы и коллагенозы;
7) для профилактики и лечения симптомов старения кожи, фотоиндуцированного или возрастного, или для уменьшения пигментаций и кератозов, возникающих под действием света, или любых кожных патологий, связанных с возрастным или фотоиндуцированным старением;
8) для профилактики или лечения нарушений заживления или профилактики или лечения рубцов;
9) для борьбы против нарушений жировой функции, таких как угревая гиперсеборея или простая себорея или себорейная экзема;
10) для лечения некоторых офтальмологических заболеваний, в частности корнеопатий;
11) в терапии или профилактике раковых или предраковых состояний раков, представляющих, или которые могут быть спровоцированы таким образом, чтобы они представляли рецепторы витамина D, такие как, но без ограничения, рак почки, лейкемия, миелодисплакийные синдромы и лимфомы, карциномы мальпигиевых клеток эпителия и желудочно-кишечных раков, меланомы и остеосаркомы;
12) в терапии воспалительных заболеваний, таких как артрит или ревматоидный полиартрит;
13) в терапии любых заболеваний вирусной природы на кожном или общем уровне;
14) в терапии или профилактике облысения различной природы, в частности облысения, возникшего в результате химиотерапии или воздействия излучений;
15) в терапии дерматологических или общих заболеваний с иммунологическим компонентом;
16) в терапии заболеваний, относящихся к иммунитету, таких как аутоиммунные болезни (как, но без ограничения, сахарный диабет типа 1, рассеянный склероз, волчанка и заболевания типа волчанки, астма, гломерулонефрит и.т.д.), селективные дисфункции иммунной системы (например, СПИД) и предупреждение иммунного отторжения [как отторжения трансплантатов (например, почки, сердца, костного мозга, печени, панкреатических островков или целой поджелудочной железы, кожи, и т.д.) или профилактика болезни "трансплантат против хозяина";
17) в терапии эндокринных заболеваний, так как дано, что аналоги витамина D могут осуществлять модуляцию гормональной секреции, такую как увеличение секреции инсулина или селективное подавление секреции паратиреоидного гормона (например, при хронической почечной недостаточности и вторичном гиперпаратиреозе);
18) в терапии заболеваний, характеризующихся ненормальным управлением внутриклеточного кальция, и
19) в терапии или в профилактике недостатков витамина D и других нарушений гомеостаза неорганических веществ в плазме и костях, таких как рахит, остеомаляция, остеопороз, в частности, в случае женщин в периоде менопаузы, почечная остеодистрофия, нарушения функции паращитовидной железы.
Предметом настоящего изобретения является также фармацевтическая композиция, содержащая по меньшей мере одно соединение, такое как определенное выше, в фармацевтически приемлемом носителе.
Введение соединений согласно изобретению может быть осуществлено тонкокишечным, парентеральным, местным или глазным путем.
При тонкокишечном пути фармацевтические композиции могут находиться в форме таблеток, желатиновых капсул, драже, сиропов, суспензий, растворов, порошков, гранул, эмульсий, суспензий микросферических или наносферических частиц, или липидных или полимерных везикул, дающих возможность контролируемого высвобождения.
При парентеральном пути композиции могут находиться в форме растворов или суспензий для перфузии или для инъекций.
Соединения согласно изобретению прописывают обычно в дневной дозе, приблизительно, от 0,001 мкг/кг до 1000 мкг/кг, предпочтительно, приблизительно от 0,01 мкг/кг до 100 мкг/кг массы тела за 1-3 приема.
При местном пути фармацевтические композиции на основе соединений согласно изобретению предназначены для лечения кожи, кожи волосистой части головы и слизистых оболочек и находятся в форме мазей, кремов, молочка, помад, пудр, пропитанных тампонов, растворов, гелей, аэрозолей, лосьоновили суспензий. Равным образом, они могут находиться в форме суспензий микросферических или наносферических частиц, или липидных или полимерных везикул, или полимерных пластырей и гидрогелей, дающих возможность контролируемого высвобождения. Данные композиции для местного введения могут находиться либо в безводной форме, либо в водной форме сообразно клиническим показаниям.
При введении глазным путем они представляют собой, главным образом, примочки для глаз.
Упомянутые композиции, предназначенные для введения местным или глазным путем, содержат, по меньшей мере, одно соединение согласно изобретению в концентрации, находящейся в интервале, предпочтительно, от 0,0001% до 5%, предпочтительно, от 0,001% до 1% по отношению к общей массе композиции.
Соединения согласно изобретению находят также применение в области косметики, в частности, в гигиене тела и волос, и, в частности, для ухода за кожами, склонными к образованию угрей, для восстановления роста волос, или для замедления их выпадения, для борьбы с жирным внешним видом кожи или волос, для защиты от пагубных воздействий солнца или при уходе засухой кожей, для профилактики и/или лечения фотоиндуцированного или возрастного старения кожи.
Следовательно, настоящее изобретение нацелено также на косметическую композицию, содержащую в косметически приемлемом носителе, по меньшей мере, одно соединение, такое как определенное выше.
Упомянутая косметическая композиция может находиться, в частности, в форме крема, молочка, лосьона, геля, суспензии микросферических или наносферических частиц, или липидных или полимерных везикул, мыла или шампуня.
Концентрация соединений общей формулы (I) в косметической композиции согласно изобретению может находиться в интервале от 0,001 до 3 мас.% по отношению к общей массе композиции.
В фармацевтической и косметической областях соединения согласно изобретению могут быть предпочтительно применены в сочетании с инертными, или даже фармакодинамически или косметически активными добавками, или с комбинациями упомянутых добавок, в частности, такими как:
- смягчающие добавки;
- добавки, улучшающие вкус;
- консерванты, такие как сложные эфиры п-гидроксибензойной кислоты;
- стабилизаторы;
- добавки, регулирующие влажность;
- добавки, регулирующие рН;
- добавки, модифицирующие осмотическое давление;
- эмульгаторы;
- УФ-А и УФ-В фильтры;
-антиоксиданты, такие как α-токоферол, бутилгидроксианизол, бутилгидрокситолуол, супероксиддисмутаза, убихинол или некоторые вещества, образующие внутрикомплексные соединения с металлами;
- депигментирующие добавки, такие как гидрохинон, азелаиновая, кофейная или койевая кислоты;
- смягчающие добавки;
- увлажняющие добавки, такие как глицерин, ПЭГ 400, тиаморфолинон и его производные или карбамид;
- противосеборейные или противоугревые добавки, такие как S-карбоксиметилцистеин, S-бензилцистеамин, их соли и их производные, или пероксид бензоила;
- антибиотики, такие как эритромицин и его сложные эфиры, неомицин, клиндамицин и его сложные эфиры, тетрациклины;
- противогрибковые добавки, такие как кетоконазол или полиметилен-4,5-изотиазолиноны-3;
- добавки, способствующие восстановлению роста волос, такие как миноксидил (Minoxidil) (2,4-диамино-6-пиперидинопиримидин-3-оксид) и его производные, диазоксид (Diazoxide) (7-хлор-3-метил-1,2,4-бензотиадиазин-1,1-диоксид) и фенитоин (Phenytoin) (5,4-дифенилимидазолидин-2,4-дион);
- нестероидные противовоспалительные компоненты;
- каротиноиды, в частности β-каротин;
- антипсориатические компоненты, такие как антралин и его производные;
- эйкоза-5,8,11,14-тетраиновая и эйкоза-5,8,11-триноиновая кислоты, их сложные эфиры и амиды;
- ретиноиды, то есть лиганды рецепторов RAR или RXR,природные или синтетические;
- кортикостероиды или эстрогены;
- α-гидроксикислоты и α-кетокислоты или их производные, такие как молочная, яблочная, лимонная, гликолевая, миндальная, винная, глицериновая, аскорбиновая кислоты, а также их соли, амиды или сложные эфиры, или β-гидроксикислоты или их производные, такие как салициловая кислота, а также их соли, амиды или сложные эфиры;
- блокаторы ионных каналов, таких как калиевые каналы;
- или, более конкретно, для фармацевтических композиций, в сочетании с известными лекарствами для воздействия на иммунную систему (например, циклоспорин, FK 506, глюкокортикоиды, моноклональные антитела, цитокины или факторы роста...).
Разумеется, специалист будет выбирать возможное соединение или возможные соединения для добавления в упомянутые композиции таким образом, чтобы полезные свойства соединений настоящего изобретения не были бы, или существенным образом не были изменены предполагаемым добавлением.
Теперь, для иллюстрации и без какого-либо ограничительного характера, будут даны примеры получения активных соединений общей формулы (I) согласно изобретению, а также различные конкретные рецепты на основе таких соединений и тесты для оценки биологической активности соединений согласно изобретению.
ПРИМЕР 1: {5-[4'-(1-этил-1-гидроксипропил)-6-метил-2'-пропилбифенил-3-илоксиметил]-2-гидроксиметилфенил}метанол
(а) 1-(4-гидрокси-3-пропилфенил)пропан-1-он
В колбу в токе азота вводят 7,1 г (53 ммоль) хлорида алюминия в 70 мл нитробензола. Смесь нагревают при 70°С до полного растворения. Затем смесь охлаждают до 0°С и добавляют 7,2 мл (52 ммоль) 2-пропилфенола. Дают смеси вернуться к температуре окружающей среды, затем нагревают ее до 40°С. Затем по каплям добавляют 4,6 мл (52 ммоль) пропионилхлорида. Реакционную среду нагревают при 40°С в течение 2 часов, затем перемешивают 48 часов при температуре окружающей среды. Затем среду выливают в склянку с 20 мл концентрированной соляной кислоты. После экстракции простым этиловым эфиром органическую фазу промывают 2 н. гидроксидом натрия. Водные фазы подкисляют соляной кислотой и экстрагируют простым эфиром. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Полученное черное твердое вещество растирают в гептане, фильтруют и сушат. Получают 3,5 г (35%) целевого продукта в форме черного порошка.
(b) 4-пропионил-2-пропилфенил-1,1,1-трифторметансульфонат
В колбу в токе азота вводят 3,4 г (18 ммоль) 1-(4-гидрокси-3-пропилфенил)пропан-1-она в 100 мл дихлорметана. Реакционную среду охлаждают до 0°С, затем добавляют 3,3 мл (23 ммоль) триэтиламина. Через 15 минут добавляют 4,3 мл (26 ммоль) трифторметансульфонового ангидрида. Через 1 час среду выливают в насыщенный водный раствор хлорида аммония и экстрагируют дихлорметаном. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Полученный остаток очищают хроматографией на колонке с диоксидом кремния, элюируемой смесью гептана и этилацетата (70/30). После выпаривания растворителей получают 5,4 г (93%) целевого продукта в форме масла каштанового цвета.
(с) 3-бром-4-метилфениламин
В колбу в токе азота вводят 30 г (139 ммоль) 2-бром-4-нитротолуола в 180 мл воды, 400 мл этанола и 110 мл уксусной кислоты. Среду нагревают до 70°С и добавляют маленькими порциями 31 г (556 ммоль) железа. Греют в колбе с обратным холодильником в течение 2 часов, затем, после охлаждения, медленно добавляют 180 мл 34%-ного гидроксида аммония. Смесь фильтруют через целит и органическую фазу экстрагируют водой и этилацетатом. Затем ее сушат над сульфатом магния, фильтруют, затем упаривают. Получают 25,5 г (100%) целевого продукта в форме масла каштанового цвета.
(d) 3-бром-4-метилфенол
В колбу вводят 25 г (134 ммоль) 2-бром-4-аминотолуола в 400 мл 1 М серной кислоты, затем смесь охлаждают до 0°С. Затем к 13 г (190 ммоль) нитрита натрия, растворенным в 30 мл воды, добавляют 21 мл концентрированной серной кислоты. Смесь нагревают в колбе с обратным холодильником в течение 4 часов. Затем ее экстрагируют простым этиловым эфиром. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Полученный остаток очищают хроматографией на колонке с диоксидом кремния, элюируемой смесью гептана и этилацетата (90/10), и получают 12,1 г (48%) целевого продукта в форме масла каштанового цвета.
(e) 2-бром-4-этоксиметокси-1-метилбензол
В колбу в токе азота вводят 12,1 г (65 ммоль) 3-бром-4-метилфенола в 100 мл сухого диметилформамида. При 0°С медленно добавляют 3,1 г (78 ммоль) 60%-ного гидрида натрия. Через 1 час по каплям добавляют 7,3 мл (78 ммоль) метоксиэтилхлорида. Смесь перемешивают при температуре окружающей среды в течение ночи. Затем смесь выливают в воду и экстрагируют этилацетатом. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Полученный остаток очищают хроматографией на колонке с диоксидом кремния, элюируемой смесью гептана и этилацетата (85/15), и получают 13,2 г (83%) целевого продукта в форме масла.
(f) 5-этоксиметокси-2-метилфенилбороновая кислота
В колбу в токе азота вводят 1,4 г (59 ммоль) магниевых опилок в тетрагидрофуране. Медленно добавляют 13,2 г (54 ммоль) 2-бром-4-этоксиметокси-1-метилбензола, разбавленных в небольшом количестве ТГФ. Среду кипятят с обратным холодильником в течение 20 минут. Затем в нее при помощи стеклянного наконечника добавляют 15 мл (65 ммоль) триизопропилбората. Смесь возрастает по массе и затем ее выливают в раствор 1 н. соляной кислоты и экстрагируют простым эфиром. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Получают 9,8 г (87%) целевого продукта в форме масла каштанового цвета.
(g) 1-(5'-этоксиметокси-2'-метил-2-пропилбифенил-4-ил)пропан-1-он
В колбе в токе азота в 50 мл 1,2-диметоксиэтана растворяют 1,56 г (7,4 ммоль) 5-этоксиметокси-2-метилфенилбороновой кислоты, 2 г (6,2 ммоль) 4-пропионил-2-пропилфенил-1,1,1-трифторметансульфоната, 517 мг (12 ммоль) хлорида лития и 7,4 мл раствора 2 М карбоната калия. Смесь кипятят в колбе с обратным холодильником в течение 10 часов. Затем ее выливают в воду и экстрагируют этилацетатом. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Получают масло каштанового цвета, которое используют для продолжения синтеза таким, как оно получено.
(h) 1-(5'-гидрокси-2'-метил-2-пропилбифенил-4-ил)пропан-1-он. CS 755.064
В метаноле растворяют 1-(5'-этоксиметокси-2'-метил-2-пропилбифенил-4-ил)пропан-1-он, полученный на стадии (g), и добавляют несколько капель серной кислоты. Перемешивание поддерживают всю ночь, затем среду экстрагируют этилацетатом и водой. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Полученный остаток очищают хроматографией на колонке с диоксидом кремния, элюируемой смесью гептана и этилацетата (75/25), и получают 1,53 г (88%) целевого продукта в форме масла каштанового цвета.
(i) Диметил-4-гидроксиметилфталат
В колбу в токе азота вводят 50 г (260 ммоль) тримеллитового ангидрида в 500 мл диоксана. По каплям добавляют 520 мл (520 ммоль) борана (1 М/ТГФ) и перемешивают 48 часов при температуре окружающей среды. Затем реакционную среду медленно выливают в насыщенный водный раствор хлорида аммония и экстрагируют дихлорметаном. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Остаток растворяют в 400 мл метанола и добавляют 5 мл серной кислоты. Нагревают при 80°С в течение ночи. Метанол выпаривают, и осадок извлекают в этилацетат и промывают водой. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Получают 52,7 г (90%) целевого продукта в форме масла желтого цвета.
(j) Диметил-4-(трет-бутилдиметилсиланилоксиметил)фталат
В колбу в токе азота вводят 19 г (84,8 ммоль) диметил-4-гидроксиметилфталата в 250 мл диметилформамида. Добавляют 14 г (93 ммоль) трет-бутилдиметилсиланхлорида и 8 г (118 ммоль) имидазола. Реакционную среду перемешивают 3 часа при температуре окружающей среды, затем ее концентрируют, остаток растворяют в простом эфире, затем фильтруют. Фильтрат выпаривают и продукт очищают хроматографией на колонке с диоксидом кремния, элюируемой смесью гептана и этилацетата (50/50), и получают 23,7 г (83%) целевого продукта в форме масла желтого цвета.
(k) [4-(трет-бутилдиметилсиланилоксиметил)-2-гидроксиметилфенил]метанол
В колбу в токе азота вводят 17,8 г (469 ммоль) литийалюминийгидрида в 800 мл простого этилового эфира. При 0°С по каплям добавляют раствор 66,4 г (196 ммоль) диметил-4-(трет-бутилдиметилсиланилоксиметил)фталата в 200 мл простого эфира и 100 мл ТГФ. Реакционную среду перемешивают при 0°С в течение 2 часов. Очень медленно добавляют 18 мл воды, 18 мл 15%-ного раствора гидроксида натрия, затем 54 мл воды. Образовавшийся осадок фильтруют, промывают простым эфиром и фильтрат выпаривают. Получают 52 г (94%) целевого продукта в форме бесцветного масла.
(l) 2-бензоилоксиметил-4-(трет-бутилдиметилсиланилоксиметил)бензилбензоат
В колбу в токе азота вводят 40 г (141 ммоль) [4-(трет-бутилдиметилсиланилоксиметил)-2-гидроксиметилфенил]метанола в 400 мл ТГФ. При 0°С добавляют 49 мл (352 ммоль) триэтиламина, затем по каплям 34,5 мл (297 ммоль) бензоилхлорида. Реакционная среда образует осадок, и затем добавляют 350 мг (2,8 ммоль) диметиламинопиридина. Дают среде вернуться к температуре окружающей среды в течение ночи. Среду фильтруют и твердое вещество промывают этилацетатом. Фильтрат выпаривают и остаток извлекают дихлорметаном. Органическую фазу промывают насыщенным водным раствором хлорида аммония, затем водой. Затем ее сушат над сульфатом магния, фильтруют и упаривают. Получают 69,5 г (100%) целевого продукта в форме оранжевого масла.
(m) 2-бензоилоксиметил-4-гидроксиметил)бензилбензоат
В колбу в токе азота вводят 69 г (140 ммоль) 2-бензоилоксиметил-4-(трет-бутилдиметилсиланилоксиметил)бензилбензоата в 450 мл этилацетата. Добавляют 178 мл тетрабутиламмонийфторида (1 М/ТГФ). Среду перемешивают 30 минут при температуре окружающей среды. Затем ее выливают в насыщенный водный раствор хлорида аммония и экстрагируют этилацетатом. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Остаток очищают хроматографией на колонке с диоксидом кремния, элюируемой смесью гептана и этилацетата (40/60), и получают 46,6 г (88%) целевого продукта в форме белого порошка с температурой плавления 92°С.
(n) (3,4-бис-бензоилоксиметил)бензилбромид
В колбу в токе азота вводят 40 г (106 ммоль) 2-бензоилоксиметил-4-гидроксиметил)бензилбензоата в 500 мл дихлорметана и 77,6 г (234 ммоль) тетрабромметана. При 0°С по каплям добавляют раствор 61,3 г (233 ммоль) трифенилфосфина в 200 мл дихлорметана. Дают вернуться к температуре окружающей среды в течение 2 часов. Реакционную среду выливают в воду и экстрагируют дихлорметаном. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Остаток очищают хроматографией на колонке с диоксидом кремния, элюируемой смесью гептана и этилацетата (70/30), и получают 32,6 г (70%) целевого продукта в форме белого порошка.
(o) 1-[5'-(3,4-бис-бензоилоксиметилбензилокси)-2'-метил-2-пропилбифенил-4-ил]-пропан-1-он
В колбу в токе азота вводят 1,5 г (5,4 ммоль) 1-(5'-гидрокси-2'-метил-2-пропилбифенил-4-ил)пропан-1-она, 2,5 г (5,7 ммоль) (3,4-бис-бензоилоксиметил)бензилбромида и 750 мг (5,4 ммоль) карбоната калия в 50 мл метилэтилкетона. Смесь кипятят с обратным холодильником всю ночь, затем, после охлаждения, фильтруют через целит. Фильтрат экстрагируют водой и этилацетатом. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Полученный остаток очищают хроматографией на колонке с диоксидом кремния, элюируемой смесью гептана и этилацетата (85/15), и получают 1,93 г (56%) целевого продукта в форме темно-желтого масла.
(p) 1-[5'-(3,4-бис-гидроксиметилбензилокси)-2'-метил-2-пропилбифенил-4-ил]-пропан-1-он
В колбе, в 40 мл 2%-ного метанольного раствора карбоната калия растворяют 1,9 г (3 ммоль) 1-[5'-(3,4-бис-бензоилоксиметилбензилокси)-2'-метил-2-пропилбифенил-4-ил]-пропан-1-она. Смесь перемешивают при температуре окружающей среды всю ночь. Затем ее выливают в воду и экстрагируют этилацетатом. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Полученный остаток очищают хроматографией на колонке с диоксидом кремния, элюируемой смесью гептана и этилацетата (70/30), и получают 890 мг (69%) целевого продукта.
(q) {5-[4'-(1-этил-1-гидроксипропил)-6-метил-2'-пропилбифенил-3-илоксиметил]-2-гидроксиметилфенил}метанол
В колбу в токе азота вводят 890 мг (2 ммоль) 1-[5'-(3,4-бис-гидроксиметилбензилокси)-2'-метил-2-пропилбифенил-4-ил]пропан-1-она в 40 мл сухого ТГФ. При 0°С по каплям добавляют 4,1 мл (12 ммоль) этилмагнийбромида. Реакционную среду перемешивают 1 час 30 минут при температуре окружающей среды, затем выливают в насыщенный водный раствор хлорида аммония и экстрагируют этилацетатом. Органическую фазу сушат над сульфатом магния, фильтруют, затем упаривают. Полученный остаток очищают хроматографией на колонке с диоксидом кремния, элюируемой смесью гептана и этилацетата (50/50), и получают 550 мг (64%) {5-[4'-(1-этил-1-гидроксипропил)-6-метил-2'-пропилбифенил-3-илоксиметил]-2-гидроксиметилфенил}метанола в форме белых кристаллов с температурой плавления 97°С.
ПРИМЕР 2: {5-[6,2'-диэтил-4'-(1-этил-1-гидроксипропил)бифенил-3-илоксиметил]-2-гидроксиметилфенил}метанол
(а) 4-бром-2-этилфенол
В колбу в токе азота вводят 5,57 г (45 ммоль) 2-этилфенола в 250 мл хлороформа. Добавляют небольшими порциями 43,4 г (90 ммоль) трибромида тетрабутиламмония. Среду перемешивают 1 час при температуре окружающей среды, затем ее гидролизуют насыщенным водным раствором тиосульфата натрия. Органическую фазу промывают водой, сушат над сульфатом магния, фильтруют и затем упаривают. Получают 9,1 г (100%) целевого продукта в форме масла желтого цвета.
(b) (4-бром-2-этилфенокси)-трет-бутилдиметилсилан
Способом, аналогичным примеру 1(j), исходя из 9,1 г (45 ммоль) 4-бром-2-этилфенола, получают, после хроматографической очистки на колонке с диоксидом кремния, элюируемой гептаном, 11,9 г (83%) целевого продукта в форме бесцветного масла.
(с) 1-[4-(трет-бутилдиметилсиланилокси)-3-этилфенил]пропан-1-ол
В колбу в токе азота вводят 11,9 г (38 ммоль) (4-бром-2-этилфенокси)-трет-бутилдиметилсилана в 200 мл ТГФ. Реакционную среду охлаждают до -78°С и по каплям добавляют 16,6 мл (41 ммоль) н-бутиллития (2,5 М/ТГФ)