Применение аннелированных соединений пиррола при лечении дегенерации суставного хряща или структурных изменений субхондральной кости
Иллюстрации
Показать всеИзобретение относится к медицине. Описано лечение или профилактика дегенерации или деструкции суставного хряща и/или субхондральной кости в поврежденном суставе млекопитающего, заключающееся во введении соединения формулы (I), где переменные имеют значения, данные в настоящем описании. Это лечение улучшает, усиливает эффект лечения, реверсирует или предотвращает любую дегенерацию или деструкции суставного хряща и/или субхондральной кости, являющуюся результатом ранней стадии указанной дегенерации. 4 н. и 6 з.п. ф-лы, 10 ил.
Реферат
Настоящее изобретение относится к применению у млекопитающих аннелированных соединений пиррола и, в частности, ML3000, их солей или производных, при лечении и профилактике повреждения хрящевой и/или субхондральной кости и разрушения воспаленных суставов у таких млекопитающих. Такое повреждение хрящевой и/или субхондральной кости является естественным следствием процесса остеопороза и его последствий, когда он происходит у млекопитающего. Возможность достижения такого неожиданного эффекта названа «хондрозащитой».
Предпосылки изобретения
Нестероидные противовосполительные средства (NSAID), такие как ацетилсалициловая кислота (ASA), диклофенак, индометацин, ибупрофен и напроксен, широко используются в клинической медицине. С фармакологической точки зрения, они действуют как ингибиторы циклооксигеназы (COX).
Пирролизины, которые обладают сходным фармакологическим действием, известны из многих публикаций. Например, противовоспалительные активные пирролизины описаны в Arch. Pharm. 319, 65-69 (1986); 319, 231-234 (1986); 318, 661-663 (1985); 318, 663-664 (1985); 319, 500-505 (1986); 319, 749-755 (1986); 327, 509-514 (1994); 330, 307-312 (1997), а также в J. Med. Chem. 1987, 30, 820-823 и 1994, 37, 1894-1897.
Также можно указать пирролизины, описанные в US 5260451 (соответствует EP 0397175), а также в WO 95/32970; WO 95/32971; и WO 95/32972. Эти соединения представлены структурной формулой
и содержат аннелированную диарилпиррольную группу, а также кислотный остаток R3 в качестве третьего заместителя. Эти соединения характеризуются высокой липофильностью, хорошей биодоступностью и средним уровнем продолжительности периода полувыведения, см. Drugs of the Future, 1995, 20 (10):1007-1009.
Кроме того, пирролизины подобного строения описаны в DE 19845446.6 и WO 01/05792. Более того, утверждается, что пирролизины, замещенные алкилсульфинилбензоилом и алкилсульфонилбензоилом, в соответствии с US 4232038, обладают противовоспалительными, аналгетическими и жаропонижающими свойствами. В соответствии с DE 19624290.8 и DE 19624289.4, некоторые соединения этого типа понижают уровень липидов.
ML3000 ([2,2-диметил-6-(4-хлорфенил)-7-фенил-2,3-дигидро-1H-пирролизин-5-ил]уксусная кислота) формулы (Ia)
не обладая антиоксидантной активностью, является двойным сбалансированным ингибитором COX и 5-липоксигеназ (5-LO) (3). Препарат является неселективным ингибитором COX, ингибируя как COX-1, так и COX-2. Он обладает аналгетической, жаропонижающей и противовоспалительной активностью и, как было показано, оказывает сильный противовоспалительный эффект в большом количестве моделей на животных, включая отек конечности, вызванный каррагенаном, у крыс и адъювантный артрит крыс (4).
Остеоартрит (OA) является самым распространенным заболеванием среди болезней опорно-двигательного аппарата. В основном это заболевание поражает истинные суставы (диартрозы) несущих нагрузку конечностей, такие как тазобедренные и коленные суставы, а также поражает другие суставы, такие как межфаланговые суставы и суставы позвоночника. Структурные изменения при данном заболевании включают в себя прогрессирующее разрушение суставного хряща, образование остеофитов и, на клинической стадии заболевания, различную степень синовиального воспаления. С этими изменениями также связана значительная перестройка субхондральной кости, которая, по некоторым данным, вероятно, связана с чрезмерной резорбцией кости на ранних стадиях заболевания, с последующим чрезмерным костеобразованием, приводящим к склерозу кости и утолщению субхондральной кости.
Эти механизмы, приводящие к развитию и прогрессированию структурных изменений, наблюдаемых при остеоартрите (OA), включают в себя много факторов и являются многообразными и в большенстве своем остаются непонятными. Они вовлекают не только хрящ, в котором наблюдается большое число морфологических изменений, но также и синовиальную мембрану, которая является участком воспалительной реакции различной степени и тяжести (1). Вероятно, существует множество путей, ответственных за катаболизм матрикса хряща, включая повышение регуляции растворимых факторов, таких как интерлейкин-1 (IL-1), фактор некроза опухолей-α (TNF-α) и простагландины, которые могут индуцировать разрушение суставного хряща. Непосредственное повреждение хрондроцитов также стимулирует активность металлопротеазы матрикса (MMP), например, коллагеназ, стромелизинов и желатиназ, и продукцию различных медиаторов воспаления (2).
Предполагают, что метаболические процессы, постоянно протекающие в любом указанном выше суставе и необходимые для его восстановления и последующего нормального состояния, подвергают повреждению, такому как травматическое повреждение.
Следовательно, для того, чтобы соединение было приемлемым хондрозащитным агентом, оно, прежде всего, должно поддерживать такую метаболическую активность хондроцитов, то есть не ингибировать или не влиять на клеточное деление и биосинтез компонентов матрикса, которые является частью восстановительного процесса. В этом отношении, специалисту в данной области будет понятно, что большое количество NSAID обладают выраженной ингибиторной активностью в отношении биосинтеза главных компонентов внеклеточного матрикса.
В то же время, приемлемый хондрозащитный агент должен препятствовать деградирующей активности медиаторов, таких как различные цитокины, простагландины и протеиназы, в отношении хряща. Поэтому, что понятно специалисту в данной области, возможные хондрозащитные препараты следует оценивать как с точки зрения положительных эффектов в отношении анаболических путей, так и по их способности ингибировать катаболические процессы. Катаболические события, которые обычно рассматриваются, среди прочего, включают в себя высвобождение и ингибирование ферментов, деградирующих матрикс, действие на биосинтез простагландинов и лейкотриенов и способность препарата ингибировать IL-1, вызывающий деградацию суставного хряща.
Многие годы использовали ряд препаратов, таких как NSAID, активность которых была непосредственно связана с ингибированием ферментов COX. Хотя они способны эффективно снижать симптомы остеоартрита, такие как боль, они имеют ограниченную способность к снижению прогрессирования OA в экспериментах in vivo (8,9). При лечении тенидапом и царпрофеном - оба препарата являются NSAID с ингибиторной активностью в отношении как циклооксигеназы-1 (COX-1), так и COX-2, - эти препараты показали анти-OA действие (8,9), тогда как другие NSAID, такие как диклофенак или ASA, были неэффективны (10) или даже усиливали повреждение хряща в экспериментах на модели OA у собак (11). Аналогично, на людях последние исследования на основании критериев рентгенологического анализа пациентов, страдающих OA коленного сустава, показали, что, при лечении тиапрофеновой кислотой, другим представителем NSAID, в течение периода свыше 5 лет прогрессия повреждения хряща может не уменьшаться, а при лечении индометацином эта прогрессия может даже усиливаться (15).
Неожиданно были обнаружено, что некоторые аннелированные производные пиррола, такие как ML3000, значительно снижают развитие поражений экспериментального OA у собак. Защитный эффект этих соединений, в частности, был особенно очевиден в снижении развития поражений хряща. Этот феномен связывали не только со значительным ингибированием продукции как PGE2, так и LTB4, но также и со снижением in situ двух главных катаболических факторов, вовлеченных в деградацию хряща, а именно IL-1 и коллагеназы-1.
Краткое описание изобретения
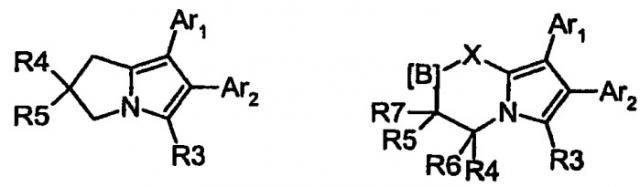
Таким образом, настоящее изобретение относится к применению аннелированных производных пиррола, представленных общей формулой (I):
где X представляет собой CR8R9, S, O, NR12 или C(O);
A представляет собой CR10R11 или связь между X и атомом, несущим радикалы R6 и R7;
первый из радикалов R1, R2, R3 представляет собой арил, необязательно замещенный одним или более заместителями, независимо выбранными из группы, включающей в себя галоген, алкил, галогеналкил, алкокси, арилокси, галогеналкокси, алкилтио, гидрокси, нитро, алкилсульфинил, алкилсульфонил, сульфамоил, N-алкилсульфамоил, N, N-ди-алкилсульфамоил, алкилсульфонамидо и алкилсульфон-N-алкиламидо; или ароматическую или неароматическую, моно- или бициклическую, необязательно бензоаннелированную, гетероциклическую группу с 1, 2 или 3 гетероатомами, независимо выбранными из N, O и S и, необязательно, замещенную одним или более одного заместителями, независимо выбранными из группы, включающей в себя галоген, алкил, галогеналкил, алкокси, арилокси, галогеналкокси, алкилтио, гидрокси, нитро, алкилсульфинил, алкилсульфонил, сульфамоил, N-алкилсульфамоил, N,N-ди-алкилсульфамоил, алкилсульфонамидо и алкилсульфон-N-алкиламидо;
второй из радикалов R1, R2, R3 представляет собой алкил, необязательно замещенный одним или более заместителями из группы, включающей в себя галоген, циклоалкил, алкокси, трифторметокси, гидрокси и трифторметил; циклоалкил, необязательно замещенный одним или более заместителями, независимо выбранными из группы, включающей в себя галоген, алкил, галогеналкил, циклоалкил, алкокси, галогеналкокси и гидрокси; арил, необязательно замещенный одним или более заместителями, независимо выбранными из группы, включающей в себя галоген, алкил, галогеналкил, алкокси, арилокси, галогеналкокси, алкилтио, гидрокси, нитро, алкилсульфинил, алкилсульфонил, сульфамоил, N-алкилсульфамоил, N,N-ди-алкилсульфамоил, алкилсульфонамидо и алкилсульфон-N-алкиламидо; или ароматическую или неароматическую, моно- или бициклическую, необязательно бензоаннелированную, гетероциклическую группу с 1, 2 или 3 гетероатомами, независимо выбранными из N, O и S, и необязательно замещенную одним или более заместителями, независимо выбранными из группы, включающей в себя галоген, алкил, галогеналкил, алкокси, арилокси, галогеналкокси, алкилтио, гидрокси, нитро, алкилсульфинил, алкилсульфонил, сульфамоил, N-алкилсульфамоил, N,N-ди-алкилсульфамоил, алкилсульфонамидо и алкилсульфон-N-алкиламидо;
третий из радикалов R1, R2, R3 представляеют собой H, алкил, галогеналкил, гидроксиалкил, -CHO, -COOH, галоген, циано, алкилсульфонил, сульфамоил или B-Y,
где
B представляет собой алкилен или алкенилен, необязательно замещенный гидрокси или алкокси;
Y представляет собой -COOH, SO3H, OPO(OH)2, OP(OH)2, -CHO или тетразолил; или
второй и третий радикалы из радикалов R1, R2, R3 представляют собой, вместе с атомом, к которому они присоединены, насыщенный или ненасыщенный циклоалкил;
R4-R11, которые могут быть одинаковыми или различными, представляют собой водород, алкил, гидроксиалкил, алкоксиалкил, гидрокси, COOH или ацилокси, где соседние радикалы могут также представлять связи или геминальные радикалы, вместе с атомом С, к которому они присоединены, могут также представлять собой карбонил или циклоалкил;
R12 представляет собой водород, алкил или фенил,
и к оптическим изомерам, физиологически приемлемым солям и производными, для лечения или профилактики дегенерации или деструкции суставного хряща и/или субхондральной кости.
Термин «алкил, алкокси и тому подобное» включает в себя линейные или разветвленные алкильные группу, такие как CH3, C2H5, н-пропил, CH(CH3)2, н-бутил, CH(CH3)-C2H5, изобутил, C(CH3)3, н-пентил или н-гексил, в частности, CH3, C2H5 или CH(CH3)2, предпочтительно содержащие, если не указано иного, от 1 до 8, в частности, от 1 до 6 и, более предпочтительно, от 1 до 4 атомов углерода; в качестве заместителей радикала R1-R12 «алкил, алкокси и тому подобное» предпочтительно содержат от 1 до 4 атомов углерода.
Замещенные «алкил, алкокси и тому подобное» включают в себя, в частности,
галогеналкил, то есть, алкил, который частично или полностью замещен фтором, хлором, бромом и/или йодом, например, CH2F, CHF2, CF3, CH2Cl, 2-фторэтил, 2-хлорэтил или 2,2,2-трифторэтил; в качестве заместителя радикала R1-R12 галогеналкил предпочтительно обозначает CHF2 и особенно CF3;
галогеналкокси, то есть алкокси, который частично или полностью замещен фтором, хлором, бромом и/или йодом, например, группы галогеналкокси соответствуют вышеуказанным группам галогеналкила; как заместитель радикала R1-R12 галогеналкокси предпочтительно обозначает OCHF2 и особенно OCF3;
алкоксиалкил, то есть, алкил, замещенный алкокси, например, -CH2-OCH3 или 2-метоксиэтил;
гидроксиалкил, то есть алкил, который предпочтительно монозамещен гидрокси, например, гидроксиметил или 2-гидроксиэтил;
трифторметилалкил, то есть алкил, который предпочтительно монозамещен трифторметилом, например, группы, описанные в отношении гидроксиалкила, которые замещены трифторметилом вместо гидрокси;
трифторметоксиалкил, то есть алкил, который предпочтительно монозамещен трифторметокси, например, группы, описанные в отношении гидроксиалкила, которые замещены трифторметокси вместо гидрокси;
циклоалкилалкил, то есть, алкил, который предпочтительно монозамещен циклоалкилом, например, группы, описанные в отношении гидроксиалкила, который замещен циклопропилом, циклобутилом, циклопентилом или циклогексилом вместо гидрокси.
Термин «циклоалкил» включает в себя моно- или бициклические алкильные группы, такие как циклопропил, циклобутил, циклопентил, циклогексил и тому подобное, предпочтительно содержащие, если не указано иного, от 3 до 9, в частности, от 3 до 7 и, более предпочтительно, от 5 до 6 атомов углерода.
Термин «алкилен» включает в себя линейные или разветвленные алкиленовые группы, такие как метилен и этилен, предпочтительно содержащие, если не указано иного, от 1 до 8, в частности, от 1 до 6 и, более предпочтительно, от 1 до 4 атомов углерода. Если алкилен замещен гидроксилом или алкокси, то предпочтительно, если он является монозамещенным.
Термин «алкенилен» включает в себя линейные или разветвленные, моно- или полиненасыщенные алкиленовые группы, такие как этенилен, предпочтительно содержащие, если не указано иного, от 2 до 8, в частности, от 2 до 6 и, более предпочтительно, от 2 до 4 атомов углерода. Если алкенилен замещен гидроксилом или алкокси, то предпочтительно, если он является монозамещенным.
Ацилокси означает -OCOR, где R представляет собой алкил или арил. Предпочтительными примерами являются ацетилокси и бензоилокси.
-СООАлкил означает алкоксикарбонил, такой как CO-OCH3, CO-OC2H5, CO-OCH2-C2H5, CO-OCH(CH3)2, н-бутоксикарбонил, CO-OCH(CH3)-C2H5, CO-OCH2-CH(CH3)2, CO-OC(CH3)3, в частности, CO-OCH3, CO-OC2H5, CO-OCH(CH3)2 или CO-OCH2-CH(CH3)2.
-СООАлкФенил означает алкоксикарбонильную группу, которая замещена на алкильной группе фенилом, такую как бензилоксикарбонил.
Алкилтио означает -S-Алкил и также относится к алкилсульфанилу или алкилмеркапто, такому как SCH3, SC2H5, SCH2-C2H5, SCH(CH3)2, н-бутилтио, 1-метилпропилтио, 2-метилпропилтио, SC(CH3)3. Метилтио является предпочтительным.
Алкилсульфинил означает -S(O)-Алкил и также относится к алкилсульфоксо, такому как SO-CH3, SO-C2H5, н-пропилсульфинил, 1-метилэтилсульфинил, н-бутилсульфинил, 1-метилпропилсульфинил, 2-метилпропилсульфинил, 1,1-диметилэтилсульфинил. Метилсульфинил является предпочтительным.
Алкилсульфонил означает -S(O)2-алкил и также относится к алкилсульфону, такому как SO2-CH3, SO2-C2H5, н-пропилсульфонил, SO2-CH(CH3)2, н-бутилсульфонил, 1-метилпропилсульфонил, 2-метилпропилсульфонил, SO2-C(CH3)3. Метилсульфонил является предпочтительным.
Сульфамоил означает -S(O)2NH2 и также относится к амидосульфонилу или амиду сульфоновой кислоты.
N-Алкилсульфамоил означает монозамещенный сульфамоил-S(O)2NH-алкил, например, -S(О)2NH-CH3.
N,N-Диалкилсульфамоил означает ди-замещенный сульфамоил-S(O)2N-(алкил)2, где N-присоединенные алкильные группы могут быть одинаковыми или различными, например, -S(O)2N(CH3)2.
Алкилсульфонамидо означает -NHS(O)2-алкил, такой как NHSO2-CH3, NHSO2-C2H5, н-пропилсульфонамидо, NHSO2-CH(CH3)2, н-бутилсульфонамидо, 1-метилпропилсульфонамидо, 2-метилпропилсульфонамидо, NHSO2-C(CH3)3. Метилсульфонамидо является предпочтительным.
Алкилсульфон-N-алкиламидо означает -N(алкил)S(O)2-алкил, где N- и S-присоединенные алкильные группы могут быть одинаковыми или различными, например, N(CH3)SO2-CH3.
Карбонил, CHO, -COOH, -SO3H обозначает >C=O, формил, карбокси, карбоксикарбонил и сульфо- соответственно.
«Арил» предпочтительно означает нафтил и, в частности, фенил.
Термин «галоген» включает в себя атом фтора, хлора, брома или йода. Обычно предпочтительными являются фтор и хлор, и в некоторых случаях также бром.
«Гетероциклические остатки» включают в себя, в частности, 5- или 6-членные гетероциклические остатки, которые могут быть ароматическими или неароматическими, моно- или бициклическими и/или бензоаннелированными. Примерами являются азотсодержащие гетероциклические остатки, такие как пирролил, имидазолил, пиразолил, пиридазинил, пиразинил, индолил, хинолинил, особенно пиридил, пиримидил и изохинолинил. Ароматические остатки также включают в себя гетероциклические остатки, которые содержат атом кислорода или серы, такие как тиенил, бензотиенил, фуранил и особенно бензофуранил. Они также включают в себя гетероциклические остатки, содержащие 2 или более чем 2 различных гетероатомов, такие как тиазолил, изотиазолил, тиадиазолил, изоксазолил и оксазолил. Тиенил, пиридил и тиазолил являются предпочтительными ароматическими гетероциклическими остатками. Неароматические остатки включают в себя азотсодержащие гетероциклические остатки, такие как пирролидинил, пиперидинил и пиперазинил. Они также включают в себя гетероциклические остатки, которые содержат 2 или более 2 различных гетероатомов, такие как морфолинил.
Замещенные остатки, в частности, алкил, циклоалкил, арил и гетероарил являются предпочтительно моно-, ди- или тризамещенными.
[α]-Аннелированные соединения могут быть 6- или, особенно, 5-членными, гетероциклическими или - в особенности - алициклическими соединениями, если алициклическими, то ненасыщенными или, особенно, насыщенными, и/или замещенными или незамещенными.
[α]-Аннелированные производные пиррола формулы (I) включают в себя, в частности, производные, где Х представляет собой CR8R9, и A представляет собой связь между X и атомом, несущим радикалы R6 и R7 (пирролизины); X представляет собой CR8R9, и A представляет собой CR10R11 (индолизины); X представляет собой NR12, и A представляет собой связь между X и атомом, несущим радикалы R6 и R7 (пирроло[1,2-a]имидазолы); X представляет собой S, и A представляет собой связь между X и атомом, несущим радикалы R6 и R7 (пирроло[2,1-b]тиазолы); X представляет собой S, и A представляет собой CR10R11 (пирроло[2,1-b]1,3-тиазины); X представляет собой O, и A представляет собой CR10R11 (пирроло[2,1-b]1,3-оксазины); X представляет собой O, и A представляет собой связь между X и атомом, несущим радикалы R6 и R7 (пирроло[2,1-b]оксазолы), не указанные остатки имеют значения, определяемые выше.
Если [α]-аннелированное производное является 5-членным ненасыщенным остатком, то главным образом R4 и R6 представляют собой связь, так, например, как в пирролизине, пирроло[2,1-b]имидазоле и пирроло[2,1-b]тиазоле. Если [α]-аннелированное соединение является 6-членным ненасыщенным остатком, то главным образом R4 и R6, так, например, как в пирроло[2,1-b]1,3-тиазине, пирроло[2,1-b]-1,3-оксазине или 5,6-дигидроиндолизине, и, необязательно, также R8 и R10, так, например, как в индолизине, представляют собой связь.
Не ограничиваясь конкретным [α]-аннелированным производным по конкретному воплощению данного изобретения, R4-R7, которые могут быть одинаковыми или различными, представляют собой водород или алкил. В соответствии еще с одним из конкретных воплощений данного изобретения, по крайней мере одни из радикалов R4, R5, R6 и R7 представляет собой гидроксиалкил, в частности, гидроксиметил и оставшиеся радикалы из числа R4, R5, R6 и R7 независимо представляют собой H или алкил. В соответствии с этим воплощением, предпочтительно, чтобы R4 представлял собой гидроксиалкил, в частности, гидроксиметил, и R5 представлял бы собой H или алкил, а R6, R7 независимо представляли бы собой H или алкил. В соответствии еще с одним конкретным воплощением данного изобретения, один из радикалов R8 и R9 представляет собой H, алкил, гидроксиалкил или алкоксиалкил, а другой представляет собой гидроксил, алкокси, карбоксил или ацилокси, или R8 и R9, вместе с атомом C, к которому они присоединены, представляют собой карбонильную группу.
Особенно полезными являются 6,7-дигидро-5H-пирролизины, то есть соединения формулы (I), где X представляет собой CR8R9, A представляет собой связь между X и атомом, несущим радикалы R6 и R7, и R4, R5, R6, R7, R8, R9, которые могут быть одинаковыми или различными, имеют значения, приведенные выше, и предпочтительно представляют собой водород или алкил. Особенно предпочтительными являются 6,7-дигидро-5H-пирролизины, где R4-R9 представляют собой водород или по крайней мере один или два радикала R4-R9, например, R6 и/или R7 представляют собой алкил, в частности, метил.
В соответствии с важным аспектом настоящего изобретения, наиболее эффективными являются соединения формулы (I), где первый и второй радикал из радикалов R1, R2, R3, предпочтительно R1 и R2, независимо представляют собой систему, богатую π-электронами, выбранную из арильных и ароматических гетероциклических остатков, в частности, фенила, необязательно замещенных одним или более чем одним заместителем, которые, в частности, независимо выбраны из группы, включающей в себя галоген, алкил и галогеналкил, в частности, CF3, R1 предпочтительно представляет собой незамещенный фенил, и R2 предпочтительно представляет собой 4-замещенный фенил.
В соответствии еще с одним важным аспектом данного изобретения, особенно эффективными являются соединения формулы (I), где третий радикал из радикалов R1, R2, R3, предпочтительно R3, представляет собой кислотный остаток, такой как COOH, или B-Y, где Y представляет собой COOH, и B предпочтительно представляет собой алкилен, или представляет собой предшественник кислотной группы, такой как B-Y, где Y представляет собой тетразолил.
Особенно предпочтительным является применение соединения [6-(4-хлорфенил)-2,2-диметил-7-фенил-2,3-дигидро-1H-пирролизин-5-ил]уксусной кислоты (ML3000), представленной формулой (Ia):
его физиологически приемлемых солей и производных, например физиологически гидролизируемых сложных эфиров.
Физиологически приемлемые соли включают в себя соли добавления кислот или оснований.
Солям добавления кислот являются, например, соли соединений формулы (I) с неорганическими кислотами, такими как хлористо-водородная кислота, серная кислота, азотная кислота или фосфорная кислота, или с органическими кислотами, в частности, карбоновыми кислотами, например, уксусной кислотой, винной кислотой, молочной кислотой, лимонной кислотой, яблочной кислотой, миндалевой кислотой, аскорбиновой кислотой, малеиновой кислотой, фумаровой кислотой, глюконовой кислотой или сульфоновой кислотой, например метансульфоновой кислотой, фенилсульфоновой кислотой и толуолсульфоновой кислотой и т.п.
Солями добавления основания являются, например, соли соединений формулы (I) с неорганическими основаниями, такими как гидроксид натрия или калия, или с органическими основаниями, такими как моно-, ди- или триэтаноламином и т.п.
Физиологически приемлемые производные включают в себя, в частности, пролекарства соединений формулы (I), которые преобразуются in vivo в соединения формулы (I) или их активные формы (метаболиты). Примерами являются гидролизируемые сложные эфиры соединений формулы (I), где третий радикал из радикалов R1, R2, R3 представляет собой кислотный остаток, например, его алкильный (третий радикал из радикалов R1, R2, R3, включающий в себя функциональную группу СООалкил), аралкильный (третий радикал из радикалов R1, R2, R3, включающий в себя функциональную группу СООалкарил, например, СООалкфенил), пивалоилоксиметильный, ацетоксиметильный, фталидильный, инданильный и метоксиметиловый сложный эфир.
В соответствии с особым аспектом, настоящее изобретение относится к применению хондрозащитных агентов, которые выбраны из числа соединений формулы (I).
Понятно, что используемый здесь термин «хондрозащитный агент» относится к тем соединениям, чье основное действие направлено на хрящ. Также нужно принять во внимание, что такие хондрозащитные агенты могут также обладать противовоспалительным действием в отношении синовиальной оболочки, могут положительно влиять на биосинетез клеток в субхондральной кости и в других соединительных тканях, таких как синовиальные фибробласты, и могут опосредовать миграцию клеток воспаления, с тем, чтобы препятствовать воспалительному процессу.
Настоящее изобретение относится к способу лечения и к эффективным в этом отношении фармацевтическим композициям, также вследствие этого подходящим образом упакованным, которые применимы для млекопитающих, имеющих или тех, которые могут иметь в будущем, повреждение или поражение суставного хряща и/или субхондральной кости в одном или нескольких суставах этого млекопитающего.
Использование соединений формулы (I) имеет определенные преимущество по сравнению с NSAID, особенно по сравнению с широко известными для применения, которые могут в действительности обострять прогресс остеоартрита, особенно тогда, когда показано длительное применение. Удивительно, что соединения формулы (I) эффективны при лечении или профилактике таких повреждений суставного хряща, при этом не оказывая побочного действия на процесс воспаления в таком суставе млекопитающего.
Способность соединений формулы (I) инвертировать процесс заболевания, которое в конце концов приводит к деструкции и поражению суставного хряща и/или субхондральной кости, имеет важное значение с точки зрения безопасности и эффективности лечения млекопитающих, особенно тех, у которых процесс дегенерации или деструкции суставного хряща и/или субхондральной кости находится на ранних стадиях.
Здесь под термином «млекопитающее(ие)» понимают любое млекопитающее, предпочтительно человека, кошку, собаку или лошадь и большое разнообразие их различных пород.
В соответствии с настоящим изобретением, лечение или профилактика дегенерации или деструкции суставного хряща и/или субхондральной кости в одном или нескольких суставах млекопитающих, при неоходимости такого лечения, заключается во введении указанному млекопитающему терапевтически эффективного количества для лечения или профилактики указанной дегенерации или деструкции суставного хряща и/или субхондральной кости одного или более одного соединения формулы (I).
Указанное лечение или профилактика главным образом включает в себя улучшение, уменьшение, усиление эффекта лечения, реверсию или профилактику любой дегенерации или деструкции, например, травмы, повреждения или поражения суставного хряща и/или субхондральной кости, особенно на указанных ранних стадиях указанной дегенерации или деструкции. Используемое здесь выражение «лечение или профилактика», относящееся к введению хондрозащитных соединений согласно настоящему изобретению относится как к терапевтической цели указанного введения, так и к терапевтическим результатам, по существу достигаемым указанным введением. Как рассматривается выше, объем терапии, осуществляемый введением указанного соединения, может находиться в области от улучшения состояния до значительного улучшения течения заболевания, и затем до активного лечения заболевания, включая реверсию патологического процесса. Наивысшую степень терапевтической эффективности дает профилактика любого повреждения или поражения суставного хряща и/или субхондральной кости на ранних стадиях дегенерации указанного суставного хряща и/или субхондральной кости.
Под выражением «ранние стадии дегенерации в суставном хряще и/или субхондральной кости» понимают самое начало определяемых патологических изменений в суставном хряще и/или субхондральной кости, которые являются результатом патологического процесса.
Хрящ представляет собой волокнистую соединительную ткань, существующую в нескольких формах, например, гиалиновый хрящ, эластический хрящ и волокнистый хрящ. Эта соединительная ткань состоит из воды, коллагена и протеогликанов, которые совместно образуют уникальный гидратированный гель, укрепленный волокнами, который является неэластичным, но упругим, и который обладает важной амортизационной способностью. Суставной хрящ представляет собой хрящ, находящийся в суставах млекопитающих. Он состоит из живых клеток (хондроцитов), которые синтезируют (и окружены им) интерстициальное вещество, обычно называемое внеклеточным матриксом. Хондроциты, продуцирующие внеклеточный матрикс в хряще, являются высокоактивными, и целостность такого матрикса поддерживается равновесием между действием катаболических цитокинов IL-1α, β и TNFα и анаболических цитокинов IGF и TGFβ. IL-1α, β и TNFα индуцируют продукцию специфических металлопротеаз, деградирующих матрикс, тогда как IGF и TGFβ действуют как факторы роста, индуцируют продукцию макромолекулярных строительных блоков хряща, коллагена и протеогликанов. Другие цитокины и их ингибиторы, а также тканевые ингибиторы металлопротеазы (TIMP) также влияют на это равновесие, называемое гомеостазом матрикса.
Использующийся здесь термин «металлопротеаза» относится к металлопротеазам матрикса (MMP), особенно включая те металлопротеазы этого ферментативного семейства, концентрация которых обычно увеличивается в процессе дегенерации суставного хряща, то есть, стромелизины, коллагеназы и желатиназы. Коллагеназа обычно отвечает за деградацию природного коллагена; стромелизин обычно отвечает за дегенерацию протеогликанов; и желатиназа обычно отвечает за деградацию денатурированного коллагена. Фермент аггреканаза со свойствами MMP также относится к этому классу, так как она отвечает за протеолиз агрегатов протеогликанов хряща, которые присутствуют на ранних стадиях дегенерации хряща. Тремя коллагеназами, присутствующими в суставном хряще на ранних стадиях дегенерации, являются коллагеназа-1 (MMP-1), коллагеназа-2 (MMP-8) и коллагеназа-3 (MMP-13). Из трех стромелизины, стромелизина-1 (MMP-3), стромелизина-2 (MMP-10) и стромелизина-3 (MMP-11), в суставном хряще на ранних стадиях его дегенерации присутствует только стромелизин-1.
Так как остеоартрит определен здесь как повреждение истинных суставов (подвижное, синовиальное сочленение), следовательно, в таких суставах всегда находится по крайней мере две поверхности кости, которые могут соприкасаться, но которые фактически окружены синовиальной мембраной, которая секретирует синовиальную жидкость, прозрачную щелочную вязкую жидкость, наполняющую суставную полость, и суставной хрящ, который вставлен между поверхностями сочлененных костей, обычно вместо синовиальной мембраны на этом месте.
Самые ранние макроскопические данные о патологии связаны с размягчением суставного хряща в обычно перегружаемых областях суставной поверхности, которые, в случае коленного сустава млекопитающего, особенно на моделях остеоартрита, включающих рассечение крестообразной связки в коленном суставе, состоят из бедренных мыщелков и большеберцового плато. С развитием остеоартрита целостность хрящевой поверхности повреждается, и суставной хрящ истончается с появлением вертикальных расщеплений, распространяющихся на всю толщину хряща, в процессе, называемом фибрилляцией. Движение сустава может вызвать фибрилляцию хряща до отщепления сегментов, оставляя без защиты нижнюю части кости (субхондральной), которая затем склерозируется. Также развиваются субхондральные кисты, которые могут быть наполнены синовиальной жидкостью. На границах сустава образуются остеофиты (костные шпоры).
Также в патологии дегенерации и деструкции хряща играют роль изменения в субхондральной кости. Изучение суставов млекопитающих, главным образом собак, которых подвергали фронтальному рассечению крестообразной связки, показали наличие субхондрального склероза и остеопении, то есть поражение кости в трубекуле субхондральной кости. Следствием этих изменений является утолщение субхондральной пластинки. Поражение субхондральной кости увеличивает механическое напряжение на расположенный выше суставной хрящ, что приводит к его дегенерации. Последующее утолщение субхондральной пластинки отрицательно влияет на основные механизмы восстановления и, таким образом, способствует прогрессии разрушения хряща.
Разрушение экстрацеллюлярного матрикса хряща сопровождается митотическим деление хондроцитов, которые затем образуют кластеры. Также происходит сокращение гликозаминогликановых компонентов хряща и неоднородное уменьшение протеогликанов. Во многих областях волокнистый хрящ, характеризующийся экстрацеллюлярным матриксом из толстых, компактных параллельных коллагеновых пучков, заменяется на гиалиновый хрящ. Однако необходимо отметить, что эти и вышеописанные патологические изменения в суставном хряще характерны для более поздних стадий остеоартрита, и что сначала возникает гипертрофия, то есть утолщение суставного хряща, как показано на модели с рассечением крестообразной связки млекопитающего, главным образом, на модели коленного сустава собак. Утолщение хряща происходит вследствие увеличения водного компонента, усиления синтеза протеогликанов и увеличения как содержания, так и концентрации протеогликанов в суставном хряще. Эта стадия гипертрофического восстановления суставного хряща может длиться некоторое время, но восстановленная хрящевая ткань лишена упругости и устойчивости к механическому стрессу, имеющихся в нормальном гиалиновом хряще. В конце концов, продукция протеогликанов ослабевает, и хондроциты не могут больше поддерживать свой внеклеточный матрикс. Эта заключительная стадия приводит к глубокому поражению суставного хряща.
Ранние стадии патологических изменений, приводящие к повреждению и поражению хряща, включают в себя попытку восстановления посредством увеличения синтеза макромолекул матрикса. Однако состав восстановленного хряща имеет дефекты в результате изменения композиции и распределения гликозаминогликанового компонента и изменения его способности к агрегации с гиалуроновой кислотой. Частицы, высвобождаемые в процессе патологических изменений, также могут вызывать воспалительные изменения синовиальной мембраны. Однако, несмотря на существующую патологию, начальные стадии повреждения и поражение хряща могут протекать без симптомов, с относительно слабой болью. Следовательно, существующей целью является идентификация тех компонентов внеклеточного матрикса и цитокинов, измеряемые изменения которых могут быть идентифицированы, профиль которых у млекопитающего на ранних стадиях повреждения и утраты хряща до возникновения фокального поражения хряща может быть идентифицирован радиографически. Достижение этой цели дает возможность диагностической классификации млекопитающих, являющихся кандидатами на раннее фармакологическое вмешательство еще до возникновения значительной дегенерации хряща.
Указанные патологические изменения в суставном хряще подразумевают изменения в составе, форме и плотности суставного хряща по сравнению с теми, которые были до начала указанного патологического процесса, приводящие к деградации полезных свойств указанного суставного хряща, включая силу, упругость, эластичность, конформационная целостность и стабильность, жизнеспособность и способность успешно противостоять различным типам механического стресса, особенно способность амортизировать механические удары. Эти патологические изменения в композиции главным образом включают в себя изменения в типе и количестве гликозаминогликанов и коллаг