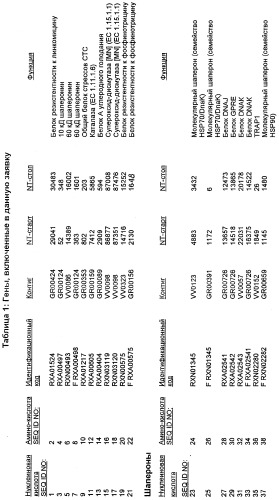
Гены corynebacterium glutamicum, кодирующие белки резистентности и толерантности к стрессам
Иллюстрации
Показать всеИзобретение относится к биотехнологии и представляет собой выделенные молекулы нуклеиновой кислоты Corynebacterium glutamicum, которые кодируют полипептид с активностью белка резистентности к линкомицину. Изобретение относится к также рекомбинантным экспрессирующим векторам, содержащим такие молекулы нуклеиновых кислот, и клеткам-хозяевам, в которые были введены эти экспрессирующие векторы. Данное изобретение касается также способа получения аминокислот при помощи культивирования указанных клеток. Изобретение позволяет расширить ассортимент ферментов и получать аминокислоты с высокой степенью эффективности. 24 н. и 12 з.п. ф-лы, 4 табл.
Реферат
Родственные заявки
В настоящей заявке испрашивается приоритет ранее поданной предварительной заявки на патент США рег.№60/141031, поданной 25 июня 1999, предварительной заявки на патент США рег. №60/142692, поданной 1 июля 1999, а также предварительной заявки на патент США рег. №60/151214, поданной 27 августа 1999. В этой заявке также испрашивается приоритет заявки на патент Германии №19930429.7, поданной 1 июля 1999, заявки на патент Германии №19931413.6, поданной 8 июля 1999, заявки на патент Германии №19931457.8, поданной 8 июля 1999, заявки на патент Германии №19931541.8, поданной 8 июля 1999, заявки на патент Германии №19932209.0, поданной 9 июля 1999, заявки на патент Германии №19932230.9, поданной 9 июля 1999, заявки на патент Германии №19932914.1, поданной 14 июля 1999, заявки на патент Германии №19940764.9, поданной 27 августа 1999, и заявки на патент Германии №19941382.7, поданной 31 августа 1999. Полное содержание всех вышеупомянутых заявок во всей своей полноте вводится в настоящее описание посредством ссылки.
Предшествующий уровень техники
Некоторые продукты и побочные продукты природных процессов метаболизма в клетках широко используются в различных областях промышленности, включая пищевую, комбикормовую, косметическую и фармацевтическую промышленность. Такими молекулами, имеющими общее название «химические продукты тонкого органического синтеза», являются органические кислоты, протеиногенные и непротеиногенные аминокислоты, нуклеотиды и нуклеозиды, липиды и жирные кислоты, диолы, углеводы, ароматические соединения, витамины и кофакторы, и ферменты. Их получение обычно осуществляют путем широкомасштабного культивирования бактерий, выращиваемых для продуцирования и секреции больших количеств конкретной нужной молекулы. Одним из ценных микроорганизмов, используемых в этих целях, является Corynebactecium glutamicum, грамположительная непатогенная бактерия. Посредством отбора штаммов был получен ряд мутантных штаммов, продуцирующих ряд нужных соединений. Однако отбор штаммов с повышенным продуцированием конкретной молекулы является длительным и трудоемким процессом.
Краткое описание изобретения
Настоящее изобретение относится к новым бактериальным молекулам нуклеиновой кислоты, имеющим широкое применение. Такими применениями являются идентификация микроорганизмов, которые могут быть использованы для продуцирования химических продуктов тонкого органического синтеза, модуляция продуцирования химических продуктов тонкого органического синтеза в С. glutamicum или родственных бактериях, типирование или идентификация С. glutamicum или родственных бактерий для использования в качестве эталонных участков для картирования генома С. glutamicum, или в качестве маркеров для трансформации. Эти новые молекулы нуклеиновой кислоты кодируют белки, называемые в данном описании белками резистентности и толерантности к стрессам (SRT).
С. glutamicum представляет собой грамположительную аэробную бактерию, которая широко используется в промышленности для широкомасштабного продуцирования ряда химических продуктов тонкого органического синтеза, а также для деградации углеводородов (например, при утечке нефти) и для окисления терпеноидов. Поэтому, молекулы нуклеиновой кислоты для SRT настоящего изобретения могут быть использованы для идентификации микроорганизмов, которые могут быть использованы для продуцирования химических продуктов тонкого органического синтеза, например, методом ферментации. Модуляция экспрессии нуклеиновых кислот, кодирующих SRT настоящего изобретения, или модификация данной последовательности молекул нуклеиновой кислоты, кодирующих SRT настоящего изобретения, могут быть осуществлены в целях модуляции продуцирования одного или нескольких химических продуктов тонкого органического синтеза из микроорганизма (например, для повышения выхода или продуцирования одного или нескольких химических продуктов тонкого органического синтеза из бактерий видов Corynebacterium glutamicum или Brevibacterium).
Нуклеиновые кислоты SRT настоящего изобретения могут быть также использованы для идентификации микроорганизма Corynebacterium glutamicum или близкородственного микроорганизма, либо для обнаружения присутствия С. glutamicum или его родственной бактерии в смешанной популяции микроорганизмов. Настоящее изобретение относится к нуклеотидным последовательностям ряда генов С. glutamicum; при этом, присутствие этого микроорганизма может быть быть установлено путем зондирования экстрагированной геномной ДНК культуры одиночной или смешанной популяции микроорганизмов в жестких условиях зондом, охватывающим область гена С. glutamicum, который является уникальным для этого микроорганизма. Хотя Corynebacterium glutamicum сам по себе является непатогенным, однако, он является родственным патогенному виду у человека, такому как Corynebacterium diphtheriae (патоген, вызывающий дифтерию); причем, детекция таких микроорганизмов имеет большое значение в медицине.
Молекулы нуклеиновых кислот, кодирующие SRT настоящего изобретения, могут также служить в качестве исходных участков для картирования генома С. glutamicum или геномов родственных микроорганизмов. Аналогичным образом, эти молекулы или их варианты или части могут служить в качестве маркеров для генетически сконструированных видов Corynebacterium или Brevibacterium.
Белки SRT, кодируемые новыми молекулами нуклеиновой кислоты настоящего изобретения, например, позволяют С. glutamicum выживать в условиях химического стресса или воздействия окружающей среды, опасных для данного микроорганизма. Если принять во внимание доступность клонирующих векторов для использования в Corynebacterium glutamicum, таких как векторы, описанные Sinskey и др. в патенте США №4649119, и способов генетической манипуляции с бактериями С. glutamicum и родственных видов Brevibacterium (например, lactofermentum} (Yoshihama et al., J.Bacteriol. 162: 591-597 (1985); Katsumata et al., J.Bacteriol. 159: 306-311 (1984) & Santamaria et al., J.Gen.Microbiol. 130: 2237-2246 (1984)), молекулы нуклеиновой кислоты настоящего изобретения можно использовать для генетического конструирования этого микроорганизма в целях получения из него лучшего или более эффективного продуцента одного или нескольких химических продуктов тонкого органического синтеза благодаря способности этих белков стимулировать рост и размножение С. glutamicum (а также непрерывное продуцирование одного или нескольких химических продуктов тонкого органического синтеза) в условиях, которые обычно препятствуют росту данного микроорганизма, таких как условия, часто встречающиеся в процессе крупномасштабного ферментативного роста. Так, например, путем сверхэкспрессии или конструирования молекулы, индуцируемой тепловым шоком протеазы, для оптимизации ее активности, может быть увеличена способность данной бактерии к разложению неправильно уложенных белков, в случае, когда данная бактерия подвергается действию высоких температур. При снижении количества неправильно уложенных (и возможно неправильно регулируемых или нефункциональных) белков, которые препятствуют осуществлению нормальных реакционных механизмов в клетке, способность этой клетки нормально функционировать в такой культуре повышается, что, в свою очередь, должно повышать ее жизнеспособность. Это общее увеличение числа клеток, обладающих большей жизнеспособностью и активностью в данной культуре, должно также приводить к увеличению выхода, продуцирования и/или эффективности продуцирования одного или нескольких нужных химических продуктов тонкого органического синтеза, что обусловлено, по крайней мере, относительно большим числом клеток, продуцирующих эти химические вещества в данной культуре.
Настоящее изобретение также относится к новым молекулам нуклеиновой кислоты, кодирующей белки SRT, которые позволяют, например, С. glutamicum выживать в условиях химического стресса или воздействия окружающей среды, опасных для данного микроорганизма. Молекулы нуклеиновых кислот, кодирующие белок SRT, называются в настоящем описании молекулами нуклеиновых кислот SRT. В предпочтительном варианте осуществления изобретения, белок SRT участвует в путях метаболизма, позволяющих С. glutamicum выживать в условиях химического стресса или воздействия окружающей среды, опасных для данного микроорганизма. Примерами таких белков являются белки, кодируемые генами, представленными в Таблице 1.
В соответствии с одним из своих аспектов, настоящее изобретение относится к изолированным молекулам нуклеиновой кислоты (например, кДНК, ДНК или РНК), содержащим нуклеотидную последовательность, кодирующую белок SRT или его биологически активные части, а также к фрагментам нуклеиновой кислоты, используемым в качестве праймеров или зондов для гибридизации в целях детекции или амплификации SRT-кодирующей нуклеиновой кислоты (например, ДНК или мРНК). В особенно предпочтительных вариантах осуществления изобретения, изолированная молекула нуклеиновой кислоты содержит одну из нуклеотидных последовательностей, представленных нечетно пронумерованными SEQ ID NOs в Списке последовательностей (например, SEQ ID NO:1, SEQ ID NO:3, SEQ ID NO:5, SEQ ID NO:7...) или кодирующую область или комплемент одной из этих нуклеотидных последовательностей. В других особенно предпочтительных вариантах осуществления настоящего изобретения, изолированная молекула нуклеиновой кислоты настоящего изобретения включает нуклеотидную последовательность, которая гибридизуется с этой молекулой или которая, по крайней мере, приблизительно на 50%, а предпочтительно, по крайней мере, приблизительно на 60%, более предпочтительно, по крайней мере, приблизительно на 70%, 80% или 90%, и даже более предпочтительно, по крайней мере, приблизительно на 95%, 96%, 97%, 98%, 99% или более является гомологичной нуклеотидной последовательности, представленной нечетно пронумерованными SEQ ID Nos в Списке последовательностей (например, SEQ ID NO:1, SEQ ID NO:3, SEQ ID NO:5, SEQ ID NO:7...) или ее части. В других предпочтительных вариантах осуществления настоящего изобретения, изолированная молекула нуклеиновой кислоты кодирует одну из аминокислотных последовательностей, представленных четно пронумерованными SEQ ID NO: в Списке последовательностей (например, SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6, SEQ ID NO:8...). Предпочтительными белками SRT настоящего изобретения также являются белки, которые, предпочтительно, обладают, по крайней мере, одной из SRT-активностей, описанных в данной заявке.
В другом варианте осуществления изобретения, изолированная молекула нуклеиновой кислоты кодирует белок или его часть, где указанный белок или его часть включает аминокислотную последовательность, которая является достаточно гомологичной аминокислотной последовательности настоящего изобретения (например, последовательности, имеющей четно пронумерованную SEQ ID NO: в Списке последовательностей), например, достаточно гомологичной аминокислотной последовательности настоящего изобретения, так, что данный белок или его часть сохраняют SRT-активность. Предпочтительно, чтобы этот белок или его часть, кодируемые данной молекулой нуклеиновой кислоты, сохраняли способность повышать выживаемость С. glutamicum в условиях химического стресса или воздействия окружающей среды, опасных для данного микроорганизма. В одном из вариантов осуществления изобретения, белок, кодируемый данной молекулой нуклеиновой кислоты, является, по крайней мере, примерно на 50%, а предпочтительно, по крайней мере, примерно на 60%, более предпочтительно, по крайней мере, примерно на 70%, 80% или 90%, а наиболее предпочтительно, по крайней мере, примерно на 95%, 96%, 97%, 98% или 99% или более гомологичным аминокислотной последовательности настоящего изобретения (например, всей аминокислотной последовательности, выбранной из четно пронумерованных последовательностей SEQ ID NO: в Списке последовательностей). В другом предпочтительном варианте осуществления изобретения, указанным белком является полноразмерный белок С. glutamicum, который является, в основном, гомологичным всей аминокислотной последовательности настоящего изобретения (кодируемой открытой рамкой считывания, показанной соответствующими нечетно пронумерованными SEQ ID NO: в Списке последовательностей (например, SEQ ID NO:1, SEQ ID NO:3, SEQ ID NO:5, SEQ ID NO:7...).
В другом предпочтительном варианте осуществления изобретения, изолированная молекула нуклеиновой кислоты происходит от С. glutamicum и кодирует белок (например, гибридный белок SRT), включающий биологически активный домен, который является, по крайней мере, приблизительно на 50% или более гомологичным одной из аминокислотных последовательностей настоящего изобретения (например, одной из четно пронумерованных последовательностей SEQ ID NO: в Списке последовательностей) и обладает способностью повышать выживаемость С. glutamicum в условиях химического стресса или воздействия окружающей среды, опасных для данного микроорганизма, или обладает одной или более активностями, указанными в Таблице 1, и указанная изолированная молекула также включает гетерологичные последовательности нуклеиновой кислоты, кодирующие гетерологичный полипептид или регуляторные области.
В другом варианте осуществления изобретения, указанная изолированная молекула нуклеиновой кислоты имеет длину, по крайней мере, в 15 нуклеодитов и гибридизуется в жестких условиях с молекулой нуклеиновой кислоты, включающей нуклеотидную последовательность настоящего изобретения (например, нечетно пронумерованную последовательность SEQ ID NO в Списке последовательностей). Предпочтительно, чтобы указанная изолированная молекула нуклеиновой кислоты соответствовала природной молекуле нуклеиновой кислоты. Более предпочтительно, чтобы изолированная нуклеиновая кислота кодировала природный белок SRT С. glutamicum или его биологически активную часть.
В другом своем аспекте, настоящее изобретение относится к векторам, например, к рекомбинантным экспрессирующим векторам, содержащим молекулу нуклеиновой кислоты настоящего изобретения, и к клеткам-хозяевам, в которые были введены указанные векторы. В одном из вариантов осуществления изобретения, указанная клетка-хозяин используется для продуцирования белка SRT путем ее культивирования в подходящей среде. Затем, указанный белок SRT может быть выделен из данной среды или клетки-хозяина.
В еще одном своем аспекте, настоящее изобретение относится к генетически модифицированному микроорганизму, в который был введен ген SRT или в котором он был модифицирован. В одном из вариантов осуществления изобретения, геном указанного микроорганизма был модифицирован путем введения молекулы нуклеиновой кислоты настоящего изобретения, кодирующей последовательность SRT дикого типа или мутированную последовательность SRT в качестве трансгена. В другом варианте осуществления изобретения, эндогенный ген SRT в геноме данного микроорганизма был модифицирован, например, функционально разрушен посредством гомологичной рекомбинации с модифицированным геном SRT. В другом варианте осуществления изобретения, эндогенный или введенный ген SRT в микроорганизме был модифицирован с помощью одной или нескольких точковых мутаций, делеций или инверсий, но, при этом, он кодирует функциональный белок SRT. В еще одном варианте осуществления изобретения, одна или несколько регуляторных областей (например, промотор, репрессор или индуктор) гена SRT в микроорганизме были модифицированы (например, посредством делеций, усечений, инверсии или точковой мутации), так, чтобы модулировалась экспрессия гена SRT. В предпочтительном варианте осуществления изобретения, данный микроорганизм принадлежит к роду Corynebacterium или Brevibacterium, при этом, особенно предпочтительным является Cocynebacterium glutamicum. В предпочтительном варианте осуществления изобретения, указанный микроорганизм также используют для продуцирования нужного соединения, такого как аминокислота, при этом, особенно предпочтительным является лизин.
В другом своем аспекте, настоящее изобретение относится к способу идентификации присутствия или активности Corynebacterium diphtheriae у индивидуума. Этот способ предусматривает обнаружение у индивидуума одной или нескольких нуклеотидных или аминокислотных последовательностей настоящего изобретения (например, последовательностей, представленных в Списке последовательностей как SEQ ID NO:1-304), и тем самым обнаружение у данного индивидуума присутствия или активности Corynebacterium diphtheriae.
В еще одном своем аспекте, настоящее изобретение относится к изолированному белку SRT или его части, например, к его биологически активной части. В предпочтительном варианте осуществления изобретения, изолированный белок SRT или его часть обладает способностью повышать выживаемость С. glutamicum в условиях химического стресса или воздействия окружающей среды, опасных для данного микроорганизма. В другом предпочтительном варианте осуществления изобретения, изолированный белок SRT или его часть являются достаточно гомологичными аминокислотной последовательности настоящего изобретения (например, четно пронумерованной последовательности SEQ ID NO: в Списке последовательностей), при этом, указанный белок или его часть сохраняют способность повышать выживаемость С. glutamicum в условиях воздействия химических веществ или окружающей среды, опасных для данного микроорганизма.
Настоящее изобретение также относится к изолированному препарату белка SRT. В предпочтительных вариантах осуществления изобретения, белок SRT включает аминокислотную последовательность настоящего изобретения (например, одну из четно пронумерованных последовательностей SEQ ID NO в Списке последовательностей). В другом предпочтительном варианте своего осуществления, настоящее изобретение относится к изолированному полноразмерному белку, который, в основном, гомологичен полной аминокислотной последовательности настоящего изобретения (например, последовательности SEQ ID NO, имеющей четный номер в Списке последовательностей) (кодированной открытой рамкой считывания в соответствующей SEQ ID NO, имеющей нечетный номер в Списке последовательностей). В еще одном варианте осуществления изобретения, данный белок, по крайней мере, примерно на 50%, предпочтительно, по крайней мере, примерно на 60%, более предпочтительно, по крайней мере, примерно на 70%, 80% или 90%, а наиболее предпочтительно, по крайней мере, примерно на 95%, 96%, 97%, 98% или 99% или более гомологичен полной аминокислотной последовательности настоящего изобретения (например, последовательности SEQ ID NO, имеющей четный номер в Списке последовательностей). В других вариантах осуществления изобретения, изолированный белок SRT содержит аминокислотную последовательность, которая, по крайней мере, примерно на 50% или более гомологична одной из аминокислотных последовательностей настоящего изобретения (например, последовательности SEQ ID NO, имеющей четный номер в Списке последовательностей), и которая способна повышать степень выживания С. glutamicum в условиях воздействия химических веществ или окружающей среды, опасных для данного микроорганизма, или обладает одной или более активностями, указанными в Таблице 1.
Альтернативно, изолированный белок SRT включает аминокислотную последовательность, кодируемую нуклеотидной последовательностью, которая гибридизуется, например в жестких условиях, с одной из последовательностей SEQ ID NO, пронумерованных четными цифрами в Списке последовательностей, или которая, по крайней мере, примерно на 50%, предпочтительно, по крайней мере, примерно на 60%, более предпочтительно, по крайней мере, примерно на 70%, 80% или 90%, а наиболее предпочтительно, по крайней мере, примерно на 95%, 96%, 97%, 98% или 99% или более гомологична указанной последовательности. Также предпочтительно, чтобы предпочтительные формы белков SRT также имели одну или несколько биологических SRT-активностей, описанных в данной заявке.
Полипептид SRT или его биологически активная часть могут быть функционально присоединены к полипептиду, не являющемуся SRT, с образованием гибридного белка. В предпочтительных вариантах осуществления изобретения, указанный гибридный белок обладает активностью, которая отличается от активности, присущей лишь одному белку SRT. В других предпочтительных вариантах осуществления изобретения, этот гибридный белок способствует повышению выходов, продуцирования и/или эффективности продуцирования нужного химического продукта тонкого органического синтеза из С. glutamicum. В особенно предпочтительных вариантах осуществления изобретения, интеграция указанного гибридного белка в клетку-хозяина способствует модуляции продуцирования нужного соединения из данной клетки.
В другом своем аспекте, настоящее изобретение относится к способам скрининга молекул, которые модулируют активность белка SRT, либо путем взаимодействия с самим белком, либо с его субстратом, или путем связывания с партнером белка SRT, либо путем модуляции транскрипции или трансляции молекулы нуклеиновой кислоты SRT настоящего изобретения.
В другом своем аспекте, настоящее изобретение относится к способу продуцирования химических продуктов тонкого органического синтеза. Этот способ предусматривает культивирование клетки, содержащей вектор, направляющий экспрессию молекулы нуклеиновой кислоты SRT настоящего изобретения, так, чтобы продуцировались химические продукты тонкого органического синтеза. В предпочтительном варианте осуществления изобретения, указанный способ, кроме того, включает стадию получения клетки, содержащей указанный вектор, где клетку трансфецируют вектором, направляющим экспрессию нуклеиновой кислоты SRT. В другом предпочтительном варианте осуществления изобретения, указанный способ, кроме того, включает стадию выделения химического продукта тонкого органического синтеза из данной культуры. В особенно предпочтительном варианте осуществления изобретения, указанную клетку получают от бактерий рода Corynebacterium или Brevibacterium, или выбирают из штаммов, указанных в таблице 3.
В другом своем аспекте, настоящее изобретение относится к способам модуляции продуцирования молекулы из микроорганизма. Такие способы предусматривают контактирование данной клетки с агентом, который модулирует активность белка SRT или экспрессию SRT-кодирующей нуклеиновой кислоты так, чтобы клеточно-ассоциированная активность была изменена по сравнению с той же самой активностью, но в отсутствие данного агента. В предпочтительном варианте осуществления изобретения, модулируют резистентность указанной клетки к одному или более токсических химических продуктов или резистентность к одному или нескольким воздействиям окружающей среды, так, чтобы это приводило к увеличению выхода или степени продуцирования данным микроорганизмом нужного химического продукта тонкого органического синтеза. Указанным агентом, модулирующим активность белка SRT, может быть агент, который стимулирует активность белка SRT или экспрессию нуклеиновой кислоты SRT. Примерами агентов, стимулирующих активность белка SRT или экспрессию нуклеиновой кислоты, кодирующей SRT, являются небольшие молекулы, активные белки SRT и нуклеиновые кислоты, кодирующие белки SRT, которые были введены в данную клетку. Примерами агентов, ингибирующих активность или экспрессию SRT, являются небольшие молекулы и антисмысловые молекулы нуклеиновых кислот SRT.
В другом своем аспекте, настоящее изобретение относится к способам модуляции выходов нужного соединения из клетки, предусматривающим введение гена SRT дикого типа или мутантного гена SRT в клетку, либо находящегося на отдельной плазмиде, либо интегрированного в геном клетки-хозяина. Если ген интегрируется в геном, то такая интеграция может происходить беспорядочно, либо она может осуществляться путем гомологичной рекомбинации, так, чтобы нативный ген заменялся введенной копией, что приводит к продуцированию нужного соединения из модулируемой клетки. В предпочтительном варианте осуществления изобретения, указанные выходы являются повышенными. В другом предпочтительном варианте осуществления изобретения указанным химическим веществом является химический продукт тонкого органического синтеза. В особенно предпочтительном варианте осуществления изобретения, указанным химическим продуктом тонкого органического синтеза является аминокислота. В особенно предпочтительных вариантах осуществления изобретения, указанной аминокислотой является L-лизин.
Подробное описание изобретения
Настоящее изобретение относится к молекулам нуклеиновой кислоты и белка SRT, которые способствуют выживанию С. glutamicum при воздействии на этот микроорганизм химических веществ или условий окружающей среды, опасных для данного микроорганизма. Молекулы настоящего изобретения могут быть использованы для модуляции продуцирования химических продуктов тонкого органического синтеза из микроорганизмов, поскольку эти белки SRT обеспечивают непрерывный рост и размножение С. glutamicum в присутствии токсических химических условий или неблагоприятных условий окружающей среды, таких, которые могут возникать в процессе крупномасштабного ферментативного культивирования. При увеличения скорости роста или, по крайней мере, при поддержании нормального роста в плохих, если не токсических, условиях, можно увеличить выход, продуцирование и/или эффективность продуцирования одного или нескольких химических продуктов тонкого органического синтеза из такой культуры, что обусловлено, по крайней мере, относительно более высоким числом клеток, продуцирующих указанный химический продукт тонкого органического синтеза в данной культуре. Аспекты настоящего изобретения будут более подробно описаны ниже.
I. Химические продукты тонкого органического синтеза
Термин «химический продукт тонкого органического синтеза» известен специалистам и означает молекулы, продуцируемые микроорганизмом, применяемым в различных отраслях промышленности, таких как, но не ограничивающихся ими, фармацевтическая промышленность, сельское хозяйство и косметическая промышленность. Такими соединениями являются органические кислоты, такие как винная кислота, итаконовая кислота и диаминопимелиновая кислота, протеиногенные и непротеиногенные аминокислоты, пуриновые и пиримидиновые основания, нуклеозиды и нуклеотиды (как описано например, в работе Kuninaka A. (1996) Nucleotides and related compounds, p.561-612, in Biotechnology vol.6, Rehm et al., eds. VCH: Weinheim и в приведенных в ней ссылках), липиды, насыщенные и ненасыщенные жирные кислоты (например, арахидоновая кислота), диолы (например, пропандиол и бутандиол), углеводы (например, гиалуроновая кислота и трегалоза), ароматические соединения (например, ароматические амины, ванилин и индиго), витамины и кофакторы (описанные в Ullmann's Encyclopedia of Industrial Chemistry, vol.A27, «Vitamins», p.443-613 (1996) VCH: Weinheim и в имеющихся там ссылках; и Ong, A.S., Niki E. & Packer, L. (1995) «Nutrition, Lipids, Health and Disease» Proceedings of the UNESCO/Confederation of Scientific and Technological Associations in Malaysia and the Society for Free Radical Research - Asia, held Sept. 1-3, 1994 at Penang, Malaysia, AOCS Press, (1995)), ферменты, поликетиды (Cane et al. (1998) Science 282: 63-68) и другие химические соединения, описанные Gutcho (1983) Chemicals by Fermentation, Noyes Data Corporation, ISBN: 0818805086 и в имеющихся там ссылках. Метаболизм и использование некоторых из этих химических продуктов тонкого органического синтеза будут более подробно описаны ниже.
А. Метаболизм и использование аминокислот
Аминокислоты включают основные структурные звенья всех белков и, таким образом, являются необходимыми для нормального функционирования всех организмов. Термин "аминокислота" хорошо известен специалистам. Протеиногенные аминокислоты, всего 20 видов, служат в качестве структурных единиц белка, в котором они соединены пептидными связями, а непротеиногенные аминокислоты (несколько сотен из которых являются известными) обычно не встречаются в белках (см. Ullmann's Encyclopedia of Industrial Chemistry, vol.A2, p.57-97 VCH: Weinheim (1985)). Аминокислоты могут иметь оптическую D- или L-конфигурацию, хотя L-аминокислоты обычно являются единственным типом, обнаруживаемым в природных белках. Пути биосинтеза и деградации каждой из указанных 20 протеиногенных аминокислот были охарактеризованы в прокариотических и эукариотических клетках (см., например, Stryer, L. Biochemistry, 3rd edition, pages 578-590 (1988)). «Незаменимые» аминокислоты (гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, треонин, триптофан и валин), называемые так потому, что они, в основном, удовлетворяют требованиям, предъявленным к питанию, что обусловлено сложностью их биосинтеза, легко превращаются в ходе метаболизма путем простого биосинтеза в остальные 11 «заменимых» аминокислот (аланин, аргинин, аспарагин, аспартат, цистеин, глутамат, глутамин, глицин, пролин, серии и тирозин). Высшие животные сохраняют способность синтезировть некоторые из этих аминокислот, но незаменимые аминокислоты должны поступать с пищей для нормального синтеза белка в организме.
Помимо своей функции в биосинтезе белка, эти аминокислоты, сами по себе, представляют интерес как химические соединения, и многие из них, как известно, находят свое применение в пищевой, комбикормовой, химической, косметической, сельскохозяйственной и фармацевтической промышленности. Лизин является важной аминокислотой для питания не только человека, но также и животных с однокамерным желудком, таким как домашняя птица и свиньи. Глутамат является наиболее широко используемым соединением в качестве ароматизирующих добавок (моно-глутамат натрия, МГН) и широко применяется в пищевой промышленности как и аспартат, фенилаланин, глицин и цистеин. Глицин, L-метионин и триптофан используются в фармацевтической промышленности. Глутамин, валин, лейцин, изолейцин, гистидин, аргинин, пролин, серин и аланин используются как в фармацевтической, так и в косметической промышленности. Треонин, триптофан и D/L-метионин являются широко распространенными пищевыми добавками (Leuchtenberger, W. (1996) Amino aids-technical production and use, p. 466-502, Rehm et al. (eds.) Biotechnology vol.6, chapter 14a, VCH: Weimheim). Кроме того, было установлено, что указанные аминокислоты могут быть использованы в качестве предшественников для синтеза синтетических аминокислот и белков, таких как N-ацетилцистеин, S-карбоксиметил-L-цистеин, (S)-5-гидрокситриптофан и др., описанные в Ullmann's Encyclopedia of Industrial Chemistry, vol.A2, p.57-97 VCH: Weinheim, 1985.
Биосинтез этих природных аминокислот в организмах, способных к их продуцированию, таких как бактерии, был хорошо охарактеризован (обзор бактериального биосинтеза аминокислот и его регуляцию см. в Umbarger, H.E. (1978) Ann.Rev. Biochem. 47: 533-606). Глутамат синтезируется путем восстановительного аминирования α-кетоглутарата, промежуточного соединения в цикле лимонной кислоты. Каждый из глутамина, пролина и аргинина последовательно продуцируется из глутамата. Биосинтез серина представляет собой трехстадийный процесс, начинающийся с 3-фосфоглицерата (промежуточного соединения при гликолизе) и кончающийся образованием этой аминокислоты после стадий окисления, трансаминирования и гидролиза. Цистеин и глицин продуцируются из серина; при этом, первый образуется путем конденсации гомоцистеина с серином, а второй образуется путем переноса атома β-углерода боковой цепи на тетрагидрофолат в реакции, катализируемой серин-трансгидроксиметилазой. Фенилаланин и тирозин синтезируются из предшественников гликолитического и пентозо-фосфатного пути метаболизма, то есть, эритрозо-4-фосфата и фосфоенолпирувата в 9-стадийном пути биосинтеза, который отличается только последними двумя стадиями после синтеза префената. Триптофан также продуцируется из этих двух исходных молекул, но его синтез проходит в 11 стадий. Тирозин может также синтезироваться из фенилаланина в реакции, катализируемой фенилаланин-гидроксилазой. Аланин, валин и лейцин являются биосинтетическими продуктами пирувата, конечного продукта гликолиза. Аспартат образуется из оксалоацетата, промежуточного соединения цикла лимонной кислоты. Аспарагин, метионин, треонин и лизин, каждый, продуцируются путем превращения аспартата. Изолейцин образуется из треонина. Сложный 9-стадийный путь метаболизма приводит к продуцированию гистидина из 5-фосфорибозил-1-пирофосфата, активированного сахара.
При избыточном синтезе белка, аминокислоты, необходимые для данной клетки, не могут сохраняться, а вместо этого они деградируют с образованием промежуточных соединений, участвующих в главных путях метаболизма, протекающих в данной клетке (обзор см. Stryer L. Biochemistry 3rd ed. Ch.21 «Amino Acid Degradation and the Urea Cycle» p.495-516 (1988)). Хотя данная клетка обладает способностью превращать нежелательные аминокислоты в нужные промежуточные соединения метаболизма, получение аминокислот является дорогостоящим с точки зрения энергетических затрат, затрат на получение молекул-предшественников и ферментов, необходимых для их синтеза. Таким образом, не удивительно, что биосинтез аминокислоты регулируется путем ингибирования по типу обратной связи, где присутствие конкретной аминокислоты служит для замедления или полного прекращения ее собственного продуцирования (обзор механизмов обратной связи в реакциях биосинтеза аминокислот см. Stryer L. Biochemistry 3rd ed. Ch.24 «Biosynthesis of Amino Acid and Heme» p.575-600 (1988)). Таким образом, выход любой конкретной аминокислоты ограничен количеством аминокислоты, присутствующей в клетке.
В. Метаболизм витаминов, кофакторов и питательных фармацевтических продуктов и их использование
Витамины, кофакторы и питательные фармацевтические продукты содержат молекулы другой группы, способность к синтезу которых у высших животных была утрачена и которые должны поставляться с пищей, хотя они легко синтезируются другими организмами, такими как бактерии. Эти молекулы сами по себе являются либо биологически активными веществами, либо предшественниками биологически активных веществ, которые могут служить в качестве носителей электрона или в качестве промежуточных соединений в различных путях метаболизма. Помимо их питательного значения, эти соединения также имеют важное промышленное значение как окрашивающие агенты, антиоксиданты и катализаторы или другие технологические добавки. (Обзор структуры, активности и промышленного применения этих соединений см., например, в Ullmann's Encyclopedia of Industrial Chemistry, vol. A27, «Vitamins», p.443-613 VCH: Weinheim, 1996). Термин "витамин" известен специалистам и означает питательные вещества, которые необходимы организму для нормального функционирования, но которые он сам не может синтезировать. Группа витаминов может охватывать кофакторы и питательные фармацевтические соединения. Понятие "кофактор" включает небелковые соединения, необходимые для нормальной ферментативной активности. Такими соединениями могут быть органические или неорганические соединения; при этом, молекулами кофакторов настоящего изобретения предпочтительно являются органические соединения. Термин "питательный фармацевтический препарат" включает пищевые добавки, полезные для жизнедеятельности растений и животных, а особенно для здоровья человека. Примерами таких молекул являются витамины, антиоксиданты, а также некоторые липиды (например, полиненасыщенные жирные кислоты).
Биосинтез этих молекул в организмах, способных их продуцировать, таких как бактерии, был хорошо охарактеризован (Ullman's Encyclopedia of Industrial Chemistry, vol.A27, «Vitamins», p.443-613 VCH: Weinheim, 1996; Michal, G. (1999) Biochemical Pathways: An Atlas of Biochemistry and Molecular Biology, John Wiley & Sons; Ong, A.S., Niki E. & Packer, L. (1995) «Nutrition, Lipids, Health and Disease» Proceedings of the UNESCO/Confederation of Scientific and Technological Associations in Malaysia and the Society for Free Radical Research - Asia, held Sept. 1-3, 1994 at Penang, Malaysia, AOCS Press: Champaign, IL X, 374 S).
Тиамин (витамин B1) продуцируется путем химического соединения пиримидина и тиазольных групп. Рибофлавин (витамин B2) синтезируется из гуанозин-5'-трифосфата (GTP) и рибозо-5'-фосфата. Рибофлавин, в свою очередь, используется для синтеза флавин-мононуклеотида (FMN) и флавин-аденин-динуклеотида (FAD). Семейство соединений под общим названием «витамин В6» (например, пиридоксин, пиридоксамин, пиридокса-5'-фосфат и коммерчески используемый гидрохлорид пиридоксина) представляет собой производные общей структурной единицы, 5-гидрокси-6-метилпиридина. Пантотенат (пантотеновая кислота, (R)-(+)-N-(2, 4-дигидрокси-3,3-диметил-1-оксобутил)-(β-аланин) может быть продуцирован либо путем химического синтеза, либо путем ферментации. Конечные стадии в биосинтезе пантотената состоят из АТР-регулируемой конденсации β-аланина и пантоевой кислоты. Ферменты, ответственные за стадии биосинтеза для превращения в пантоевую кислоту, в β-аланин и для конденсации в пантотеновую кислоту, известны специалистам. Метаболически активной форм