Способ получения фотореактивных полимеров для иммобилизации на них биомолекул
Иллюстрации
Показать всеИзобретение относится к быстрому способу получения фотореактивных полимеров и иммобилизации биомолекул на указанных полимерах. Описывается способ получения фотореактивных полимеров с последующей иммобилизацией молекул на них, включающий в себя: (а) воздействие на смесь из фотолинкера, полимера и растворителя микроволнового излучения, (b) промывание полимера соответствующим растворителем, с последующей сушкой при температуре окружающей среды, с получением фотореактивного полимера, (с) добавление биомолекулы, растворенной в соответствующем буфере, на фотореактивный полимер, (d) обработку смеси источником фотоэнергии в течение периода от 2 минут до 2 часов для иммобилизации молекулы на указанном полимере, и (е) промывание указанного полимера, имеющего иммобилизованную молекулу, в соответствующем буфере, с последующей сушкой указанного полимера при температуре окружающей среды, с получением фотореактивного полимера с иммобилизованными на нем молекулами. 21 з.п. ф-лы, 4 табл., 13 ил.
Реферат
Область изобретения
Данное изобретение относится к быстрому способу получения фотореактивных полимеров и иммобилизации биомолекул на этих полимерах. Фотореактивными полимерами являются полимеры, которые под воздействием света определенной длины волны становятся сильно реактивными и образуют ковалентную связь с биомолекулами. Этот способ иммобилизации является мягким, простым и не зависит от рН и температуры. Преимуществом изобретения является то, что технология фотоиммобилизации является легкоуправляемой и контролируемой.
Предпосылки создания изобретения
Потребность в иммобилизации биомолекул на органических и неорганических полимерах сильно возросла в последние годы, особенно в пост-геномную эру. Иммобилизованные молекулы имеют многостороннее применение в клинических лабораториях, биодатчиках, мембранных биореакторах, диагностике, геномике, протеомике, скрининге лекарственных средств, аффинной хромотографии и многих других смежных областях. Существует много способов иммобилизации биомолекул на инертной плоскости, таких как (i) активация плоскости полимера, (ii) активация биомолекул или (iii) активация и плоскости полимера, и биомолекулы перед иммобилизацией. С практической точки зрения способ (i) является наиболее удачным, так как в большинстве случаев биомолекулы являются весьма чувствительными в отношении химикатов и в процессе активации могут быть потеряны.
Биомолекулы, иммобилизованные на инертной поверхности, широко используются в диагностике, биодатчиках, мембранных биореакторах, геномике, протеомике, скрининге лекарственных средств, аффинной хромотографии и во многих других смежных областях. [Krysteva, et. al., Covalent binding of enzymes to synthetic membrane containing acrylamide units, using formaldehyde, Biotechnol Appl. Biochem. 13:106-111 (1991); Pandey, et. al., Amperometric enzyme sensor for glucose based on graphite paste-modified electrodes, Appl. Biochem. Biotechnol. 33:139-144 (1992)].
Потребность в простом и быстром способе иммобилизации биомолекул на инертной поверхности продолжает расти в пост-геномную эру.
Есть различные способы иммобилизации биомолекул на инертной поверхности полимера. Ковалентная иммобилизация может улучшить биомолекулярную активность, сократить неспецифическую адсорбцию и повысить стабильность. [Tiller, J. et. al., A novel efficient enzyme-immobilization reaction on NH2 polymers by means of L-ascorbic acid, Biotechnol. Appl. Biochem. 30, 155-162 (1992)].
Существует много способов ковалентной иммобилизации биомолекул на различных полимерных подложках. Глюкозооксидаза, уриказа, ксантиноксидаза и пенициллинацилаза были иммобилизованы на алкиламиновом стекле или силикагеле способом глютаральдегидного спаривания. [Guo, et. al., Immobilization of glucose oxidase and peroxidase and their application in flow injection analysis for glucose in serum, Appl. Biochem. Biotechnol. 23 (1): 15-24 (1990); Nakamura, et. al., Immobilization of uricase on protamine bound to glass beads and its application to determination of uric acid, Anal. Biochem. 152 (2): 386-390 (1986); Tawa, et. al., Immobilization of xanthine oxidase to controlled pore-glass. Application to high-performance liquid chromatography, Nucleic Acids Symp. Ser. 12: 107-110 (1983) ]. Глюкозооксидаза, холестериноксидаза и уриказа, иммобилизованные на стекле с контролируемым размером пор, использовались соответственно для определения глюкозы, холестерина и мочевины в сыворотке.
Тионилхлорид-активированное пористое стекло с сукцинамидопропил-контролируемым размером пор использовался для ковалентной иммобилизации антибычьего IgG. [Stabel, et. al., Anti-IgG immobilized controlled pore glass. Thionyl chloride-activated succinamidopropyl glass as a covalent immobilization matrix, Appl. Biotechnol. 36 (2):87-96 (1992)]. Такие ферменты, как ацетилкоэнзим A-синтетаза, были иммобилизованы на CNBr-активированном пористом стекле. Как сообщалось, активация инертных органических полимерных поверхностей, таких как полистирол, полипропилен или полиэтилен, происходит путем радиационной графт-полимеризациии или техники газовой плазмы [deQueiroz et. al., Surface studies of albumin immobilized onto PE and PVC films, J. Biomater. Sci. Polym. 8: 667-681 (1997); Siephia et. al., Immobilization of enzymes on polypropylene bead surfaces byanhydrous ammonia gaseous plasma technique. J Biomed. Mater. Res. 22 (5): 417-22 (1988)].
Однако все эти способы имеют один или более недостатков, например (i) они трудоемки, (ii) они отнимают много времени, (iii) в них используются опасные химикаты или (iv) требуются жесткие условия для реакции.
Опосредованная фотолинкером технология обеспечивает ковалентную иммобилизацию биомолекул на твердой поверхности в мягких условиях реакции. Этот способ основан на наличии у фотолинкера как минимум двух функциональных групп, одна из которых, как правило, является фотоактивируемой группой.
Есть много способов, пригодных для иммобилизации биомолекул посредством фотолинкера. У Elsner et. al., патент США No. 5427799, описан способ активации инертной плоскости посредством двухкольцевого гетероциклического фотолинкера, такого как псорален, путем фотохимической реакции.
У Jacobsen et al., патент США No. 6033784, раскрыт способ фотохимической активации поверхности полимера с использованием хинона. Используя производные хинона, содержащие первичный амин, аминогруппы наносят на полистироловую поверхность. Однако эти группы не так легко связываются с протеином без добавки одного или более активирующих реагентов. Подготовка таких пластинок и фотолинкера является продолжительным и громоздким процессом.
Недавно Nahar et. al. и Bora, et. al [Nahar, et. al., Light-induced activation of an inert surface for covalent immobilization of a protein ligand, Anal. Biochem. 294: 148-153 (2001); Nahar P. находящаяся на рассмотрении патентная заявка США, Method for photochemical activation of polymer surface and immobilization of biomolecules onto activated surface; Bora, et. al., Covalent immobilization of proteins onto photoactivated polystyrene microtiter plates for enzyme-linked immunosorbent assay procedures, J. Immunol. Methods. 268: 171-177 (2002)] и позднее Naqvi et. al. [Naqvi, et. al., Introduction of functional groups onto polypropylene and polyethylene surfaces for immobilization of enzymes, Anal. Biochem. 306: 74-78 (2002)] опубликовали простой, быстрый и мягкий способ индуцированной светоактивации инертного полимера, такого как полистирол, полипропилен и полиэтилен, с использованием 1-фтор-2-нитро-4-азидобензола.
Однако во многих из этих опосредованных фотолинкером способов поверхности активировали посредством фотохимической реакции, тогда как биомолекулы были иммобилизованы посредством термохимической реакции. Следовательно, биомолекулы должны иметь одну или более функциональных групп для реакции с активированной поверхностью, создающей ковалентную связь. Тогда как в фотохимическом способе иммобилизации биомолекулы могут быть иммобилизованы независимо от их функциональной группы. Встречаются лишь немногочисленные сообщения о фотохимической иммобилизации биомолекул.
Sigrist H. et al. проводили иммобилизацию биомолекулы на инертной поверхности с использованием фотолинкерного полимера, полученного посредством реакции между BSA и 3-(триэтиламин)-3-(м-изотиоцианофенилдиазирином). Затем фотолинкерный полимер использовали для связывания стрептавидина, тогда как поверхность полистирола одновременно подвергали воздействию света. [Sigrist et. al., Light dependent, Covalent immobilization of biomolecules on inert surface, Biotechnology 10: 1026-1028 (1992)]. Однако подготовка такого фотолинкера является многоступенчатой, продолжительной процедурой.
У Guire, патент США No. 3959078, раскрыт способ иммобилизации фермента с использованием фотолинкера 1-фтор-2-нитро-4-азидобензола. В этом способе аминосодержащий матрикс активируют 1-фтор-2-нитро-4-азидобензолом в процессе термохимической реакции при 37°C в течение 20 часов. На следующем стадии производят иммобилизацию фермента в течение 16 часов на активированной поверхности посредством фотохимической реакции. Несовершенство этого способа состоит в длительности реакции на обеих стадиях. Ни один из этих способов не позволяет просто и быстро подготовить фотореактивную поверхность и быстро иммобилизовать биомолекулу на этой фотореактивной поверхности. В представленной ниже таблице показаны недостатки предшествующего уровня техники.
| Таблица I | ||
| Предшествующий уровень техники | Недостатки | |
| 1 | С-H-несущий матрикс активировали фотохимически с помощью 1-фтор-2-нитро-4-азидобензола, с последующим присоединением фермента посредством термохимической реакции (Nahar et al., 2001) | Способ давал ограничивающий выбор биомолекулы, т.к. выбранные биомолекулы должны иметь аминогруппу или другие нуклеофильные группы для взаимодействия с активированной поверхностью. |
| 2 | У Jorg Tiller (Tiller et al.) описан способ активации NH2-полимерных пленок посредством (i) погружения пленки в концентрированный раствор аскорбиновой кислоты до тех пор, пока набухание не станет заметным невооруженным глазом. Затем ферменты были иммобилизованы на активированной пленке в течение 16 часов,(ii) полимерной пленке давали набухнуть в диметилацетамиде, с последующим помещением ее в 10 мл охлажденного на льду 0,5M раствора HCl, и в него добавляли по капле 1 мл раствора 1M NaNO2. Далее фермент подвергали иммобилизации в течение 12 часов при температуре 4°С. | Процедура активации аминополимерной пленки громоздка. Стадия иммобилизации отнимает много времени. |
| 3 | Биомолекулу подвергали иммобилизации на инертной поверхности с использованием полимера-фотолинкера, полученного реакцией BSA и 3-(триэтиленамин)-3-(м-изотиоцианофенилдиазирина). Далее полимер-фотолинкер использовали для одновременного связывания под воздействием света и со стрептавидином, и с полистирольной поверхностью. Sirgis H. et al., (1992) | Процесс подготовки фотолинкера является трудоемким и отнимает много времени. |
| 4 | У Guir et al., патент США № 500258 описан способ модификации спиртосодержащего полимера посредством выдерживания его в темноте при комнатной температуре в течение 16 часов с использованием фотолинкера. | Процедура активации требует больших временных затрат. |
| 5 | В патенте США № 3959078 описана процедура модификации аминосодержащего полимера под действием фотолинкера, содержащего азидогруппу, в течение 20 часов. Иммобилизацию на этом полимере выполняли при 0°С-150°С в течение 16 часов при фотохимической реакции с использованием вольфрамовой лампы в 40 ватт. | Обе стадии, активации и иммобилизации, требуют больших временных затрат. |
Цель изобретения
Основной целью изобретения является создание простого и быстрого способа подготовки фотореактивного полимера и быстрой иммобилизации биомолекул на таких полимерах.
Другой целью изобретения является обеспечение фотореактивного полимера в результате опосредованной микроволновым спектром реакции 1-фтор-2-нитро-4-азидобензола с полимером. Другой задачей настоящего изобретения является обеспечение простого, мягкого и быстрого способа иммобилизации биомолекул, не зависящего от их функциональных групп, посредством фотохимической реакции.
Еще одной целью данного изобретения является создание фотореактивной полимерной поверхности для эффективной и быстрой иммобилизации биомолекулы посредством ультрафиолетового (УФ) света.
Еще одной целью данного изобретения является создание фотореактивной полимерной поверхности, пригодной для светоиндуцированной иммобилизации биомолекулы, требуемой для использования в химической промышленности, фармакологической промышленности, диагностике, разделительной технике и во многих других смежных областях.
Новизной настоящего изобретения является быстрый способ получения фотореактивного полимера, который занимает от одной до десяти минут, в зависимости от конкретного полимера.
Краткое описание изобретения
Для того чтобы достичь заявленного в настоящем изобретении и обойти недостатки способов предыдущего уровня техники, разработан быстрый, простой и эффективный способ получения предпочтительно опосредованного микроволновым облучением фотореактивного полимера и быстрой иммобилизации биомолекулы под воздействием света, независимо от наличия на полимере функциональных групп.
Соответственно, настоящим изобретением предусматривается способ получения фотореактивных полимеров с иммобилизованными на них молекулами, причем указанный способ включает в себя:
(а) взаимодействие полимера, содержащего нуклеофильную группу, с молекулой фотолинкера, растворенной в соответствующем растворе,
(b) промывание полимера в подходящем растворе, с последующей сушкой промытого полимера при температуре окружающей среды, для получения фотореактивного полимера,
(с) присоединение молекулы, растворенной в соответствующем буфере, к фотореактивному полимеру,
d) воздействие на смесь фотоэнергетическим источником в течение периода от 2 минут до 2 часов для иммобилизации молекулы на указанном выше фотореактивном полимере, и
(е) промывание указанного полимера, имеющего иммобилизованную молекулу, соответствующим буфером и последующее подсушивание при температуре окружающей среды для получения фотореактивных полимеров с иммобилизованными на них молекулами.
В одном из воплощений настоящего изобретения фотолинкер имеет термохимическую группу, выбранную из группы, способной к образованию ковалентной связи с нуклеофильной группой полимера.
В следующем воплощении настоящего изобретения термохимическую группу фотолинкера выбирают из группы, состоящей из альдегида, карбонила, изотиоцианата, галогенида и изоцианата.
В другом воплощении настоящего изобретения фотолинкер имеет фотохимическую группу, которая фотореактивна и способна к образованию ковалентной связи с молекулой в результате фотохимической реакции, без использования каких-либо других реагентов.
В следующем воплощении настоящего изобретения фотохимическую группу фотолинкера выбирают из группы, состоящей из предшественников карбена, предшественников нитрена и кислородного радикала.
В еще одном воплощении настоящего изобретения фотолинкер представляет собой 1-фтор-2-нитро-4-азидобензол (FNAB).
В другом воплощении настоящего изобретения полимер включает в себя любой полимер, имеющий амино-, гидроксильную, тиольную или любую другую реактивную нуклеофильную группу, например такую, как силикагель, пористое стекло с длинноцепочечным алкиламино-контролируемым размером пор, поливиниловый спирт, аминополистирол и алкиламиносиликагель.
В другом воплощении настоящего изобретения реакцию на стадии (а) осуществляют посредством воздействия на смесь фотолинкера, полимера и растворителя микроволновым облучением или посредством тепловой инкубации при температуре 37°C, микроволновое облучение наиболее эффективно при частоте от 2000 до 2600 Гц и прикладываемой мощности в диапазоне от 100 до 1000 ватт в течение периода от 10 секунд до 20 минут.
В другом воплощении настоящего изобретения растворитель, используемый для промывания полимера, полученного на стадии (а), обладает способностью растворять фотолинкер и продукты его растворения, не вызывая деградации полимера, такой как метанол и этанол.
В другом воплощении настоящего изобретения растворитель, используемый на стадии (а), выбирают из группы, содержащей диметилформамид и толуол.
Предпочтительно реакцию на стадии (а) осуществляют в присутствии катализатора, такого как 30% KOH.
В еще одном воплощении настоящего изобретения полимер выбирают в форме бусины, полусферы, листа, порошка, стержня, пластины, полоски или трубки.
В еще одном воплощении настоящего изобретения молекулу, иммобилизованную на полимерной поверхности, выбирают из группы, состоящей из органической молекулы, органического полимера, биомолекулы и любой молекулы с C-H-связью.
В следующем воплощении настоящего изобретения биомолекулу выбирают из группы, состоящей из протеина, нуклеиновых кислот, углеводорода, олигонуклеотида, фермента, антигена, антитела и пептида.
Ферментом предпочтительно является пероксидаза хрена.
В еще одном воплощении настоящего изобретения источник фотоэнергии выбирают из группы, содержащей ультрафиолетовый (УФ) свет, солнечный свет, световой поток и лазерный пучок.
В следующем воплощении настоящего изобретения ультрафиолетовый (УФ) свет, используемый в качестве источника фотоэнергии, имеет длину волны в диапазоне от 300 до 400 нм, и процесс иммобилизации молекулы осуществляют в интервале от 2 минут до 2 часов.
Реакцию между нуклеофильной группой полимера и фотолинкером на стадии (а) осуществляют предпочтительно в микроволновой печи в присутствии растворителя.
Изобретение также относится к применению фотореактивного полимера с иммобилизованной на нем молекулой для диагностики, аффинной хромотографии, протеомики, геномики и скрининга лекарственных средств.
Краткое описание сопровождающих чертежей.
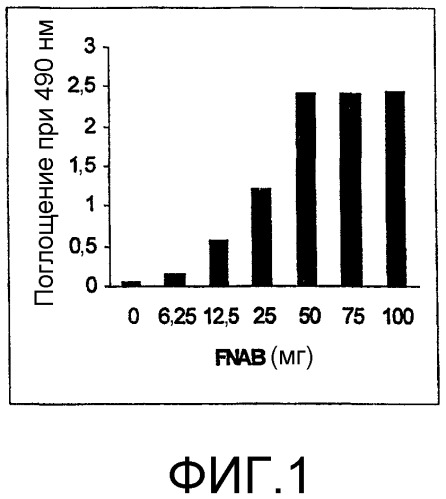
Фиг.1. Оптимизация количества FNAB для получения фотореактивного силикагеля (Пример 1)
Оптимизацию количества FNAB, необходимого для получения фотореактивного силикагеля, производили путем добавления различных количеств FNAB (0, 6,25, 12,5, 50, 75 и 100 мг) в каждую реактивную пробу, содержащую 50 мг алкиламиносиликагеля, с последующей обработкой микроволновым облучением в течение 60 секунд.
Фотореактивный алкиламиносиликагель, полученный таким образом в каждой реактивной пробе, проверяли путем иммобилизации HRP (мкг) на подложке (50 мг) в результате фотохимической реакции. Поглощение измеряли после колориметрического анализа иммобилизованного фермента.
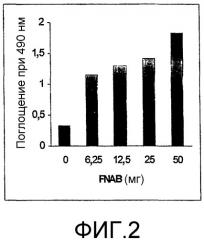
Фиг.2. Оптимизация количества FNAB для получения фотореактивного LCAA-CPG (Пример 2)
Оптимизированное количество FNAB, необходимое для получения фотореактивного LCAA-CPG, определяли путем варьирования концентрации FNAB (0, 6,25, 12,5, 25 и 50 мг) в каждой реактивной пробе, содержащей 50 мг LCAA-CPG, с последующей обработкой микроволновым облучением в течение 60 секунд. Полученный таким образом в каждой реактивной пробе LCAA-CPG проверяли путем фотооблучения HRP (1 мкг) с 50 мг подложки и колориметрического анализа иммобилизованного фермента.
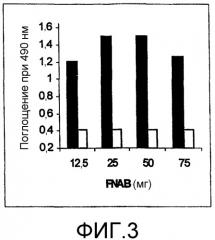
Фиг.3. Оптимизация количества FNAB для получения фотореактивного поливинилацетата (ПВА) (Пример 3)
Оптимизированное количество FNAB, необходимое для получения фотореактивного ПВА, определяли путем добавления различных количеств FNAB (12,5, 25, 50 и 75 мг) к реакционной смеси, состоящей из 50 мг ПВА, 6,5 мкл 30% KOH и 5 мл толуола. Реакционные смеси выдерживали при комнатной температуре в течение одного часа. Полученный таким образом в каждой реакционной смеси ПВА тестировали облучением HRP (16 мкг) с 50 мг подложки. Поглощение измеряли после добавления субстрата к иммобилизованному ферменту.
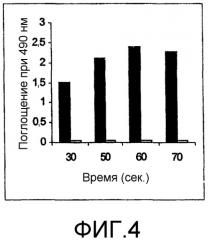
Фиг.4. Оптимизация времени воздействия микроволнового облучения для получения фотореактивного алкиламиносиликагеля (Пример 4)
Время воздействия микроволнового облучения в процессе получения фотореактивного алкиламиносиликагеля оптимизировали путем варьирования времени воздействия микроволнового облучения (30, 50, 60, и 70 секунд) в реакционной смеси 50 мг алкиламиносиликагеля с 50 мг FNAB. Полученную таким образом в каждой реакционной смеси фотореактивную поверхность тестировали путем облучения 1 мкг HRP с 50 мг подложки и колориметрически анализировали иммобилизованный фермент.
Фиг.5. Оптимизация времени воздействия микроволнового облучения для активации аминополистирола (Пример 5)
Время воздействия микроволнового облучения для получения фотореактивного аминополистирола оптимизировали посредством варьирования времени воздействия (40, 50 и 60 секунд) в каждой реакционной смеси 20 мг аминополистирола с 20 мг FNAB. Полученную таким образом фотореактивную поверхность проверяли посредством облучения HRP (35 мкг) с 20 мг подложки. Поглощение измеряли после добавления субстрата к иммобилизованному ферменту.
Фиг.6. Оптимизация концентрации KOH при получении фотореактивного ПВА (Пример 6)
Концентрацию KOH при получении фотореактивного ПВА оптимизировали путем добавления различных количеств 30%-ного раствора KOH (1,62, 3,25, 6,5, 13 и 20 мкл) в реакционную смесь, содержащую 50 мг ПВА и 50 мг FNAB в 5 мл толуола. Полученную таким образом в каждой реакционной смеси фотореактивную поверхность тестировали путем облучения HRP (16 мкг) с 50 мг подложки и колориметрического анализа иммобилизованного фермента.
Фиг.7. Оптимизация времени активации ПВА при комнатной температуре (Пример 7)
Время активации при получении фотореактивного ПВА оптимизировали путем использования различных периодов инкубации (5, 10, 60, 180 и 300 минут) для каждой реакционной смеси из 50 мг ПВА, 50 мг FNAB в 5 мл толуола и 6,5 мкл 30%-ного KOH. Полученную таким образом в каждой реакционной смеси фотореактивую поверхность тестировали путем облучения HRP (16 мкг) с 50 мг подложки и колориметрического анализа иммобилизованного фермента.
Фиг.8. Оптимизация времени облучения для иммобилизации фермента на поверхности алкиламиносиликагеля (Пример 8)
Время иммобилизации оптимизировали путем изменения времени облучения ультрафиолетовым (УФ) светом смеси HRP (1 мкг) с 50 мг фотореактивного алкиламиносиликагеля (2, 5, 10, 20, 40, 60 и 80 минут) для каждой реакционной смеси. Поглощение измеряли после добавления субстрата к иммобилизованному ферменту.
Фиг.9. Оптимизация времени фотооблучения для иммобилизации фермента на фотореактивной поверхности LCAA-CPG (Пример 9)
Время иммобилизации оптимизировали путем изменения времени облучения ультрафиолетовым (УФ) светом смеси 50 мг фотореактивного LCAA-CPG с HRP (1 мкг) (2, 10, 20, 40 и 60) для каждой реакционной смеси. Иммобилизованный фермент тестировали колориметрически после добавления субстрата.
Фиг.10. Оптимизация времени облучения ультрафиолетовым (УФ) светом для иммобилизации фермента на фотореактивной поверхности ПВА (Пример 10)
Время иммобилизации оптимизировали путем изменения времени облучения ультрафиолетовым (УФ) светом смеси 50 мг фотореактивного ПВА с HRP (16 мкг) (5, 20, 30, 60, 120 и 180 минут) для каждой реакционной смеси. Поглощение измеряли после добавления буфера для окрашивания субстрата (substrate dye buffer) к иммобилизованному ферменту.
Фиг.11. Оптимизация концентрации фермента для его иммобилизации на фотореактивном ПВА (Пример 11)
Концентрацию HRP оптимизировали, используя различные количества фермента (0,25, 0,5, 1,0, 2,0, 4,0, 8,0 и 16,0 мкг) на 50 мг фотореактивного ПВА в каждой реакционной смеси, с последующим ультрафиолетовым облучением в течение 30 минут. Иммобилизованный фермент тестировали колориметрически после добавления субстрата.
Фиг.12. Оптимизация концентрации фермента для его иммобилизации на активированной микроволновым облучением фотореактивной поверхности LCAA-CPG (Пример 12)
Концентрацию HRP оптимизировали, используя различные количества фермента (0,2, 0,5, 1, 2 и 4 мкг) для 50 мг фотореактивного LCAA-CPG, с последующим ультрафиолетовым облучением в течение 20 минут. Поглощение измеряли после добавления буфера для окрашивания субстрата к иммобилизованному ферменту.
Фиг.13. Оптимизация концентрации фермента для его иммобилизации на активированной микроволновым облучением фотореактивной поверхности алкиламиносиликагеля (Пример 13)
Оптимизацию концентрации HRP на 50 мг фотореактивного алкиламиносиликагеля производили, используя различные количества фермента (0,5, 1,0, 2,0, 4,0 и 6,0 мкг) для каждой реакционной смеси, с последующим ультрафиолетовым облучением в течение 20 минут. Иммобилизованный фермент тестировали колориметрически после добавления субстрата.
Подробное описание изобретения
Настоящее изобретение представляет собой быстрый и эффективный способ модификации поверхности полимера для внесения латентной реактивной группы в указанную поверхность полимера и иммобилизации биомолекул на указанной модифицированной поверхности полимера посредством световой энергии. Более конкретно, поверхность полимера с латентной фотореактивной группой быстро получают путем опосредованной микроволновым спектром реакции 1-фтор-2-нитро-4-азидобензола с полимером, содержащим реактивную нуклеофильную группу. Модифицированный полимер (фотореактивный полимер), полученный таким образом, имеет фотореактивную азидогруппу, которая под воздействием ультрафиолетового света (УФ) создает высокореактивный нитрен, способный к связыванию с биомолекулой.
Концентрация фотолинкера играет важную роль в получении фотореактивного полимера. Наилучший результат был получен при соотношении фотолинкера (FNAB) и полимера 1:1 (мас./мас.). Последующее повышение концентрации FNAB не приводит к увеличению фотореактивных групп в полимере. Эффективность фотореактивной поверхности определяли путем иммобилизации HRP на указанной поверхности и последующего тестирования иммобилизованного фермента. При использовании необработанной поверхности (FNAB: 0 мг) на ней практически не обнаруживали иммобилизованных биомолекул (Фиг.1, Фиг.2 и Фиг.3).
Как было обнаружено, микроволны являются прекрасным инструментом для создания фотореактивной поверхности. Таким образом, фотореактивный LCAA-CPG, полученный при микроволновом облучении 70, как выяснилось, дает лучшие результаты, чем фотореактивная поверхность, полученная по технологии предшествующего уровня техники, т.е. при 37°C в течение 20 часов (Таблица 1).
Также было обнаружено, что микроволновое облучение в течение 60 секунд дает фотореактивную аминированную поверхность диоксида кремния с хорошими результатами (Фиг.4). Для получения фотореактивного аминополистирола 60-секундного микроволнового облучения было достаточно для реакции полимера и FNAB (Фиг.5). В противоположность аминополимеру, гидроксильная группа, содержащая полимер, нуждается в основном катализаторе для реакции с FNAB. Оптимизацию количества KOH (катализатора) определяли путем проведения реакции ПВА и FNAB при перемешивании при комнатной температуре в течение одного часа в присутствии толуола и различных количеств KOH в водном растворе. Оптимальным количеством KOH для реакции ПВА и FNAB (50 мг каждого) в присутствии 5 мл толуола оказалось 6,5 мкл 30%-ного KOH (Фиг.6). Авторы изобретения также оптимизировали время, необходимое для получения фотореактивного ПВА, с использованием KOH при комнатной температуре. Оптимальное время составляло 60 минут (Фиг.7). Однако при 10-минутном микроволновом облучении были получены сравнимые результаты.
В процедуре фотоактивации ПВА активировали путем воздействия ультрафиолетовым светом на FNAB, покрытый ПВА. Фотоактивированный ПВА затем использовали для иммобилизации пероксидазы хрена при 37°C в течение 1 часа. В способе согласно изобретению фотореактивный ПВА получали путем реакции ПВА и FNAB под воздействием микроволнового облучения (или путем тепловой инкубации при 37°C). Иммобилизацию пероксидазы хрена на указанном фотореактивном ПВА затем проводили под воздействием ультрафиолетового света. В таблице 2 показано, что фотореактивный полимер (поверхность полимера активирована термическим путем) дает лучшие результаты по иммобилизации на ней биомолекул, чем термореактивный полимер (поверхность полимера активируются под воздействием света). Следовательно, процедура фотохимической иммобилизации (термохимическая активация и фотохимическая иммобилизация), как описано в способе согласно изобретению, является лучшим вариантом, по сравнению с термохимической иммобилизацией (фотохимическая активация и термохимическая иммобилизация).
Авторы изобретения оптимизировали концентрацию линкера FNAB и время инкубации с полимером (ПВА) при получении фотореактивного полимера. На второй стадии производили иммобилизацию фермента (HRP) на полимере посредством его фотореактивной группы под воздействием световой энергии. Таким образом, иммобилизацию фермента на поверхности алкиламиносиликагеля осуществляли под воздействием ультрафиолетового света на установке «UV stratalinker» в течение различных интервалов времени. Было обнаружено, что оптимальное время иммобилизации фермента на фотореактивном алкиламиносиликагеле составляет 10 минут. Однако увеличение времени ультрафиолетового облучения свыше 10 минут не приводило к повышению степени иммобилизации (Фиг.8). Иммобилизация HRP на фотореактивной поверхности LCAA-CPG оптимальна за период времени в 20 минут (Фиг.9). Однако фотореактивный ПВА требует 60-минутного ультрафиолетового облучения для оптимальной иммобилизации HRP. Дальнейшее увеличение времени ультрафиолетового облучения снижает поглощение, что может происходить за счет того, что возможна инактивация некоторых иммобилизованных ферментов (Фиг.10). Концентрация фермента также является важным фактором для иммобилизации. Концентрация 2 мкг HRP/50 мг оказалась оптимальной для иммобилизации на фотореактивном ПВА, и дальнейшее повышение концентрации не приводило к ощутимому увеличению иммобилизации фермента (Фиг.11). Тем не менее, оптимальным количеством HRP оказалось 4 мкг/50 мг подложки для иммобилизации на фотореактивном LCAA-CPG (Фиг.12) и алкиламиносиликагеле (Фиг.13). Было обнаружено, что полная активность иммобилизованного фермента на 20 мг LCAA-CPG и 20 мг алкиламиносиликагеля составляет соответственно 160 ед. и 120 ед.
Таким образом, способ получения фотореактивных подложек согласно изобретению является простым, быстрым и позволяет обойти недостатки опубликованных способов. И, кроме того, иммобилизация биомолекул на фотореактивных поверхностях протекает быстро и просто.
В таблице II представлены преимущества способа согласно изобретению.
| Таблица IIНАСТОЯЩЕЕ ИЗОБРЕТЕНИЕ И ЕГО ПРЕИМУЩЕСТВА | ||
| Способ согласно изобретению | Преимущество | |
| 1 | Способ согласно изобретению обеспечивает быстрый опосредованный микроволновым облучением способ получения фотореактивных полимеров, способных к образованию ковалентной связи с биомолекулами, независимо от наличия в биомолекуле функциональной группы. | Способ согласно изобретению позволяет активировать аминополимеры в течение 50 секунд, а спиртосодержащие полимеры - в течение 10 минут путем микроволнового облучения. Следовательно, позволяет ускорить получение фотореактивного полимера. |
| 2 | Способ согласно изобретению также представляет собой быструю технологию, которая позволяет варьировать время для иммобилизации биомолекул на фотореактивном полимере в интервале от 10 до 70 минут. | В способе согласно изобретению1) Оптимальное время иммобилизации биомолекул составляет 10-70 минут, что значительно меньше, чем (12-16 часов) при использовании того же фотолинкера, что и в предыдущих разработках2) Потенциально активированная поверхность имеет применение в хроматографических сепараторах, геномике, протеомике, где используются иммобилизованные молекулы.3) 1-фтор-2-нитро-4-азидобензол, используемый в качестве фотолинкера, может быть получен более простым путем. |
Пероксидаза хрена, пористое стекло с длинноцепочечным алкиламино-контролируемым размером пор (Long chain alkyl amine-Controlled pore glass) (нормальный диаметр 500 Е, размер ячейки: 80-120), о-фенилендиамин были приобретены у производителя Sigma, США. Силикагель LR (100-200 меш) был приобретен у производителя S.D fine chemicals. H2О2, метанол, диметилформамид, толуол и 3-аминопропилтриэтоксисилан, хлорид натрия, однозамещенный ортофосфат натрия, дизамещенный ортофосфат натрия, лимонная кислота аналитической степени чистоты были приобретены у производителя Мерк, Индия. FNAB получали из 4-фтор-3-нитроанилина реакцией диазотирования, как публиковалось ранее [15]. Опосредованную микроволновым облучением реакцию осуществляли в микроволновой печи BPL Sanyo, работающей на частоте 2450 Гц, при мощности 700 ватт. Фотоиммобилизацию проводили при длине волны 365 нм, с использованием установки «UV stratalinker»; модель 2400, (Stratagene, США), состоящей из пяти 15-ваттных трубок. Все растворы готовили в троекратно дистиллированной воде непосредственно перед использованием. Забуференный фосфатом солевой раствор (PBS) готовили путем смешивания 0,85% NaCl с 0,01M фосфатным буфером (pH 7,2). Буфер для промывания готовили путем добавления 0.1% Твин 20 в PBS. Свежеприготовленный буфер для окрашивания субстрата содержал 12 мл цитратного буфера (0,025M лимонной кислоты и 0,5M Na2HPO4·2H2О, pH 5), 5 мкл H2О2 (30% масс/объем) и 4 мг о-фенилендиамина.
Пример 1. Оптимизация количества 1-фтор-2-нитро-4-азидобен-зола для получения фотореактивного силикагеля (Фиг.1)
5 г сухого (освобожденного от влаги) силикагеля, смешанного с 10 мл 3-аминопропилтриэтиоксисилена и 80 мл толуола, перемешивали при 28°С в течение 3-х часов. Затем смесь фильтровали и промывали метанолом, водой, смесью метанол:вода (1:1) и метанолом, соответственно. Затем подложку сушили и проверяли на наличие аминогруппы с помощью нингидрина. Положительный результат теста на нингидрид подтверждает связывание аминогруппы с силикагелем. Коническую колбу, содержащую 50 мг алкиламиносиликагеля, 6,25 мг FNAB и 10 мл ДМФА, подвергали микроволновому облучению в течение 60 с. После чего подложку, извлеченную из конической колбы, промывали метанолом, сушили и помещали в чашку Петри. Концентрацию FNAB оптимизировали, проводя такой же эксперимент с различными количествами FNAB (12,5, 25, 50, 75 и 100 мг, соответственно). Далее HRP (1 мкг/80 мкл PBS) добавляли к 50 мг силикагеля и облучали с использованием установки «UV stratalinker» при 365 нм в течение 20 минут. Подложку промывали в буфере для промывания с последующим добавлением 300 мкл буфера для окрашивания субстрата. Окрашенный раствор перемещали в соответствующие полистироловые лунки микротитровального планшета и измеряли поглощение при 490 нм с помощью считывающего устройства. Контрольный эксперимент таким же способом проводили с использованием необработанного алкиламиносиликагеля (FNAB: 0 мг).
Пример 2. Оптимизация концентрации 1-фтор-2-нитро-4-азидобензола для получения фотореактивного пористого стекла с длинноцепочечным алкиламино-контролируемым размером пор (LCAA-CPG) (Фиг.2)
Смесь из 50 мг LCAA-CPG, 6,25 мг FNAB и 10 мл ДМФА помещали в коническую колбу, облучали микроволнами в течение 60 с. Концентрацию FNAB оптимизировали путем проведения аналогичного эксперимента, используя различное количество FNAB (12,5, 25 и 50 мг, соответственно).
Иммобилизацию фермента и его тестирование проводили аналогично примеру 1. Контрольный эксперимент выполняли с использованием необработанного LCAA-CPG (FNAB: 0 мг).
Пример 3. Оптимизация концентрации 1-фтор-2-нитро-4-азидобензола для получения фотореактивного ПВА (Фиг.3)
Коническую колбу, содержащую 50 мг ПВА, 50 мг FNAB, 6,5 мкл 30%-ного KOH и 5 мл толуола, выдерживали в темноте при перемешивании, при комнатной температуре (28°C) в течение 1 часа. Подобную процедуру проводили с еще тремя коническими колбами, но реакционную смесь готовили с концентрацией FNAB 12,5, 25 и 75 мг, соответственно. По истечении часа подложки из конической колбы промывали метанолом, сушили и помещали в чашки Петри. Далее добавляли HRP (16 мкг/80 мкл PBS) к каждому фотореактивному ПВА (50 мг) и подвергали облучению с использованием установки «UV stratalinker» при 365 нм в течение 30 минут. Иммобилизацию фермента и его тестирование проводили так же, как в примере 1. Контрольный эксперимент выполняли таким же способом с использованием необработанного ПВА в форме бусины.
Пример 4. Оптимизация времени воздействия микроволнового облучения для активации алкиламиносиликагеля (Фиг.4)
Четыре конические колбы, содержащие 50 мг алкиламиносиликагеля, 50 мг FNAB и 10 мл ДМФА каждая, подвергали микроволновому облучению в течение 30, 50, 60 и 70 секунд, соответственно. По истечении назначенного времени подложки из каждой конической колбы отдельно промывали метанолом, сушили и помещали в четыре чашки Петри. Иммобилизацию HRP и проводили так же, как описано в примере 1. Контрольный эксперимент выполняли таким же способом с использованием необработанных бусин алкиламиносиликагеля.
Пример 5. Оптимизация времени воздействия микроволнового облучения для активации аминополистирола (Фиг.5)
20 мг аминополистирола, 20 мг FNAB и 10 мл этанола помещали в 50-миллилитровую коническую колбу и подвергали воздействию микроволнового облучения в течение 40 секунд. Другие два эксперимента проводили подобным образом, но со временем воздействия микроволнового облучения, составляющим 50 и 60 секунд соответственно. По истечении назначенного времени подложку из конических колб промывали этанолом, сушили и помещали в чашки Петри. Далее добавляли HRP (35 мкг/80 мкл PBS) к каждому фотореактивному ПВА (50 мг) и подвергали облучению с использованием установки «UV stratalinker» при 365 нм в течение 20 минут. Фермент тестировали так же, как в примере 1. Контрольный эксперимент выполняли таким же способом с использованием необработанного аминополистирола.
Пример 6. Оптимизация концентрации KOH при термоактивации ПВА (Фиг.6)
Коническую колбу, содержащую 50 мг ПВА, 50 мг FNAB, 1,62 мкл 30%-го KOH и 5 мл толуола, выдерживали в темноте при постоянном перемешивании при ком