Способ получения неароматических l-аминокислот с использованием бактерии, принадлежащей к роду escherichia, в которой инактивирован ген csra
Иллюстрации
Показать всеИзобретение относится к биотехнологии и представляет собой способ получения неароматической L-аминокислоты с использованием бактерии, принадлежащей к роду Escherichia, которая модифицирована таким образом, что в указанной бактерии ген csrA инактивирован. Заявленное изобретение позволяет получать неароматические L-аминокислоты с высокой степенью эффективности. 2 н. и 1 з.п. ф-лы, 2 ил., 2 табл.
Реферат
Область техники
Настоящее изобретение относится к микробиологической промышленности, в частности к способу получения неароматической L-аминокислоты с использованием бактерии семейства Enterobacteriaceae, модифицированной таким образом, что экспрессия гена csrA в указанной бактерии ослаблена.
Описание предшествующего уровня техники
Белок CsrA, кодируемый плейотропным геном csrA Escherichia coli, является регулятором метаболизма углеводов, воздействуя на биосинтез гликогена, глюконеогенез, размеры клеток и свойства клеточной поверхности (Romeo, Т et al, J. Bacteriol., 175(15): 4744-47-4755 (1993)), деградацию гликогена (Yang, H. et al, J. BacterioL, 178(4): 1012-7 (1996)), глюконеогенез и гликолиз (Sabnis, N.A. et al, J. Biol. Chem., 270, 49, 29096-29104 (1995)). Белок CsrA также играет регуляторную роль в формировании биопленки (Jackson, D.W., J. Bacteriol., 184(1): 290-301 (2002)).
Был описан ген csrA, кодирующий полипептид CsrA бактерии Escherichia coli, и было высказано предположение, что изменение экспрессии гена csrA может быть применено для регуляции синтеза продуктов зависимых метаболических путей и само по себе или в сочетании с другими мутациями может использоваться для получения бактериальных продуктов (US patent 5684144).
Также был описан микроорганизм с повышенным синтезом ароматических соединений, что является особенно полезным для получения фенилаланина, обладающий пониженной активностью белка-регулятора запасания углерода (CsrA) и повышенным содержанием эритрозо-4-фосфата (W00073484A1).
Также был описан способ получения неароматических L-аминокислот, в частности L-треонина, путем повышения экспрессии гена csrA или сходных с ним нуклеотидных последовательностей (WO 03046184 A1).
Но в настоящее время нет сообщений, описывающих использование инактивации гена csrA для получения неароматических L-аминокислот.
Описание изобретения
Целями настоящего изобретения являются повышение продуктивности штаммов-продуцентов неароматической L-аминокислоты и предоставление способа получения неароматической L-аминокислоты с использованием этих штаммов.
Вышеупомянутые цели были достигнуты путем установления того факта, что инактивация гена csrA может привести к повышению продукции неароматических L-аминокислот, таких как L-треонин, L-лизин, L-цистеин, L-лейцин, L-гистидин, L-глутаминовая кислота, L-пролин и L-аргинин.
Настоящее изобретение предоставляет бактерию семейства Enterobacteriaceae, обладающую способностью к повышенной продукции неароматических аминокислот, таких как L-треонин, L-лизин, L-цистеин, L-лейцин, L-гистидин, L-глутаминовая кислота, L-пролин и L-аргинин.
Целью настоящего изобретения является предоставление бактерии-продуцента неароматической L-аминокислоты семейства Enterobacteriaceae, модифицированной таким образом, что экспрессия гена csrA в указанной бактерии ослаблена.
Также целью настоящего изобретения является предоставление описанной выше бактерии, в которой ослабление экспрессии гена csrA осуществлено благодаря инактивации гена csrA.
Также целью настоящего изобретения является предоставление описанной выше бактерии, при этом указанная бактерия принадлежит к роду Escherichia.
Также целью настоящего изобретения является предоставление описанной выше бактерии, при этом указанная бактерия принадлежит к роду Pantoea.
Также целью настоящего изобретения является предоставление описанной выше бактерии, при этом указанная неароматическая L-аминокислота выбрана из группы, состоящей из L-треонина, L-лизина, L-цистеина, L-метионина, L-лейцина, L-изолейцина, L-валина, L-гистидина, L-глицина, L-серина, L-аланина, L-аспарагина, L-аспартата, L-глутамина, L-глутаминовой кислоты, L-пролина и L-аргинина.
Также целью настоящего изобретения является предоставление способа получения неароматической L-аминокислоты, который включает в себя:
- выращивание описанной выше бактерии в питательной среде с целью продукции и накопления неароматической L-аминокислоты в питательной среде, и
- и выделение указанной неароматической L-аминокислоты из культуральной жидкости.
Также целью настоящего изобретения является предоставление описанного выше способа, при этом указанная неароматическая L-аминокислота выбрана из группы, состоящей из L-треонина, L-лизина, L-цистеина, L-метионина, L-лейцина, L-изолейцина, L-валина, L-гистидина, L-глицина, L-серина, L-аланина, L-аспарагина, L-аспартата, L-глутамина, L-глутаминовой кислоты, L-пролина и L-аргинина.
Более детально настоящее изобретение описано ниже.
1. Бактерия согласно настоящему изобретению
Бактерия согласно настоящему изобретению - это бактерия-продуцент неароматической L-аминокислоты семейства Enterobacteriaceae, модифицированная таким образом, что экспрессия гена csrA в указанной бактерии была ослаблена.
Согласно настоящему изобретению «бактерия-продуцент L-аминокислоты» означает бактерию, обладающую способностью к продукции и выделению L-аминокислоты в питательную среду, когда бактерия согласно настоящему изобретению выращивается в указанной питательной среде.
Используемый здесь термин «бактерия-продуцент неароматической L-аминокислоты» также означает бактерию, которая способна к продукции неароматической L-аминокислоты и вызывает накопление неароматической L-аминокислоты в ферментационной среде в больших количествах по сравнению с природным или родительским штаммом Е.coli, таким как штамм Е.coli К-12, и предпочтительно означает, что указанный микроорганизм способен накапливать в среде целевую L-аминокислоту в количестве не менее чем 0.5 г/л, более предпочтительно не менее чем 1.0 г/л. Термин «неароматическая L-аминокислота» включает в себя L-треонин, L-лизин, L-цистеин, L-метионин, L-лейцин, L-изолейцин, L-валин, L-гистидин, L-глицин, L-серин, L-аланин, L-аспарагин, L-аспартат, L-глутамин, L-глутаминовую кислоту, L-пролин и L-аргинин. Наиболее предпочтительны L-треонин, L-лизин, L-цистеин, L-лейцин, L-гистидин, L-глутаминовая кислота, L-пролин и L-аргинин.
Семейство Enterobacteriaceae включает в себя бактерии, принадлежащие к родам Escherichia, Enterobacter, Erwinia, Klebsiella, Pantoea, Photorhabdus, Providencia, Salmonella, Serratia, Shigella, Morganella, Yersinia и т.д. Более конкретно, могут быть использованы бактерии, классифицируемые как принадлежащие к семейству Enterobacteriaceae в соответствии с таксономией, используемой в базе данных NCBI (National Center for Biotechnology Information) (http://www.ncbi.nlm.mh.gov/htbinpost/Taxonomy/wgetorg?mode=Tree&id=1236&lvl=3&keep=l&srchmode=l&unlock). Бактерия, принадлежащая к родам Escherichia или Pantoea, предпочтительна.
Термин «бактерия, принадлежащая к роду Escherichia» означает, что бактерия относится к роду Escherichia в соответствии с классификацией, известной специалисту в области микробиологии. В качестве примера микроорганизма, принадлежащего к роду Escherichia, использованного в настоящем изобретении, может быть упомянута бактерия Escherichia coli (Е.coli).
Круг бактерий, принадлежащих к роду Escherichia, которые могут быть использованы в настоящем изобретении, не ограничен каким-либо образом, однако, например, бактерии, описанные в книге Neidhardt, F.C. et al. (Escherichia coli and Salmonella typhimurium, American Society for Microbiology, Washington D.C., 1208, Таблица 1), могут быть включены в число бактерий согласно настоящему изобретению.
Термин «бактерия, принадлежащая к роду Pantoea» означает, что бактерия относится к роду Pantoea в соответствии с классификацией, известной специалисту в области микробиологии. Недавно несколько видов Enterobacter agglomerans были классифицированы как Pantoea agglomerans, Pantoea ananatis, Pantoea stewartii или подобные им, на основе анализа нуклеотидной последовательности 16S рРНК и т.д.
Термин "бактерия модифицирована таким образом, что экспрессия гена csrA ослаблена" означает, что указанная бактерия была модифицирована таким образом, что в результате модификации такая бактерия содержит пониженное количество белка CsrA по сравнению с немодифицированной бактерией, или указанная бактерия не способна синтезировать белок CsrA.
Термин «инактивация гена csrA» означает, что указанный ген модифицирован таким образом, что такой модифицированный ген или оперон кодирует полностью неактивный белок. Также возможно, что естественная экспрессия модифицированного участка ДНК невозможна из-за делеции целевого гена или его части, сдвига рамки считывания данного гена, введения missense/nonsense мутации или модификации прилегающих к гену областей, которые включают последовательности, контролирующие экспрессию гена, такие как промотор(ы), энхансер(ы), аттенуатор(ы), сайт(ы) связывания рибосомы и т.д.
Уровень экспрессии гена можно оценить путем измерения количества мРНК, транскрибируемой с целевого гена, с использованием различных известных методик, включая гибридизацию по Нозерну (Northern blotting), количественный метод ОТ-ПЦР (RT-PCR) и подобные им. Количество белка, кодируемого данным геном, может быть измерено с помощью известных методов, включающих метод SDS-PAGE с последующим иммуноблотингом (Western blotting) и подобные им.
Ген csrA кодирует белок CsrA - регулятор запасания углерода. Ген csrA (номера нуклеотидов с 2816983 по 2817168 в последовательности с инвентарным номером NC_000913.2 в базе данных GenBank; gi:49175990) расположен на хромосоме штамма Е.coli К-12 между открытой рамкой считывания yqaB и геном alaS. Нуклеотидная последовательность гена csrA и соответствующая ей аминокислотная последовательность белка CsrA приведены в Списке последовательностей под номерами 1 (SEQ ID NO:1) и 2 (SEQ ID NO:2) соответственно.
Поскольку у представителей различных родов и штаммов семейства Enterobacteriaceae возможны некоторые вариации в нуклеотидных последовательностях, понятие инактивируемого гена csrA не ограничивается геном, последовательность которого приведена в Списке последовательностей под номером 1 (SEQ ID NO:1), но также может включать и гомологичные ему гены. Таким образом, вариант белка, кодируемого геном csrA, может быть представлен белком с гомологией не менее 80%, предпочтительно не менее 90% и наиболее предпочтительно не менее 95%, по отношению к полной аминокислотной последовательности, приведенной в Списке последовательностей под номером 2 (SEQ ID NO:2), при условии, что активность белка CsrA сохраняется.
Кроме того, ген csrA может быть представлен вариантом, который гибридизуется в жестких условиях с нуклеотидной последовательностью, приведенной в Списке последовательностей под номером 1 (SEQ ID NO: 1), или с зондом, который может быть синтезирован на основе указанной нуклеотидной последовательности, при условии, что указанный вариант кодирует функциональный белок CsrA. «Жесткие условия» включают такие условия, при которых специфические гибриды образуются, а неспецифические гибриды - не образуются. Практическим примером жестких условий является однократная отмывка, предпочтительно двух или трехкратная, при концентрации солей, соответствующей стандартным условиям отмывки при гибридизации по Саузерну, например 1 х SSC, 0.1% SDS, предпочтительно 0.1 х SSC, 0.1% SDS при 60°С. Длина зонда может быть выбрана в зависимости от условий гибридизации, обычно она составляет от 100 п.н. до 1 т.п.н.
Инактивация указанного гена может быть произведена традиционными методами, такими как мутагенез с использованием УФ-излучения или обработка нитрозогуанидином (N-метил-N'-нитро-N-нитрозогуанидин), сайт-направленный мутагенез, инактивация гена с помощью гомологичной рекомбинации, или/и инсерционно-делеционного мутагенеза (Yu, D. et al., Proc. Natl. Acad. Sci. USA, 2000, 97:12: 5978-83 и Datsenko K.A. and Wanner B.L., Proc. Natl. Acad. Sci. USA, 2000, 97:12: 6640-45), также называемого "Red-зависимой интеграцией".
Наличие активности белка CsrA может быть обнаружено путем комплементации мутации csrA-. Мутация гена csrA приводит к намного большему уровню накопления гликогена в бактерии, что может быть определено с помощью метода, описанного, например, Romeo, Т et al (J.Bacteriol., 175(15): 4744-4755 (1993)). Таким образом, снижение или отсутствие активности белка CsrA в бактерии согласно настоящему изобретению может быть определено путем сравнения указанной бактерии с родительской немодифицированной бактерией.
Методами получения плазмидной ДНК, разрезания и лидирования ДНК, трансформации, выбора олигонуклеотидов в качестве праймеров и подобными им могут являться обычные методы, хорошо известные специалисту в данной области. Эти методы описаны, например, в книге Sambrook, J., Fritsch, E.F., and Maniatis, Т., "Molecular Cloning A Laboratory Manual, Second Edition", Cold Spring Harbor Laboratory Press (1989).
Бактерия-продуцент L-аминокислоты
В качестве бактерии согласно настоящему изобретению, модифицированной таким образом, что экспрессия гена csrA ослаблена, может быть использована бактерия, способная к продукции неароматической L-аминокислоты.
Бактерия согласно настоящему изобретению может быть получена путем инактивации гена csrA в бактерии, уже обладающей способностью к продукции L-аминокислот. С другой стороны, бактерия согласно настоящему изобретению может быть получена путем придания бактерии, в которой ген csrA уже инактивирован, способности к продукции L-аминокислот.
Бактерия-продуцент L-треонина
Примеры родительского штамма для получения бактерии-продуцента L-треонина согласно настоящему изобретению включают, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штамм Е.coli TDH-6/pVIC40 (ВКПМ В-3996) (патенты США 5175107 и 5705371), штамм Е.coli NRRL-21593 (патент США 5939307), штамм Е.coli PERM BP-3756 (патент США 5474918), штаммы Е.coli FERM ВР-3519 и FERM ВР-3520 (патент США 5376538), штамм Е.coli MG442 (Гусятинер и др., Генетика, 14, 947-956 (1978)), штаммы Е.coli VL643 и VL2055 (Европейская патентная заявка ЕР 1149911 А) и подобные им.
Штамм TDH-6 является дефицитным по гену thrC, способен ассимилировать сахарозу и содержит ген UvA с мутацией типа "leaky". Указанный штамм содержит мутацию в гене rhtA, которая обусловливает устойчивость к высоким концентрациям треонина и гомосерина. Штамм В-3996 содержит плазмиду pVIC40, которая была получена путем введения в вектор, производный от вектора RSF1010, оперона thrA*BC, включающего мутантный ген thrA, кодирующий аспартокиназа-гомосериндегидрогеназу I, у которой существенно снижена чувствительность к ингибированию треонином по типу обратной связи. Штамм В-3996 был депонирован 19 ноября 1987 года во Всесоюзном научном центре антибиотиков (РФ, 117105 Москва, Нагатинская ул., 3-А) с инвентарным номером РИА 1867. Указанный штамм также был депонирован во Всероссийской коллекции промышленных микроорганизмов (ВКПМ) (РФ, 117545 Москва, 1-й Дорожный проезд, 1) с инвентарным номером В-3996.
Предпочтительно, чтобы бактерия согласно настоящему изобретению была далее модифицирована таким образом, чтобы иметь повышенную экспрессию одного или нескольких следующих генов:
- мутантного гена thrA, кодирующего аспартокиназа-гомосериндегидрогеназу I, устойчивую к ингибированию треонином по типу обратной связи;
- гена thrB, кодирующего гомосеринкиназу;
- гена thrC, кодирующего треонинсинтазу;
- гена rhtA, предположительно кодирующего трансмембранный белок;
- гена asd, кодирующего аспартат-β-семиальдегиддегидрогеназу, и
- гена aspC, кодирующего аспартатаминотрансферазу (аспартаттрансаминазу). Нуклеотидная последовательность гена thrA, кодирующего аспартокиназа-гомосериндегидрогеназу I Escherichia coli, известна (номера нуклеотидов с 337 по 2799 в последовательности с инвентарным номером NC_000913.2 в базе данных GenBank, gi: 49175990). Ген thrA расположен на хромосоме штамма Е.coli К-12 между генами thrL и thrB. Нуклеотидная последовательность гена thrB, кодирующего гомосеринкиназу из Escherichia coli, известна (номера нуклеотидов с 2801 по 3733 в последовательности с инвентарным номером NC_000913.2 в базе данных GenBank, gi: 49175990). Ген thrB расположен на хромосоме штамма Е.coli К-12 между генами thrA и thrC. Нуклеотидная последовательность гена thrC, кодирующего треонинсинтазу из Escherichia coli, известна (номера нуклеотидов с 3734 по 5020 в последовательности с инвентарньм номером NC_000913.2 в базе данных GenBank, gi: 49175990). Ген thrC расположен на хромосоме штамма Е.coli К-12 между геном thrB и открытой рамкой считывания уааХ. Все три указанных гена функционируют как один треониновый оперон.
Мутантный ген thrA, кодирующий аспартокиназу-гомосериндегидрогеназу I, устойчивую к ингибированию треонином по типу обратной связи, также, как и гены thrB и thrC, может быть получен в виде единого оперона из хорошо известной плазмиды pVIC40, которая представлена в штамме-продуценте Е.coli ВКПМ В-3996. Плазмида pVIC40 подробно описана в патенте США 5705371.
Ген rhtA расположен на 18 минуте хромосомы Е.coli около оперона ginHPQ, который кодирует компоненты транспортной системы глутамина, ген rhtA идентичен открытой рамке считывания ORF1 (reuybiF, номера нуклеотидов с 764 по 1651 в последовательности с инвентарным номером ААА218541 в базе данных GenBank, gi:440181), расположенной между генами рехВ и отрХ. Участок ДНК, экспрессирующийся с образованием белка, кодируемого открытой рамкой считывания ORF1, был назван геном rhtA (rht: resistance to homoserine and threonine). Также было показано, что мутация rhtA23 представляет собой замену А-на-G в положении - 1 по отношению к старт-кодону ATG (ABSTRACTS of 17th International Congress of Biochemistry and Molecular Biology in conjugation with 1997 Annual Meeting of the American Society for Biochemistry and Molecular Biology, San Francisco, California August 24-29,1997, abstract No. 457, EP 1013765 A).
Нуклеотидная последовательность гена asd из E.coli известна (номера нуклеотидов с 3572511 по 3571408 в последовательности с инвентарньм номером NC_000913.1 в базе данных GenBank, gi: 16131307) и может быть получена с помощью ПЦР (полимеразная цепная реакция; ссылка на White, T.J. et al.. Trends Genet., 5,185 (1989)) с использованием праймеров, синтезированных на основе нуклеотидной последовательности указанного гена. Гены asd из других микроорганизмов могут быть получены сходным образом.
Также нуклеотидная последовательность гена aspC E. coli известна (номера нуклеотидов с 983742 по 984932 в последовательности с инвентарным номером NC_000913.1 в базе данных GenBank, gi:16128895) и может быть получена с помощью ПЦР. Гены aspC из других микроорганизмов могут быть получены сходным образом.
Бактерия-продуцент L-лизина
Примеры бактерий-продуцентов L-лизина, принадлежащих к роду Escherichia, включают мутанты, обладающие устойчивостью к аналогу L-лизина. Аналог L-лизина ингибирует рост бактерий, принадлежащих к роду Escherichia, но это ингибирование полностью или частично снимается, когда в среде также присутствует L-лизин. Примеры аналога L-лизина включают, но не ограничиваются оксализином, лизингидроксаматом, S-(2-аминоэтил)-L-цистеином (АЕС), γ-метиллизином, α-хлорокапролактамом и так далее. Мутанты, обладающие устойчивостью к указанным аналогам лизина, могут быть получены путем обработки бактерий, принадлежащих к роду Escherichia, традиционными мутагенами. Конкретные примеры бактериальных штаммов, используемых для получения L-лизина, включают штамм Escherichia coli АЛ 1442 (PERM BP-1543, NRRL В-12185; смотри патент США 4346170) и штамм Escherichia coli VL611. В этих микроорганизмах аспартокиназа устойчива к ингибированию L-лизином по принципу обратной связи.
Штамм WC196 может быть использован в качестве бактерии-продуцента L-лизина Escherichia coli. Данный бактериальный штамм был получен путем селекции фенотипа устойчивости к АЕС у штамма W3110, производного от штамма Escherichia coli K-12. Полученный штамм был назван Escherichia coli АЛ 3069 и был депонирован в Национальном Институте Биологических Наук и Человеческих Технологий, Агенство Промышленной Науки и Технологии (National Institute of Bioscience and Human-Technology, Agency of Industrial Science and Technology), в настоящее время называющийся Национальный Институт Прогрессивной Промышленной Науки и Технологии, Международный Депозитарий Организмов для Целей Патентования, Централ 6, 1-1, Хигаши 1-Чоме, Тсукуба-ши, Ибараки-кен, 305-8566, Япония (National Institute of Advanced Industrial Science and Technology, International Patent Organism Depositary, Central 6,1-1, Higashi 1-Chome, Tsukuba-shi, Ibaraki-ken, 305-8566, Japan), 6 декабря 1994 года с инвентарным номером PERM P-14690. Затем было произведено международное депонирование этого штамма согласно условиям Будапештского Договора от 29 сентября 1995 года, и штамм получил инвентарный номер FERM ВР-5252 (патент США 5827698).
Бактерия-продуцент L-цистеина
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-цистеина согласно настоящему изобретению, включают в себя, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штамм Е.coli JM15, трансформированный различными аллелями гена cysE, кодирующими устойчивые к ингибированию по типу обратной связи серинацетилтрансферазы (патент США 6218168; патентная заявка РФ 2003121601); штамм Е.coli W3110, содержащий гены с повышенной экспрессией, кодирующие белки, способные к секреции соединений, токсичных для клетки (патент США 5972663); штаммы Е.coli со сниженной активностью цистеиндесульфогадразы (патент Японии JP 11155571 А);
штамм Е.coli W3110 с повышенной активностью позитивного транскрипционного регулятора цистеинового регулона, кодируемого геном cysB (международная заявка РСТ W00127307A1), и подобные им.
Бактерия-продуцент L-лейцина
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-лейцина согласно настоящему изобретению, включают в себя, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штаммы Е.coli, устойчивые к аналогам лейцина, включающие, например, Р-2-тиенилаланин, 3-гидроксилейцин, 4-азалейцин и 5,5,5-трифлуоролейцин (выложенные патентные заявки Японии JP 62-34397 В и JP 8-70879 A), штаммы Е.coli, полученные с помощью генно-инженерных методов, описанных в заявке РСТ WO 96/06926; штамм Е.coli H-9068 (JP 08-70879А), и подобные им.
Бактерия согласно настоящему изобретению может быть улучшена путем усиления экспрессии одного или нескольких генов, вовлеченных в биосинтез L-лейцина. Примеры таких генов включают в себя гены оперона leuABCD и предпочтительно представлены мутантным геном leuA, кодирующим изопропилмалатсинтазу со снятым ингибированием L-лейцином по типу обратной связи (патент США 6403342). Кроме того, бактерия согласно настоящему изобретению может быть улучшена путем усиления экспрессии одного или нескольких генов, кодирующих белки, которые экспортируют L-аминокислоту из бактериальной клетки. Примеры таких генов включают в себя гены Ь2682 и b2683 (гены ygaZH) (патентная заявка РФ 2001117632).
Бактерия-продуцент L-гистидина
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-гистидина согласно настоящему изобретению, включают в себя, но не ограничиваются бактериями-продуцентами L-гистидина, принадлежащими к роду Escherichia, такими как штамм Е.coli 24 (ВКПМ В-5945, патент РФ 2003677); штамм Е.coli 80 (ВКПМ В-7270, патент РФ 2119536); штаммы Е.coli NRRL В-12116 - В12121 (патент США 4388405); штаммы Е.coli H-9342 (FERM ВР-6675) и Н-9343 (FERM ВР-6676) (патент США 6344347); штамм Е.coli H-9341 (FERM BP-6674) (Европейский патент ЕР 1085087); штамм Е.coli AI80/pFM201 (патент США 6258554) и подобными им.
Бактерия-продуцент L-глутаминовой кислоты. Примеры родительских штаммов, используемых для получения бактерии-продуцента L-глутаминовой кислоты согласно настоящему изобретению, включают в себя, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штамм Е.coli VL334 thrC+ (Европейский патент ЕР 1172433). Штамм Е.coli VL334 (ВКПМ В-1641) является ауксотрофом по L-изолейцину и L-треонину с мутациями в генах thrC и ilvA (патент США 4278765). В этот штамм была перенесена природная аллель гена thrC методом общей трансдукции с использованием бактериофага Р1, выращенного на клетках природного штамма Е.coli K12 (ВКПМ В-7). В результате был получен штамм VL334thrC+(ВКПМ В-8961), ауксотроф по L-изолейцину. Этот штамм обладает способностью к продукции L-глутаминовой кислоты.
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-глутаминовой кислоты согласно настоящему изобретению, включают в себя мутантные штаммы, лишенные активности α-кетоглутаратдегидрогеназы или обладающие сниженной активностью α-кетоглутаратдегидрогеназы. Бактерии, принадлежащие к роду Escherichia, лишенные активности α-кетоглутаратдегидрогеназы или обладающие сниженной активностью α-кетоглутаратдегидрогеназы, и способы их получения описаны в патентах США 5378616 и 5573945. Конкретно, примеры таких штаммов включают в себя следующие штаммы:
E.coli W 3110 sucA::Kmr
Е.coli AJ 12624 (FERM BP-3853)
Е.coli AJ 12628 (FERM BP-3854)
Е.coli AJ 12949 (FERM BP-4881)
Штамм Е.coli W3110 sucA::Kmr - это штамм, полученный в результате разрушения гена α-кетоглутаратдегидрогеназы (далее называемого «ген sucA») штамма E.coli W3110. У этого штамма активность α-кетоглутаратдегидрогеназы отсутствует полностью.
Другие примеры бактерии-продуцента L-глутаминовой кислоты включают в себя бактерии, принадлежащие к роду Pantoea, которые лишены активности α-кетоглутаратдегидрогеназы или имеют сниженную активность α-кетоглутаратдегидрогеназы, и могут быть получены описанным выше способом. Примером таких штаммов является штамм Pantoea ananatis AJ 13356 (патент США 6331419). Штамм Pantoea ananatis AJ 13356 был депонирован в Национальном Институте Биологических Наук и Человеческих Технологий, Агенство Промышленной Науки и Технологии, Министерство Международной Торговли и Промышленности (National Institute of Bioscience and Human-Technology, Agency of Industrial Science and Technology, Ministry of International Trade and Industry), в настоящее время называющемся Национальным Институтом Прогрессивной Промышленной Науки и Технологии, Международный Депозитарий Организмов для Целей Патентования, Централ 6, 1-1, Хигаши 1-Чоме, Тсукуба-ши, Ибараки-кен, 305-8566, Япония (National Institute of Advanced Industrial Science and Technology, International Patent Organism Depositary, Central 6,1-1, Higashi 1-Chome, Tsukuba-shi, Ibaraki-ken, 305-8566, Japan), 19 февраля 1998 года и получивший инвентарный номер FERM Р-16645. Затем было произведено международное депонирование этого штамма согласно условиям Будапештского Договора от 11 января 1999 года, и штамм получил инвентарный номер FERM ВР-6615. В штамме Pantoea ananatis АJ13356 отсутствует активность α-KGDH в результате разрушения гена субъединицы αKGDH-El (sucA). Вышеупомянутый штамм при выделении был идентифицирован как Enterobacter agglomerans и депонирован как штамм Enterobacter agglomerans A J 13355. Тем не менее позднее он был классифицирован как Pantoea ananatis на основе нуклеотидной последовательности 16S рРНК и других доказательств (смотри раздел Примеры). Несмотря на то, что штамм АJ13356 был депонирован в указанный выше депозитарий как Enterobacter agglomerans, для целей данного описания он будет упоминаться как Pantoea ananatis.
Бактерия-продуцент L-пролина
Примеры бактерий-продуцентов L-пролина, используемых в качестве родительского штамма согласно настоящему изобретению, включают в себя, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штамм E.coli 702 ilvA (ВКПМ В-8012), дефицитного по гену HvA и способного к продукции L-пролина (Европейский патент ЕР 1172433). Бактерия согласно настоящему изобретению может быть улучшена путем усиления экспрессии одного или нескольких генов, вовлеченных в биосинтез L-пролина. Предпочтительно примеры таких генов для бактерий-продуцентов L-пролина включают ген proB, кодирующий глутаматкиназу с десенсибилизированной регуляцией L-пролином по типу обратной связи (патент Германии 3127361). Кроме того, бактерия согласно настоящему изобретению может быть улучшена путем усиления экспрессии одного или нескольких генов, кодирующих белки, секретирующие L-аминокислоту из бактериальной клетки. Примерами таких генов являются гены b2682 и b2683 (гены ygaZH) (Европейская патентная заявка ЕР 1239041 А2).
Примеры бактерий, принадлежащих к роду Escherichia и обладающих способностью к продукции L-пролина, включают следующие штаммы Е.coli: NRRL В-12403 и NRRL В-12404 (патент Великобритании GB 2075056), ВКПМ В-8012 (патентная заявка РФ 2000124295), плазмидные мутанты, описанные в патенте Германии DE 3127361, плазмидные мутанты, описанные Bloom F.R. et al (The 15th Miami winter symposium, 1983, p.34), и подобные им.
Бактерия-продуцент L-аргинина
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-аргинина согласно настоящему изобретению, включают в себя, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штамм Е.coli 237 (ВКПМ В-7925) (патентная заявка США US 2002058315) и его производные, содержащие мутантную N-ацетилглутаматсинтазу (патентная заявка РФ 2001112869), штамм Е.coli 382 (ВКПМ В-7926) (Европейская патентная заявка ЕР 1170358), штамм-продуцент аргинина, в который введен ген argA, кодирующий N-ацетилглутаматсинтетазу (выложенная патентная заявка Японии 57-5693А), и подобные им.
2. Способ согласно настоящему изобретению.
Способом согласно настоящему изобретению является способ получения неароматической L-аминокислоты, включающий стадии выращивания бактерии согласно настоящему изобретению в питательной среде с целью продукции и накопления L-аминокислоты в питательной среде, и выделения L-аминокислоты из культуральной жидкости.
Согласно настоящему изобретению выращивание, выделение и очистка L-аминокислоты из культуральной или подобной ей жидкости может быть осуществлена способом, подобным традиционным способам ферментации, в которых аминокислота продуцируется с использованием бактерии.
Питательная среда, используемая для выращивания, может быть как синтетической, так и натуральной, при условии, что указанная среда содержит источники углерода, азота, минеральные добавки и, если необходимо, соответствующее количество питательных добавок, необходимых для роста микроорганизмов. К источникам углерода относятся различные углеводы, такие как глюкоза и сахароза, а также различные органические кислоты. В зависимости от характера ассимиляции используемого микроорганизма могут использоваться спирты, такие как этанол и глицерин. В качестве источника азота могут использоваться различные неорганические соли аммония, такие как аммиак и сульфат аммония, другие соединения азота, такие как амины, природные источники азота, такие как пептон, гидролизат соевых бобов, ферментолизат микроорганизмов. В качестве минеральных добавок могут использоваться фосфат калия, сульфат магния, хлорид натрия, сульфат железа, сульфат марганца, хлорид кальция и подобные им соединения. В качестве витаминов могут использоваться тиамин, дрожжевой экстракт и подобные им соединения.
Выращивание осуществляется предпочтительно в аэробных условиях, таких как перемешивание культуральной жидкости на качалке, взбалтывание с аэрацией, при температуре в пределах от 20 до 40°С, предпочтительно в пределах от 30 до 38°С. рН среды поддерживают в пределах от 5 до 9, предпочтительно от 6.5 до 7.2. рН среды может регулироваться путем добавления аммиака, карбоната кальция, различных кислот, оснований и буферных растворов. Обычно, выращивание в течение от 1 до 5 дней приводит к накоплению целевой L-аминокислоты в культуральной жидкости.
После выращивания твердые остатки, такие как клетки, могут быть удалены из культуральной жидкости методом центрифугирования или фильтрацией через мембрану, а затем L-аминокислота может быть выделена и очищена методами ионообменной хроматографии, концентрирования и/или кристаллизации.
Краткое описание чертежей
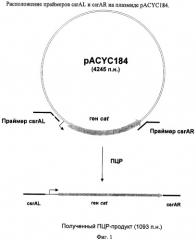
На Фиг.1 изображено расположение праймеров csrAL и csrAR на плазмиде pACYC184, используемой для амплификации гена cat.
На Фиг.2 изображено конструирование фрагмента хромосомной ДНК, содержащего инактивированный ген csrA.
Примеры
Настоящее изобретение будет более подробно описано ниже со ссылкой на следующие не ограничивающие настоящее изобретение Примеры.
Пример 1. Конструирование штамма с инактивированным геном csrA.
1. Деления гена csrA.
Штамм, содержащий делецию в гене csrA, был сконструирован с использованием методики, разработанной Datsenko, К.А. и Wanner, B.L. (Proc. Natl. Acad. Sci. USA, 2000,97(12), 6640-6645), известной как "Red-зависимая интеграция". В соответствии с этой методикой были сконструированы ПЦР-праймеры csrAL (SEQ ID NO: 3) и csrAR (SEQ ID NO: 4), гомологичные областям хромосомы, прилегающим к гену csrA, и гену устойчивости к антибиотику плазмиды, используемой в качестве матрицы для ПЦР. В качестве матрицы для ПЦР была использована плазмида pACYC184 (NBL Gene Sciences Ltd., UK) (инвентарный номер Х06403 в базе данных GenBank/EMBL). Использовался следующий температурный профиль для ПЦР: денатурация при 95°С в течение 3 мин; два первых цикла: 1 мин при 95°С, 30 сек при 50°С, 40 сек при 72°С; последующие 25 циклов: 30 сек при 95°С, 30 сек при 54°С, 40 сек при 72°С и заключительная полимеризация: 5 мин при 72°С.
Полученный продукт ПЦР длиной 1093 п.н. (Фиг.1) был очищен в агарозном геле и может быть использован для электропорации в штамм Е.coli MG1655 (АТСС 700926), содержащий плазмиду pKD46 с температурно-чувствительным репликоном. Плазмида pKD46 (Datsenko, К.А. and Wanner, B.L., Proc. Natl. Acad. Sci. USA, 2000, 97:12:6640-45) содержит фрагмент ДНК фага А, длиной 2154 нуклеотида (позиции с 31088 по 33241 нуклеотидной последовательности с инвентарным номером J02459 в базе данных GenBank), а также содержит гены λ Red-гомологичной системы рекомбинации (гены γ, β, ехо) под контролем промотора Рагав, индуцируемого арабинозой. Плазмида pKD46 необходима для интеграции продукта ПЦР в хромосому штамма MG1655.
Электрокомпетентные клетки были получены следующим образом: ночную культуру штамма Е.coli MG1655 выращивали при 30°С в среде LB с добавкой ампициллина (100 мг/л), развели в 100 раз, добавив 5 мл среды SOB (Sambrook et al, "Molecular Cloning A Laboratory Manual, Second Edition", Cold Spring Harbor Laboratory Press (1989)), содержащей ампициллин и L-арабинозу (1 мМ). Полученную культуру растили с перемешиванием при 30°С до достижения OD600≈0.6, после чего делали клетки электрокомпетентными путем концентрирования в 100 раз и трехкратного отмывания ледяной деионизированной H2O. Электропорацию проводили с использованием 70 мкл клеток и 100 нг продукта ПЦР. После электропорации клетки инкубировали в 1 мл среды SOC (Sambrook et al, "Molecular Cloning A Laboratory Manual, Second Edition", Cold Spring Harbor Laboratory Press (1989)) при 37°С в течение 2.5 часов, после чего высевали на чашки с L-агаром и выращивали при 37°С для отбора CmR-рекомбинантов. Затем для удаления плазмиды pKD46 проводили 2 пассажа на L-агаре с Cm при 42°С и полученные колонии проверяли на чувствительность к ампициллину.
2. Подтверждение делеции гена csrA с помощью ПЦР.
Мутанты с делегированным геном csrA, содержащие ген устойчивости к Cm, были проверены с помощью ПЦР. Локус-специфичные праймеры csrA1 (SEQ ID NO: 5) и csrA2 (SEQ ID NO: 6) использовались для проверки делеции с помощью ПЦР. Использовался следующий температурный профиль для ПЦР-проверки: денатурация при 94°С в течение 3 мин; профиль для 30 циклов: 30 сек при 94°С, 30 сек при 54°С, 1 мин при 72°С; заключительный шаг: 7 мин при 72°С. Длина продукта ПЦР, полученного с использованием в качестве матрицы клеток родительского штамма MG1655 csrA+, составляет 547 п.н. Длина продукта ПЦР, полученного с использованием в качестве матрицы клеток мутантного штамма MG1655 AcsrA::cat, составляет 1453 п.н. (Фиг.2).
Пример 2. Продукция L-треонина штаммом Е.coli B-3996-AcsrA. Для оценки влияния инактивации гена csrA на продукцию треонина ДНК-фрагменты хромосомы описанного выше штамма Е.coli MG1655 AcsrA::cat были перенесены в штамм-продуцент L-треонина Е.coli В-3996 (ВКПМ В-3996) с помощью P1-трансдукции (Miller, J.H. (1972) Experiments in Molecular Genetics, Cold Spring Harbor Lab. Press, Plainview, NY).
Оба штамма Е.coli В-3996 и В-3996-AcsrA выращивали в течение 18-24 часов при температуре 37°С на чашках с L-агаром, содержащим хлорамфеникол (30 мкг/мл). Для получения посевной культуры указанные штаммы выращивали при 32°С в течение 18 часов на роторной качалке (250 об/мин) в пробирках размером 20×200 мм, содержащих 2 мл L-бульона с 4% сахарозой. Затем в ферментационную среду было внесено по 0.21 мл (10%) посевной культуры. Ферментацию проводили в 2 мл минимальной ферментационной среды в пробирках размером 20×200 мм. Клетки выращивали в течение 65 часов при 32°С с перемешиванием (250 об/мин).
После выращивания количество накопленного в среде L-треонина определяли с помощью бумажной хроматографии, с использованием подвижной фазы следующего состава: бутанол: уксусная кислота: вода=4:1:1 (v/v). Раствор (2%) нингидрина в ацетоне использовали для визуализации. Пятно, содержащее L-треонин, было вырезано, L-треонин был элюирован 0.5% водным раствором CdCl2, после чего количество L-треонина оценивалось спектрофотометрическим методом при длине волны 540 нм.
Результаты 10 независимых пробирочных ферментации приведены в Таблице 1. Использовали следующий состав ферментационной среды, г/л:
| Глюкоза | 80.0 |
| (NH4)2SO4 | 22.0 |
| NaCl | 0.8 |
| КН2PO4 | 2.0 |
| MgSO4·7H2O | 0.8 |
| FeSO4·7H2O | 0.02 |
| MnSO4·5H2O | 0.02 |
| Тиамин гидрохлорид | 0.0002 |
| Дрожжевой экстракт | 1.0 |
| СаСО3 | 30.0 |
Глюкозу и MgSO4·7H2O стерилизовали отдельно. СаСО3 стерилизовали сухим жаром при 180°С в течение 2 часов. рН доводили до 7.0. Антибиотик добавляли в среду после стерилизации.
Как видно из Таблицы 1, штамм B-3996-AcsrA накапливал большее количество L-треонина по сравнению со штаммом В-3996.
Пример 3. Продукция L-лизина штаммом Е.coli АЛ 1442-AcsrA. Для оценки влияния инактивации гена csrA на продукцию лизина ДНК-фрагменты хромосомы описанного выше штамма Е.coli MG1655 AcsrA::cat могут быть перенесены в штамм-проду