Жидкофазное окисление галогенированных орто-ксилолов
Иллюстрации
Показать всеИзобретение относится к усовершенствованному способу получения галогенфталевой кислоты, включающему смешивание от 3 до 7 весовых частей уксусной кислоты с 1 весовой частью галоген-орто-ксилола, с от 0,25 до 2 мол. процентами в расчете на указанный галоген-орто-ксилол источника кобальта, с от 0,1 до 1 мол. процентом в расчете на указанный галоген-орто-ксилол источника марганца, с от 0,01 до 0,1 мол. процентом в расчете на указанный галоген-орто-ксилол источника металла, выбранного из циркония, гафния и их смесей, с от 0,02 до 0,1 мол. процента в расчете на указанный галоген-орто-ксилол источника бромида; причем галоген-орто-ксилол имеет формулу СН,
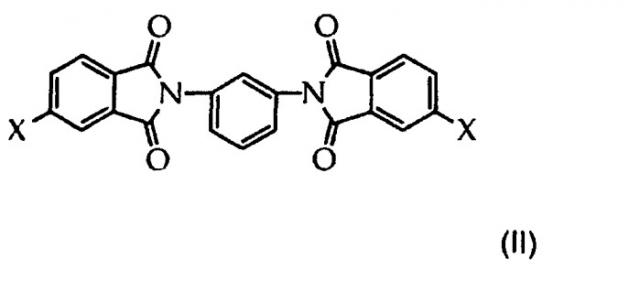
где Х представляет собой галоген, выдерживание реакционной смеси при давлении, по меньшей мере, 1600 КПа и при температуре от 130°С до 200°С; введение газа, содержащего молекулярный кислород, в реакционную смесь при расходе, по меньшей мере, 0,5 норм. м3 газа/час на килограмм галоген-орто-ксилола в реакционной смеси в течение времени, достаточного для 90-процентной конверсии галоген-орто-ксилола с получением галогенфталевой кислоты. Изобретение также относится к способу получения галогенфталевого ангидрида путем дистилляции и дегидратации галогенфталевой кислоты и к способу получения полиэфиримида, включающему взаимодействие галогенфталевого ангидрида с 1,3-диаминобензолом с образованием бис(галогенфталимида) (II)
где Х является галогеном; и
взаимодействие бис(галогенфталимида) (II) с солью щелочного металла дигидроксизамещенного ароматического углеводорода, имеющего формулу (IV) ОН-А2-ОН, где А2 является двухвалентным радикалом ароматического углеводорода, с образованием полиэфиримида. 3 н. и 17 з.п. ф-лы, 2 табл.
Реферат
Данное изобретение относится к жидкофазному окислению галогенозамещенных алкилароматических соединений. В частности, данное изобретение относится к жидкофазному окислению галоген-орто-ксилола с получением галогенфталевой кислоты, которая может быть дегидрирована с получением галогенфталевого ангидрида.
Жидкофазное окисление давно используется для получения дикарбоновых кислот из диалкилбензолов. Особый интерес представляло окисление диметилбензола (ксилола) с получением фталевой кислоты, особенно окисление пара-ксилола с получением терефталевой кислоты, которая используется для производства полибутилентерефталата. Жидкофазное окисление ксилола до фталевой кислоты требует использования катализатора, обычно кобальт/марганцево/бромной (бромидной) каталитической системы, и обычно выполняется в растворителе - карбоновой кислоте, таком как уксусная кислота. Каталитическая система может быть усилена путем использования сокатализатора, такого как цирконий, гафний или церий. Фталевая кислота легко выделяется в виде твердого вещества, которое может быть отфильтровано от реакционной смеси.
Жидкофазное окисление с использованием кобальт/марганцево/бромной каталитической системы и растворителя - карбоновой кислоты также успешно применялось в случае галогенированного ксилола. Окисление галогенированного ксилола является более затрудненным, чем окисление ксилола из-за присутствия галогена, который является электроноакцепторным заместителем бензольного кольца. Большая затрудненность окисления приводит к более низкой селективности реакции, большей степени частичного окисления и большему количеству побочных продуктов, чем наблюдаемые при жидкофазном окислении ксилола в похожих условиях. Кроме того, галогенированную фталевую кислоту трудно отделить от частично окисленных и побочных продуктов даже путем дистилляции. Таким образом, понятно, что для того, чтобы способ жидкофазного окисления галогенированного ксилола был коммерчески выгодным, выход реакции и селективность реакции должны быть очень высокими. Оптимально для промышленного использования способа, чтобы селективность реакции была достаточно высокой с тем, чтобы в результате образовывались только незначительные количества частично окисленных и побочных продуктов, с устранением, таким образом, необходимости выделения галогенфталевой кислоты.
Способ получения галогенфталевой кислоты согласно изобретению включает приготовление реакционной смеси, включающее смешивание примерно от 7 до примерно 3 весовых частей уксусной кислоты с 1 весовой частью галоген-орто-ксилола, примерно от 0,25 до примерно 2 мол.процентами в расчете галоген-орто-ксилол источника кобальта, примерно от 0,1 до примерно 1 мол.процента в расчете на галоген-орто-ксилол источника марганца, примерно от 0,01 до примерно 0,1 мол.процента в расчете на галоген-орто-ксилол источника металла, выбранного из циркония, гафния и их смесей, и от примерно 0,02 до примерно 0,1 мол.процента в расчете на галоген-орто-ксилол источника бромида; выдерживание реакционной смеси при давлении, по меньшей мере, около 1600 килопаскалей (КПа) и при температуре примерно от 130°С до примерно 200°С; введение газа, содержащего молекулярный кислород, в реакционную смесь со скоростью, по меньшей мере, примерно 0,5 норм. м3 газа/час на килограмм (кг) галоген-орто-ксилола в реакционной смеси в течение времени, достаточного для 90-процентной конверсии галоген-орто-ксилола с получением галогенфталевой кислоты.
В другой форме выполнения способ получения галогенфталевого ангидрида состоит из приготовления реакционной смеси, включающего смешивание примерно от 7 до примерно 3 весовых частей уксусной кислоты с 1 весовой частью галоген-орто-ксилола, примерно от 0,25 до примерно 2 мол. процентами в расчете на указанный галоген-орто-ксилол источника кобальта, примерно от 0,1 до примерно 1 мол. процента в расчете на указанный галоген-орто-ксилол источника марганца, примерно от 0,01 до примерно 0,1 мол. процента в расчете на указанный галоген-орто-ксилол источника металла, выбранного из циркония, гафния и их смесей, и от примерно 0,02 до примерно 0,1 мол. процента в расчете на указанный галоген-орто-ксилол источника бромида; выдерживания реакционной смеси при давлении, по меньшей мере, около 1600 килопаскалей (КПа) и при температуре примерно от 130°С до примерно 200°С; введения газа, содержащего молекулярный кислород, в реакционную смесь со скоростью, по меньшей мере, примерно 0,5 норм. м3 газа/час на килограмм (кг) галоген-орто-ксилола в течение времени, достаточного для 90-процентной конверсии галоген-орто-ксилола с получением галогенфталевой кислоты с менее чем примерно 600 частями на миллион (ч/млн) галогенфталида; удаления уксусной кислоты и любой воды, образовавшейся в результате реакции, путем дистилляции; и дегидратирования галогенфталевой кислоты с образованием галогенфталевого ангидрида.
В еще одной форме выполнения способ получения галогенфталевой кислоты состоит из приготовления реакционной смеси, включающего смешивание примерно от 7 до примерно 3 весовых частей уксусной кислоты с 1 весовой частью галоген-орто-ксилола, примерно от 0,8 до примерно 1,2 мол. процента в расчете на галоген-орто-ксилол источника кобальта, примерно от 0,4 до примерно 0,6 мол. процента в расчете на указанный галоген-орто-ксилол источника марганца, примерно от 0,04 до примерно 0,06 мол. процента в расчете на указанный галоген-орто-ксилол источника металла, выбранного из циркония, гафния и их смесей, и менее примерно 0,04 мол. процента в расчете на указанный галоген-орто-ксилол источника бромида; выдерживания реакционной смеси при давлении, по меньшей мере, около 1600 килопаскалей (кПа) и при температуре примерно от 130°С до примерно 200°С; введения газа, содержащего молекулярный кислород, в реакционную смесь со скоростью, по меньшей мере, примерно 0,5 норм. м3 газа/час на килограмм (кг) галоген-орто-ксилола в течение времени, достаточного для 90-процентного превращения указанного галоген-орто-ксилола в галогенфталевую кислоту.
В другой форме выполнения способ получения галогенфталевого ангидрида состоит из приготовления реакционной смеси, включающего смешивание примерно от 7 до примерно 3 весовых частей уксусной кислоты с 1 весовой частью галоген-орто-ксилола, примерно от 0,8 до примерно 1,2 мол. процента в расчете на указанный галоген-орто-ксилол ацетата кобальта или гидратацетата кобальта, примерно от 0,4 до примерно 0,6 мол. процента в расчете на указанный галоген-орто-ксилол ацетата марганца или гидратацетата марганца, примерно от 0,04 до примерно 0,06 мол. процента в расчете на указанный галоген-орто-ксилол ацетата циркония или гидратацетата циркония, менее 0,04 мол. процента в расчете на указанный галоген-орто-ксилол бромида натрия; выдерживания реакционной смеси при давлении, по меньшей мере, около 1600 килопаскалей (КПа) и при температуре примерно от 130°С до примерно 200°С; введения газа, содержащего молекулярный кислород, в реакционную смесь со скоростью, по меньшей мере, примерно 0,5 норм. м3 газа/час на килограмм (кг) галоген-орто-ксилола в реакционной смеси в течение времени, достаточного для 90-процентного превращения указанного галоген-орто-ксилола в галогенфталевую кислоту; удаления уксусной кислоты и любой воды, образовавшейся в результате реакции, путем дистилляции; отделения воды от уксусной кислоты и рециркуляции уксусной кислоты; и дегидратирования галогенфталевой кислоты с образованием галогенфталевого ангидрида.
В еще одной форме выполнения способ получения полиэфиримида состоит из приготовления реакционной смеси, включающего смешивание примерно от 7 до примерно 3 весовых частей уксусной кислоты с 1 весовой частью галоген-орто-ксилола, примерно от 0,25 до примерно 2 мол. процентами в расчете на галоген-орто-ксилол источника кобальта, примерно от 0,1 до примерно 1 мол. процента в расчете на указанный галоген-орто-ксилол источника марганца, примерно от 0,01 до примерно 0,1 мол. процента в расчете на указанный галоген-орто-ксилол источника металла, выбранного из циркония, гафния и их смесей, и от примерно 0,02 до примерно 0,1 мол. процента в расчете на указанный галоген-орто-ксилол источника бромида; выдерживания реакционной смеси при давлении, по меньшей мере, около 1600 килопаскалей (КПа) и при температуре примерно от 130°С до примерно 200°С; введения газа, содержащего молекулярный кислород, в реакционную смесь со скоростью, по меньшей мере, примерно 0,5 норм. м3 газа/час на килограмм (кг) галоген-орто-ксилола в реакционной смеси в течение времени, достаточного для 90-процентного превращения галоген-орто-ксилола в галогенфталевую кислоту с менее чем примерно 600 частями на миллион (ч/млн) галогенфталида; удаления уксусной кислоты и любой воды, образовавшейся в результате реакции, путем дистилляции; и дегидратирования галогенфталевой кислоты с образованием галогенфталевого ангидрида; взаимодействия галогенфталевого ангидрида с 1,3-диаминобензола с образованием бис(галогенфталимида) (II)
где Х представляет галоген; и взаимодействия бис(галогенфталимида) с солью щелочного металла дигидроксизамещенного ароматического углеводорода, имеющего формулу (IV)
ОН-А2ОН (IV)
где А2 представляет двухвалентный ароматический углеводородный радикал, с образованием полиэфиримида.
Способ получения галогенфталевой кислоты состоит из приготовления реакционной смеси, включающего смешивание примерно от 7 до примерно 3 весовых частей уксусной кислоты с 1 весовой частью галоген-орто-ксилола, примерно от 0,25 до примерно 2 мол. процентами в расчете на галоген-орто-ксилол источника кобальта, примерно от 0,1 до примерно 1 мол. процента в расчете на галоген-орто-ксилол источника марганца, примерно от 0,01 до примерно 0,1 мол. процента в расчете на галоген-орто-ксилол источника металла, выбранного из циркония, гафния и их смесей, и от примерно 0,02 до примерно 0,1 мол. процента в расчете на галоген-орто-ксилол источника бромида. Реакционную смесь выдерживают при давлении, по меньшей мере, около 1600 КПа и при температуре примерно от 130°С до примерно 200°С. Вводят газ, содержащий молекулярный кислород, в реакционную смесь со скоростью, по меньшей мере, примерно 0,5 норм. м3 содержащего кислород газа/час на килограмм (кг) галоген-орто-ксилола в течение времени, достаточного, по меньшей мере, для 90-процентного превращения галоген-орто-ксилола в галогенфталевую кислоту. Введение газа, содержащего молекулярный кислород, приводит к получению содержащего кислород отходящего газа, который предпочтительно имеет концентрацию кислорода менее примерно 3 объемных процентов в расчете на отходящий газ.
При использовании способа получения галогенфталевой кислоты и ангидрида, описанного выше, возможен синтез с высоким выходом галогенфталевой кислоты и галогенфталевого ангидрида высокой чистоты в промышленном масштабе с использованием сотен килограммов галоген-орто-ксилола путем жидкофазного окисления в присутствии от примерно 0,25 до примерно 2 мол. процентов (мол.%) источника кобальта, от примерно 0,1 до примерно 1 мол.% источника марганца, от примерно 0,01 до примерно 0,1 мол.% источника металла, выбранного из циркония, гафния и их смесей, и от примерно 0,02 до примерно 0,1 мол.% источника бромида. Было показано, что при крупномасштабном жидкофазном окислении с использованием галоген-орто-ксилола количество бромида может значительно влиять на количество примесей, присутствующих в конечном продукте. Использование пониженного молярного процентного содержания бромида приводит к образованию продукта, галогенфталевой кислоты или ангидрида, со сниженным содержанием примесей, таких как галогенфталид. Поскольку причины этого феномена не полностью понятны, полагают, что даже более низкие количества бромида, молярной концентрации менее примерно 0,02, могут быть пригодны для производства галогенфталевой кислоты или галогенфталевого ангидрида с высокой чистотой даже при более крупномасштабном жидкофазном окислении, например, с использованием тысяч килограммов галоген-орто-ксилола.
Галоген-орто-ксилол, подходящий для использования в реакции окисления, имеет структуру (IV)
где Х представляет галоген. Предпочтительно Х является хлором. Галогеновый заместитель может быть в 3 положении (3-изомер) или 4 положении (4-изомер). Галоген-орто-ксилол, используемый в жидкофазном окислении, может быть также смесью 3-изомера и 4-изомера.
При жидкофазном окислении в качестве растворителя предпочтительно используется уксусная кислота, хотя можно использовать и другие низшие карбоновые кислоты, что понятно специалисту в данной области. В основном можно использовать уксусную кислоту с содержанием воды до примерно 3 процентов. Обычно уксусная кислота присутствует в количестве от 7 до 3 весовых частей на 1 весовую часть галоген-орто-ксилола. Предпочтительно уксусная кислота присутствует в количестве от 5 до 3 весовых частей на одну весовую часть галоген-орто-ксилола.
Подходящие газы, содержащие молекулярный кислород, включают газы или комбинации газов, которые являются источником молекулярного кислорода (О2), например 100% кислород и смеси кислорода с инертным газом с концентрацией кислорода, достаточной для осуществления окисления. Достаточные концентрации кислорода обычно больше или равны примерно 6% кислорода, предпочтительно более или равны примерно 15%, более предпочтительно более или равны примерно 20%. Понятно, что можно также использовать смеси с содержанием более или равным 50% кислорода. Как будет понятно специалисту в данной области, концентрация кислорода может влиять на скорость реакции. Предпочтительным газом, содержащим кислород, является воздух.
Пригодными источниками кобальта, марганца, бромида, циркония и гафния являются источники, растворимые в уксусной кислоте. Источники кобальта, марганца, циркония или гафния включают сами металлы или любые их соли, комплексы или соединения. Эти вещества включают, но не ограничиваются этим, ацетаты, цитраты, стеараты, нафтенаты, ацетилацетонаты, бензоилацетонаты, карбонаты, сульфаты, бромиды, хлориды, фториды, нитраты, гидроксиды, алкоксиды, нитриды, трифлаты, их гидраты и их смеси. Предпочтительно кобальт в источнике кобальта находится в +2 или +3 окисленном состоянии. Предпочтительно марганец в источнике марганца находится в +2 или +3 окисленном состоянии. Примеры бромидных источников включают, но не ограничиваются этим, бром, бромистый водород, бромидную соль металла, такую как бромид натрия, и органические бромиды. Примеры органических бромидов включают тетрабромэтан, этилбромид, этиленбромид, бромоформ, ксилилбромид, ксилиленбромид и смеси, содержащие, по меньшей мере, один из органических бромидов.
Мольный процент (мол.%) кобальта, марганца, циркония, гафния и брома (бромида) рассчитывают на количество галоген-орто-ксилола, присутствующего в начале реакции. Источник кобальта обычно присутствует в количестве от примерно 0,25 до примерно 2 мол.%. Предпочтительно источник кобальта присутствует в количестве менее примерно 1,2 мол.%. Кроме того, предпочтительно также, чтобы источник кобальта присутствовал в количестве, более или равном примерно 0,5 мол.%, и более предпочтительно в количестве, более или равном примерно 0,8 мол.%. Особенно предпочтительно, чтобы источник кобальта составлял примерно 1%.
Источник марганца присутствует в количестве от примерно 0,1 до примерно 1 мол.%. Предпочтительно источник марганца присутствует в количестве, менее или равном примерно 0,6 мол.%. Кроме того, предпочтительно, чтобы источник марганца присутствовал в количестве, более или равном примерно 0,3 мол.%, более предпочтительно более или равном примерно 0,4 мол.%. В особенно предпочтительной форме выполнения источник марганца присутствует в количестве, равном примерно 0,5 мол.%.
Источник бромида обычно присутствует в количестве от примерно 0,02 до примерно 0,1 мол.%. Предпочтительно количество источника бромида менее или равно 0,8 мол.%, более предпочтительно менее или равно примерно 0,5 мол.%, еще предпочтительнее менее или равно 0,4% и наиболее предпочтительно менее или равно 0,3 мол.%.
Источник циркония, источник гафния или их смесь обычно присутствуют в количествах от примерно 0,01 до примерно 0,1 мол.%. Предпочтительно источник циркония, источник гафния или их смесь обычно присутствуют в количестве, менее или равном примерно 0,06 мол.%. Кроме того, предпочтительно также, чтобы источники циркония, источники гафния или их смеси присутствовали в количестве, более или равном примерно 0,03 мол.%, более предпочтительно более 0,04 мол.%. В особенно предпочтительной форме выполнения источник циркония, источник гафния или их смесь присутствуют в количестве примерно 0,05 мол.%.
При типовом способе галогенфталевая кислота может быть получена путем смешивания галоген-орто-ксилола, источника кобальта, источника марганца, источника брома и источника циркония, источника гафния или их смеси в уксусной кислоте в реакционном сосуде. В реакционном сосуде устанавливается давление более примерно 1600 КПа при желаемой температуре. Температура реакция обычно составляет от примерно 130°С до примерно 200°С, предпочтительно от примерно 150°С до 170°С и более предпочтительно более примерно 160°С. Затем вводят содержащий кислород газ. Поток газа, содержащего молекулярный кислород, обеспечивается содержащим кислород отходящим газом, который предпочтительно имеет концентрацию кислорода менее 3 об.%, предпочтительно менее примерно 1 об.%. Концентрация кислорода в отходящем газе может быть определена с помощью анализа парамагнитной трансдукции кислорода или другого известного специалистам метода. Используемый расход газа обычно более или равен 0,5 норм. куб. метра (м3)/час на килограмм (кг) галоген-орто-ксилола и предпочтительно более или равен 1,0 норм. куб. метру (м3)/час на килограмм (кг) галоген-орто-ксилола. Норм. куб. метр определяется как кубический метр в условиях стандартных температуры и давления. Предпочтительно реакционную смесь перемешивают, используя стандартные методы, такие как механическое перемешивание. Поток газа, содержащего молекулярный кислород, поддерживают до тех пор, пока, по меньшей мере, примерно 90% галоген-орто-толуола не превратится в галогенфталевую кислоту, предпочтительно до тех пор, пока не превратится 95%. Степень конверсии, достигаемая при реакции, может быть легко определена посредством использования газовой хроматографии, масс-спектрометрии или других способов, известных специалистам. На практике время, необходимое для достижения 90% конверсии галоген-орто-ксилола, составляет от примерно 3 до примерно 6 часов.
Кроме того, способ получения галогенфталевой кислоты или галогенфталевого ангидрида может включать необязательную стадию контроля концентрации кислорода в отходящем газе. Если концентрация кислорода в отходящем газе превышает примерно 3 об.%, имеет место замедление реакции. Если концентрация кислорода в отходящем газе превышает примерно 3 об.%, поток газа, содержащего молекулярный кислород, может быть модифицирован таким образом, чтобы поддерживать концентрацию кислорода в отходящем газе ниже примерно 5 об.%. Поток газа, содержащего молекулярный кислород, может быть изменен несколькими путями. Газ, содержащий молекулярный кислород, может быть разбавлен инертным газом таким образом, чтобы снизить концентрацию кислорода в газе, содержащем молекулярный кислород; расход газа, содержащего молекулярный кислород, может быть снижен; источник газа, содержащего молекулярный кислород, может быть изменен с тем, чтобы использовался газ, содержащий молекулярный кислород с более низкой концентрацией кислорода, или эти способы можно комбинировать, чтобы поддерживать концентрацию кислорода в отходящем газе ниже 5 об.%. Измененный поток газа, содержащего молекулярный кислород, может затем сохраняться до тех пор, пока, по меньшей мере, примерно 90% галоген-орто-ксилола не будет превращено в галогенфталевую кислоту, предпочтительно до тех пор, пока не будет превращено более 95%. Степень конверсии, достигаемая при реакции, может быть легко определена с помощью газовой хроматографии, масс-спектрометрии и других методов, известных специалистам.
После того как реакция достигает желаемого уровня завершенности, галогенфталевая кислота может быть выделена в виде галогенфталевой кислоты или галогенфталевого ангидрида. Во многих случаях использования, таких как фармацевтическое применение и полимерный синтез, требуется галогенфталевая кислота и галогенфталевый ангидрид высокой степени чистоты. Такая высокая степень чистоты может быть достигнута способами, раскрытыми в описании. Фактически, легко можно получить галогенфталевую кислоту и галогенфталевый ангидрид, содержащие менее примерно 600 ч/млн галогенфталида, предпочтительно менее примерно 500 ч/млн галогенфталида и более предпочтительно менее примерно 400 ч/млн галогенфталида. Кроме того, можно также получить хлорфталевую кислоту и хлорфталевый ангидрид, содержащие менее примерно 1 вес.% фталевого ангидрида и хлорбензойной кислоты. Хлортолуиловые кислоты и дихлорфталевые кислоты обычно не обнаруживаются.
Большая часть уксусной кислоты, а также воды, получаемой при реакции, может быть удалена путем дистилляции при примерно атмосферном давлении, обычно при нагревании до примерно 200°С при 200 КПа. Уксусную кислоту и воду удаляют в виде пара и конденсируют. Воду затем можно отделить от уксусной кислоты, и уксусная кислота может быть направлена на рециклизацию. Некоторая дегидратация галогенфталевой кислоты с образованием галогенфталевого ангидрида может происходить одновременно с удалением уксусной кислоты и воды. Кроме того, удаление уксусной кислоты и воды может быть объединено с дегидратацией в виде одной стадии. Дегидратация обычно осуществляется термически путем дистилляции под вакуумом при повышенной температуре, обеспечивающей одновременное проведение дегидратации и отделения галогенфталевого ангидрида от какого-либо количества остаточной уксусной кислоты и воды. Дегидратацию можно также осуществлять путем других химических реакций, хорошо известных специалистам в данной области, таких как обработка уксусным ангидридом. После дистилляции галогенфталевый ангидрид обычно имеет чистоту более примерно 95%, предпочтительно более примерно 97% и наиболее предпочтительно более примерно 99%. Галогенфталевые ангидриды высокой чистоты используют при синтезе полиэфиримида, огнеупорных технологических пластмасс.
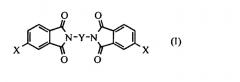
Полиэфиримиды являются огнеупорными технологическими пластмассами, имеющими разное применение. Один из путей синтеза полиэфиримидов проходит через бис(4-галогенфталимид), имеющий следующее строение (I):
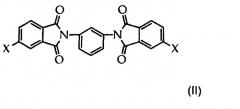
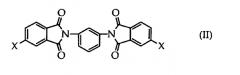
где Y представляет двухвалентную алкиленовую, циклоалкиленовую или ариленовую группу, и Х представляет галоген. Особенно пригоден бис(4-галогенфталимид), где Y представляет собой 1,3-фенильную группу (II).
Бис(галогенфталимид)ы (I) и (II) обычно образуются путем конденсации аминов, например 1,3-диаминобензола с ангидридами, например 4-галогенфталевым ангидридом (III):
Полиэфиримиды могут быть синтезированы путем реакции бис(галогенфталимида) с солью щелочного металла дигидроксизамещенного ароматического углеводорода в присутствии или в отсутствие катализатора фазового переноса. Подходящие катализаторы фазового переноса описаны в патенте США № 5229482, который включен в данное описание в виде ссылки. Подходящие дигидроксизамещенные ароматические углеводороды включают соединения формулы (IV)
ОН-А2-ОН (IV)
где А2 представляет двухвалентный ароматический углеводородный радикал. Подходящие А2 радикалы включают м-фенилен, п-фенилен, 4,4'-бифенилен, 4,4'-би(3,5-диметил)фенилен, 2,3-бис(4-фенилен)пропан и подобные радикалы, такие как название и формула которых описаны в патенте США № 4217438.
Радикал А2 предпочтительно имеет формулу (V)
-А3-Q-А4- (V)
где каждый из А3 и А4 представляет моноциклический двухвалентный ароматический углеводородный радикал, а Q представляет мостиковый углеводородный радикал, в котором один или два атома отделяют А3 от А4. Свободные валентные связи в формуле (V) обычно находятся в мета- или пара-положении А3 и А4 по отношению к Y. А3 и А4 могут быть замещены фениленом или его углеводородозамещенным производным, иллюстративными заместителями (одним или более) являются алкил и алкенил. Незамещенные фениленовые радикалы являются предпочтительными. Как А3, так и А4 предпочтительно являются п-фениленом, хотя оба могут быть о- или м-фениленом, или один о- или м-фениленом, а другой п-фениленом.
Мостиковый радикал Q является радикалом, в котором один или два атома, предпочтительно один атом, отделяют А3 от А4. Иллюстративными радикалами этого типа являются метилен, циклогексилметилен, 2-(2,2,1)-бициклогептилметилен, этилен, изопропилиден, неопентилиден, циклогексилиден и адамантилиден. Предпочтительным радикалом формулы (IV) является 2,2-бис(4-фенилен)пропановый радикал, который является производным от бисфенола А и в котором Q является изопропилиденом, и А3 и А4, каждый, является п-фениленом.
Специалисту в данной области понятно, что любые примеси, присутствующие в галогенфталевом ангидриде, будут проходить через последующие стадии в синтезе полиэфиримида. Присутствие значительного количества примесей на последующих стадиях может мешать полимеризации и вызывать изменение окраски конечного продукта, полиэфиримида.
Все процитированные патенты включены в данное описание в виде ссылки.
Далее изобретение поясняется нижеследующими примерами, не ограничивающими объема притязаний.
ПРИМЕРЫ 1-5
В реакторе в лабораторных условиях объединяли 492 грамма (г) (3,5 моль) хлор-орто-ксилола (смесь примерно 30% 3-хлор-орто-ксилола и примерно 70% 4-хлор-орто-ксилола), 1925 г ледяной уксусной кислоты, 8,7 г (1 мол.%) тетрагидрата ацетата кобальта, 4,3 г (0,05 мол.%) тетрагидрата ацетата марганца, 1,0 г (0,06 мол.%) раствора ацетата циркония, 4,3 г (1,5 мол.%) ацетата натрия и разные количества бромида натрия. Реактор заполняли азотом, создавали давление до 1900 кПа и нагревали до примерно 160°С. Затем в реактор вводили воздух через погруженную трубку. Сначала концентрация кислорода в отходящем газе была больше 0, но менее 1 процента. Реакционную смесь перемешивали в течение реакции. Через примерно 3 часа концентрация кислорода в отходящем газе повышалась до более 3 процентов. Подачу воздуха прекращали. В реактор вводили воздух, разбавленный азотом, чтобы концентрация кислорода в отходящем газе была равна примерно 5%, и температуру в реакторе повышали до примерно 190°С. Поток разбавленного воздуха поддерживали постоянным в течение от примерно 1 до 3 часов. Было установлено, что хлорфталевая кислота присутствует в количестве 25 мас.% от общего веса реакционной смеси. Большую часть воды, образовавшуюся при реакции, и уксусную кислоту удаляли при атмосферном давлении путем дистилляции. Хлорфталевую кислоту дегидратировали и любую остаточную воду и уксусную кислоту удаляли при нагревании и пониженном давлении с образованием хлорфталевого ангидрида. Хлорфталевый ангидрид отделяли от катализатора путем дистилляции под вакуумом при температуре дистилляции около 170°С. Выделенную хлорфталевую кислоту анализировали газовой хроматографией. Результаты представлены в таблице 1.
| Таблица 1 | |||
| Пример | NaBr | Количество полученных хлорфталидов | |
| мол.% | мас.% | ч/млн | |
| 1* | 1,0 | 0,57 | 5700 |
| 2* | 0,29 | 0,25 | 2500 |
| 3* | 0,14 | 0,01 | 100 |
| 4 | 0,03 | 0,46 | 4600 |
| 5* | 0,014 | 2,35 | 23500 |
| * сравнительные примеры |
Как можно видеть из примеров 1-5, хлорфталевый ангидрид с очень малыми количествами хлорфталида может быть получен в лабораторных условиях, однако необходимое количество бромида составляет более 0,05 мол.%.
ПРИМЕРЫ 6-10
При реакции в условиях пилотной установки объединяли 200 килограммов (кг) хлор-орто-ксилола (смесь 3-хлор-орто-ксилола и 4-хлор-орто-ксилола), 780 кг уксусной кислоты, 3,5 кг (1,0 мол.%) тетрагидратацетата кобальта, 1,75 кг (0,5 мол.%) тетрагидратацетата марганца, 0,4 кг (0,05 мол.%) раствора ацетата циркония, 1,75 кг (1,5 мол.%) ацетата натрия и разное количество бромида натрия. Количество бромида натрия изменяли, например, как показано в таблице 2. Реактор заполняли азотом, повышали давление до 1900 КПа и нагревали до примерно 160°С. В реактор вводили воздух через погруженную трубку при расходе, постепенно повышающемся до 200 норм. м3/час. Сначала концентрация кислорода в отходящем газе была больше 0, но менее 1 процента. Реакционную смесь перемешивали в течение реакции. Через 1 час температура реакции повышалась до 175°С. Через примерно 3 часа концентрация кислорода в отходящем газе повышалась до более 3 процентов. Подачу воздуха прекращали. В реактор вводили воздух, разбавленный азотом, чтобы концентрация кислорода в отходящем газе была равна примерно 5%, и температуру в реакторе повышали до примерно 190°С. Подачу разбавленного воздуха поддерживали постоянной в течение примерно 3 часов. Конечный вес содержимого реактора находился в соответствии с высокой конверсией хлор-орто-ксилола, определенной по поглощению 3 молей О2 с получением дикислоты и двух молей воды. Большую часть воды, образовавшуюся при реакции, и уксусную кислоту удаляли в условиях дистилляции при атмосферном давлении. Хлорфталевую кислоту дегидратировали и любую остаточную воду и уксусную кислоту удаляли при нагревании и пониженном давлении с образованием хлорфталевого ангидрида. Хлорфталевый ангидрид отделяли от катализатора путем дистилляции под вакуумом при температуре дистилляции около 170°С. Выделенную хлорфталевую кислоту анализировали газовой хроматографией. Результаты представлены в таблице 2.
| Таблица 2 | |||
| Пример | NaBr | Количество полученных хлорфталидов | |
| мол.% | мас.% | ч/млн | |
| 6* | 1,02 | 5,4 | 54000 |
| 7* | 0,14 | 0,24 | 2400 |
| 8* | 0,10 | 0,12 | 1200 |
| 9 | 0,03 | 0,02 | 200 |
| 10 | 0,02 | 0,03 | 300 |
| * сравнительные примеры |
Как можно видеть из приведенных примеров, можно получить хлорфталевый ангидрид с очень низким содержанием хлорфталида при проведении реакции в большом масштабе. Общая чистота полученной хлорфталевой кислоты в примерах 9 и 10 была более 98%.
ПРИМЕР 11
В реакторе в лабораторных условиях объединяли 40 граммов (г) (284 миллимоль (ммоль)) хлор-орто-ксилола (смесь примерно 30% 3-хлор-орто-ксилола и примерно 70% 4-хлор-орто-ксилола), 160 г ледяной уксусной кислоты, 567 миллиграммов (мг) (0,8 мол.%) тетрагидратацетата кобальта, 349 мг (0,5 мол.%) тетрагидратацетата марганца, 9,1 мг (0,06 мол.%) раствора ацетата циркония и 91 мг 30 вес.% раствора гидробромистого водорода в уксусной кислоте. Реактор заполняли азотом, повышали давление до 1900 КПа и нагревали до примерно 160°С. Затем в реактор вводили воздух через погруженную трубку. Сначала концентрация кислорода в отходящем газе была больше 0, но менее 1 процента. Реакционную смесь перемешивали в течение реакции. После 1 часа при температуре 160°С температура повышалась до примерно 175°С. Через примерно 3 часа концентрация кислорода в отходящем газе повышалась до более 3 процентов. Подачу воздуха прекращали. В реактор вводили воздух, разбавленный азотом, чтобы концентрация кислорода в отходящем газе была равна примерно 5%, и температуру в реакторе повышали до примерно 190°С. Подачу разбавленного воздуха продолжали в течение от примерно 1 до 3 часов. Реакционную смесь анализировали жидкостной хроматографией (ЖХ) и показали, что хлорфталевая кислота образовалась с выходом и чистотой, сравнимыми с результатами примера 2.
При использовании способа получения галогенфталевой кислоты и галогенфталевого ангидрида, раскрытого в описании, возможен синтез с высоким выходом галогенфталевой кислоты и галогенфталевого ангидрида высокой чистоты в большом масштабе с использованием сотен килограммов галоген-орто-ксилола путем жидкофазного окисления в присутствии от примерно 0,25 до примерно 2 мол.% источника кобальта, от примерно 0,1 до примерно 1 мол.% источника марганца, от примерно 0,01 до примерно 0,1 мол.% источника металла, выбранного из циркония, гафния и их смесей, и от примерно 0,02 до примерно 0,1 мол.% источника бромида. Показано, что при крупномасштабном жидкофазном окислении с использованием галоген-орто-ксилола количество бромида может значительно влиять на количество примесей, присутствующих в конечном продукте. Использование пониженного молярного процентного содержания бромида приводит к получению как галогенфталевой кислоты, так и галогенфталевого ангидрида со сниженным содержанием примесей, таких как галогенфталид. Хотя причины этого феномена точно не выяснены, полагают, что даже более низкие количества бромида, содержание в мол. процентах менее примерно 0,02, могут быть пригодны для получения галогенфталевой кислоты и галогенфталевого ангидрида высокой чистоты даже при крупномасштабном жидкофазном окислении с использованием тысяч килограммов галоген-орто-ксилола.
Хотя данное изобретение было описано со ссылками на предпочтительные формы осуществления, специалистам в данной области понятно, что могут быть произведены различные изменения и элементы могут быть заменены их эквивалентами, не выходя из объема притязаний данного изобретения. Кроме того, могут быть произведены многие изменения, чтобы адаптировать конкретную ситуацию или вещество в соответствии с указаниями данного изобретения, не выходя из объема притязаний изобретения. Поэтому предполагается, что данное изобретение не ограничивается конкретными формами выполнения, описанными как наилучший способ, предложенный для осуществления данного изобретения, и данное изобретение будет включать все формы выполнения, соответствующие объему прилагаемой формулы изобретения.
1. Способ получения галогенфталевой кислоты, включающий приготовление реакционной смеси, включающее
смешивание от 3 до 7 вес.ч. уксусной кислоты с 1 вес.ч. галоген-орто-ксилола,
с от 0,25 до 2 мол.% в расчете на указанный галоген-орто-ксилол источника кобальта,
с от 0,1 до 1 мол.% в расчете на указанный галоген-орто-ксилол источника марганца,
с от 0,01 до 0,1 мол.% в расчете на указанный галоген-орто-ксилол источника металла, выбранного из циркония, гафния и их смесей,
с от 0,02 до 0,1 мол.% в расчете на указанный галоген-орто-ксилол источника бромида;
причем галоген-орто-ксилол имеет формулу (IV)
где Х представляет собой галоген;
выдерживание реакционной смеси при давлении, по меньшей мере, 1600 кПа и при температуре от 130 до 200°С;
введение газа, содержащего молекулярный кислород, в реакционную смесь при расходе, по меньшей мере 0,5 норм. м3 газа/час на килограмм (кг) галоген-орто-ксилола в реакционной смеси в течение времени, достаточного для 90%-ной конверсии галоген-орто-ксилола с получением галогенфталевой кислоты.
2. Способ по п.1, в котором введение газа, содержащего молекулярный кислород, в указанную реакционную смесь производится отходящим газом, содержащим кислород, причем концентрация кислорода в указанном отходящем газе, содержащем кислород, составляет менее примерно одного объемного процента в расчете на указанный отходящий газ и, кроме того, включает поддержание введения газа, содержащего молекулярный кислород, до тех пор, пока концентрация кислорода в отходящем газе не превысит 3 об.% в расчете на указанный отходящий газ, и изменение введения указанного газа, содержащего молекулярный кислород, для поддержания концентрации кислорода в отходящем газе в количестве ниже 5 об.% в расчете на указанный отходящ