Тоник для роста волос
Иллюстрации
Показать всеИзобретение относится к биологически активному соединению, применимому в медицине и косметологии для изготовления средств, способствующих росту волос. Соединение представлено формулой (I), где R1 и R2 являются одинаковыми или разными, и каждый из них представляет собой атом водорода, C1-6-алкильную группу или С2-6-алканоильную группу; Х представляет собой атом водорода или атом галогена; R3a и R3b являются разными, и каждый из них представляет собой атом водорода или гидроксильную группу; и R4, R5, R6, R7, R8 и R9 являются одинаковыми или разными, и каждый из них представляет собой атом водорода, гидроксильную группу, атом галогена или С2-6-алканоилоксигруппу, или указанные группы, которые являются смежными, вместе образуют π связь или эфирную связь, или R5 и R8 или R5 и R9 вместе образуют эфирную связь. Техническим реультатом является расширение арсенала химических соединений, обладающих активностью ингибирования продукции WNT-5A и стимулирующих рост клеток сосочков дермы. 8 ил., 4 табл.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к промотору роста клеток сосочков дермы, к стимулятору роста волос и к тонику для роста волос. Более конкретно, оно относится к промотору роста клеток сосочков дермы, к стимулятору роста волос и к тонику для роста волос, включающему в качестве активного ингредиента ингибитор функции WNT-5A. Кроме того, настоящее изобретение относится к способу скрининга промотора роста клеток сосочков дермы, основанному на эффекте ингибирования функции WNT-5A.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Волосяные фолликулы человека состоят из эпителиальных и мезенхимальных клеток дермы, таких как кератиноциты, клетки сосочков дермы, фибробласты и сальные клетки, и цикл роста волос (цикл развития волоса) контролируется через взаимодействия между этими клетками. Стержневая структура волоса формируется посредством пролиферации/дифференцировки (кератинизации) фолликулярных кератиноцитов. Сосочки дермы регулируют пролиферацию, дифференцировку и апоптоз этих фолликулярных кератиноцитов и, таким образом, играют ключевую роль в контроле цикла развития волоса. Поэтому при разработке стимулятора роста волос/тоника для роста волос, важно исследовать действие на клетки сосочков дермы. Однако молекулярный механизм, регулирующий способность клеток сосочков дермы к пролиферации и способность контролировать цикл роста волос, до настоящего времени оставался практически не выясненным.
С другой стороны, WNT-5A представляет собой секреторный гликопротеин, относящийся к семейству WNT. Семейство WNT включает около 20 видов молекул, встречающихся в широком ряде организмов, от нематод до млекопитающих. Известно, что эти WNT являются важными межклеточными сигнальными молекулами, регулирующими формирование позвоночника и формирование органов на стадии развития плода (Annu. Rev. Cell Dev. Biol., 14, 59-88 (1998); Genes & Dev. 11, 3286-3305 (1997)). У человека существует 10 видов рецепторов WNT, которые являются Frizzled семиканальными трансмембранными рецепторами (Annu. Rev. Cell Dev. Biol., 14, 59-88 (1998), Genes & Dev., 11, 3286-3305 (1997)). В зависимости от комбинаций связи WNT-Frizzled существует 3 типа пути сигнальной трансдукции (т.е., путь WNT/β-катенин, путь PCP и путь WNT/Ca2+) (Annu. Rev. Cell Dev. Biol., 14, 59-88 (1998)).
В последние годы было выяснено, что путь WNT/β-катенин является фундаментальным для формирования волосяных фолликул (Genes & Dev., 8, 2691-2703 (1994); Cell, 95, 605-614 (1998); Dev. Biol., 207, 133-149 (1999); Genes & Dev., 14, 1181-1185 (2000); Cell, 105, 533-545 (2001)). В 1988 была получена трансгенная мышь со стабилизированным β-катенином в коже. Сообщалось, что такая мышь демонстрировала повышенный de novo фолликулярный морфогенез, и в результате это приводило к гипертрихозу (Cell, 95, 605-614 (1998)). В 2000 году было сообщение, что сигнальный путь WNT/β-катенин играет важную роль в поддержании активности сосочков дермы, индуцирующих рост волос (Genes & Dev., 14, 1181-1185 (2000)).
Однако было выяснено, что сигнальная трансдукция от WNT-5A опосредована не путем WNT/β-катенин, а путем Ca2+ (Dev. Biol., 182, 114-120 (1997); Curr. Biol., 9, 695-698 (1999)), и до настоящего времени не было никаких сообщений относительно взаимосвязи между WNT-5A и фолликулярным морфогенезом.
Кроме того, сообщалось, что дупликация эмбрионной оси индуцируется инъекцией мРНК WNT-5A Xenopus laevis вместе с мРНК Frizzled 5 человека в эмбрион Xenopus laevis на ранней стадии развития (Science, 275, 1652-1654 (1997)), тогда как дупликация оси, индуцированная инъекцией мРНК WNT-1 или WNT-8, ингибируется посредством WNT-5A (J. Cell Biol., 133, 1123-1137 (1996)), и что WNT-5A Xenopus laevis связывается с Frizzled 2 крысы и активирует CamKII (Ca2+/калмодулин-зависимая протеинкиназа II) и PKC (протеинкиназа II) через путь Ca2+ (Curr. Biol., 9, 695-698 (1999)). Однако физиологическое значение этого до сих пор остается неизвестным, и не было никаких сообщений относительно взаимосвязи между WNT-5A и стимуляцией роста волос/промотированием роста волос.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Целью настоящего изобретения является разработка способа скрининга с использованием молекулы, регулирующей пролиферацию клеток сосочков дермы, промотора роста клеток сосочков дермы и стимулятора роста волос, а также тоника для роста волос на основе новой функции.
Для достижения этих целей авторы настоящего изобретения провели интенсивные исследования. В результате они обнаружили, что WNT-5A является высоко экспрессируемым в клетках сосочков дермы и что WNT-5A связан с пролиферирующей способностью клеток сосочков дермы. В результате последующих исследований на основании этого открытия авторы, кроме того, обнаружили, что рост клеток сосочков дермы может быть существенно активирован и такие части фолликул, как волосяные луковицы могут быть увеличены путем ингибирования функции WNT-5A, таким образом, было создано настоящее изобретение.
В одном варианте осуществления настоящее изобретение относится к промотору роста клеток сосочков дермы, который включает соединение, обладающее активностью ингибирования функции WNT-5A.
В другом варианте осуществления настоящее изобретение относится к промотору роста клеток сосочков дермы, который включает соединение, обладающее активностью ингибирования продукции WNT-5A.
Еще в одном варианте осуществления настоящее изобретение относится к соединению, представленному формулой (I):
где R1 и R2 являются одинаковыми или разными, и каждый из них представляет собой атом водорода, C1-6-алкильную группу или С2-6-алканоильную группу;
X представляет собой атом водорода или атом галогена;
R3a и R3b являются одинаковыми или разными, и каждый из них представляет собой атом водорода или гидроксильную группу; и
R4, R5, R6, R7, R8 и R9 являются одинаковыми или разными, и каждый из них представляет собой атом водорода, гидроксильную группу, атом галогена или С2-6 алканоилокси группу, или указанные группы, которые являются смежными, вместе образуют π связь или эфирную связь, или R5 и R8, или R5 и R9 вместе образуют эфирную связь.
Еще в одном варианте осуществления настоящее изобретение относится к промотору роста клеток сосочков дермы, который включает соединение, представленное формулой (II):
где R1 и R2 являются одинаковыми или разными, и каждый из них представляет собой атом водорода, C1-6-алкильную группу или С2-6-алканоильную группу;
X представляет собой атом водорода или атом галогена;
R3c и R3d являются одинаковыми или разными, и каждый из них представляет собой атом водорода, гидроксильную группу или С1-6-алкоксигруппу, или R3c и R3d вместе образуют оксогруппу, гидроксииминогруппу или С1-6-алкоксииминогруппу; и
R4, R5, R6, R7, R8 и R9 являются одинаковыми или разными, и каждый из них представляет собой атом водорода, гидроксильную группу, атом галогена или С2-6-алканоилоксигруппу, или указанные группы, которые являются смежными, вместе образуют π связь или эфирную связь, или R5 и R8, или R5 и R9 вместе образуют эфирную связь.
В следующем варианте осуществления настоящее изобретение относится к промотору роста клеток сосочков дермы, включающему соединение, представленное формулой (IX):
где R1a и R2a являются одинаковыми или разными, и каждый из них представляет собой атом водорода, C1-6-алкильную группу, C2-6-алканоильную группу,
группу, представленную формулой (CH2)pCO-Y-R10 (где Y представляет собой атом кислорода или атом серы; R10 представляет собой атом водорода, C1-6-алкильную группу или замещенную или незамещенную арильную группу; и p имеет значение 0 или 1),
группу, представленную формулой (CH2)qR11 (где R11 представляет собой замещенную или незамещенную циклоалкильную группу или замещенный или незамещенный C2-10 гетероцикл; и q имеет значение 0 или 1), или
группу, представленную формулой COR12 (где R12 представляет собой замещенную или незамещенную арильную группу или замещенный или незамещенный C2-10-гетероцикл);
X представляет собой атом водорода или атом галогена;
R3e и R3f являются одинаковыми или разными, и каждый из них представляет собой атом водорода, гидроксильную группу, C1-6-алкоксигруппу или С1-6-алканоилоксигруппу, или R3e и R3f вместе образуют оксогруппу, гидроксиимино группу или С1-6-алкоксииминогруппу; и
R4a, R5a, R6a, R7a, R8a и R9a являются одинаковыми или разными, и каждый из них представляет собой атом водорода, гидроксильную группу, атом галогена или
группу, представленную формулой Z-R13 (где Z представляет собой атом кислорода или атом серы; и R13 представляет собой C1-6-алкильную группу, C1-6-алканоильную группу или замещенную или незамещенную арильную группу), или
указанные группы, которые являются смежными, вместе образуют π связь или эфирную связь, или
R5a и R8a или R5a и R9a вместе образуют эфирную связь; и
R6b представляет собой атом водорода, или вместе с R3e или R3f образует эфирную связь.
В следующем варианте осуществления настоящее изобретение относится к стимулятору роста волос или к тонику для роста волос, содержащему в качестве активного ингредиента указанный выше промотор роста клеток сосочков дермы.
В следующем варианте осуществления настоящее изобретение относится к способу скрининга промотора роста клеток сосочков дермы, который включает отбор вещества, ингибирующего функцию WNT-5A.
И в еще одном варианте осуществления настоящее изобретение относится к способу отбора вещества, ингибирующего функцию WNT-5A, который представляет собой способ скрининга промотора роста клеток сосочков дермы, включающий следующие стадии (a)-(c):
(a) стадию культивирования клеток, экспрессирующих WNT-5A человека, в среде, к которой добавлено испытываемое соединение;
(b) стадию лизинга клеток, экспрессирующих WNT-5A человека, культивированных на стадии (a), для экстракции РНК и определения количества мРНК WNT-5A; и
(c) стадию сравнения количества мРНК WNT-5A, определенного на стадии (b).
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1 показывает картину электрофореза, демонстрирующую, что мРНК WNT-5A экспрессируется в клетках сосочков дермы.
Фиг. 2 показывает картину электрофореза, демонстрирующую, что испытываемые соединения вызывают снижение количества мРНК WNT-5A в клетках сосочков дермы.
Фиг. 3 показывает график, демонстрирующий, что испытываемые соединения обладают активностью промотора роста клеток сосочков дермы.
Фиг. 4 показывает картину электрофореза, демонстрирующую снижение количества мРНК WNT-5A в органной культуре кожи обезьяны.
Фиг. 5 показывает результаты PCNA-окрашивания в телогенных и анагенных волосяных фолликулах в органной культуре кожи обезьяны.
Фиг. 6 показывает гистограммы, демонстрирующие, что Соединение 7 увеличивает диаметр волосяной луковицы в органной культуре кожи обезьяны.
Фиг. 7 показывает гистограммы, демонстрирующие, что Соединение 3 увеличивает диаметр волосяной луковицы в органной культуре кожи обезьяны.
Фиг. 8 показывает фотографии кожи до и после применения испытываемого соединения в течение 6 месяцев в испытании роста волос у медвежьего макака (Macaca arctoides).
ЛУЧШИЙ СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Далее настоящее изобретение описывается более подробно.
<Соединение, ингибирующее функцию WNT-5A>
Термин "соединение, ингибирующее функцию WNT-5A" (далее в некоторых случаях называется "ингибитор функции WNT-5A"), в настоящем изобретении означает соединение, ингибирующее связывание WNT-5A с рецептором WNT-5A, или соединение, ингибирующее продукцию WNT-5A, предпочтительно соединение, ингибирующее продукцию WNT-5A.
Было подтверждено, что WNT-5A, являющийся секреторным гликопротеином, принадлежащим к семейству WNT, экспрессируется в организме человека, мыши, крысы, Xenopus laevis и т.д. С точки зрения применения в качестве лекарственного средства, соединение, ингибирующее функцию WNT-5A человека (SEQ ID NO:1), является предпочтительным.
Соединение, ингибирующее связывание WNT-5A с рецептором WNT-5A, означает соединение, которое действует на WNT-5A или рецептор WNT-5A и, таким образом, ингибирует связывание WNT-5A с рецептором WNT-5A, регулируя тем самым трансдукцию сигнала, осуществляемую WNT-5A, предпочтительно представляет собой соединение, регулирующее трансдукцию сигнала через Ca2+ путь. Примеры таких соединений включают антагонист рецептора WNT-5A. Конкретные примеры рецептора WNT-5A включают Frizzled 5 человека (SEQ ID NO:4) и Frizzled 2 крысы (SEQ ID NO:6). Хотя такое соединение может быть как пептидным, так и непептидным, непептидный ингибитор является предпочтительным, имеет преимущество более длительного действия. Соединение может быть отобрано при помощи системы скрининга, использующей меченый WNT-5A и рецептор WNT-5A, и предпочтительно имеет ИК50, равную 30 мкМ или меньше, и более предпочтительно ИК50, равную 10 мкМ или меньше.
Соединение, ингибирующее продукцию WNT-5A, означает соединение, ингибирующее экспрессию гена WNT-5A. Хотя такое соединение может быть как пептидным, так и непептидным, непептидный ингибитор является предпочтительным, имеет преимущество более длительного действия. Соединение может быть выбрано с использованием в качестве показателя снижения количества белка WNT-5A (SEQ ID NO:1) или количества мРНК WNT-5A (SEQ ID NO:2), и предпочтительно имеет ИК50, равную 30 мкМ или меньше, и более предпочтительно 10 мкМ или меньше, как определено в испытании с использованием нуклеиновокислотного зонда в соответствии с методом Hartley et al. (Drug Metabolism and Disposition, 28(5), 608-616 (2000); Пример испытания 4, описанный ниже).
Соединения, представленные формулами (I), (II) и (IX), являются особенно предпочтительными.
В соединениях, представленных формулами (I), (II) и (IX), C1-6-алкильная группа означает линейную или разветвленную алкильную группу, содержащую от 1 до 6 атомов углерода, и примеры такой группы включают метильную группу, этильную группу, пропильную группу, изопропильную группу, бутильную группу, изобутильную группу, трет-бутильную группу, пентильную группу, 2-этилпропильную группу, гексильную группу и т.д.
C1-6-алканоильная группа означает линейную или разветвленную алканоильную группу, содержащую от 1 до 6 атомов углерода, и примеры таких групп включают ацетильную группу, пропионильную группу, бутирильную группу, трет-бутирильную группу и т.д.
Группа C1-6-алкокси означает линейную или разветвленную алкоксигруппу, содержащую от 1 до 6 атомов углерода, и примеры таких групп включают метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу, бутоксигруппу, изобутоксигруппу, втор-бутоксигруппу, трет-бутоксигруппу, пентилоксигруппу, изопентилоксигруппу, неоизопентилоксигруппу, трет-пентилоксигруппу, 1-метилбутоксигруппу, 2-метилбутоксигруппу, 1,2-диметилпропоксигруппу, гексилоксигруппу, изогексилоксигруппу и т.д.
Группа C1-6-алкоксиимино означает линейную или разветвленную алкоксииминогруппу, содержащую от 1 до 6 атомов углерода, и примеры таких групп включают N-метоксииминогруппу, N-этоксииминогруппу, N-пропоксииминогруппу, N-изопропоксииминогруппу, N-бутоксииминогруппу, N-изобутоксииминогруппу, N-пентилоксииминогруппу, N-гексилоксииминогруппу и т.д.
Группа C1-6-алканоилокси означает линейную или разветвленную алканоилоксигруппу, содержащую от 1 до 6 атомов углерода, и примеры таких групп включают ацетоксигруппу, пропионилоксигруппу, пивалоилоксигруппу и т.д.
C3-10-циклоалкильная группа означает циклоалкильную группу, содержащую от 3 до 10 атомов углерода, и примеры таких групп включают циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, циклогептильную группу, циклооктильную группу, циклононильную группу и т.д.
Примеры замещенной C3-10-циклоалкильной группы включают циклоалкильную группу, где атом(атомы) водорода в циклоалкильной группе является/являются замещенным(ми) по меньшей мере одной группой, выбранной из группы, состоящей из атома галогена, замещенной или незамещенной C1-10-алкильной группы, гидроксильной группы, C1-5-гидроксиалкильной группы, карбоксильной группы, меркаптогруппы, индолильной группы, C1-5-алкилтиогруппы, аминогруппы, амидогруппы и C1-5-алкоксигруппы.
Примеры арильной группы включают фенильную группу, нафтильную группу, антраценовую группу и т.д.
Примеры замещенной арильной группы включают арильные группы, в которых атом(атомы) водорода в арильной группе является/являются замещенным(ми) по меньшей мере одной группой, выбранной из группы, включающей замещенную или незамещенную C1-10-алкильную группу, гидроксильную группу, C1-5-гидроксиалкильную группу, карбоксильную группу, меркаптогруппу, индазолильную группу, индолильную группу, C1-5-алкилтиогруппу, цианогруппу, нитрогруппу, аминогруппу, амидогруппу, ацетиламиногруппу и C1-5-алкоксигруппу.
Примеры C2-10-гетероцикла включают фуран, пиррол, тиофен, оксазол, изоксазол, тиазол, имидазол, пиразол, пиран, пиридин, пиперидин, пиридазин, пиримидин, пиразин, хинолин и т.д.
Примеры замещенного C2-10-гетероцикла включают гетероцикл, в котором атом(атомы) водорода в гетероцикле является/являются замещенным(ми) по меньшей мере одной группой, выбранной из группы, включающей атом галогена, замещенную или незамещенную
C1-10-алкильную группу, гидроксильную группу, C1-5-гидроксиалкильную группу, карбоксильную группу, меркаптогруппу, индазолильную группу, индолильную группу, C1-5-алкилтиогруппу, цианогруппу, нитрогруппу, аминогруппу, амидогруппу и C1-5-алкоксигруппу.
Эфирная связь означает -O-, формулу -(CH2)m-O-(CH2)n- (где m и n каждый означает целое число от 1 до 3, и алкиленовые группы в формуле могут быть замещены алкильной группой(ами)), или формулу -O-(CH2)m-O- (где m означает целое число от 1 до 3, и алкиленовые группы в формуле могут быть замещены алкильной группой(ами)).
Примеры комбинаций смежных групп, которые могут образовывать π связь или эфирную связь, включают (R4 и R5), (R5 и R6), (R6 и R7), (R7 и R8) и (R8 и R9) (то же относится и к R4a - R9a в формуле (IX)).
Из соединений, представленных формулой (IX), соединение, представленное формулой (I), является предпочтительным, а соединение, в котором R3a представляет собой атом водорода и R3b представляет собой гидроксильную группу, является более предпочтительным. С точки зрения стабильности соединения, предпочтительными являются соединения, представленные формулами (IIa), (IIb) и (IIc).
Соединение формулы (II), где (R4 и R5) и (R6 и R7) образуют π связь:
(где R1, R2, R3c, R3d, R8, R9 и X определены выше).
Соединение формулы (II), где (R4 и R5) образуют π связь и R6 и R7 представляют собой атом водорода:
(где R1, R2, R3c, R3d, R8, R9 и X определены выше).
Соединение формулы (II), где R4, R5, R6 и R7 представляют собой атом водорода:
(где R1, R2, R3c, R3d, R8, R9 и X определены выше).
Из соединений, представленных формулой (IX), соединение, в котором R3e и R6b, взятые вместе, образуют эфирную связь, а (R3f и R4a) и (R5a и R6a) образуют π связь (например, Соединение 77, и т.д.), являются предпочтительными, поскольку они эффективно ингибируют экспрессию мРНК WNT-5A в клетках сосочков дермы и промотируют рост клеток сосочков дермы.
Из соединений, представленных формулой (IX), соединение, в котором R1a и R2a представляют собой (CH2)pCO-Y-R10 (где Y представляет собой атом кислорода или атом серы; R10 представляет собой атом водорода, C1-6-алкильную группу или замещенную или незамещенную арильную группу; и p имеет значение 0 или 1) (например, Соединение 52 и т.д.), и соединение, в котором R1a и R2a представляют собой COR12 (где R12 представляет собой замещенную или незамещенную арильную группу или замещенный или незамещенный гетероцикл) (например, Соединение 58 и т.д.), являются предпочтительными, поскольку они эффективно ингибируют экспрессию мРНК WNT-5A в клетках сосочков дермы и промотируют рост клеток сосочков дермы.
Также соединение, в котором R7a представляет собой Z-R13 (где Z представляет собой атом кислорода или атом серы; и R13 представляет собой C2-6 алканоильную группу или замещенную или незамещенную арильную группу) (например, Соединение 53 и т.д.), является предпочтительным, поскольку такие соединения эффективно ингибируют экспрессию мРНК WNT-5A в клетках сосочков дермы и промотируют рост клеток сосочков дермы.
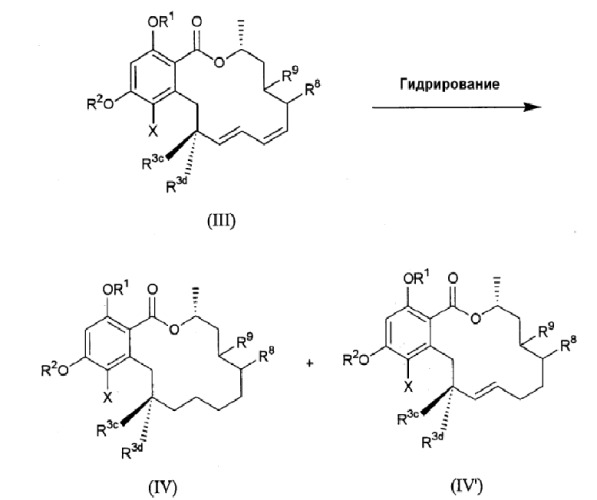
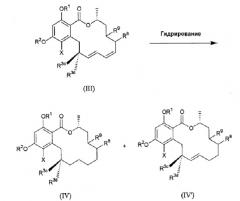
Соединение, представленное формулой (II), можно получить, например, путем сочетания следующих способов получения.
Схема реакций 1
(где R1, R2, R3c, R3d, R8, R9 и X определены выше).
Соединение, представленное формулой (III), подвергают реакции гидрирования в присутствии катализатора, такого как палладий на углероде, в органическом растворителе (например, этилацетате, тетрагидрофуране, диэтиловом эфире, этиловом спирте, метиловом спирте и т.д.) с получением соединения, представленного формулой (IV) или (IV'), или смеси этих соединений. Соединения формул (IV) и (IV') можно разделить и очистить обычным методом разделения, таким как колоночная хроматография.
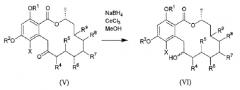
Схема реакций 2
(где R1, R2, R4, R5, R6, R7, R8, R9 и X определены выше).
Осуществляют взаимодействие соединения формулы (V) с восстановителем, таким как борогидрид калия, борогидрид натрия или борогидрид лития, если это необходимо, также в присутствии соли, такой как LiCl, MgCl2, CeCl3, CaCl2 или NiCl, в органическом растворителе (например, тетрагидрофуране, диэтиловом эфире, этиловом спирте, метиловом спирте, и т.д.) при температуре в пределах -20 до 100°C, предпочтительно при температуре от 0 до 20°C, с получением соединения формулы (VI). Соединение формулы (VI) можно разделить и очистить обычным методом разделения, таким как колоночная хроматография.
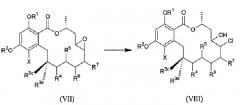
Схема реакций 3
(где R1, R2, R3c, R3d, R4, R5, R6, R7 и X определены выше).
Соединение формулы (VII) обрабатывают кислотой или основанием в подходящем органическом растворителе (например, тетрагидрофуране, диэтиловом эфире, этаноле, метаноле и т.д.) с получением соединения формулы (VIII).
Соединения, представленные формулой (IX) (1, 60-78), получают путем культивирования штамма Pochonia chalamydosporia var. chlamydosporia TF-0480 в среде, содержащей различные питательные вещества, в основном, в соответствии с методами, обычно используемыми для получения продуктов ферментации.
В качестве среды в основном используют жидкую среду, при этом такая среда содержит источник углерода, источник азота и неорганическую соль, необязательно, вместе с витаминами, соединениями-предшественниками и противопенным агентом, и pH доводят примерно до уровня около 7. Источник углерода включает глюкозу, декстрин, глицерин, крахмал и т.д., которые могут использоваться отдельно или в виде смеси этих веществ. Источник азота включает мясной экстракт, овсяную муку, дрожжевой экстракт, соевую муку, полипептон, раствор замоченной кукурузы, мочевину, соль аммония и т.д., которые могут использоваться отдельно или в виде смеси этих веществ. Неорганическая соль включает монофосфат калия, сульфат магния, хлорид натрия, карбонат кальция и т.д., которые могут использоваться отдельно или в виде смеси этих веществ. Противопенный агент, который может быть использован, включает Adekanol или силиконовое соединение. В качестве метода культивирования подходящими являются методы аэробного культивирования, такие как культивирование со встряхиванием или культивирование с аэрацией-взбалтыванием. Культивирование осуществляют при pH 4-10 и при температуре в пределах от 25 до 35°C в течение 2-5 дней, предпочтительно при 25-28°C в течение 3 дней.
Полученные таким способом при помощи культуральной среды соединения 1 и 60-78 могут быть выделены в соответствии с методами, обычно используемыми для сбора продуктов ферментации. Например, следующие методы являются эффективными. А именно, после завершения культивирования культуральный фильтрат получают центрифугированием или фильтрацией. Затем его адсорбируют при помощи полистирольной смолы, такой как DIAION HP-20 (товарное наименование, изготовитель Mitsubishi Chemical) и элюируют органическим растворителем, таким как низший спирт или ацетон. Клетки экстрагируют органическим растворителем, таким как низший спирт или ацетон. Затем клеточный экстракт и элюат из адсорбирующей смолы объединяют и концентрируют при пониженном давлении. К оставшейся водной фазе добавляют для экстракции органический растворитель, такой как этилацетат, хлороформ или н-бутанол, и экстракт концентрируют. Полученный остаток снова растворяют в органическом растворителе, таком как бензол, этилацетат, ацетон, метанол или хлороформ, и затем подвергают колоночной хроматографии на силикагеле, гель-фильтрационной колоночной хроматографии, хроматографии на колонке, заполненной ODS, для обращенно-фазового разделения и высокоэффективной жидкостной хроматографии для очистки и выделения соединения по настоящему изобретению.
Штамм, продуцирующий активный ингредиент в соответствии с настоящим изобретением, является новым штаммом, который был впервые выделен из почвы авторами настоящего изобретения. Микроорганизм был назван "Pochonia chlamydosporia var. chlamydosporia TF-0480" и был депонирован как в "FERM BP-8332" в International Patent Organism Depository, National Institute of Advanced Industrial Science and Technology.
Микробиологические свойства этого штамма следующие.
1) Рост на среде
Данный микроорганизм хорошо растет в различных средах на агаровых пластинах и показывает хорошее или умеренное спорообразование в испытываемых средах. В Таблице 1 обобщены характеристики колоний, образованных после культивирования при 26°C в течение 2 недель на различных средах. Цвет указан в соответствии с кодами цвета, предложенными A. Kornerup et al., Dizionario dei colori, Musterschmidt (1978).
| Таблица 1 | |
| Среда | Результаты наблюдения за колониями невооруженным глазом |
| PDA*-1 | Показывает относительно хороший рост и спорообразование. Диаметр колонии: 23-28 мм. Шерстистые и несколько конусообразные колонии с войлочным центром и небольшими радиальными морщинками. Несколько неправильной формы периферия (оконечность колонии). Секретируют бледный светло-желтый [3A6] пигмент в среду. Цвет поверхности колонии: белый [1A1] на периферии и бледно-желтый [4A3] в центре. Цвет обратной стороны: красновато-желтый [4A6] на периферии и желтовато-коричневый [5D8] в центре. Иррегулярное или радиальное растрескивание агаровой среды. |
| OMA*-2 | Показывает хороший рост и спорообразование. Диаметр колонии: 48-50 мм. Несколько тонкие и шерстистые колонии с войлочным центром и промежуточной частью. Относительно правильной формы периферия. Не секретируют никакого пигмента. Цвет поверхности колонии: белый [1A1] на периферии и бледно-желтый [3A4] в центре. Цвет обратной стороны: светло-желтый [3А4], такой же, как на поверхности. |
| CMA*-3 | Показывает хороший рост и умеренное спорообразование. Диаметр колонии: 47-51 мм. Тонкие и войлочные колонии. Относительно правильной формы периферия. Не секретируют никакого пигмента в среду. Цвет поверхности колонии/цвет обратной стороны: с обеих сторон от белого [1A1] до желтовато-белого [1А2]. |
| MA*-4 | Показывает относительно хороший рост и спорообразование. Диаметр колонии: 26-27 мм. Толстые и шерстистые колонии с войлочным центром. Относительно правильной формы периферия. Секретируют слегка красновато-желтый [4А7] пигмент в среду. Цвет поверхности колонии: белый [1A1] на периферии и бледно-желтый [4А3] в центре. Цвет обратной стороны: светло-оранжевый [5А4] на периферии, коричневый [7E8] в центре и оранжевый [6B7] в промежуточной части. |
| SA*-5 | Показывает относительно хороший рост и спорообразование. Диаметр колонии: 23-28 мм. Шерстистые и несколько конусообразные колонии с войлочным центром. Несколько неправильной формы периферия и небольшие радиальные морщинки. Секретируют красновато-желтый [4А7] пигмент в среду. Цвет поверхности колонии: белый [1A1] на периферии и оранжевато-белый [5А2] в других частях. Цвет обратной стороны: светло-оранжевый [5А4] на периферии и в центре и коричневый [7Е8] в других частях. Иррегулярное или радиальное растрескивание агаровой среды. |
| LCA*-6 | Показывает хороший рост и умеренное спорообразование. Диаметр колонии: 42-44 мм. Тонкие войлочные до слегка шерстистых колонии. Относительно правильной формы периферия. Не секретируют никакого пигмента в среду. Цвет поверхности колонии/цвет обратной стороны: с обеих сторон белый [1A1]. |
*-1: среда картофельного агара с декстрозой (E-MF21, изготовитель Eiken Chemical Co., Ltd.).
*-2: 1/2-Разбавленная агаровая среда на отваре из овсяной муки (изготовитель Difco, получена путем 1/2-разбавления агара Bacto на отваре из овсяной муки и добавления агара с получением конечной концентрации агара 2%).
*-3: Агаровая среда на отваре из овсяной муки (изготовитель Difco, Corn meal agar).
*-4: Солодовая агаровая среда (Nakase, T., 6th ed., pp,617, Japan Collection of Microorganisms, the Institute of Physical and Chemical Research, Saitama, 1995)
*-5: Агаровая среда Сабуро (изготовитель Eiken Chemical Co., Ltd., E-MF03)
*-6: Агаровая среда Миуры (Miura, K. and M. Kudo, Trans. Mycol. Soc. Japan, 11, 116-118 (1970))
2) Морфология
Колонии, образованные после культивирования штамма на агаровой среде на отваре из овсяной муки при 26°C в течение 14 дней, наблюдали под оптическим микроскопом. В результате, наблюдали образование фиало-конидий. Образование одной конидия-образующей клетки (фиалиды) или 2-4 мутовчатых фиалид происходило непосредственно на гифе. Конидиофоры нельзя было четко отличить от вегетативных гиф. Происходило образование множества конидий на переднем крае фиалиды с образованием вязкой массы. Фиалида имела форму конусообразного цилиндра и ровную и бесцветную поверхность. Ее длина составляла 13-15 мкм, а толщина на конце 0,8-1,7 мкм. Конидии имели элипсообразную форму или форму полусфер (редко) и большинство из них имели слегка выступающее основание. Конидии имели ровную и бесцветную поверхность и размер 2,2-5,0×1,8-2,8 мкм. Образование единственной бледно-желтой и многоклеточной хламидоспоры (диктиохламидоспоры) происходило на поверхности среды или на конце короткого ростка гифы на среде. Также происходило образование в среде небольшого количества диктиохламидоспор. Эти диктиохламидоспоры имели размер 14-20×12-22 мкм. При продолжении культивирования в течение одного месяца или дольше не наблюдали никакого телеоморфа.
3) Физиологические свойства
(1) Пределы температуры роста и оптимальная температура
В агаровой среде Сабуро при pH 6,0 этот штамм растет в температурных пределах 15-31°C, и оптимальная температура составляет от 25 до 27°C.
(2) Пределы значений pH для роста и оптимальное значение pH
В жидкой среде YpSs при 26°C этот штамм растет в пределах значений pH 3-10, и оптимальное значение pH составляет от 5 до 7.
4) Аэробный/анаэробный: аэробный.
На основании описанных выше морфологических характеристик и свойств культуры, характеристики этого штамма сравнивали с различными известными видами, о которых сообщалось в (1) K.H. Domsch et al., Compendium of soil fungi,Vol. 1, IHW-Verlag (1980) и (2) G.L. Barron, The Genera of Hyphoomycetes from soil, Williams & Wilkins (1968) и т.д. В результате было обнаружено, что этот штамм является очень схожим с неполным видом, известным под классификационными названием Verticillium chlamydosporia или Diheterospora chlamydosporia, и поэтому, вероятно, относится к этому виду. В (3) R. Zare, W. Gams and H.C. Evans, A revision of Verticillium section Prostrata. V. The genus Pochonia, with notes on Rotiferophthora, 73, 1-2, p51-86 (2001), этот вид был молекулярно систематически повторно исследован и, в свою очередь, назван как относящийся к роду Pochonia, как к подходящему для него роду. Более того, предлагается назвать такой вид, образующий несвязанные конидии типа Verticillium, как штамм по настоящему изобретению, вариантом Pochonia chlamydosporia var. chlamydosporia.
На основании этих данных, этот штамм был назван "Pochonia chlamydosporia var. chlamydosporia TF-0480".
<Промотор роста клеток сосочков дермы>
Термин "промотор роста клеток сосочков дермы", как он использован в настоящем изобретении, означает лекарственное средство или реагент, обладающие действием по увеличению количества клеток сосочков дермы.
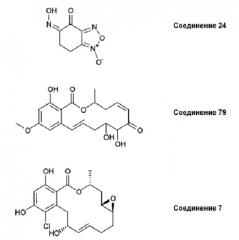
Промотор роста клеток сосочков дермы по настоящему изобретению характеризуется тем, что он основан на действии по ингибированию функции WNT-5A. Поскольку WNT-5A ингибирует функции молекул класса WNT-1 (WNT-1, WNT-8 и т.д.), которые являются активаторами пути WNT/β-катенина, рост клеток сосочков дермы контролируется регулированием функции WNT-5A или регулированием экспрессии WNT-5A. Поэтому, даже соединения, имеющие совершенно разные структуры (например, Соединение 24, Соединение 79, Соединение 7 и т.д.), обладают отличным действием промотирования роста клеток сосочков дермы, если эти соединения обладают отличным эффектом ингибирования функции WNT-5A.
Рост клеток можно измерить методом, хорошо известным специалистам в данной области. Примеры методов измерения включают подсчет жизнеспособных клеток с использованием подходящего проявляющего цвет субстрата, и метод поглощения [3H]-тимидина. В качестве, проявляющего цвет субстрата предпочтительно используют соли тетразолия, такие как MTT, MTS и XTT и Alamar Blue.
<Стимулятор роста волос/тоник для роста волос>
Термин "стимулятор роста волос или тоник для роста волос", как он использован в настоящем изобретении, означает продукты, предназначенные для индуцирования роста волос, промотирования роста волос, предотвращения алопеции и т.д. В случае использования стимулятора роста волос и тоника для роста волос по настоящему изобретению в качестве лекарственных средств, объект изобретения включает улучшение или профилактику гнездной алопеции и алопеции мужского типа.
Эффекты стимулятора роста волос и тоника для роста волос по настоящему изобретению достигаются посредством действия по промотированию роста клеток сосочков дермы путем ингибирования функции WNT-5A. На основании механизма этой функции, способность к росту клеток, подавленная в сосочках дермы на участке алопеции, повышается и образуется хорошо развитая дермальная сосочковая ткань. Поэтому ожидается, что стимулятор роста волос/тоник для роста волос по настоящему изобретению должны быть эффективными против симптомов, на которые, как было установлено, известные в настоящее время стимуляторы роста волос и тоники для роста волос оказывают слабое действие.
Кроме того, ожидается, что может быть достигнут синергический эффект путем объединения стимулятора роста волос и тоника для роста волос по настоящему изобретению с другими стимуляторами роста волос и тониками для роста волос, обладающими другими функциональными свойствами.
Стимулятор роста волос/тоник для роста волос по настоящему изобретению можно вводить различными дозами и в различных лекарственных формах, в зависимости от конкретных соединений.
В случае введения соединения, представленного формулой (IX), путем нанесения (лосьон, мазь, гель и т.д.), его можно вводить, например, при дозе 0,0001-10% масс., предпочтительно 0,001-5% масс., и более предпочтительно 0,001-1% масс., хотя доза варьирует в зависимости от типа и лекарственной формы тоника для роста волос. В случае перораль