Средство, обладающее местно-анестезирующим действием
Иллюстрации
Показать всеИзобретение относится к области медицины, конкретно к производному 2,9-дизамещенного имидазо[1,2-а]бензимидазола, обладающему более эффективным местноанестезирующим действием, в качестве которого предлагается дигидрохлорид 9-(2-пирролидиноэтил)-2-(4-фторофенил)-имидазо[1,2-а]бензимидазола формулы I:
6 табл.
Реферат
Изобретение относится к области медицины, конкретно к средству, обладающему местно-анестезирующим действием, которое после проведения клинических испытаний может быть предложено для местного обезболивания при различных хирургических вмешательствах, в послеоперационном периоде, для терапии хронических болевых синдромов и т.д.
В последнее время, несмотря на довольно большое количество препаратов, относящихся к группе лекарственных местно-анестезирующих средств, все большее значение приобретает изыскание новых обезболивающих препаратов. Это диктуется потребностями клиник, которые не всегда удовлетворены эффективностью известных препаратов. Тем более данные экспериментальных исследований и практика обезболивания в клинике показывают, что у ряда веществ местно-анестезирующая активность при разных видах анестезии может быть неодинакова. Так, некоторые высокоактивные при инфильтрационной и проводниковой анестезии препараты малоактивны при терминальном способе обезболивания, так как плохо проникают через кожу и слизистые оболочки. Кроме того, местно-анестезирующие препараты обладают довольно высокой токсичностью, при этом последняя, как правило, возрастает с повышением эффективности средств и проявляется в виде их резорбтивного действия (наиболее опасные - воздействие на ЦНС и кардиодепрессорные эффекты) и местнораздражающих эффектов (вплоть до некробиотического действия).
Местно-анестезирующим средством нового поколения является лидокаин, который находит широкое применение при инфильтрационном, проводниковом, спинномозговом и, иногда, терминальном методах обезболивания (А.И.Левшанков, А.Л.Костюченко, Е.Т.Ростомашвили и др. Каудальная эпидуральная анестезия при операциях на нижних конечностях в травматологии и ортопедии. Анестезиол. и реаниматол., 1992, №5-6, с.15-17; М.Д.Машковский, 1998).
Лидокаин обычно хорошо переносится, однако иногда может вызывать коллапс, анафилактическую реакцию, изменения в содержании цитоплазматических белков, поверхности и форме эритроцитов (Г.И.Карицкий, А.Н.Куйбида и др. Выведение из анафилактического шока с клинической смертью после введения лидокаина. Вестн. хир. им. И.И.Грекова, 1987, №4, с.131; Н.Х.Вахидов, И.А.Абдуллаева, Т.Р.Мурадов. Успешная реанимация больных после побочной токсической реакции на введение лидокаина. Журнал ушных, носовых и горловых болезней, 1989, №6, с.60-61; E.Nidhiguchi et al. Factors of the share change of human erythrocytes induced with lidocaine. Cell. struct, and Funct, 1989, Vol.14, p.569-577; М.Д.Машковский, 1998).
Большого внимания заслуживает также местный анестетик маркаин (бупивакаин), который находит практическое применение в качестве средства для спинномозговой, эпидуральной, каудальной, внутрисуставной анестезии, при проведении парацервикальной и ретробульбарной блокад (например, R.P.Alston. Spinal anaecthisis with 0,5% bupivacaine 3 ml: Comparison of plain and hyperbarric solutions administered to seated patients. Brit. J. Anaesrth, 1988, Vol.61, №4, p.385 - 389; A.R.Wolf, R.D.Val-ley, D.W.Fear et al. Bupivacaine for caudal analgesia in infants and children: the optimal effective concentration. Anaesthesiology, 1988, Vol.69, №1, p.101-105).
Следует отметить, что маркаин, подобно дикаину, не только высокоактивный, но и весьма токсичный анестетик (Н.Б.Рациборинская. Местно-анестезирующие свойства некоторых новых производных пиперидина и индола. Автореф. дис.... канд. мед. наук. Ростов-на-Дону, 1991; J.Kambarn, B.Mets, R.Hickman et al. Comparative systemic toxicity of intravenously infused bupivacaine (B), cocaine (C) and lidocaine (L) inpigs: [Abstr.] Int. Anesth. Res. Soc. 66th Congr., San Francisco, Calif., March 13-17, 1992; Anesth. and Analg., 1992, Vol.74, №25, p.87), что требует повышенного внимания при его использовании в практической медицине. Кроме того, маркаин может вызывать генерализованную сыпь, отек Квинке, стридор гортани, бронхоспазм (H.Gacl, V.Reichert, R.Kaufmann. Localanastheticaintoleranz auf Leitungsanasthesia mit Prilocain und Bupivacain. Allergologie, 1992, Bd. 15, №3, S.89-91).
Известно производное в ряду 1,2-дизамещенных имидазо[1,2-а]-бензимидазола, а именно дигидрохлорид 1-(3-пирролидинопропил)-2-фенилимидазо[1,2-а]бензимидазола, обладающий местно-анестезирующим действием при инфильтрационной, проводниковой и спинномозговой анестезии /патент РФ №2160265, C07D 487/04, А61К 31/4188,2000 г./. Соединение обладает высокой местно-анестезирующей активностью, в том числе инфильтрационной (ЭК50 в мМ=0,31), однако имеет достаточно высокую острую токсичность (ЛД50 в мМ/кг=0,110) и соответственно недостаточно высокий терапевтический индекс инфильтрационной активности (ЛД50/ЭК50=3538,5).
Техническим результатом изобретения является уменьшение токсичности и увеличение широты терапевтического действия инфильтрационной активности местно-анестезирующего средства.
Технический результат достигается выявлением местно-анестезирующего эффекта при поверхностной (терминальной), инфильтрационной и спинальной анестезии у дигидрохлорида 9-(2-пирролидиноэтил)-2-(4-фторфенил)имидазо[1,2-а]бензимидазола формулы I:
Изобретение обладает изобретательским уровнем, так как в ряду 2,9-дизамещенных имидазо[1,2-а]бензимидазола не известны соединения, проявляющие местно-анестезирующее действие.
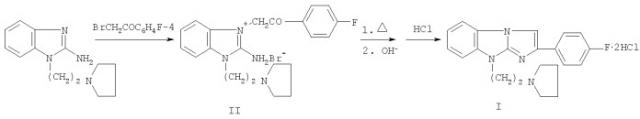
Ниже приведен способ получения соединения I, который заключается во взаимодействии 1-пирролидиноэтил-2-аминобензимидазола с 4-фтор-фенацилбромидом и дальнейшей циклизации промежуточно образующегося бромида 1-пирролидиноэтил-3-(4-фторфенацил)-2-аминобензимидазолия II до 9-пирролидиноэтил-2-(4-фторфенил)имидазо[1,2-а]бензимидазола и переводе трициклического основания в дигидрохлорид I:
Пример. Стадия 1. Бромид 2-амино-1-(2-пирролидиноэтил)-3-(4-фтор-фенацил)бензимидазолия (II). В горячий раствор 2,3 г (10 ммоль) 2-амино-1-(2-пирролидиноэтил)бензимидазола в 150 мл ацетона вносят 2,17 г (10 ммоль) 4-фторфенацилбромида. Смесь перемешивают до растворения последнего, нагревают до начала выпадения осадка и оставляют стоять в течение 4-6 ч при комнатной температуре. Затем выпавший осадок отфильтровывают, тщательно промывают ацетоном. Выход 88,8%, т.пл. 179-180°С. Найдено, %: С 56,34; Н 5,45; Br 17,68; F 4,36; N 12,56. C21H24BrFN4O. Вычислено, %: С 56,38; Н 5,41; Br 17,86; F 4,25; N 12,52.
Стадия 2. Дигидрохлорид 9-(2-пирролидиноэтил)-2-(4-фторфенил)имидазо[1,2-а]бензимидазола (I). Кипятят 0,89 г (2 ммоль) соли II в 50 мл воды до полного протекания реакции (3-5 ч, контроль - ТСХ). Затем раствор подщелачивают и выделившееся основание экстрагируют хлороформом. Экстракт пропускают через слой Al2О3 (элюент - CHCl3). Остаток после испарения CHCl3 из элюата растворяют в ацетоне и подкисляют раствором HCl в 2-PrOH, получая дигидрохлорид I. Выход 81,63%, т.пл. 257-258°С (разл., 2-PrOH). Спектр ЯМР 1Н, δ, м.д.: 2,08 (4Н, кв, -(СН2)2-); 3,31 (2Н, т, NCH2); 3,64 (2Н, т, NCH2); 3,76 (2Н, т, NCH2); 5,17 (2Н, т, NCH2); 7,21 (2Н, т, 3',5'-Н); 7,47 (2Н, дт, 2',6'-Н); 7,86-8,20 (4Н, м, аром. Н); 8,48 (1Н, с, 3-Н); 12,40 (1Н, ушир. с, N+H); H+ в обмене.
Найдено, %: С 59,79; Н 5,60; Cl 16,78; F 4,44; N 13,39. C21H21FN4·2HCl.
Вычислено, %: С 59,86; Н 5,50; Cl 16,83; F 4,51; N 13,30.
Ниже приведены результаты фармакологических исследований соединения I.
В основу исследований положены Методические указания по изучению местно-анестезирующей активности фармакологических веществ (Игнатов Ю.Д., Червякова И.В., Васильев Ю.Н., Галенко-Ярошевский А.П., Жуков В.Н. Методические указания по изучению местно-анестезирующей активности фармакологических веществ //В кн.: Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ /Под общей редакцией чл.-корр. РАМН, проф. Р.У.Хабриева, 2-изд., перераб. и доп., М.,ОАО Изд-во "Медицина", 2005, с.364-392).
Эксперименты проведены в соответствии со статьей 11-й Хельсинкской декларации Всемирной медицинской ассоциации (1964), "Международными рекомендациями по проведению медико-биологических исследований с использованием животных" (1985) и Правилами лабораторной практики в Российской Федерации (приказ МЗ РФ №267 от 19.06.2003 г.).
Поверхностную (терминальную) анестезию исследовали в экспериментах на роговице глаз кроликов с использованием метода Ренье-Валета (Прянишникова Н.Т., Шаров Н.А. Тримекаин. Фармакология и клиническое применение. Л.: Медицина, 1967, 239 с.), при этом параллельно изучали возможное раздражающее действие по Setnicar (Setnicar I. Tolerance indices of some phenoxyethylamino derivatives with local anaesthitic properties //Arzneim. Forsch., 1966, Bd. 16, №5, S.623).
Инфильтрационную анестезию исследовали в опытах на морских свинках (Ю.Д.Игнатов и соавт., 2005; Bulbring E., Wajda J. Biological comparison of local anaesthetica II]. pharmacol. and exp. therap., 1945, vol.85, №1, p.78-84).
Спинальную анестезию изучали в экспериментах на крысах "бескровным" методом, разработанным в НИИ фармакологии РАМН (Ю.Д.Игнатов и соавт., 2005). При этом изменение болевых порогов определяли путем механического раздражения корня хвоста.
Острую токсичность исследовали [определяли среднюю летальную (смертельную) дозу - ЛД50] в опытах на мышах при подкожном введении (Прозоровский В.Б. Использование метода наименьших квадратов для пробит-анализа кривых летальности //Фармакол. и токсикол., 1962, Т. 25, №1, с.115-119).
В качестве препарата сравнения были взяты лидокаин (при исследовании поверхностной и инфильтрационной анестезии) и маркаин (при изучении спинальной анестезии).
Статистическую обработку данных, учитываемых в градированной форме, проводили по М.Л.Беленькому (Беленький М.Л. Элементы количественной оценки фармакологического эффекта., Л., 1963, 152 с.) и с помощью таблиц Н.Н.Самойлова (Самойлов Н.Н. Таблицы значений средней ошибки и доверительного интервала средней арифметической величины вариационного ряда., Томск, 1970, 63 с.).
Учет результатов исследований, выраженных в альтернативной форме, определение ЛД50, ЭК50, границ доверительного интервала и терапевтического индекса, или широты терапевтического действия (ЛД50/ЭК50) осуществляли по методам, описанным В.Б.Прозоровским (1962) и М.Л.Беленьким (1963).
Установлено, что в условиях поверхностной анестезии в опытах на роговице глаз кроликов индексы Ренье, выражающие силу обезболивающего действия в исследованных концентрациях, для соединения I в 0,25, 0,5 и 1,0% растворах составляют 210,7, 1078,8 и 1204,7, тогда как для лидокаина в 1,0, 2,0 и 5,0% растворах - 297,9, 354,8 и 676,9 соответственно (табл.1).
Соединение I, как и лидокаин, в исследованных растворах не оказывает раздражающего действия на конъюнктиву глаз.
| Таблица 1. | ||
| Сравнительная активность (по индексам Ренье) соли I и лидокаина при поверхностной анестезии в опытах на роговице глаз кроликов | ||
| Концентрация, % | Индекс Ренье1 | |
| I | лидокаин | |
| 0,25 | 210,7±60,8(64,2÷356,2) | - |
| 0,5 | 1078,8±63,3(926,8÷1230,8) | - |
| 1,0 | 1204,7±48,8(1087,5÷1321,9) | 297,9±20,7(248,2÷347,6) |
| 2,0 | 354,8±17,8(315,6÷394,0) | |
| 5,0 | 676,9±21,3(625,7÷728,2) | |
| 1Представлены средние арифметические, вычисленные из 6 (для I) и 8 (для лидокаина) опытов, со стандартной ошибкой средней. | ||
| Примечание. В скобках: круглых - доверительные границы при р=0,05. |
Временные интервалы наступления анестезии и начала полного обезболивания при инстилляции в конъюнктивальный мешок глаза растворов соединения I (0,5 и 1,0%) и лидокаина (1,0, 2,0 и 5,0%) были в пределах 2 и 3 мин соответственно; исключение составлял 0,25% раствор соли I, для которого первый показатель был равен 3-5 мин, второй - 5 - 8 мин. Время окончания полной анестезии и общая продолжительность обезболивания под влиянием 0,25, 0,5 и 1,0% растворов соединения I составляло 12,5 и 31,7, 34,2 и 66,7, 55,8 и 75,0 мин, а при использовании 1,0, 2,0 и 5,0% растворов лидокаина - 5,8 и 18,8, 7,4 и 22,5, 25,6 и 35,4 мин соответственно (табл.2).
По местно-анестезирующей активности - при сопоставлении ЭК50, выраженных в мМ, и терапевтических индексов - соединение I соответственно в 20,1 раза более значимо и в 9,6 раза имеет большую широту терапевтического действия, чем лидокаин (табл.3).
При инфильтрационной анестезии в экспериментах на морских свинках минимальной обезболивающей концентрацией для соли I является 0,0156%, для лидокаина - 0,0625%. Полный обезболивающий эффект (100%-ная анестезия в течение 30 мин) вызывает соль I в 0,125% растворе, тогда как лидокаин - в 0,5% растворе (табл.4).
Сопоставление ЭК50, выраженных в мМ, показало (табл.5), что соединение I в 6,95 раза более активно, чем лидокаин. При этом по широте терапевтического действия его в 3,30 раза превосходит лидокаин.
В условиях спинальной анестезии в опытах на крысах соединение I и маркаин, взятые в 0,5% растворе, вызывали обезболивающий эффект практически сразу после введения их в спинномозговой канал. Глубина анестезии через 5 мин (для обоих веществ) и в течение 40-45 мин (для соли I) и 30-35 мин (для маркаина) составляла 100%. Длительность обезболивающего действия под влиянием I была равна 76,0, а при использовании маркаина - 44,5 мин, т.е. по этому показателю первое вещество в 1,71 раза превосходило второе (табл.6). Соединение I, подобно маркаину, вызывало слабовыраженное угнетение дыхания в течение 7-15 мин.
Таким образом, соединение I по активности при поверхностной и инфильтрационной анестезии и широте терапевтического действия значительно превосходит лидокаин, а при спинальном обезболивании - маркаин.
Кроме того, соединение I менее токсично (ЛД50 в мМ/кг=0,500) и превосходит по терапевтическому индексу инфильтрационной активности (ЛД50/ЭК50=9152,2; таблица 5) дигидрохлорид 1-(3-пирролидинопропил)-2-фенилимидазо[1,2-а]бензимидазола (ЛД50 в мМ/кг=0,110; ЛД50/ЭК50=3538,5; таблица 4 описания к патенту №2160265) соответственно в 4,5 и 2,6 раза.
На основе соединения I представляется возможным создание местно-обезболивающего лекарственного средства, предназначенного для поверхностной, инфильтрационной и спинальной анестезий.
| Таблица 2 | |||||
| Сравнительная характеристика временных параметров действия соли I и лидокаина при поверхностной анестезии в опытах на роговице глаз кроликов | |||||
| Соединение и препарат | Концентрация, % | Начало анестезии, мин | Начало полной анестезии, мин | Окончание полной анестезии1, мин | Общая продолжительность анестезии1, мин |
| I | 0,25 | 3-5 | 5-8 | 12,5±0,90 | 31,7±1,77 |
| 0,5 | 2 | 3 | 34,2±1,77 | 66,7±5,30 | |
| 1 | 2 | 3 | 55,8±7,07* | 75,0±7,95* | |
| Лидокаин | 1 | 2 | 3 | 5,8±0,66 | 18,8±1,33 |
| 2 | 2 | 3 | 7,4±0,66 | 22,5±0,66 | |
| 5 | 2 | 3 | 25,6±1,33 | 35,4±1,99 | |
| 1Представлены средние арифметические, вычисленные из 6 (для I) и 8 (для лидокаина) опытов, со стандартной средней ошибкой. *p<0,001 - относительно лидокаина, взятого в соответствующей (1%) концентрации |
| Таблица 3 | ||||||||
| Сравнительная активность [по ЭК50 и терапевтическому индексу (широте терапевтического действия)] соединения I и лидокаина при поверхностной анестезии в опытах на роговице глаз кроликов | ||||||||
| Соединение и препарат | Местно-анестезирующая активность | Токсичность 0,5% раствора при подкожном введении мышам | Терапевтический индекс | |||||
| ЭК50 | относительная1 | ЛД50 | относительная1 | абсолютный | относительный1 | |||
| % | мМ | мг/кг | мМ/кг | |||||
| I | 0,39 [18] (0,28÷0,54) | 9,3 | 20,1 | 210,5 [40] (204,9÷216,3) | 0,500 | 0,47 | 539,7 | 9,6 |
| Лидокаин | 5,05 [24] (3,87÷6,57) | 187,0 | 1,0 | 258,1 [35] (271,9±299,0) | 1,056 | 1,0 | 56,5 | 1,0 |
| Примечание. В скобках: круглых - доверительные границы при p=0,05, квадратных - количество опытов. |
| Таблица 4 | ||||||
| Сравнительная активность (по индексам Бюльбринг и Уэйд) соединения I и лидокаина при инфильтрационной анестезии в опытах на коже морских свинок (n=6) | ||||||
| Соединение и препарат | Индексы Бюльбринг и Уэйд при концентрациях, % | |||||
| 0,0156 | 0,0312 | 0,0625 | 0,125 | 0,25 | 0,5 | |
| I | 16,5 [45,8] (14,3÷18,7) | 18,2 [50,5] (17,2÷19,1) | 30,7 [85,2] (27,1÷34,2) | 36,0 [100,0] | ||
| Лидокаин | 9,8 [27,3] (7,2÷12,4) | 22,7 [63,0] (19,0÷26,4) | 29,8 [82,9] (26,2÷33,5) | 36,0 [100,0] | ||
| Примечание. В скобках: круглых - доверительные границы при p=0,05, квадратных - количество опытов. |
| Таблица 5 | ||||||||
| Сравнительная активность [по ЭК50 и терапевтическому индексу (широте терапевтического действия)] соединения I и лидокаина при инфильтрационной анестезии в опытах на коже морских свинок | ||||||||
| Соединение и препарат | Местно-анестезирующая активность | Токсичность 0,5% раствора при подкожном введении мышам | Терапевтический индекс | |||||
| ЭК50 1 | относительная | ЛД50 | относительная | абсолютный | относительный | |||
| % | мМ | мг/кг | мМ/кг | |||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| I | 0,023 [18] (0,015÷0,035) | 0,55 | 6,95 | 210,5 [40] (204,9÷216,3) | 0,500 | 0,47 | 9152,2 | 3,30 |
| Лидокаин | 0,103 [18] (0,080÷0,133) | 3,82 | 1,0 | 285,1 [35] (271,9÷299,0) | 1,056 | 1,0 | 2765,3 | 1,0 |
| 1При расчете ЭК50 для соединения I использованы индексы Бюльбринг и Уэйд (в %) при концентрациях 0,0156, 0,0312 и 0,0625%, для лидокаина - 0,0625, 0,125 и 0,25%. | ||||||||
| Примечание. В скобках: круглых - доверительные границы при p=0,05, квадратных - количество опытов. |
| Таблица 6 | ||||||
| Сравнительная активность соединения I и маркаина при спинальной анестезии в опытах на крысах | ||||||
| Соединение и препарат | Концентрация, % | Количество животных | Анестезия | Количество животных, у которых анестезия не наступила, % | Количество погибших животных, % | |
| глубина, % | длительность, мин | |||||
| I | 0,5 | 10 | 100,0 | 76,0±7,25* | 30 | 10 |
| Маркаин | 0,5 | 10 | 100,0 | 44,5±3,18 | 20 | 10 |
Применение дигидрохлорида 9-(2-пирролидиноэтил)-2-(4-фторофенил)имидазо[1,2-а]бензимидазола формулы I
в качестве средства, обладающего местно-анестезирующим действием.