Пептид neisseria meningitidis для терапевтического и диагностического применения
Иллюстрации
Показать всеИзобретение относится к области биотехнологии. Пептид N. meningitidis имеет последовательность SEQ ID NO:10 и применяется для лечения или диагностики. Также предложены полинуклеотид, кодирующий такой пептид, клетка-хозяин, экспрессирующая пептид, микроорганизм, вакцина и антитело, специфичное к пептиду. Изобретение может быть использовано в медицине. 13 н. и 3 з.п. ф-лы, 2 табл.
Реферат
Область изобретения
Данное изобретение относится к бактериальным генам и белкам и их применениям. Более конкретно, оно относится к их применению в терапии, для иммунизации и в скрининге лекарственных средств.
Предпосылки изобретения
Neisseria meningitidis является грамотрицательным патогеном, который вызывает септический шок и бактериальный менингит. Эта бактерия является главной причиной бактериального менингита в развивающихся странах и причиной крупномасштабных эпидемий в Африке и Китае. В Великобритании Neisseria meningitidis является главной причиной смерти в детском возрасте, наряду с дорожными происшествиями. Эта бактерия в норме обитает в носоглотке человека и затем приобретает доступ к кровотоку, в котором обусловливает тяжелую септицемию или менингит. Хотя существующие в настоящее время противомикробные средства эффективно элиминируют эту бактерию из организма, смертность от менингококковой септицемии остается существенной. Было бы желательным обеспечение средств для лечения или предупреждения состояний, вызываемых Neisseria meningitidis, например, посредством иммунизации.
Сущность изобретения
Данное изобретение основано на обнаружении генов в Neisseria meningitidis, продукты которых могут быть локализованы на наружной поверхности этого организма и, следовательно, могут быть использованы в качестве мишеней для иммунотерапии.
Согласно одному аспекту данного изобретения описан пептид, кодируемый геном, имеющим любую из нуклеотидных последовательностей, идентифицированных в пункте 1 формулы изобретения, или его гомолог или функциональный фрагмент. Такой пептид пригоден для терапевтического или диагностического применения, например, после выделения.
Согласно второму аспекту данного изобретения полинуклеотид, кодирующий определенный выше пептид, может быть также применим в терапии или диагностике.
Согласно следующему аспекту данного изобретения этот пептид или полинуклеотид может быть использован для скрининга потенциальных противомикробных лекарственных средств.
Следующим аспектом данного изобретения является применение любого из идентифицированных здесь продуктов для лечения или предупреждения состояния, связанного с инфекцией Neisseria или грамотрицательными бактериями.
Описание изобретения
Данное изобретение основано на обнаружении генов, кодирующих пептиды, которые локализованы на клеточной поверхности Neisseria и которые, следовательно, применимы для приготовления лекарственных средств для лечения инфекции. Должно быть понятно, что ссылки на лечение включают в себя также превентивные мероприятия, например вакцинацию. Кроме того, хотя продукты данного изобретения предназначены прежде всего для лечения инфекций у пациентов-людей, предполагается, что ветеринарные применения также находятся в рамках данного изобретения.
Данное изобретение описывается со ссылкой на Neisseria meningitidis. Однако все штаммы Neisseria и многие другие грамотрицательные бактериальные штаммы включают в себя, по-видимому, родственные пептиды или белки, имеющие идентичность или гомологию аминокислотной последовательности с аминокислотными последовательностями, идентифицированными здесь. Организмы, которые, по-видимому, содержат эти пептиды, включают в себя, но не ограничиваются ими, роды Salmonella, Enterobacter, Klebsiella, Shigella и Yersinia.
Предпочтительно пептиды, которые могут быть применимы в различных аспектах данного изобретения, имеют большую, чем 40%-ную, гомологию с идентифицированными здесь пептидами. Более предпочтительно эти пептиды имеют большую, чем 60%-ную, гомологию последовательности. Наиболее предпочтительно эти пептиды имеют большую, чем 80%-ную, гомологию последовательности, например 95%-ную гомологию. Что касается полинуклеотидных последовательностей, идентифицированных здесь, родственные полинуклеотиды, которые могут быть применимы в различных аспектах данного изобретения, могут иметь большую, чем 40%-ную, идентичность с идентифицированными здесь последовательностями. Более предпочтительно эти полинуклеотидные последовательности имеют большую, чем 60%-ную, идентичность. Наиболее предпочтительно эти полинуклеотидные последовательности имеют большую, чем 80%-ную, идентичность, например 95%-ную идентичность.
Термины «гомология» и «идентичность» известны в данной области. Применение термина «идентичность» относится к сравнению последовательностей, основанному на идентичных совпадениях между соответственно идентичными положениями в сравниваемых последовательностях. Термин «гомология» относится к сравнению между аминокислотными последовательностями и учитывает не только идентичные аминокислоты в соответствующих положениях, но также функциональность гомологичных аминокислот в соответствующих положениях. Таким образом, гомология между полипептидными последовательностями указывает на функциональную гомологию, наряду с гомологией последовательностей.
Уровни идентичности между генными последовательностями и уровни идентичности или гомологии между аминокислотными последовательностями могут быть рассчитаны с использованием известных способов. В отношении данного изобретения публично доступные основанные на применении компьютера способы для определения идентичности и гомологии включают в себя BLASTP, BLASTN и FASTA (Altschul et al., J. Molec. Biol., 1990; 215:403-410, программу BLASTX, доступную из NCBI, и программу Gap из Genetics Computer Group, Madison WI. Уровни гомологии и идентичности, обеспеченные здесь, были получены с применением программы Gap, с использованием штрафа за пропуск 12 и штрафа за длину пропуска 4 для аминокислотных последовательностей и штрафа за пропуск 50 и штрафа за длину пропуска 3 для сравнений полинуклеотидных последовательностей.
Охарактеризовав ген в соответствии с данным изобретением, можно применять последовательность этого гена для поиска на родственные гены или пептиды в других микроорганизмах. Это может проводиться посредством поиска в существующих базах данных, например EMBL (Европейской лаборатории молекулярной биологии) или GenBank.
Упоминаемые здесь способы хорошо известны в данной области. Однако делается ссылка, в частности, на Sambrook et al., Molecular Cloning: A Laboratory Manual (1989) и Ausubel et al., Protocols in Molecular Biology (1995), John Wiley and Sons, Inc.
Пептиды или белки данного изобретения могут быть очищены и выделены способами, известными в данной области. В частности, после идентификации последовательности генов становится возможным применение рекомбинантных способов для экспрессии этих генов в подходящем хозяине. Активные фрагменты и родственные молекулы могут быть идентифицированы и могут быть применимы в терапии. Например, пептиды или их активные фрагменты могут быть использованы в качестве антигенных детерминант в вакцине для индуцирования иммунной реакции. Они могут быть также использованы в получении антител для пассивной иммунизации или диагностических применений. Подходящие антитела включают в себя моноклональные антитела или их фрагменты, в том числе одноцепочечные Fv-фрагменты. Гуманизированные антитела также находятся в объеме данного изобретения. Способы получения антител будут очевидными для специалистов с квалификацией в данной области.
Активными фрагментами пептидов являются фрагменты, которые сохраняют биологическую функцию пептида. Например, при применении для индуцирования иммунной реакции этот фрагмент должен быть достаточного размера, так что антитела, генерируемые в ответ на этот фрагмент, будут различать между данным пептидом и другими пептидами на бактериальном микроорганизме. Обычно этот фрагмент будет иметь размер по меньшей мере 30 нуклеотидов (10 аминокислот), предпочтительно 60 нуклеотидов (20 аминокислот) и наиболее предпочтительно более чем 90 нуклеотидов (30 аминокислот).
Должно быть также понятно, что, кроме родственных молекул из других микроорганизмов, данное изобретение включает в себя модификации, произведенные относительно идентифицированных здесь пептидов и полинуклеотидов, которые не изменяют значимо биологическую функцию. Специалисту с квалификацией в данной области будет понятно, что вырожденность генетического кода может обусловливать полинуклеотиды с незначащими изменениями оснований в сравнении с указанными здесь полинуклеотидами, которые, однако, кодируют те же самые пептиды. Комплементарные полинуклеотиды также находятся в рамках данного изобретения. Рассматриваются также консервативные замены на уровне аминокислот, т.е. различные кислые или основные аминокислоты могут заменяться друг другом без существенной потери функции.
Приготовление вакцин на основе идентифицированных пептидов будет известным для специалистов в данной области. Вакцинные композиции могут быть приготовлены с подходящими носителями или адъювантами, например квасцами, по мере необходимости или по желанию, для обеспечения эффективной иммунизации против инфекции. Приготовление вакцинных композиций будет очевидным для квалифицированного специалиста.
Более часто, как хорошо известно специалистам с квалификацией в данной области, может быть выбрано подходящее количество активного компонента данного изобретения для терапевтического применения, как могут быть также выбраны подходящие носители или наполнители и способы введения. Эти факторы должны выбираться или определяться в соответствии с известными критериями, такими как природа/тяжесть подлежащего лечению состояния, тип и/или состояние здоровья субъекта и т.д.
В отдельном варианте продукты данного изобретения могут быть использованы в анализах скрининга для идентификации потенциальных противомикробных лекарственных средств или для определения вирулентности. Рутинные анализы скрининга известны специалистам с квалификацией в данной области и могут быть адаптированы с использованием продуктов данного изобретения подходящим образом. Например, продукты данного изобретения могут быть использованы в качестве мишени для потенциального лекарственного средства, причем способность данного лекарственного средства инактивировать мишень или связываться с этой мишенью указывает на его потенциальную противомикробную активность.
Гены данного изобретения могут также участвовать в вирулентности микроорганизма, и, следовательно, делетирование или инактивация такого гена может быть достаточной для получения аттенуированного (авирулентного) микроорганизма.
Аттенуированные микроорганизмы могут быть получены посредством мутации, которая нарушает экспрессию любого из идентифицированных здесь генов. Квалифицированному специалисту известны способы нарушения экспрессии конкретных генов. Способы, которые могут быть использованы, включают в себя способы инсерционной инактивации или делеции генов. Аттенуированные микроорганизмы данного изобретения могут также содержать дополнительные мутации в других генах, например во втором идентифицированном здесь гене или в отдельном гене, требующемся для роста данного микроорганизма, например, мутацию aro или, в связи с Salmonella, мутацию в гене, локализованном в районе SPI2, идентифицированном в WO-А-96/17951.
Аттенуированные микроорганизмы могут быть также использованы в качестве систем-носителей для доставки гетерологичных антигенов, терапевтических белков или нуклеиновых кислот (ДНК или РНК). В этом варианте аттенуированные микроорганизмы используют для доставки гетерологичных антигена, белка или нуклеиновой кислоты к конкретному сайту in vivo. Введение гетерологичных антигена, пептида или нуклеиновой кислоты в аттенуированный микроорганизм может проводиться общепринятыми способами, включающими в себя применение рекомбинантных конструкций, например векторов, содержащих полинуклеотиды, которые экспрессируют гетерологичный антиген или лекарственный белок, а также включают в себя подходящие промоторные последовательности. Альтернативно, ген, который кодирует гетерологичный антиген или белок, может быть включен в геном данного организма и использовать эндогенные промоторы для регуляции экспрессии.
Различные продукты данного изобретения могут быть также использованы в ветеринарных применениях.
Пептиды данного изобретения были идентифицированы следующим образом.
Идентификация пептидов
Частичную библиотеку генов хромосомной ДНК Neisseria meningitidis (штамма С311+) получали с использованием плазмидных векторов pFW-phoA1, pFW-phoA2 и pFW-phoA3 (Podbielski, A. et al., Gene 1996; 177:137-147). Эти плазмиды имеют конститутивную спектиномицин-аденилтрансферазу, являющуюся маркером устойчивости к антибиотику, который придает высокий уровень устойчивости к спектиномицину и, следовательно, облегчает отбор. Кроме того, эти векторы содержат укороченный (не имеющий лидерной последовательности) ген phoA щелочной фосфатазы Escherichia coli. Эти три вектора отличаются только в отношении рамки считывания, в которой существует безлидерный ген phoA, в сравнении с сайтом рестриктазы BamHI против хода транскрипции (слева) в рамке считывания. Поскольку этот укороченный ген phoA E. coli не имеет подходящей лидерной последовательности для экспорта этого фермента через бактериальную мембрану, внеклеточная активность щелочной фосфатазы отсутствует при размножении этих плазмид в phoA-мутанте E. coli (например, штамме DH5α). Хромогенный субстрат щелочной фосфатазы, ХР (5-бром-4-хлор-3-индолилфосфат), не входит в интактные бактериальные клетки и, следовательно, может быть детектирована только активность экспортируемой или поверхностно-связанной щелочной фосфатазы. Когда активность экспортируемой или поверхностно-связанной щелочной фосфатазы присутствует, хромогенный субстрат ХР расщепляется с образованием синего пигмента, и соответствующие бактериальные колонии могут быть идентифицированы по их синему цвету.
Плазмидную ДНК расщепляли полностью BamHI и дефосфорилировали с использованием щелочной фосфатазы мелкого ракообразного. Геномную ДНК Neisseria частично расщепляли Sau3AI, так что большинство фрагментов имели, по-видимому, размер 0,5-1,0 т.п.н. при наблюдении в виде полос на 1% агарозном геле, окрашенном бромидом этидия. Эти Sau3AI-фрагменты лигировали в приготовленные векторы pFW-phoA. Штамм E. coli DH5α был выбран в качестве клонирующего хозяина, так как он не содержит функционального гена phoA. Рекомбинантные плазмиды отбирали на агаре Луриа, содержащем 100 мкг/мл спектиномицина и 40 мкг/мл хромогенного субстрата ХР. Трансформанты E. coli, несущие плазмиды, содержащие инсерт ДНК Neisseria meningitidis, который добавляет сигнальную последовательность экспорта безлидерного гена phoA, были идентифицированы по синему цвету колоний.
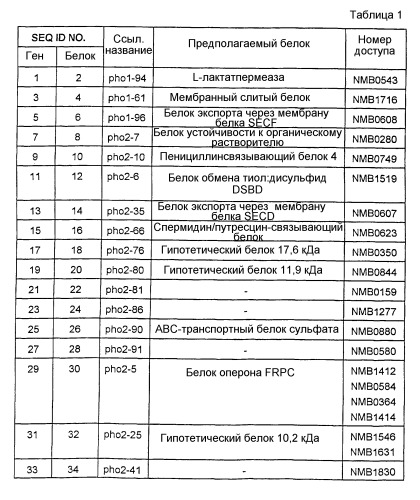
ДНК-инсерт Neisseria meningitidis, который добавляет сигнальную последовательность экспорта безлидерного гена phoA, секвенировали, и был проведен поиск на полученную последовательность среди известных белков в базе данных GenBank. Результаты показаны в таблице 1.
Защитные свойства содержащих белок-кандидат вакцин
Гены, идентифицированные в этом скрининге, оценивали в качестве потенциальных кандидатов на белковые вакцины на основе способности этих клонированных, экспрессируемых белков индуцировать иммунную реакцию у кроликов, выражающуюся в том, что полученные антитела способны стимулировать опосредованный комплементом бактериолиз Neisseria meningitidis. Защитные реакции определяли заражением живыми бактериями мышей, иммунизированных рекомбинантными белками.
В целом, гены-кандидаты амплифицировали при помощи ПЦР, клонировали и кодируемый белок экспрессировали и очищали. Очищенный белок использовали для генерирования антител для применения в твердофазном иммуноферментном анализе (ELISA). Ген PorA также ПЦР-амплифицировали, клонировали, экспрессировали и очищали. Было показано, что моноклональные антитела против PorA пассивно защищали животных в крысиной модели инфекции с детенышами крыс (Saukkonen et al., Microb. Pathog., 1987; 3(4): 261-267). Таким образом, этот белок использовали в качестве положительного контроля в некоторых экспериментах. Было показано, что PorA был неспособен защищать животное против заражения различными штаммами N. meningitidis (Poolman, Infect. Dis., 1995; 4: 13), следовательно, любой кандидат, который способен генерировать иммунную реакцию против разнообразного диапазона штаммов N. meningitidis, представляет преимущества в сравнении с PorA.
ПЦР-амплификация ДНК
Гены-кандидаты амплифицировали при помощи ПЦР с использованием геномной ДНК из штамма МС58 в качестве матрицы (McGuinness et al., Lancet, 1991; 337:514). Праймеры приведены в списке в таблице 2. F обозначает прямой праймер, и R обозначает обратный праймер. Пару праймеров PRAF и PRAR использовали для амплификации ДНК гена PorA.
Клонирование вакцинных кандидатов
ПЦР-амплифицированную ДНК из кандидатов клонировали непосредственно в вектор pCRT7/CT-TOPO InVitrogen. Этот вектор обеспечивает слияние промотора Т7, сайта связывания рибосом и С-концевой метки 6хHis для облегчения экспрессии и очистки рекомбинантных белков с использованием металл-аффинной хроматографии.
Для клонирования реакцию (реакционную смесь) лигирования трансформировали в клетки ТОР10F' (Invitrogen). Препараты ДНК из ДНК-клонов трансформантов подвергали скринингу для проверки ориентации ДНК-инсерта. Клоны из кандидатов, которые, по-видимому, имеют ДНК-инсерт в правильной ориентации, секвенировали для подтверждения целостности 5'-района данной конструкции.
Экспрессия и очистка
Клоны-кандидаты испытывали на экспрессию генов-кандидатов после трансформации в компетентные клетки НMS174(DE3)pLysS (Invitrogen). Экспрессию клонов-кандидатов индуцировали IPTG (изопропилтиогалактозидом) и экспрессию анализировали при помощи электрофореза в ДСН-ПААГ и вестерн-блоттинга с использованием антител против His спустя четыре часа после индукции. Белок-кандидат очищали с использованием смолы Talon (металл-аффинной колонки, использующей метку 6хHis, клонированную на карбоксиконце данного белка (Clontech)), с использованием градиента имидазольного буфера для элюции белка из смолы (10-100 мМ).
Получение антител
Перед получением антител сыворотку животного подвергали скринингу на низкую реактогенность в отношении цельноклеточных Neisseria meningitidis в анализах ELISA. Антитела индуцировали против каждого из клонированных и очищенных кандидатов-белков в кроликах с использованием 100 мкг белков для начальной вакцинации с адъювантом Фрейнда и трех последующих бустер-иммунизаций (ревакцинаций) при 28-дневных интервалах с неполным адъювантом Фрейнда. Сыворотку собирали после каждой бустер-иммунизации для генерирования проб сыворотки.
ELISA против цельноклеточных убитых нагреванием N. meningitidis
Анализы ELISA против убитых нагреванием N. meningitidis проводили для подтверждения, что антитела, индуцированные к очищенным белкам, узнают клетки N. meningitidis. Эти анализы проводили на штамме МС58, а также на:
Neisseria meningitidis (В) Типа 1000
Neisseria meningitidis (В) Типа SW2 107
Neisseria meningitidis (В) Типа NGH38
Neisseria meningitidis (В) Типа NGE28
Neisseria meningitidis (В) Типа 2996
Эти штаммы являются преобладающими вызывающими заболевание штаммами и охватывают генетическое разнообразие этого вида на основе дендрограммы, генерируемой мультилокусным типированием последовательности.
Получение убитых нагреванием N. meningitidis
N. meningitidis выращивали на Колумбийском агаре с содержащей шоколад лошадиной кровью (Oxoid) в течение 14 часов при 37°С в 5% СО2. Клетки соскребали из чашки с агаром и ресуспендировали эти клетки в 20 мл PBS в пробирке на 50 мл. Клеточную суспензию нагревали в течение 30 минут при 56°С для убивания бактерий.
Пробу 50 мкл убитых нагреванием N. meningitidis распределяли на Колумбийском агаре с содержащей шоколад лошадиной кровью (Oxoid) и инкубировали в течение 18 часов при 37°С, 5% СО2. Это позволяет подтвердить, что все клетки N. meningitidis были убиты. Затем убитые нагреванием клетки промывали в PBS. ОП620 этой суспензии доводили до 0,1 отн. единиц против PBS.
ELISA убитых нагреванием N. meningitidis
Анализы ELISA проводили с использованием убитых нагреванием цельноклеточных N. meningitidis. Планшеты ELISA покрывали в течение ночи убитыми нагреванием клетками (50 мкл убитых бактерий в PBS помещали в каждую лунку 96-луночного планшета и инкубировали при 4°С). Использовали стандартные протоколы ELISA, в которых все инкубации проводили при 37°С в течение 1 часа. Использовали блокирующий раствор PBS/3% БСА, промывной раствор PBS/Твин 0,1%, АР-конъюгированное вторичное антитело против кроличьего иммуноглобулина (Sigma) и реагент детектирования нитрофенилфосфата Sigma Fast P (Sigma). Данные считывали при 405 нм с использованием подходящего микропланшет-ридера. Эти данные получали с использованием сывороток, получаемых спустя семь дней после первой бустер-вакцинации (день 35 после первой вакцинации).
Данные ELISA.
Результаты показали, что антисыворотки, индуцированные против каждого белка-кандидата, индуцировали сильную реакцию против различных штаммов N. meningitidis.
Скрининг in vivo.
Для оценки защитной эффективности вакцинных кандидатов взрослых мышей иммунизировали рекомбинантными белками и защитную реакцию определяли посредством заражения живыми бактериями.
Для каждого вакцинного кандидата 15 шестинедельных мышей balb/C вакцинировали (подкожно) 25 мкг антигена в два разных дня с интервалами три недели. Спустя одну неделю после конца схемы иммунизации группу заражали гомологичным бактериальным штаммом МС58. Бактерии инокулировали внутрибрюшинно в объеме 500 мкл раствором для инфузий головной мозг/сердце/средой с 0,5% железо-декстраном при дозе 1х106 КОЕ. Предварительные результаты показали, что железо необходимо для инициации бактериемического заболевания в этих животных. Эту модель использовали ранее для демонстрации защитной эффективности вакцинации (Lissolo et al., Infect. Immunol., 1995; 63: 884-890).
Контрольные группы включали животных, вакцинированных только адъювантом (отрицательный контроль), адъювантом, объединенным с очищенным PorA (положительный контроль), или аттенуированным гомологичным штаммом. После заражения выживание подвергали мониторингу.
Животные, вакцинированные кандидатом pho2-5, показали 80% (12/15) выживание в сравнении с невакцинированными контролями, где выживали 15% (2/15). Кандидат pho2-4 показал уровни защиты, эквивалентные относительно белка porA (13/15).
Животные, вакцинированные кандидатами pho2-10, pho1-94 или pho2-66, имели выживание 40% (6/15), 47% (7/15) или 27% (4/15), соответственно, в сравнении с невакцинированными контролями, где выживали 13% (2/15).
1. Пептид, содержащий аминокислотную последовательность SEQ ID NO:10, или его гомолог в грамотрицательной бактерии, который представляет собой пенициллин-связывающий белок 4, или который по меньшей мере на 60% гомологичен или идентичен последовательности на пептидном уровне, или его фрагмент, состоящий по меньшей мере из 10 аминокислот, и который вызывает иммунный ответ, специфичный для пептида, для лечебного или диагностического применения.
2. Пептид по п.1, где гомолог по меньшей мере на 80% гомологичен или идентичен последовательности на пептидном уровне.
3. Пептид по п.1 или 2, где гомолог по меньшей мере на 90% гомологичен или идентичен последовательности на пептидном уровне.
4. Полинуклеотид, кодирующий пептид по любому из предыдущих пунктов, для лечебного или диагностического применения.
5. Клетка-хозяин, трансформированная гетерологичным полинуклеотидом по п.4 и, таким образом, экспрессирующая пептид по любому из пп.1-3.
6. Микроорганизм для лечебного или диагностического применения, содержащий мутацию, которая нарушает экспрессию любой из нуклеотидной последовательности, кодирующей пептид по п.1, где мутация является инсерционной инактивацией или делецией гена.
7. Микроорганизм по п.6, где этим микроорганизмом является Neisseria meningitidis.
8. Вакцина, содержащая пептид по любому из пп.1-3, использующаяся для лечения инфекции, вызванной грам-отрицательными бактериями.
9. Антитело, индуцированное против пептида по любому из пп.1-3, использующееся для лечения инфекции, вызванной грам-отрицательными бактериями.
10. Применение пептида по любому из пп.1-3 в скрининговом исследовании.
11. Применение полинуклеотида по п.4 в скрининговом исследовании.
12. Применение клетки-хозяина по п.5, в скрининговом исследовании.
13. Применение пептида по любому из пп.1-3 для производства лекарственного препарата для терапии или профилактики состояния, связанного с инфекцией, вызванной Neisseria или грам-отрицательными бактериями.
14. Применение полинуклеотида по п.4 для производства лекарственного препарата для терапии или профилактики состояния, связанного с инфекцией, вызванной Neisseria или грам-отрицательными бактериями.
15. Применение клетки-хозяина по п.5 для производства лекарственного препарата для терапии или профилактики состояния, связанного с инфекцией, вызванной Neisseria или грам-отрицательными бактериями.
16. Применение микроорганизма по п.6 или 7 для производства лекарственного препарата для терапии или профилактики состояния, связанного с инфекцией, вызванной Neisseria или грам-отрицательными бактериями.