Способ получения органорастворимой соли полигуанидина и органорастворимая соль полигуанидина
Иллюстрации
Показать всеОписан способ получения органорастворимой соли полигуанидина. Способ включает получение основания полигуанидина щелочным дегидрохлорированием гидрофильной соли полигуанидина с последующей нейтрализацией основания полигуанидина гидрофобной органической кислотой. В качестве гидрофобной органической кислоты используют пеларгоновую, или бензойную, или ундециленовую кислоту, а в качестве гидрофильной соли полигуанидина используют полигексаметиленгуанидингидрохлорид или поли-(4,9-диоксадодекангуанидин) гидрохлорид. Описана также органорастворимая соль полигуанидина, обладающая биоцидными и гидрофобными свойствами, со следующей структурной формулой:
где n=5-70; R=˜(СН2)6˜; ˜(СН2)3О(СН2)4O(СН2)3˜; R1=СН3(СН2)4СН=СН(СН2)4˜, СН3(СН2)7˜. 2 н.п. ф-лы, 2 табл.
Реферат
Изобретение относится к области полимерной органической химии, в частности к синтезу органорастворимых биоцидных полимеров. Такие полимеры могут быть использованы в качестве биоцидной добавки в органорастворимые полимерные и лакокрасочные материалы, нефтепродукты, резинотехнические изделия и т.п.
Известны биоцидные гидрофильные высокомолекулярные основания полигуанидинов (ПГ) - полигексаметиленгуанидин (ПГМГ) и поли-(4,9-диоксадодекангуанидин) (ПДДГ):
| где n=5-70 | |
| ПГМГ | ПДДГ |
Биоцидные свойства этим полимерам придают расположенные в полимерной цепи гуанидиновые группировки, которые являются активным началом многих природных и синтетических лекарственных веществ и антисептиков.
На практике обычно используются не сами высокомолекулярные основания ПГ, а их гидрофильные соли с минеральными или органическими кислотами, которые являются более стабильными веществами.
Гидрофильные соли ПГ обладают биоцидными свойствами: эффективны против грамположительных и грамотрицательных бактерий (включая микобактерии туберкулеза); одновременно воздействуют на аэробную и анаэробную микрофлору; вирусы, дерматофиты, плесневые, дрожжеподобные дереворазрушающие и деревоокрашивающие грибы; в водной среде эффективно подавляют нежелательную микрофлору и водоросли. В отличие от многих известных биоцидных препаратов соли ПГ обладают низкой токсичностью для человека и животных. Их разбавленные водные растворы используют в качестве дезинфицирующих средств (Биопаг, Фосфопаг, Экосепт и др.), а также в качестве биоцидных добавок в воду (питьевую, плавательные бассейны, сточные воды) и водоразбавляемые композиции (побелку, водоэмульсионные лакокрасочные материалы, цемент).
Среди гидрофильных солей ПГ наиболее известен фосфат ПГМГ, который получают путем обменного разложения гидрохлорида ПГМГ с двузамещенным фосфатом аммония (Пат. №2142451, кл. 6 С07, С279/02, А61L 2/16, 1999 г.). По другому способу из гидрохлорида ПГМГ сначала получают основание ПГМГ под действием раствора едкого натра, электродиализным методом, а затем основание ПГМГ нейтрализуют фосфорной кислотой (Пат. №2214426, кл. С08G 73/02, 2001 г.; Пат. №1728256, кл. С08G 73/02, 1988 г.).
Наиболее близким к предлагаемому изобретению является способ получения глюконата ПГМГ, который получают, обрабатывая гидрохлорид ПГМГ щелочью и добавляя к полученному основанию ПГМГ водный раствор глюконата. Глюконат ПГМГ легко растворяется в воде и является наиболее эффективным и наименее токсичным дезинфицирующим средством из всех известных солей ПГМГ (Пат. №1687261, кл. А61L 2/16, 2/18, 1989 г.).
Недостатком глюконата ПГМГ и других гидрофильных солей ПГ является их нерастворимость в органических растворителях и, как следствие, несовместимость с органорастворимыми композиционными материалами (лаки, краски, полимерные материалы, нефтепродукты и другие неводные системы). Для введения их в качестве биоцидной добавки в неводные лакокрасочные материалы приходится использовать смесь растворителей, что усложняет технологию, а также отрицательно сказывается на стабильности лакокрасочных материалов и качестве лакокрасочных покрытий.
Технической задачей, решаемой данным изобретением, является получение нового вида солей ПГ, а именно гидрофобных солей ПГ, которые, сохраняя присущие ПГ биоцидные свойства, растворяются в органических растворителях и легко совмещаются с органорастворимыми композиционными материалами.
Техническая задача решается за счет того, что сначала получают основание ПГ щелочным дегидрохлорированием гидрофильной соли ПГ, а затем полученное основание ПГ нейтрализуют гидрофобной органической кислотой. В качестве гидрофобной органической кислоты используют пеларгоновую, бензойную или ундециленовую кислоту, а в качестве гидрофильной соли ПГ используют полигексаметиленгуанидин гидрохлорид или поли-(4,9-диоксадодекангуанидин)гидрохлорид.
Сущность изобретения поясняется следующим образом.
В результате получают органорастворимую соль полигуанидина, обладающую биоцидными и гидрофобными свойствами, со следующей структурной формулой:
где n=5-70;
R=˜(CH2)6˜; ˜(СН2)3О(СН2)4O(СН2)3˜;
R1=СН3(СН2)4СН=CH(СН2)4˜, СН3(СН2)7˜.
Пеларгоновая, ундециленовая кислоты представляют собой не растворимые в воде высококипящие вязкие жидкости; растворяются в ароматических и хлорированных углеводородах, этаноле, эфире. Эти кислоты обладают биоцидными свойствами, которые хорошо сочетаются с биоцидными свойствами ПГ.
Ундециленовая кислота [СН3(СН2)4СН=СН(СН2)4СООН] - высшая одноосновная ненасыщенная карбоновая кислота. Ундециленовая кислота - известное антигрибковое средство.
Пеларгоновая кислота [СН3(СН2)7СООН] - высшая жирная одноосновная карбоновая кислота, используется в составе биостимуляторов, душистых веществ, красителей, стабилизаторов; способна пробуждать споры спорообразующих микроорганизмов.
Бензойная кислота [С6Н5СООН] - ароматическая одноосновная карбоновая кислота; в воде ограниченно растворима, легко растворяется в спирте и эфире.
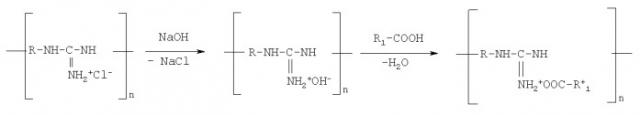
Получение органорастворимой соли ПГ проводят в две стадии: сначала гидрохлорид ПГ обрабатывают едкой щелочью, а затем полученное основание ПГ нейтрализуют гидрофобной органической кислотой. Реакции протекают по схеме:
где n=5-70;
R=˜(СН2)6˜; ˜(СН2)3О(СН2)4O(СН2)3˜;
R1=СН3(СН2)4СН=СН(СН2)4˜, СН3(СН2)7˜.
На первой стадии раствор гидрохлорида ПГ смешивают при комнатной температуре с раствором едкого натра и получают сополимер гидрохлорида и основания ПГ. Для получения 100%-ного основания ПГ полученный продукт растворяют в спирте и обрабатывают 10%-ным спиртовым раствором едкого натра, выпавшую в осадок соль (NaCl) отделяют.
На второй стадии к спиртовому раствору основания ПГ добавляют эквимолярное количество гидрофобной карбоновой кислоты. После отгонки спирта получают целевой продукт.
Приведенные примеры иллюстрируют получение заявленных гидрофобных солей ПГ.
Пример 1. Получение олеата ПДДГ.
Сначала синтезировали основание ПДДГ. Для этого 130 г (0,5 м) хлорида ПДДГ растворяли в 150 мл воды и к полученному раствору добавляли при перемешивании раствор 20 г NaOH в 30 мл воды. Пастообразный продукт реакции тщательно отделяли от водного раствора NaCl и быстро промывали небольшим объемом воды (если происходило сильное растворение полимера в воде, то добавляли небольшое количество концентрированного раствора щелочи). Затем полимер растворяли в спирте и добавляли раствор 5 г NaOH в 10 мл спирта, выпавший в осадок NaCl отделяли фильтрованием.
К полученному спиртовому раствору основания ПДДГ добавляли при перемешивании 140 г (0,5 м) олеиновой кислоты, спирт отгоняли. Полученный в виде вязкой массы полимер сушили в вакууме при 70-80° до постоянного веса. Выход олеата ПДДГ 255 г.
Найдено N, %: 8,16; 8,31; вычислено (С29Н56O4N3) N - 8,23%.
Пример 2. Получение ундециленовой соли ПГМГ.
К 33%-ному спиртовому раствору 31 г (0,2 м) ПГМГ-основания, полученного по примеру 1, добавляли при перемешивании 50%-ный спиртовой раствор 56 г (0,2 м) ундециленовой кислоты. Спирт отгоняли; полимер (вязкая масса) сушили в вакууме при 70-80°С до постоянного веса. Выход ундециленовой соли ПГМГ 82 г.
Найдено N, %: 9,96; 10,01; вычислено (C25H36О2N3) N - 10,20%.
Пример 3. Получение бензоата ПГМГ.
К 33% спиртовому раствору 16 г (0,1 м) ПГМГ-основания, полученного по примеру 1, добавляли при перемешивании 50% спиртовой раствор 12 г (0,1 м) бензойной кислоты. Спирт отгоняли; полимер (вязкая масса) сушили в вакууме при 70-80°С до постоянного веса. Выход бензоата ПГМГ 25 г.
Найдено N, %: 12,64; 12,52; вычислено (C20H20O2N3) N - 12,57%.
Пример 4. Получение пеларгоновой соли ПГМГ.
К 45 г (0,3 м) ПГМГ-основания, полученного по примеру 1(120 мл 33% спиртового раствора), добавляли при перемешивании 45 г (0,3 м) пеларгоновой кислоты. Спирт отгоняли; полимер сушили в вакууме при 70-80°С до постоянного веса. Выход пеларгоновой соли ПГМГ 80 г.
Найдено N, %: 11,48; 11,29; вычислено (С22Н32O2N3) N - 11,35%.
Пример 5. Получение пеларгоновой соли ПДДГ.
26 г (0,1 м) хлорида ПДДГ растворяли в 100 мл спирта; к полученному раствору добавляли при перемешивании 40 мл 10% спиртового раствора NaOH; осадок NaCl отделяли фильтрованием. К раствору основания ПДДГ добавляли 16 г (0,1 м) пеларгоновой кислоты, спирт отгоняли, полученную бесцветную вязкую смолу сушили в вакууме при 70-80°С до постоянного веса. Выход пеларгоновой соли ПДДГ 38 г.
Найдено N, %: 10,63; 11,08; вычислено (C20H41O4N3) N - 10,85%.
Соль ПГ с непредельной кислотой (ундециленовой) имеет темно-желтую окраску; соли ПГ с пеларгоновой и бензойной кислотами бесцветные или светло-желтые. В отличие от глюконата ПГМГ (прототип) полученные соли ПГ не растворимы в воде, но полностью растворяются в спирте, эфире, в ароматических и хлорированных углеводородах, уайт-спирите, этилцеллозольве, скипидаре.
Для изучения деформационно-прочностных и биоцидных свойств полученных по примерам 1-6 гидрофобных солей ПГ готовили их 20%-ные растворы в сольвенте, которые наносили на пластины из пластика размером 10×10 см2. Пленки полимеров, образующиеся на подложке после испарения растворителя, сушили при 60-80°С в течение 24 ч.
В таблице 1 показано, что механические свойства пленок зависят от химической природы гидрофобной органической кислоты, использованной для нейтрализации основания ПГ: соли ПГ с ундециленовой, пеларгоновой и бензойной кислотами образуют из раствора липкие, матовые, не прочные пленки. По данным динамического термогравиметрического анализа термическая деструкция полученных полимеров, сопровождающаяся заметной потерей массы, начинается при температуре ˜200-250°С.
Изучение антимикробной активности пленок гидрофобных солей ПГ в условиях, имитирующих контаминацию поверхности микроорганизмами из воздуха, проводили методом «смывов» и методом «отпечатков» [«Методы испытаний дезинфекционных средств для оценки их безопасности и эффективности». М., 1998 г., ч.2]. При изучении пленок солей ПГ по методу «смывов» в качестве тест-микроорганизма использовали S.aureus. Для нейтрализации препаратов применяли универсальный нейтрализатор, содержащий твин 80, сапонин, гистидин, цистеин, воду питьевую (по другой методике нейтрализатор включал сульфанол и 0,5% молока). На пластину с изучаемой полимерной пленкой и контрольную пластину наносили по 0,5 мл суспензии тест-микроорганизма, содержащей 2×108 микробных клеток/мл S.aureus, и выдерживали в течение 1 часа. Далее с экспериментальной и контрольной поверхностей брали смывы стерильной марлевой салфеткой, смоченной стерильным раствором нейтрализатора. Салфетки помещали в пробирки с бусами, содержащие 10 мл нейтрализатора, и в течение 10 мин встряхивали в шейкере. Затем по 0,2 мл смывной жидкости сеяли на чашки Петри на твердую питательную среду (мясопептонный или казеиновый агар). Чашки Петри помещали в термостат и инкубировали в течение 24 часов при температуре 37°С. Затем производили подсчет выросших колоний в опытном и контрольном образцах; эффективность покрытия рассчитывали в % по отношению к контролю.
В таблице 1 показано, что эффективность всех полученных по примерам 1-6 солей ПГ в отношении бактерий S.aureus через 1 час контакта составляет ˜100%.
При испытаниях антимикробной активности пленок методом «отпечатков» на поверхность опытных и контрольных образцов наносили суспензии тест-культур грамотрицательных бактерий P.aeruginosa, грамположительных бактерий S.aureus, спор B.pumilus, плесневого гриба Asp.niger в физиологическом растворе в концентрации 1×106 КОЕ/см2. Образцы помещали в чашки Петри и оставляли на 1 или 24 часа при комнатной температуре. После истечения указанных сроков, с целью определения численности жизнеспособных тест-микроорганизмов, образцы были однократно наложены на поверхность плотной питательной среды и помещены в термостат при 37°С для бактерий и 29°С для грибов (питательной средой служили: в опытах с S.aureus - мясопептонный или казеиновый агар; с С.albicans и Asp.niger - агар Сабуро). Подсчет колоний бактерий производили через 24-48 часов, а для плесневых грибов через 7 дней.
Исследования показали, что бактерии видов P.aeruginosa, S.aureus, В.pumilus (спорообразующие) и плесневого гриба A.niger, нанесенные на поверхность пленок в концентрации 5×106 КОЕ/см2, полностью инактивируются через 1 час контакта. На контрольных поверхностях сохраняется ˜103 КОЕ/см2 жизнеспособных клеток. Полученная по примеру 3 соль ПГМГ с ундециленовой кислотой, так же, как и сама ундециленовая кислота, эффективна в отношении дерматофитов (Trichophyton).
Растворимость в органических растворителях гидрофобных солей ПГ позволяет совмещать их с различными полимерными связующими и использовать в качестве биоцидной добавки к неводным лакокрасочным и полимерным композициям, нефтепродуктам. Так, например, для получения биоцидных лакокрасочных материалов 20%-ные растворы полученных по примерам 1, 2, 3, 6 солей ПГ в сольвенте вводили в качестве биоцидной добавки в лак на основе хлорсульфированного полиэтилена и в пентафталевую краску ПФ-115. Лак после высыхания образует однородную бесцветную пленку с хорошей адгезией к поверхности (1 балл по 5-балльной шкале по ГОСТ 15140, разд.2) и повышенной механической прочностью (напряжение при разрыве 8 МПа). Пентафталевая краска после введения соли ПГ сохраняет свой цвет и эксплуатационные свойства.
Микробиологические испытания лакокрасочных покрытий показали, что на их поверхности грамположительтные и грамотрицательные бактерии, споры и грибы инактивируются так же быстро и эффективно, как на поверхности пленок нативных гидрофобных солей ПГ (таблица 2).
| Таблица 1.Биоцидные и механические свойства пленок органорастворимых солей ПГ. | |||
| Пример № | Вещество | Характеристика механических свойств пленки | Эффективность пленки, % (S.Aureus, 1 час) |
| 1 | Олеат ПДДГ | Прочная, глянцевая, темно-желтая | 100 |
| 2 | Ундециленовая соль ПГМГ | Липкая, не прочная, темно-желтая | 100 |
| 3 | Бензоат ПГМГ | Не однородная, матовая, желтая | 100 |
| 4 | Пеларгоновая соль ПГМГ | Липкая, не прочная, желтая | 99,87 |
| Таблица 2.Эффективность лакокрасочных композиций, содержащих в качесиве биоцидной добавки органорастворимые соли ПГ. | |||
| Лакокрасочная композиция с биоцидной добавкой | Содержание биоцидной добавки, мас.% | Характеристика механических свойств пленки | Эффективность пленки, % (S.Aureus, 1 час) |
| Лак на основе хлорсульфированного ПЭ, ПГМГ и ундецилена | 1,5 | Прочная, глянцевая, бесцветная | 100 |
| Лак на основе хлорсульфированного полиэтилена и соли ПДДГ с пеларгоновой кислотой | 1,5 | Прочная, глянцевая, бесцветная | 100 |
| Краска на основе ПФ-115 и соли ПГМГ с ундециленовой кислотой | 7,5 | Прочная, глянцевая, белая | 100 |
| Краска на основе ПФ-115 и соли ПДДГ с олеиновой кислотой | 7,5 | Прочная, глянцевая, белая | 100 |
1. Способ получения органорастворимой соли полигуанидина, включающий получение основания полигуанидина щелочным дегидрохлорированием гидрофильной соли полигуанидина и последующая нейтрализация основания полигуанидина гидрофобной органической кислотой, отличающийся тем, что в качестве гидрофобной органической кислоты используют пеларгоновую, или бензойную, или ундециленовую кислоту, а в качестве гидрофильной соли полигуанидина используют полигексаметиленгуанидингидрохлорид или поли-(4,9-диоксадодекангуанидин)гидрохлорид.
2. Органорастворимая соль полигуанидина, полученная способом по п.1, обладающая биоцидными и гидрофобными свойствами, со следующей структурной формулой:
где n=5-70;
R=˜(СН2)6˜; ˜(СН2)3О(СН2)4O(СН2)3˜;
R1=СН3(СН2)4СН=СН(СН2)4˜, СН3(СН2)7˜.