Рекомбинантная плазмидная днк pe-his8-trxl-ar2, кодирующая гибридный белок, содержащий антимикробный пептид ареницин морского кольчатого червя arenicola marina, и штамм escherichia coli bl21(de3)/pe-his8-trxl-ar2 - продуцент гибридного белка, содержащего ареницин
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, генной и белковой инженерии и может быть использовано в медицине и в фармацевтической промышленности. Конструируют рекомбинантную плазмидную ДНК pE-His8-TrxL-Ar2 размером 4059 п.о., кодирующую гибридный белок His8-TrxL-Ar2, содержащий антимикробный пептид ареницин, состоящую из BglII/XhoI-фрагмента ДНК, содержащего промотор транскрипции Т7-РНК-полимеразы, участок связывания рибосомы и последовательность гибридного полипептида His8-TrxL-Ar2, содержащего гистидиновый октамер, модифицированный тиоредоксин A(M37L) и ареницин, и BglII/XhoI-фрагмента ДНК плазмиды рЕТ20b(+), содержащего терминатор транскрипции Т7-РНК-полимеразы, сайт инициации репликации и ген β-лактамазы, детерминирующий устойчивость трансформированных плазмидой pE-His8-TrxL-Ar2 клеток Escherichia coli к ампициллину, в качестве генетического маркера. Получают штамм Escherichia coli BL21(DE3)/pE-His8-TrxL-Ar2 - продуцента гибридного белка, содержащего антимикробный пептид ареницин. Изобретение позволяет эффективно получать гибридный белок, содержащий антимикробный пептид ареницин. 2 н.п. ф-лы, 2 ил.
Реферат
Изобретение относится к области биотехнологии, генной и белковой инженерии и может быть использовано в медицине и в фармацевтической промышленности.
Ареницин является эндогенным антибиотиком беспозвоночного Arenicola marina (пескожил морской), относящегося к классу Polychaeta (многощетинковые) типа Annelida (кольчатые черви) [пат. РФ № 2261866, С07К 14/435, А61Р 31/04, 2005]. Молекула ареницина представляет собой немодифицированную пептидную цепь, содержащую 21 аминокислотный остаток и стабилизированную одной дисульфидной связью, замыкающей цикл из 18 аминокислотных остатков. Ареницин вырабатывается целомоцитами (фагоцитирующими клетками целома червя) и обладает антибактериальной и противогрибковой активностью. Механизм действия ареницина предположительно состоит в избирательном нарушении барьерной функции клеточных мембран патогенных микроорганизмов, не затрагивающем мембраны клеток организма-хозяина. Ареницин является представителем принципиально нового семейства антимикробных пептидов и может найти применение в качестве антибиотика широкого спектра действия для купирования общих и местных инфекционных процессов различной этиологии, дезинфекции хирургических инструментов, зондов, протезов.
Ввиду сравнительно низкого содержания ареницина в природном источнике масштабные структурно-функциональные исследования и клинические испытания этого вещества целесообразно проводить с использованием искусственных аналогов, получаемых методами химического синтеза или рекомбинантной экспрессии. Вследствие достаточно большой протяженности пептидной цепи химический синтез ареницина оказывается дорогостоящим и не может рассматриваться в качестве основы для масштабирования производства. Трудности генно-инженерного подхода, в свою очередь, обусловлены цитотоксичностью ареницина, которая требует обязательной нейтрализации для достижения удовлетворительного уровня экспрессии. В большинстве созданных ранее систем рекомбинантной экспрессии других антимикробных пептидов эта задача решалась, в первую очередь, путем конструирования менее токсичных гибридных белков. Однако задача создания подобной системы для рекомбинантной экспрессии ареницина ранее решена не была.
Известна система для экспрессии антимикробного пептида цекропина А, включающая штамм E.coli MC1061, трансформированный плазмидой pCAMG, в которой в качестве партнера для экспрессии используется фрагмент L-рибулокиназы. Недостатком системы является неидентичность С-концевого аминокислотного остатка получаемого пептида соответствующему остатку природного цекропина А, вследствие чего существенно сужается спектр его антимикробной активности [Callaway J.E., Lai J., Haselbeck В., Baltaian M., Bonnesen S.P., Weickmann J., Wilcox G., Lei S.P. // Modification of the С terminus of cecropin is essential for broad-spectrum antimicrobial activity. Antimicrobial Agents and Chemotherapy, 1993, v.37(8), p.1614-1619].
Известна наиболее близкая к заявленной система для экспрессии антимикробного пептида аденорегулина, представляющая собой штамм E.coli BL21(DE3), трансформированный плазмидой pET32a-adr, полученной на основе плазмиды рЕТ32а [Zhou Y.X., Cao W., Luo Q.P., Ma Y.S., Wang J.Z., Wei D.Z. // Production and purification of a novel antibiotic peptide, adenoregulin, from a recombinant Escherichia coli. Biotechnology Letters, 2005, v.27(10), p.725-730]. Недостатком системы является наличие дополнительного остатка метионина в составе природной последовательности тиоредоксина А и четырех остатков метионина в линкере, соединяющем тиоредоксин А с последовательностью целевого полипептида. Вследствие этого при расщеплении бромцианом гибридного белка наряду с основным продуктом образуется пять дополнительных коротких полипептидных фрагментов, затрудняющих дальнейшую очистку целевого пептида.
Изобретение решает задачу конструирования плазмиды, детерминирующей синтез рекомбинантного пептида в составе гибридного белка, и создания высокопродуктивного штамма-продуцента, позволяющего получать гибридный белок His8-TrxL-Ar2 с высоким выходом.
Поставленная задача решается за счет конструирования рекомбинантной плазмидной ДНК pE-His8-TrxL-Ar2 размером 4059 п.о., кодирующей гибридный белок His8-TrxL-Ar2, содержащий антимикробный пептид ареницин, состоящей из BglII/XhoI-фрагмента ДНК (фиг.1), содержащего промотор транскрипции Т7-РНК-полимеразы, участок связывания рибосомы и последовательность гибридного полипептида His8-TrxL-Ar2, содержащего гистидиновый октамер, модифицированный тиоредоксин A (M37L) и ареницин, и BglII/XhoI-фрагмента ДНК плазмиды рЕТ20b(+), содержащего терминатор транскрипции Т7-РНК-полимеразы, сайт инициации репликации и ген β-лактамазы, детерминирующий устойчивость трансформированных плазмидой pE-His8-TrxL-Ar2 клеток Escherichia coli к ампициллину, в качестве генетического маркера, а также за счет создания штамма Escherichia coli BL21(DE3)/pE-His8-TrxL-Ar2 - продуцента гибридного белка, содержащего антимикробный пептид ареницин.
Преимущество предлагаемого изобретения заключается, во-первых, в использовании при химико-ферментативном синтезе гена ареницина набора кодонов, являющихся оптимальными для продукции белка в Escherichia coli. На фиг.1 приведена аминокислотная последовательность гибридного белка His8-TrxL-Ar2, содержащего ареницин, и соответствующая ей нуклеотидная последовательность гена. Введение остатка метионина непосредственно перед N-концевым остатком рекомбинантного ареницина обеспечивает возможность избирательного химического расщепления полипептидной цепи бромцианом с высвобождением целевого пептида, не содержащего каких-либо дополнительных аминокислотных остатков по сравнению с природным ареницином. Использование тиоредоксина А в качестве партнера для рекомбинантной экспрессии позволяет нейтрализовать токсичность антимикробного пептида для штамма-продуцента и благодаря этому достичь высоких выходов гибридного белка. Преимущество замены лейцином остатка метионина в положении 37 природного тиоредоксина А, а также использования плазмиды рЕТ20b(+) в качестве основы для создания pE-His8-TrxL-Ar2 состоит в уменьшении числа индивидуальных фрагментов, получаемых в результате расщепления гибридного белка бромцианом в кислой среде, что, в свою очередь, облегчает дальнейшую очистку целевого пептида. Расщепление гибридного белка His8-TrxL-Ar2 бромцианом дает всего один побочный продукт, значительно отличающийся по молекулярной массе и физико-химическим свойствам от целевого пептида, что облегчает решение задачи по его выделению. Наличие гистидинового октамера на N-конце экспрессируемой последовательности обеспечивает возможность аффинной очистки гибридного белка His8-TrxL-Ar2 методом металло-хелатной хроматографии. Для биосинтеза рекомбинантного белка применяются оптимальные регуляторные элементы, контролирующие его экспрессию: Т7-1ас промотор для предотвращения базальной экспрессии гена до момента начала индукции и высокого уровня транскрипции соответствующей мРНК при индукции, высокоэффективный терминатор транскрипции фага Т7, и блок стоп-кодонов, исключающих биосинтез удлиненных вариантов рекомбинантного ареницина. Преимущества предлагаемого штамма E.coli BL21(DE3) заключаются в использовании бактерий с фенотипом Lon OmpT, что исключает возможность протеолитического расщепления синтезируемого de novo рекомбинантного белка и загрязнения препарата наиболее активными протеазами Е.coli. В хромосомную ДНК BL21(DE3) интегрирован ген Т7-РНК полимеразы, что совместно с использованием Т7-lac промотора и Т7 терминатора в плазмиде pE-His8-TrxL-Ar2 обеспечивает быструю и эффективную продукцию белка клетками E.coli при индукции изопропилтио-β-D-галактозидом или лактозой.
Конструирование нового гена, кодирующего гибридный белок His8-TrxL-Ar2, осуществляют на основе плазмиды рЕТ20b(+). Искусственный ген, кодирующий гистидиновый октамер, модифицированный тиоредоксин A (M37L) и ареницин, фланкированный сайтами рестриктаз BglII и XhoI, получают химическим синтезом набора олигонуклеотидных фрагментов с последующей их сборкой и амплификацией при помощи полимеразной цепной реакции (ПЦР). Перед легированием для получения липких концов амплификат и векторную плазмиду обрабатывают рестриктазами BglII и XhoI. Лигазную смесь используют для трансформации компетентных клеток E.coli DH10B. Отбор положительных клонов проводят при помощи ПЦР с использованием специфических праймеров и последующим рестриктным анализом выделенной плазмидной ДНК. Структуру гена, кодирующего гибридный белок, содержащий ареницин, определяют секвенированием по методу Сэнгера.
Рекомбинантная плазмидная ДНК pE-His8-TrxL-Ar2, кодирующая гибридный белок His8-TrxL-Ar2, содержащий антимикробный пептид ареницин, характеризуется следующими признаками:
- имеет размер молекулы 4059 п.о.;
- кодирует гибридный белок His8-TrxL-Ar2, содержащий гистидиновый октамер, модифицированный тиоредоксин А (M37L) E.coli и ареницин;
- состоит из: BglII/XhoI-фрагмента ДНК, содержащего промотор транскрипции Т7-РНК-полимеразы, участок связывания рибосомы и последовательность гибридного полипептида His8-TrxL-Ar2, содержащего гистидиновый октамер, модифицированный тиоредоксин А (M37L) и ареницин, и BglII/XhoI-фрагмента ДНК плазмиды рЕТ20b(+), содержащего терминатор транскрипции Т7-РНК-полимеразы, сайт инициации репликации и ген β-лактамазы;
- имеет уникальную совокупность признаков: промотор и терминатор транскрипции РНК-полимеразы бактериофага Т7; сайт связывания рибосомы; искусственный ген, кодирующий гибридный белок His8-TrxL-Ar2, содержащий гистидиновый октамер, модифицированный тиоредоксин A (M37L) и ареницин; ген β-лактамазы, детерминирующей устойчивость трансформированных плазмидой pE-His8-TrxL-Ar2.
Для получения штамма-продуцента гибридного белка His8-TrxL-Ar2 препаратом плазмидной ДНК pE-His8-TrxL-Ar2 трансформируют компетентные клетки Escherichia coli BL21(DE3) и проводят отбор клонов, обладающих способностью экспрессировать рекомбинантный белок. Уровень экспрессии рекомбинантных белков контролируют с помощью денатурирующего ПААГ-электрофореза.
Полученный штамм-продуцент Escherichia coli BL21(DE3)/pE-His8-TrxL-Ar2 характеризуется следующими признаками.
Морфологические признаки: клетки палочковидной формы, грамотрицательные, неспороносные.
Культуральные признаки: при росте на агаризованной среде LB колонии круглые, гладкие, мутные, блестящие, серые, край ровный. При росте на жидких средах (на минимальной среде с глюкозой или YT-бульоне) образуют интенсивную ровную муть.
Физико-биологические признаки: клетки растут при температуре от 4°С до 40°С при оптимуме рН от 6,8 до 7,5. В качестве источника азота используют как минеральные соли в аммонийной форме, так и органические соединения в виде пептона, триптона, дрожжевого экстракта, аминокислот и т.д. В качестве источника углерода используют аминокислоты, глицерин, углеводы.
Устойчивость к антибиотикам: клетки проявляют устойчивость к ампициллину (до 500 мкг/мл), обусловленную наличием в плазмиде гена β-лактамазы (bla).
Преимущества предлагаемого штамма-продуцента заключаются в использовании бактерий с фенотипом Lon OmpT, что исключает возможность протеолитического расщепления синтезируемого de novo рекомбинантного белка и загрязнения препарата наиболее активными протеазами Е.coli. В хромосомную ДНК BL21(DE3) интегрирован ген Т7-РНК полимеразы, что совместно с использованием Т7-lac промотора и Т7 терминатора в плазмиде pE-His8-TrxL-Ar2 обеспечивает быструю и эффективную продукцию белка клетками E.coli при индукции изопропилтио-β-D-галактозидом или лактозой.
Клетки E.coli BL21(DE3)/pE-His8-TrxL-Ar2 являются суперпродуцентом. При индукции изопропилтио-β-D-галактозидом происходит эффективный биосинтез гибридного белка His8-TrxL-Ar2, содержащего ареницин, который накапливается в клетках в количестве 20-25% от суммарного белка бактерии.
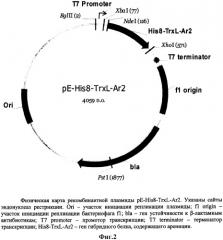
На фиг.1 представлена нуклеотидная последовательность BglII/XhoI-фрагмента ДНК, содержащего промотор транскрипции Т7-РНК-полимеразы, участок связывания рибосомы и последовательность гибридного полипептида His8-TrxL-Ar2; приведена соответствующая аминокислотная последовательность His8-TrxL-Ar2; показаны природные нуклеотидные и аминокислотные последовательности тиоредоксина A E.coli и ареницина-2 A.marina. На фиг.2 представлена физическая карта плазмиды pE-His8-TrxL-Ar2.
Изобретение иллюстрируют следующие примеры.
Пример 1.
Конструирование рекомбинантной плазмидной ДНК pE-His8-TrxL-Ar2.
Нуклеотидную последовательность, соответствующую гену His8-TrxL-Ar2, получают химико-ферментативным синтезом. Химический синтез олигонуклеотидов, используемых для сборки нуклеотидной последовательности, выполняют твердофазным фосфоамидитным методом с наращиванием олигонуклеотидной цепи в направлении от 3′-конца к 5′-концу с помощью защищенных фосфамидитов - 5′-диметокситритил-N-ацил-2′-дезоксинуклеозид-3′-O-(β-цианэтилдиизопропиламино)-фосфитов, активированных тетразолом. Фрагмент, кодирующий модифицированный тиоредоксин A (M37L) получают методом ПЦР-амплификации и направленного мутагенеза с помощью ген-специфических праймеров, используя в качестве исходной матрицы ген тиоредоксина A E.coli. Остальные участки последовательности получают путем последовательного отжига и элонгации взаимно перекрывающихся олигонуклеотидов. На завершающей стадии синтеза последовательность амплифицируют с помощью праймеров, несущих на 5′-концах сайты узнавания рестриктаз BglII и XhoI. Продукт амплификации гидролизуют указанными рестриктазами, очищают электрофорезом в 1,5% агарозном геле, полосу ДНК величиной около 570 п.о. выделяют из геля методом электроэлюции в 15% раствор ПЭГ-6000 и используют в лигазной реакции с фрагментом ДНК размером около 3,5 тыс.п.о., полученным в результате обработки плазмиды рЕТ20b(+) рестриктазами BglII и XhoI. В результате лигазной реакции образуется кольцевая ковалентно замкнутая ДНК размером 4059 п.о. Лигазную смесь используют для трансформации компетентных клеток E.coli DH-10B, приготовленных по стандартному протоколу с помощью 0,1 М хлорида кальция. После трансформации суспензию бактерий смешивают с питательной средой LB, растят 1 ч при 37°С и высевают на чашки Петри с LB-агаром, содержащим 50 мкг/мл ампициллина.
Первичный отбор клонов, содержащих нужную плазмиду, осуществляют методом "ПЦР с клонов". Отобранные клоны используют для подращивания в жидкой среде и выделения плазмидной ДНК, которую анализируют на наличие вставки с помощью рестриктного анализа. Окончательное строение плазмид, содержащих требуемый фрагмент, подтверждают определением нуклеотидной последовательности секвенированием по Сэнгеру. По данным секвенирования отбирают ту плазмиду, у которой нуклеотидная последовательность легированной вставки полностью идентична первоначально запланированной (фиг.1).
Пример 2.
Получение штамма-продуцента E.coli BL21(DE3)/pE-His8-TrxL-Ar2, вырабатывающего рекомбинантный белок His8-TrxL-Ar2, и определение его продуктивности.
Проводят трансформацию клеток E.coli BL21(DE3) плазмидой pE-His8-TrxL-Ar2, как описано в примере 1. Петлей переносят несколько колоний в 10 мл жидкой среды LB, содержащей 150 мкг/мл ампициллина, подращивают до оптической плотности OD600 0,7 на термостатируемой качалке со скоростью вращения 200 мин-1 при температуре 37°С, отбирают аликвоту культуры для последующего анализа, добавляют индуктор - изопропилтио-β-D-галактозид до концентрации 0,2 мМ и продолжают инкубацию при температуре 27°С в течение 5 ч, отбирая каждый час пробы по 0,3 мл для определения оптической плотности OD600 и последующего электрофоретического анализа. Равные аликвоты суспензии клеток, отобранных до внесения индуктора и после завершения роста, центрифугируют, отделяют супернатант и анализируют осадок клеток ПААГ-электрофорезом в денатурирующих условиях. Для этого образцы лизируют буфером, содержащим 1% SDS, 1% β-меркаптоэтанола, 8М мочевину на водяной бане в течение 5 мин. Электрофорез проводят в 15% SDS-ПААГ. Гель прокрашивают 0,025% кумасси G-250 по стандартной методике. Появление отчетливой полосы в районе 16 кДа в образцах, отобранных после индукции, свидетельствует о способности штамма синтезировать рекомбинантный His8-TrxL-Ar2. Относительное содержание рекомбинантного белка определяют путем сканирования и денситометрического анализа окрашенных гелей.
1. Рекомбинантная плазмидная ДНК pE-His8-TrxL-Ar2 размером 4059 п.о., кодирующая гибридный белок His8-TrxL-Ar2, содержащий антимикробный пептид ареницин, состоящая из
BglII/XhoI-фрагмента ДНК, приведенного на фиг.1, содержащего промотор транскрипции Т7-РНК-полимеразы, участок связывания рибосомы и последовательность гибридного полипептида His8-TrxL-Ar2, содержащего гистидиновый октамер, модифицированный тиоредоксин A (M37L) и ареницин,
BglII/XhoI-фрагмента ДНК плазмиды рЕТ20b(+), содержащего терминатор транскрипции Т7-РНК-полимеразы, сайт инициации репликации и ген β-лактамазы, детерминирующий устойчивость трансформированных плазмидой pE-His8-TrxL-Ar2 клеток Escherichia coli к ампициллину, в качестве генетического маркера.
2. Штамм Escherichia coli BL21(DE3)/pE-His8-TrxL-Ar2 - продуцент гибридного белка, содержащего антимикробный пептид ареницин.