Производные бензамида или фенилацетамида, полезные в качестве лигандов тиреоидного рецептора
Иллюстрации
Показать всеДанное изобретение относится к производные бензамида или фенилацетамида, которые являются лигандами тиреоидных рецепторов, и к способам получения данных соединений. Кроме того, заявляется фармацевтическая композиция, обладающая активностью в отношении рецептора тиреоидного гормона, содержащая эффективное количество заявленного соединения или его фармацевтически эффективной соли в сочетании с фармацевтически приемлемым носителем, и способ ее получения. В настоящем изобретении также заявляется способ профилактики, ингибирования или лечения заболевания, которое зависит от экспрессии Т3 регулируемого гена или ассоциировано с нарушением метаболизма, который включает введение пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества заявленного соединения. Целью изобретения является применение соединения для изготовления лекарственного средства для ингибирования или лечения заболевания, которое зависит от экспрессии Т3 регулируемого гена или связанного с нарушением метаболизма. 8 н. и 4 з.п. ф-лы.
Реферат
Область техники, к которой относится изобретение
Данное изобретение относится к новым соединениям, которые представляют собой лиганды тиреоидных рецепторов, а также к способам получения указанных соединений и к способам их применения, таким как регулирование метаболизма.
Предшествующий уровень техники
Хотя важная роль тиреоидных гормонов в регулировании метаболизма у людей хорошо известна, открытие и разработка новых специфических лекарственных средств для лучшего лечения гипертиреоза и гипотиреоза осуществляется медленно. Такое положение ограничивает также разработку тиреоидных агонистов и антагонистов для лечения других важных клинических симптомов, таких как гиперхолестеринемия, ожирение и сердечная аритмия.
Тиреоидные гормоны фактически воздействуют на метаболизм каждой клетки организма. При нормальных уровнях содержания данные гормоны поддерживают массу тела, показатели обмена веществ, температуру тела и настроение, а также влияют на уровни содержания в крови сывороточного липопротеина низкой плотности (low density lipoprotein - LDL). Поэтому при гипотиреозе имеет место повышение массы тела, высокие уровни содержания холестерина LDL и депрессия. При гипертиреозе данные гормоны приводят к потере массы тела, гиперметаболизму, снижению уровней содержания сывороточного LDL, сердечной аритмии, сердечной недостаточности, мышечной слабости, остеопорозу у женщин в постклемактерический период и состоянию тревоги.
В настоящее время тиреоидные гормоны используются главным образом в заместительной терапии при лечении пациентов, страдающих гипотиреозом. Терапия с использованием L-тироксина возвращает метаболические функции к нормальному состоянию и может легко контролироваться стандартными измерениями уровней содержания тиреостимулирующего гормона (ТСГ), тироксина (3,4,3',5'-тетрайод-L-тиронина или Т4) и трийодтиронина (3,5,3'-трийод-L-тиронина или Т3). Однако заместительная терапия, особенно для более пожилых пациентов, может ограничиваться некоторыми вредными эффектами тиреоидных гормонов.
Кроме того, некоторые эффекты гормонов щитовидной железы могут быть терапевтически полезными для расстройств, не связанных со щитовидной железой, если снизить до минимума или исключить их побочные эффекты. Такие потенциально полезные эффекты включают снижение массы, снижение уровней содержания сывороточного LDL, облегчение депрессии и стимулирование образования костной массы. Ранее попытки фармацевтического применения тиреоидных гормонов для лечения таких расстройств ограничивались проявлениями гипертиреоза и особенно токсичностью для сердечно-сосудистой системы.
Более того, полезные в качестве лекарственных средств тиреоидные агонисты должны сводить к минимуму возможность нежелательных последствий вследствие локально индуцированного гипотиреоза, то есть суб-нормальных уровней тиреоидной гормональной активности в некоторых тканях и органах. Такое состояние может возникать вследствие того, что повышенные концентрации циркулирующих агонистов тиреоидных гормонов могут вызывать подавление секреции гипофизом тиреостимулирующего гормона (ТСГ), в результате чего снижается синтез тиреостимулирующего гормона щитовидной железой (отрицательная регуляция с обратной связью). Поскольку уровни содержания эндогенных тиреоидных гормонов снижаются, в любом месте, где введенное лекарственное средство, представляющее собой тиреоидный агонист, недостаточно компенсирует снижение содержания эндогенных гормонов в специфических тканях, может возникать локализованный гипотиреоз. Например, если лекарственное средство, представляющее собой тиреоидный агонист, не преодолевает гематоэнцефалический барьер, влияния подавления секреции ТСГ могут приводить к гипотиреозу ЦНС и ассоциированным с ним рискам, таким как депрессия.
Разработка специфических селективных лигандов рецепторов тиреоидных гормонов, особенно агонистов рецепторов тиреоидных гормонов, может привести к получению специфических терапевтических средств для лечения этих общих расстройств, не проявляющих токсичности в отношении сердечно-сосудистой системы и другой токсичности, характерной для нативных гормонов щитовидной железы. Агонисты тиреоидных гормонов, обладающие тканевой селективностью, могут быть получены посредством селективного тканевого поглощения или проникновения, местной или локальной доставкой, направленной на клетки через другие лиганды, присоединенные к агонисту, и направленной на рецепторные подтипы. Тканевая селективность может также достигаться селективной регуляцией в ткани генов, чувствительных к тиреоидным гормонам, специфическим образом.
Соответственно, открытие соединений, которые являются лигандами рецепторов тиреоидных гормонов, в частности селективными агонистами рецепторов тиреоидных гормонов, может продемонстрировать их применимость для лечения или профилактики заболеваний или расстройств, связанных с активностью тиреоидных гормонов, например, (1) в заместительной терапии для пожилых субъектов с гипотиреозом и риском сердечно-сосудистых осложнений; (2) в заместительной терапии пожилых субъектов с субклиническим гипотиреозом и риском сердечно-сосудистых осложнений; (3) при ожирении; (4) при гиперхолестеринемии, обусловленной повышенными уровнями содержания в плазме LDL; (5) при депрессии; и (6) при остеопорозе в сочетании с ингибитором резорбции кости.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
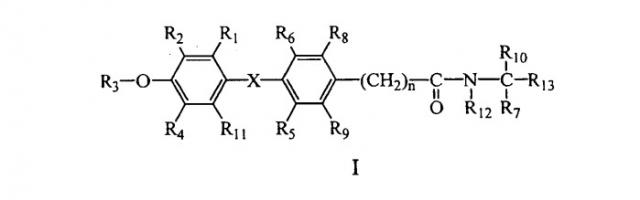
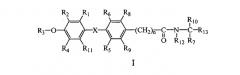
В соответствии с типичными вариантами осуществления изобретения и продемонстрированными признаками данного изобретения предлагаются соединения, которые являются лигандами тироидных рецепторов и представлены общей формулой I:
или их фармацевтически приемлемая соль, где:
R1 выбран из группы, включающей водород, галоген и С1 - С6;
R2 выбран из группы, включающей галоген, С1-С6 алкил, С2-С6 алкенил, С2-С6 алкинил, С4-С7 циклоалкенил, С3-С7 циклоалкокси, SO2(NR14R15),N(R16)SO2R17, SR17, SOR17, SO2R17, COR16 и CR18(OR16)R19; или R2 представляет собой водород, когда R4 представляет собой алкил и R1 представляет собой галоген;
R3 выбран из группы, включающей водород, алкил, бензил, ароил и алканоил;
R4 представляет собой галоген, циано или алкил;
R5 и R6 независимо выбраны из водорода, галогена, циано, С1-4 алкила, С3-С6 циклоалкила; где, по меньшей мере, один из R5 и R6 не является водородом;
R7 и R10 независимо выбраны из водорода, галогена, арила и алкила, и R7 и R10 могут соединяться, составляя цепь, содержащую от 2 до 6 метиленовых групп, с образованием 3-7-членного кольца;
R8 и R9 каждый независимо выбран из группы, включающей водород, галоген, алкокси, гидрокси (ОН), циано и алкил;
при условии, что не более чем один из R2, R4, R8 и R9 представляет собой водород;
R11 представляет собой водород, галоген или алкил;
R12 представляет собой водород или алкил;
R13 представляет собой карбоновую кислоту (СООН) или ее сложные эфиры, фосфоновую или фосфиновую кислоту или их сложные эфиры, сульфоновую кислоту, тетразол, гидроксамовую кислоту, тиазолидиндион, ацилсульфонамид или другие производные карбоновых кислот, известные в данной области техники;
R14 и R15 в каждом случае независимо выбраны из группы, включающей водород, алкил, циклоалкил, арил, гетероарил, арилалкил и гетероарилалкил, и R14 и R15 могут соединяться, составляя цепь из 3-6 метиленовых групп, с образованием 4-7-членного кольца;
R16 выбран из группы, включающей водород, алкил, циклоалкил, арил, гетероарил, арилалкил и гетероарилалкил;
R17 выбран из группы, включающей алкил, циклоалкил, арил, гетероарил, арилалкил и гетероарилалкил;
R18 и R19 в каждом случае независимо выбраны из группы, включающей водород, алкил, циклоалкил, арил, гетероарил, арилалкил или гетероарилалкил;
n представляет собой целое число 0, 1 или 2;
Х выбран из -О-, -СН2-, -CF2-, -Se-, -NH-, -S-, -SO-, -SO2- и -СО-.
Определение формулы I, представленной выше, включает все пролекарства, стереоизомеры и фармацевтически приемлемые соли формулы I.
Соединения формулы I представляют собой лиганды рецепторов тиреоидных гормонов и включают соединения, которые являются, например, селективными агонистами, частичными агонистами, антагонистами или частичными антагонистами тиреоидного рецептора. Предпочтительно соединения формулы I обладают активностью в качестве агонистов тиреоидного рецептора и могут использоваться для лечения заболеваний или расстройств, связанных с активностью тиреоидного рецептора. В частности, соединения формулы I могут использоваться для лечения заболеваний или расстройств, которые связаны с нарушением метаболизма или которые зависят от экспрессии Т3 регулируемого гена, таких как ожирение, гиперхолестеринемия, атеросклероз, сердечная аритмия, депрессия, остеопороз, гипотиреоз, зоб, рак щитовидной железы, глаукома, кожные расстройства или заболевания и застойная сердечная недостаточность.
Данное изобретение представляет соединения формулы I, фармацевтические композиции, содержащие данные соединения, и способы применения указанных соединений. В частности, данное изобретение представляет фармацевтическую композицию, содержащую терапевтически эффективное количество соединения формулы I, одного или в сочетании с фармацевтически приемлемым носителем.
Кроме того, в соответствии с данным изобретением предложен способ профилактики, ингибирования или лечения прогрессирования или начала заболеваний или расстройств, связанных с тиреоидным рецептором, таких как заболевания или расстройства, определенные выше и далее, где терапевтически эффективное количество соединения формулы I вводится млекопитающему, например человеку, нуждающемуся в таком лечении.
Соединения данного изобретения могут использоваться сами по себе, в комбинации с другими соединениями данного изобретения или в комбинации с одним или несколькими другими лекарственными средствами, активными в терапевтических областях, определенных выше.
Кроме того, представлен способ профилактики, ингибирования или лечения заболеваний, определенных выше и далее, где терапевтически эффективное количество смеси соединения формулы I и другого соединения данного изобретения и/или терапевтического средства другого типа вводится млекопитающему, нуждающемуся в таком лечении.
Соединения данного изобретения включают, но без ограничения, следующие соединения:
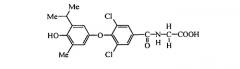
N-[3,5-дихлор-4-(4-гидрокси-3-изопропил-5-метилфенокси)бензоил]глицин (Е1);
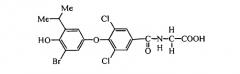
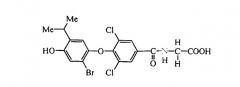
N-[3,5-дихлор-4-(3-бром-4-гидрокси-5-изопропилфенокси)бензоил]глицин (Е2);
N-[3,5-дихлор-4-(2-бром-4-гидрокси-5-изопропилфенокси)бензоил]глицин (Е3);
N-[3,5-дихлор-4-(3-хлор-4-гидрокси-5-изопропилфенокси)бензоил]глицин (Е4);
N-[3,5-дихлор-4-(3-циано-4-гидрокси-5-изопропилфенокси)бензоил]глицин (Е5);
N-[3,5-дихлор-4-(3-фтор-4-гидрокси-5-изопропилфенокси)бензоил]глицин (Е6);
N-[3,5-дихлор-2-метил-4-(3-метил-4-гидрокси-5-изопропилфенокси)бензоил]глицин (Е7);
N-[3,5-дибром-2-метил-4-(3-метил-4-гидрокси-5-изопропилфенокси)бензоил]глицин (Е8);
N-[3,5-диметил-2-метил-4-(3-метил-4-гидрокси-5-изопропилфенокси)бензоил]глицин (Е9);
L-N-[3,5-дибром-4-(3-фтор-4-гидрокси-5-изопропилфенокси)фенилацетил]валин (Е10);
D-N-[3,5-дибром-4-(3-хлор-4-гидрокси-5-изопропилфенокси)фенилацетил]фенилглицин (Е11);
L-N-[3,5-дибром-4-(4-гидрокси-3-изопропил-5-метилфенокси)фенилацетил]валин (Е12);
L-N-[3,5-дибром-4-(4-гидрокси-3-изопропил-5-метилфенокси)фенилацетил]фенилглицин (Е13);
L-N-[3,5-дибром-4-(3,5-диметил-4-гидроксифенокси)фенилацетил]фенилглицин (Е14)
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Далее приводятся определения, которые относятся к терминам, используемым в данном описании, если конкретные примеры не ограничены другими определениями.
Термин «лиганд тиреоидного рецептора» в данном изобретении относится к любому фрагменту, который связывается с тиреоидным рецептором. Лиганд может выступать в качестве агониста, антагониста и частичного агониста или частичного антагониста. Синонимом термина «лиганд тиреоидного рецептора» является «тиреомиметик».
Если не указано другого определения, термин «алкил», используемый в данном описании сам по себе или как часть другой группы, включает углеводороды с прямой и разветвленной цепью, содержащие в нормальной цепи от 1 до 12 атомов углерода (в случае алкила или алк), предпочтительно от 1 до 4 атомов углерода, такие как метил, этил, пропил, изопропил, бутил, трет-бутил, или изобутил, пентил, гексил, изогексил, гептил, 4,4-диметилпентил, окстил, 2,2,4-триметилфенил, нонил, децил, ундецил, додецил. Как определено и заявлено в данном изобретении, термин «алкил» включает алкильные группы, определенные выше, необязательно замещенные 1-4 заместителями, которые могут представлять собой галоген, например F, Br, Cl или I, или CF3, алкил, алкокси, арил, арилокси, арил(арил) или диарил, арилалкил, арилалкилокси, алкенил, алкинил, циклоалкил, циклоалкенил, циклоалкилалкил, циклоалкилалкилокси, необязательно замещенный амино, гидрокси, гидроксиалкил, ацил, оксо, алканоил, гетероарил, гетероарилокси, циклогетероалкил, арилгетероарил, арилалкоксикарбонил, гетероарилалкил, гетероарилалкокси, арилоксиалкил, арилоксиарил, алкиламидо, алканоиламино, арилкарбониламино, алкоксикарбонил, алкиаминокарбонил, нитро, циано, тиол, галогеналкил, тригалогеналкил, алкилтио или карбоксил (или его алкиловый эфир).
Если не указано другого определения, термин «циклоалкил», используемый в данном описании сам по себе или как часть другой группы, включает насыщенные циклические углеводородные группы или частично ненасыщенные (содержащие 1 или 2 двойные связи) циклические углеводородные группы, содержащие одно кольцо и включающие от 3 до 8 атомов углерода, предпочтительно от 3 до 6 атомов углерода, образующих кольцо. Как определено и заявлено в данном изобретении, термин «циклоаклил» включает циклоалкильные группы, как определено выше, необязательно замещенные 1 или несколькими заместителями, такими как заместители, определенные для алкила.
Термин «арил» или «Ar», используемый в данном описании сам по себе или как часть другой группы, относится к моноциклическим или бициклическим ароматическим группам, содержащим от 6 до 10 атомов углерода в циклической части (таким как фенил или нафтил, включая 1-нафтил или 2-нафтил). Как определено и заявлено в данном изобретении, термин «арил» включает арильные группы, как определено выше, необязательно замещенные на любом(ых) доступном(ых) атоме(ах) углерода 1 или несколькими заместителями, такими как галоген, алкил, галогеналкил, алкокси, галогеналкокси, алкенил, трифтометил, трифторметокси, алкинил, гидрокси, амино, нитро, циано, карбоксил (или его алкиловый эфир), или любыми другими заместителями, описанными для алкила.
Если не указано другого определения, термин «гетероарил» или «гетероароматический», используемый в данном описании сам по себе или как часть другой группы, относится к 5- или 6-членному ароматическому кольцу, которое включает 1, 2, 3 или 4 гетероарома, таких как атом азота, атом кислорода или атом серы, и таким кольцам, которые конденсированы с арилом, циклоалкилом, гетероарилом или циклогетероалкилом (например, бензотиофенил, индол), и включает их возможные N-оксиды. Термин «замещенная гетероарильная» группа включает гетероарил, необязательно замещенный одним или несколькими заместителями, такими как любой заместитель алкила или арила, которые описаны выше. Как определено и заявлено в данном изобретении, термин «гетероарил» включает гетероарильные группы, как определено выше, необязательно замещенные на любом(ых) доступном(ых) атоме(ах) углерода 1 или несколькими заместителями, такими как любой из заместителей, определенных для алкила или арила.
Если не указано другого определения, термин «алкенил», используемый сам по себе или как часть другой группы, относится к радикалам с прямой или разветвленной цепью, содержащим в нормальной цепи от 2 до 20 атомов углерода, предпочтительно от 2 до 12 атомов углерода, более предпочтительно от 2 до 8 атомом углерода, которые включают в нормальной цепи одну или несколько двойных связей, таким как винил, 2-пропенил, 3-бутенил, 2-бутенил, 4-пентенил, 3-пентенил, 2-гексенил, 3-гексенил, 2-гептенил, 3-гептенил, 4-гептенил, 3-октенил, 3-ноненил, 4-деценил, 3-ундеценил, 4-додеценил, 4,8,12-тетрадекатриенил и т.п. Как определено и заявлено в данном изобретении, термин «алкенил» включает алкенильные группы, определенные выше, необязательно замещенные на любом(ых) доступном(ых) атоме(ах) углерода 1 или несколькими заместителями, такими как любой из заместителей, определенных для алкила или арила.
Если не указано другого определения, термин «алкинил», используемый в данном описании сам по себе или как часть другой группы, относится к радикалам с прямой или разветвленной цепью, содержащим в нормальной цепи от 2 до 20 атомов углерода, предпочтительно от 2 до 12 атомов углерода, более предпочтительно от 2 до 8 атомов углерода, которые включают в нормальной цепи одну или несколько тройных связей, таким как 2-пропинил, 3-бутинил, 2-бутинил, 4-пентинил, 3-пентинил, 2-гексинил, 3-гексинил, 2-гептинил, 3-гептинил, 4-гептинил, 3-октинил, 3-нонинил, 4-децинил, 3-ундецинил, 4-додецинил и т.п. Как определено и заявлено в данном изобретении, термин «алкинил» включает алкинильные группы, определенные выше, необязательно замещенные на любом(ых) доступном(ых) атоме(ах) углерода 1 или несколькими заместителями, такими как любой из заместителей, определенных для алкила или арила.
Термин «циклоалкенил», используемый в данном описании сам по себе или как часть другой группы, относится к циклическим углеводородам, содержащим от 3 до 12 атомов углерода, предпочтительно от 5 до 10 атомов углерода, и 1 или 2 двойные связи. Типичные примеры циклоалкенильных групп включают циклопентенил, циклогексенил, циклогексадиенил или циклогептадиенил, которые могут быть необязательно замещенными, как определено для циклоалкила. Как определено и заявлено в данном определении, термин «циклоалкенил» включает циклоалкенильные группы, определенные выше, необязательно замещенные на любом(ых) доступном(ых) атоме(ах) углерода 1 или несколькими заместителями, такими, как любой из заместителей, определенных для алкила или арила.
Термин «галоген» или «гало», используемый в данном описании сам по себе или как часть другой группы, относится к хлору, брому, фтору или йоду, а также к группе CF3, где предпочтительны хлор или бром.
Термин «алканоил», используемый в данном описании сам по себе или как часть другой группы, относится к алкилу или циклоалкилу, соединенному с карбонильной группой.
Термин «ароил», используемый в данном описании сам по себе или как часть другой группы, означает арил или гетероарил, соединенный с карбонильной группой.
Если не указано другого определения, термины «алкокси», «арилокси» или «гетероарилокси», применяемые сами по себе или как часть другой группы, включают любую из описанных выше алкильных, арильных или гетероарильных групп, присоединенных через атом кислорода.
Термин «циано» в данном описании относится к -CN группе.
Термин «арилалкил» и термин «гетероарилалкил», используемые в данном описании сами по себе или как часть другой группы, относятся к алкильным группам, описанным выше, содержащим арильный или гетероарильный заместитель. Типичные примеры арилалкила включают, но без ограничения, бензил, 2-фенилэтил, 3-фенилпропил.
Если не указано другого определения, термины «арилалкокси» и «циклоалкокси», используемые в данном описании по себе или как часть другой группы, включают арильные и циклоалкильные группы, присоединенные через атом кислорода.
Термин «карбоновая кислота» или «карбокси», используемый в данном описании, относится к -СООН группе.
Термин «бензил», используемый в данном описании, относится к группе -СН2С6Н5, которая может быть необязательно замещенной, как определено выше для алкила.
Соединения формулы I могут быть представлены в виде солей, которые также включены в объем данного изобретения. Фармацевтически приемлемые соли (то есть нетоксичные, физиологически приемлемые) являются предпочтительными. Если соединения формулы I имеют, например, по меньшей мере, один основный центр, они могут образовывать кислотно-аддитивные соли. Такие соли образуются, например, с сильными неорганическими кислотами, такими как минеральные кислоты, например серная кислота, фосфорная кислота или галогенводородная кислота, с сильными органическими карбоновыми кислотами, такими как алканкарбоновые кислоты, содержащие от 1 до 4 атомов углерода, которые являются незамещенными или замещенными, например галогеном, например уксусная кислота, такими как насыщенные или ненасыщенные дикарбоновые кислоты, например щавелевая, малоновая, янтарная, малеиновая, фумаровая, фталевая или терефталевая кислота, такими как оксикарбоновые кислоты, например аскорбиновая, гликолевая, молочная, яблочная, винная или лимонная кислота, такими как аминокислоты (например, аспаргиновая, глутаминовая кислота, лизин или аргинин), или бензойная кислота, или с органическими сульфоновыми кислотами, такими как (С1-С4)алкил- или арилсульфоновые кислоты, которые являются незамещенными или замещенными, например, галогеном, например метил- или п-толуолсульфоновая кислота. Могут быть получены соответствующие кислотно-аддитивные соли, содержащие, если необходимо, дополнительно присутствующий основный центр. Соединения формулы I, содержащие, по меньшей мере, одну кислотную группу (например, СООН), могут также образовывать соли с основаниями. Подходящими солями с основаниями являются, например, соли металлов, такие как соли щелочных металлов или соли щелочно-земельных металлов, например натриевые, калиевые или магниевые соли, или аммониевые соли или соли с органическим амином, таким как морфолин, тиоморфолин, пиперидин, пирролидин, низший моно-, ди- или три- алкиламин, например этил-, трет-бутил-, диэтил-, диизопропил-, триэтил-, трибутил- или диметилпропиламин, или моно-, ди- или тригидрокси-низший алкиламин, например моно-, ди- или триэтаноламин. Могут быть получены соответствующие внутренние соли. В объем данного изобретения включены также соли, которые не подходят для фармацевтического применения, но которые могут применяться, например, для выделения или очистки свободных соединений формулы I или их фармацевтически приемлемых солей. Предпочтительные соли соединений формулы I, которые содержат основную группу, включают моногидрохлорид, гидросульфат, метансульфонат, фосфат или нитрат. Предпочтительные соли соединений формулы I, которые содержат кислотную группу, включают натриевые, калиевые и магниевые соли и соли фармацевтически приемлемых органических аминов.
Соединения формулы I могут также иметь пролекарственные формы. Любое соединение, которое будет превращаться in vivo в биоактивное средство (то есть соединение формулы I), является пролекарством и относится к данному изобретению.
Различные формы пролекарств хорошо известны в данной области техники. Подробное описание пролекарств и производных пролекарств можно найти в следующих публикациях:
(i) The Practice of Medicinal Chemistry, Camille G. Wermuth et al, Ch 31, (Academic Press, 1996), (ii) Design of Prodrugs, edited by H. Bundgaard, (Elsevier, 1985); and (iii) A Textbook of Drug Design and Development, P.Krogsgaard-Larson and H.Bundgaard, eds. Ch 5, pgs 113-191 (Harwood Academic Publishers, 1991).
Указанные публикации введены в данное описание посредством ссылок.
Примеры пролекарств, подходящих для применения в данном изобретении, включают сложные низшие алкиловые эфиры, такие как сложный этиловый эфир, или сложные ацилоксиалкиловые эфиры, такие как пивалоилоксиметил (POM), группы карбоновой кислоты для R13.
Варианты воплощений пролекарств, подходящих для применения в данном изобретении, включают пролекарства, которые защищают свободную фенольную гидроксильную группу, присутствующую в формуле I, как показано на структуре, представленной ниже, где пролекарственная ароильная или алканоильная группа представляет собой фрагмент R-CO-, в котором R представляет собой алкил, гетероарил или арил:
Кроме того, воплощения пролекарств, подходящих для защиты фенольной гидроксильной группы, как указано выше, включают простые фенольные алкиловые эфиры, такие как представленные на структуре ниже, где R=алкил. Метаболическое гидроксилирование углерода алкильной группы R, которая присоединена к фенольному кислороду, приводит к получению промежуточного продукта, способного подвергаться дальнейшему разложению с высвобождением свободной фенольной формы соединений формулы I:
Подразумевается, что все стереомеры соединений данного изобретения в смеси или в чистом форме, или по существу, в чистой форме относятся к данному изобретению. Соединения данного изобретения могут иметь асимметричные центры на любом из атомов углерода, включая любой один или R заместители. Следовательно, соединения формулы I могут существовать в энантиомерных или диастереомерных формах или в их смесях. В способах получения в качестве исходных веществ могут использоваться рацематы, энантиомеры или дистереомеры. При получении диастереомерных или энантиомерных продуктов они могут разделяться стандартными способами, например хроматографией или фракционированной кристаллизацией.
Введение терапевтического средства данного изобретения включает введение терапевтически эффективного количества средства данного изобретения. Термин «терапевтически эффективное количество», используемый в данном изобретении, относится к количеству терапевтического средства для лечения или профилактики состояния, которое может лечиться введением композиции данного изобретения. Указанное количество является количеством, достаточным для проявления заметного терапевтического, профилактического или облегчающего эффекта. Эффект может включать, например, лечение или профилактику состояний, перечисленных в данном описании. Точное эффективное количество для субъекта будет зависеть от массы тела субъекта и его состояния здоровья, природы и тяжести состояния, подлежащего лечению, рекомендаций лечащего врача и терапевтических средств или комбинации терапевтических средств, выбранных для введения. Следовательно, не следует заранее указывать точное эффективное количество.
Соединения формулы I могут быть получены типичными способами, представленными в приведенных далее схемах, а также в соответствии с описанными в литературе методиками, которые используются квалифицированными специалистами в данной области. Типичные реагенты и последовательности этих реакций описаны далее и в рабочих примерах. Защита и удаление защитных групп, описанные на схемах ниже, могут проводиться с использованием методик, хорошо известных в данной области (см., например, T.W. Greene&P.G.M.Wuts, "Pretecting Groups in Organic Synthesis", 3rd Edition, Wiley, 1999).
Методика получения соли йодония, представленная на схеме I, описана в литературе для синтеза аналогов тиреоидных гормонов («Novel Thyroid Receptor Ligands and Methods, Y.-L.Li, Y.Liu, A.Hedfors, J.Malm, C.Mellin, M.Zhang, PCT Int. App. WO 9900353 Al 990107; D.M.B. Hickey et al., J. Chem. Soc. Perkin Trans. I, 3103-3111, 1988; N.Yokoyama et al., J.Med.Chem, 38, 695-707, 1995)
и в целом для простых диариловых эфиров (E.A. Couladouros, V.I. Moutsos. Tetrahedron Lett., 40, 7023-7026). Взаимодействие соли йодония I с подходящей промежуточной гидроксибензойной кислотой 2 приводит к получению простого диарилового эфира 3, который способом, известным квалифицированному специалисту, может легко подвергаться превращению в соединения формулы I, где Х=О.
На схеме 2 представлен другой общий подход к синтезу соединений формулы I, в которых Х=О. Соответствующий замещенный фенол 4 подвергается алкилированию соответствующим промежуточным соединением 5, где Y представляет собой способную к замещению группу, такую как фтор, хлор, йод или бром, и активирующая группа В представляет собой группу, которая активирует группу Y для нуклеофильного замещения и способна впоследствии трансформироваться в группу карбоновой кислоты (такую как формил (СНО) или нитро (NO2)) с получением промежуточного продукта 6. Активирующая группа В в промежуточном продукте 6 затем последовательно трансформируется в группу карбоновой кислоты или ее производного, которое затем может дополнительно превращаться в соединения формулы I, где Х=О. Такие активирующие функциональные группы и их способности к превращению хорошо известны специалистам в данной области. Например, когда В представляет собой функциональную нитрогруппу в промежуточном продукте 6, нитрогруппа может восстанавливаться до аминогруппы хорошо известными способами, такими как применение каталитического гидрирования в присутствии, например, катализатора - никеля Ренея или палладия на углероде, в полярном растворителе, таком как ледяная уксусная кислота или этанол. Альтернативно, восстановление может осуществляться с использованием железного порошка в водной ледяной уксусной кислоте при температурах окружающей среды. Полученный ариламин может подвергаться превращению в соответствующую соль диазония применением, например, смеси нитрата натрия и серной кислоты в подходящих растворителях. Образующаяся диазониевая группа может затем подвергаться превращению в формильную группу (СНО) взаимодействием с моноксидом углерода в присутствии подходящего паладиевого катализатора, такого как ацетат палладия. После связывания с промежуточным продуктом 5 последовательные превращения защитной и функциональной группы приводят к получению целевых соединений формулы I, где Х=О. Другой активирующей группой является формил (С=-СНО). После связывания со вторым ароматическим кольцом альдегидная группа может подвергаться окислению до группы карбоновой кислоты и подвергаться дальнейшему превращению с получением соединений формулы I, в которых n=0. Кроме того, та же самая образующаяся группа карбоновой кислоты может подвергаться гомологизации до группы уксусной кислоты хорошо известными способами, такими как гомологизация Арндта-Эйстерта (Arndt-Eistert) для получения, в конечном счете, примеров соединений I, в которых n=1. Подход к общему синтезу простых диариловых эфиров для тиреомиметиков, представленный на схеме 2, подробно описан в литературе (P.D. Leeson, J.C. Emmett, J. Chem. Perkin Trans. I, 3085-3096, 1988; N. Yokoyama et al., J. Med, Chem., 38, 695-7078, 1995).
Дополнительные способы синтеза соединений формулы I, в которых Х=О, NH, S, CO или СН2 в целом описаны в литературе (для Х=О: D. M. B. Hickey et al., J. Chem. Soc. Perkin Trans. I, 3097-3102, 1988; Z-W. Guo et al., J. Org. Chem., 62, 6700-6701, 1997; D.M.T. Chan et al., Tetrahedron Lett., 39, 2933-2936, 1998; D. A. Evans et al., Tetrahedron Lett., 39, 2937-2940, 1998; G.M. Salamonczyk et al., Tetrahedron Lett., 38, 6965-6968, 1997; J.-F.Marcoux, J. Am. Chem. Soc., 119, 10539-10540, 1997; A. V. Kalinin et al., J. Org. Chem., 64, 2986-2987, 1999; для X =N:D.M.T. Chan et al., Tetrahedron Lett., 39, 2933-2936, 1998; J.P. Wolfe et al., J. Am. Chem. Soc., 118, 7215, 1996; M.S. Driver, J.F. Hartwig, J. Am. Chem. Soc., 118, 7217,1996, см. ссылки в обзоре C.G.Frost, P. Mendonca, J. Chem. Soc. Perkin I, 2615-2623, 1998; для X=S: C.R. Harrington, Biochem. J., 43, 434-437, 1948; A. Dibbo et al., J. Chem. Soc., 2890-2902, 1961; N. Yokoyama et al., United States Patent 5401772, 1995; для X=CO или CH2: L. Horner, H.H.G. Medem, Chem. Ber., 85, 520-530, 1952; G. Chiellini et al., Chemistry @ Biology, 5, 299-306, 1998; и для Х=CF2, см. G.S. Lal et al., J. Org. Chem., 65, 4830-4832, 2000).
Способы, применимые для синтеза соединений формулы I, в которых Х=О и R2 и R3 независимо выбраны из водорода, галогена и алкила, описаны в "Novel Thyroid Receptor Ligands and Methods", Y.-L. Li, Liu, A. Hedfors, J. Malm, C. Mellin, M. Zhang, PCT Int. App. WO 9900353 A1 990107.
На схеме 3 представлен синтез полупродукта 2, в котором R5=R6=Br или Cl, R8=Me, R9=H, R=H и n=0. Ацетофенон 7 (коммерчески доступен) подвергается взаимодействию с гипохлоритом натрия или гипобромитом натрия в условиях реакции образования галогенпроизводных для одновременного превращения ацетильной функции в карбоксильную и введения галогена в два орто-положения относительно фенольной гидроксильной группы. Этерификация приводит к получению целевого полупродукта 2, который применяется в последовательности химических превращений, описанных на схеме 4.
На схеме 4 описано применение полупродукта 2 для синтеза полупродукта 5, в котором Y=I и В=СНО. Промежуточный сложный эфир 2 подвергается восстановлению до альдегида 9 с помощью восстановителей, таких как гидрид диизобутилалюминия (DiBAl-H). Соединение 9 подвергается превращению в трифлат 10 применением ангидрида трифторметансульфоновой кислоты и органического аминного основания, такого как триэтиламин. Взаимодействия трифлата 10 с йодидом натрия приводит к получению целевого арилйодид-альдегида 5, который может использоваться в последовательности химических превращений, описанных на схеме 2 выше.
На схеме 5 описан синтез полупродукта 4, в котором R1 и R11 =H, R2 = изопропил и R3 представляет собой защитную ацетильную группу (-СОСН3). Фенол 11 подвергается окислению до хинона 12, который после восстановления гидросульфитом натрия (Na2S2O4) превращается в гидрохинон 13. Ацетилирование соединения 13 в стандартных условиях приводит к получению бис-ацетата 14, который после обработки 1 эквивалентом гидроксида натрия с удалением наименее заторможенной ацетатной группы приводит к получению целевого соединения 4, которое может использоваться в химических превращениях, описанных на схеме 2 выше.
На схеме 6 описан подход к синтезу соединений формулы I, в которых группа R4 представляет собой низшую алкильную группу, такую как метил или этил. Промежуточный арилбромид 15, полученный бромированием соответствующего свободного фенола (R3=OH; получен в соответствии с методиками, описанными на схеме 1 и схеме 2) с последующим введением защитной группы (PG) на фенольный гидроксил. Группа R4 вводится сочетанием промежуточного арилбромида 15 с алкилбороновой кислотой в присутствии соответствующего палладиевого катализатора, такого как [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий (II) (Harada et al., Synlett, 1995, 283). Промежуточный арилбромид может заменяться на соответствующий арилйодид или арилтрифлат и подвергаться такому же превращению.
На схеме 7 описаны две методики специфического введения метильной группы в положение R4. Оба способа осуществляются (1) гидроксиметилированием в орто-положение относительно фенольной гидроксильной группы (R3) в полупродукте 16 (полученном в соответствии с методиками, описанными на схеме 1 и схеме 2), с последующим (2) восстановлением гидроксиметильной группы до метильной группы с использованием такого реагента, как триэтилсилан. В реакции 7.1 гидроксиметилирование достигается применением гексаметилентетрамина в присутствии трифторуксусной кислоты. В реакции 7.2 стадия гидроксиметилирования ускоряется применением бензолбороновой кислоты, которая образует комплекс с первичным продуктом присоединения в форме диоксаборонового полупродукта. Целевое гидрок