Способ исследования центрального отдела заднего отрезка глаза
Иллюстрации
Показать всеИзобретение относится к офтальмологии. Сущность способа заключается в использовании определенного алгоритма проведения ультразвуковых исследований. Вначале проводят цифровое пространственное сканирование центральных отделов глаза и орбиты до получения четкого изображения одновременно диска зрительного нерва и макулы. Полученное изображение подвергают контрастированию с помощью цветового энергетического картирования и импульсной допплерографии. На этом изображении определяют толщину и плотность сетчатки, толщину и ангиоархитектонику сосудов хориоидеи, наличие новообразованных сосудов, толщину и плотность склеры, анализируют состояние диска зрительного нерва: его размеры, пространственную конфигурацию, плотность, характер васкуляризации, связь с оболочками глаза, определяют количественные показатели кровотока в зрительном нерве, в магистральных сосудах глазного яблока и орбиты. Затем формируют объемное виртуальное изображение исследуемой зоны. Вычисляют объем патологического участка, анализируют характер его поверхности, внутреннюю структуру, проводят анализ его пространственной сосудистой сети, определяют денситометрические индексы плотности и васкулогенности. Анализ совокупных данных, полученных в указанном алгоритме ультразвуковых исследований, позволяет уточнить характер патологического процесса и уровень поражения. Способ является высоко точным надежным способом диагностики, позволяющим не только уточнить характер патологического процесса, но и уровень поражения. Способ может быть использован при оптически непрозрачных средах глаза. 1 з.п. ф-лы, 4 ил.
Реферат
Предлагаемое изобретение относится к офтальмологии и предназначено для повышения качества диагностики при ряде заболеваний.
Уровень техники. До настоящего момента диагностику заболеваний глазного дна традиционно осуществляют с помощью флуоресцентной ангиографии (ФАГД), используя при этом различные красители, контрастирующие сосудистые структуры. Флуоресцентная ангиография (ФАГ) как метод диагностики сформировалась еще в начале 60-х годов и ознаменовала "новую диагностическую эру" в офтальмологии.
Особенности циркуляции биологических красителей в сосудистом русле глаза, выявляемые на ФАГД, отражают характер и степень вовлечения этих структур в патологический процесс, а также уровень поражения. В России базовым красителем для ФАГД, разрешенным к применению Фармакологическим комитетом и Минздравом РФ, является флуоресцеин натрия (Resorcinolphtalein Sodium), имеющий максимум поглощения в области 485-500 нм. Флуоресцеин натрия позволяет детально изучить особенности архитектоники сосудов сетчатки и состояние их проницаемости [Schats H., Burton T.C., Yannuzzi L.A., Rabb M.F. Interpretation of fundus fluorescent angiography. MOSBY 1978]. Однако визуализация сосудистого сплетения хориоидеи, из-за совпадения спектра поглощения этого красителя со спектром поглощения пигментного эпителия (490 нм), с его помощью затруднительна. Для этих целей за рубежом используют такой препарат, как индоцианин зеленый (Tricarbocyanine) с максимумом поглощения около 800-810 нм [Bischoff PM, Flower RW. Indocyanin green fluorescent angiography. Arch. Ophthalmol. - 1980. - Vol.58. - P.528-538; Hochheimer BF, D'Anna SA. //Angiography with the new dye. Exp Eye Res. - 1978. - Vol.27. - P.1-16. Yannuzzi L A, Slakter JS, Sorenson JA, GuyerDR, Oriok DA. Digital indocyanine green videoangiography and choroidal neovascularization.// Retina - 1992. - Vol.12, № 3.] Эта длина волны лазерного излучения позволяет глубже проникать в ткани глаза. Наряду с этим, в отличие от флуоресцеина, который свободно просачивается через стенку хориокапилляров, 98% индоцианина зеленого связывается с белками крови, что замедляет его прохождение через этот барьер и позволяет изучить сосуды хориоидеи. Применение ФАГД с индоцианином показано в случае наличия кровоизлияний, участков гиперпигментации или серозной отслойки ретинального пигментного эпителия, которые препятствуют диагностике патологических процессов, расположенных в субретинальном пространстве при ФАГД с флуоресцеином. Таким образом, каждый из красителей решает лишь одну из поставленных диагностических задач.
Данные ФАГ имеют важное значение в дифференцировании сосудистых, опухолевых и псевдоопухолевых заболеваний глаз [Кацнельсон Л.А, Форофонова Т.И., Бунин А.Я. Сосудистые заболевания глаза. - М.: Медицина, 1990. Кацнельсон Л.А., Лысенко B.C., Балишанская Т.И. Клинический атлас патологии глазного дна - М.: ГЭОТАР Медицина. 1997. - 198 С.].
Однако в ряде случаев ФАГД невозможна или противопоказана. Противопоказанием являются целый ряд состояний, например тромбоз вен нижних конечностей в анамнезе, бронхиальная астма, аллергические реакции на медикаменты, беременность и др. ФАГД невозможна при непрозрачности оптических сред глаза: при бельмах роговицы или при катаракте.
Наряду с этим ФАГД имеет ряд недостатков. Объем информации, полученной с помощью ФАГД ограничен. Метод не предоставляет информации о гемодинамических показателях кровотока в хориоидее, сетчатке, равно как и в любых других сосудах глазного яблока. Он не дает информации об истинной толщине и/или плотности хориоретинального комплекса.
Инновационными технологиями, полезными в диагностике заболеваний глазного дна, наряду с ФАГД, признаны сканирующая лазерная офтальмоскопия, оптическая когерентная томография и анализатор толщины сетчатки.
Сканирующая лазерная офтальмоскопия (Scanning laser ophthalmoscopy - SLO) позволяет изучить топографию поверхности сетчатки. Суть исследований заключается в том, что лазерный луч, испускаемый диодным лазером с длиной волны 670 нм, фокусируется на сетчатке. Встроенная система колеблющихся зеркал периодически отклоняет поток когерентного пучка света. При этом происходит серийная съемка двумерных изображений сетчатки с помощью отраженного лазерного луча. Количество света, отраженного от каждой точки сетчатки, измеряется специальным детектором и выражается в цифрах [Woon WH, Fitzke FW, Bird AC, et al. Confocal imaging of the fundus using a scanning laser ophthalmoscope. Br J Ophthalmol 1992; 76: 470-4]. В конфокальной системе свет попадает на детектор только при условии отражения его от малой области вблизи от фокальной плоскости. Свет, отраженный от областей вне фокальной плоскости, испытывает значительное ослабление. Получаемые при этом двумерные изображения объекта (макулы) рассматриваются как его оптические серийные сечения в фокальной плоскости. Серийные съемки таких сечений при различных положениях фокальной плоскости позволяют моделировать трехмерное изображение сетчатки. Такая информация может быть получена с помощью SLO.
Таким образом, информация, полученная с помощью SLO, касается только топографии сетчатки, носит ограниченный характер, а следовательно, имеет недостаточный объем. Это снижает его диагностическую ценность. Метод может служить лишь прекрасным дополнением к ФАГД.
Аналогом этой технологии является ретинотомография, полученная с помощью ретинального анализатора толщины сетчатки (см. ниже).
Ретинальный анализатор (retinal thickness analyser (RTA) представляет собой уникальную многоцелевую систему, объединяющую в себе цифровую фундус-камеру, компьютерную сканирующую щелевую лампу и программное обеспечение для анализа толщины сетчатки. Оптический срез сетчатки формируется лазерным лучом длиной волны 543 нм под фиксированным углом. Отражение луча происходит от слоя нервных волокон и пигментного эпителия сетчатки. Расстояние между этими слоями и определяет толщину сетчатки. Прибор выполняет 16 линейных послойных срезов (сканов) в секторе 3×3 мм за 0,3 с и выдает на экран монитора изображение в виде двух- или трехмерных сканограмм.
Таким образом, RTA предоставляет возможность не только картировать поверхность сетчатки, выявляя малейшие неровности, но и изучать толщину нейроэпителия. Установлено, что деформация поверхности сетчатки находится в тесной связи с остротой зрения (r=-0.4; р=0.03; n=22). Так, чем больше изменена поверхность сетчатки, тем хуже острота зрения (r=-0.5; р=0.01; n=22). Однако изменение такого фактора, как толщина сетчатки, не влияет на показатели остроты зрения (r=0.2; р=0.2; n=22). При гипопигментации РПЭ толщина сетчатки уменьшается [Shahidi 2002], при гиперплазии РПЭ - увеличивается.
Заметим, что этот метод исследования сетчатки дает больше информации, чем все предыдущие, но не опускается глубже РПЭ и не дает информации о состоянии мембраны Бруха или о хориоидее, а кроме того, не предоставляет сведений о новообразованных субретинальных сосудах. Вместе с тем анализ толщины сетчатки и степень деформации ее поверхности в ходе лечения позволяют судить об эффективности лечебного процесса. RTA может быть применен в этих целях.
Оптическая когерентная томография (optical coherence tomography - ОСТ) отображает строение сетчатки, РПЭ и хориоидеи, осуществляя прижизненное неинвазивное послойное сканирование сетчатки в поперечных срезах. Разрешающие возможности метода в аксиальной проекции достигают 10 мкм, при поперечном разрешении - в 20 мкм. [Нее MR, Baumal CR, Puliafito CA, et al. Optical coherence tomography of age-related macular degeneration and choroidal neovascularization. Ophthalmology 1996; 103: 1260-70].
Оптическая когерентная томография ОСТ основана на компьютерной обработке данных, полученных с помощью сверхлюминесцентного диодного лазерного излучения на длине волны 820 нм, отраженного от структур глазного дна. Лазерное излучение на этой длине волны обладает большей глубиной проникновения в ткани, чем то, что используется в RTA (для сравнения: 543 нм). Отраженный сигнал подвергается компьютерной обработке с применением принципов оптической интерферонометрии и подается на экран монитора в двумерном виде. Области с высокой рефлективностью представлены участками красного и желтого цвета, а области с низкой рефлектогенностью - зонами зеленого и голубого цвета.
Таким образом, благодаря ОСТ возможно изучение патологического очага в виде линейных и циркулярных сканирующих срезов. ОСТ позволяет не только диагностировать патологические структуры, расположенные в сетчатке, в субретинальном пространстве и хориоидее, определить их характер в ряде случаев, но и дифференцировать небольшие по площади участки отслойки нейросенсорного эпителия, степень и глубину распространения отека сетчатки или геморрагии. Использование метода в динамике на фоне проводимого лечения предоставляет все возможности наблюдения за ходом лечения и оценке его эффективности. Вместе с тем метод не дает никакой информации о гемодинамике сетчатки и/или хориоидеи и не позволяет изучать роль этих факторов при ряде заболеваний глазного дна.
Вместе с тем в последние годы появились данные о важной роли гемодинамических показателей в патогенезе таких заболеваний, как возрастная макулодистрофия. Это обосновало поиск и разработку способов изучения этого фактора. Одним из таких способов стала лазерная допплеровская флуориметрия.
Лазерная допплеровская флуориметрия позволяет получить количественную и объемную информацию о скорости кровотока в центральной артерии и вене сетчатки, скорости и объеме перфузии в различных отделах хориоидеи. Использование этого метода в динамике позволяет проанализировать эффективность проводимого лечения. Однако она не дает информации о толщине хориоретинального комплекса или патологического очага в субретинальном пространстве или в сетчатке и т.д. Это значительно снижает объем и диагностическую ценность метода.
Таким образом, применение неинвазирующих сканирующих лазерных технологий существенно повышает качество диагностики заболеваний глазного дна, а также предоставляет информацию для оценки эффективности проводимого лечения. Однако все они имеют существенные недостатки (см. выше) и лишь дополняют ФАГД.
Адекватное воспроизведение изображения, получаемого при использовании выше упомянутых диагностических способов исследований, предусматривало хорошую прозрачность преломляющих сред глаза. В тех же случаях, когда имели место помутнения роговицы и/или хрусталика и/или стекловидного тела, они становились непригодны в диагностике заболеваний зрительного нерва, центральных отделов сетчатки и хориоидеи. В этих случаях необходимы другие, альтернативные методы исследований. Примером таких методов служат ультразвуковые методы.
Ультразвуковые методы исследования глазного яблока прошлого поколения позволяли диагностировать внутриглазные патологические процессы, установить уровень их поражения (из сетчатки или из хориоидеи), степень распространенности (толщину и диаметр очага), а также определить, имеется ли выход процесса за пределы оболочек глаза, но при этом не давали никакого представлении о характере кровоснабжения самого глазного яблока или патологического очага.
Появление современных ультразвуковых цифровых сканирующих диагностических систем с встроенными опциями качественного и количественного анализа потоков крови на основе эффекта Допплера расширило диапазон информации. Появилась возможность исследовать "цветовую карту" и гемодинамические показатели магистральных сосудов глаза и оценить роль изменений гемодинамики в различных патологических процессах глазного дна.
Задачей нашего изобретения является разработка нового подхода в диагностике заболеваний глазного дна, включающего комплексную оценку ультразвуковых данных, полученных в режиме цифрового пространственного сканирования в комбинации с данными, полученными в режиме цветового и энергетического картирования, а также данных спектров допплеровского сдвига частот потоков крови в изучаемых сосудах глазного яблока и орбиты.
Заболевания глазного дна, при которых эти показатели могут носить существенное диагностическое значение, довольно широки. В него входят воспалительные заболевания инфекционного и неинфекционного генеза (например, туберкулезный хориоретинит, протекающий в ряде случаев с формированием гранулом, ретинит Коатса и саркоидоз), дегенеративно-дистрофические заболевания (например, влажная макулодистрофия, в том числе и те ее стадии формы, которые протекают по псевдотуморозному типу или с формированием неваскулярных мембран), а также многие опухоли. В диагностике этих состояний немаловажными дифференциально-диагностическими признаками являются не только проминенция или увеличение толщины хориоретинального комплекса в месте патологических реакций, но и такие признаки, как
- плотность сетчатки и прилежащей к ней сосудистой оболочки;
- состояние кровотока в хориоидее,
- отсутствие или наличие новообразованных сосудов в месте патологического очага,
- состояние гематоофтальмического барьера.
Из более ранних работ известно, что гематоофтальмический барьер формируется сосудистым сплетением, расположенным в орбите. Это сплетение складывается из слезной артерии и ее ветвей, а также глазничной артерии и ее ветвей и дренирующих вен, осуществляющих отток крови из этого региона (А.Я.Бунин, Л.А.Кацнельсон, А.А.Яковлев Микроциркуляция глаза. - Москва. - Медицина. - 1984 г. - С.173). Кровоснабжение непосредственного самого глазного яблока осуществляется ветвями глазничной артерии: передними и задними цилиарными артериями, а также центральной артерией сетчатки.
Известно, что система кровоснабжения глаза представляет собой естественную защиту органа зрения от воспаления, иммунологических реакций, а также от ряда других патологических состояний, сложившуюся в процессе эволюционного развития. Центральный отдел глазного дна представляет собой участок, лишенный сосудов сетчатки. Питание этой функционально значимой области сетчатки обеспечивается за счет сосудистой оболочки глаза [Kuwabara Т, Cogan DS, Studies of retinal vascular pattern. 1. Normal architecture. // Arch Ophthalmol. - 1990 - vol.64 - pp.904-911].
Хориоидальное кровообращение в фовеальной и парафовеальной зоне осуществляется благодаря плотному слою хориокапилляров. Эти хориокапилляры образуют своей передней поверхностью стенок плато или плоскость, как будто "выравненную катком". Безупречность прилежания их стенок к сетчатке имеет чрезвычайно важную роль в обеспечении нормального физиологического, а следовательно, и функционального состояния фовеальной области [Г.Г.Зиангирова. "Особенности хориоретинального кровообращения в макулярной области глаза." // Тезисы докладов I Всероссийского семинара - "Круглый стол" - Ростов-на-Дону - 2004 г. - стр.16-20]. В фовеолярной и парафовеолярной области нет артериол и венул. Любое изменение ангиоархитектоники этого отдела глазного дна может привести к нарушению анатомо-физиологического соотношения оболочек глаза сетчатка/хориоидея и инициировать формирование патологических тумороподобных структур. Последнее влечет за собой снижение функций. Классическим примером является субретинальная неоваскулярная мембрана. Гистоморфологическим субстратом которой, как известно, является формирование патологической сети новообразованных сосудов и клеточных фибробластных элементов, находящихся между собой в тумороподобной пропорции.
Вторым важным показателем благополучия этой области сетчатки являются показатели кровотока в хориоидее. Они отражают общие и/или местные нарушения в системном кровотоке конкретного пациента.
К системным нарушениям можно отнести ишемическую и гипертоническую болезнь, атеросклероз и другие. Местные нарушения могут быть вызваны сдавлением хориоидеи опухолевым или псевдоопухолевым пролифератом, расположенным снаружи или внутри глазного яблока.
В связи с указанными моментами мы предположили, что исследование ангиоархитектоники и гемодинамических показателей кровотока хориоретинального комплекса в центральных отделах глазного дна в совокупности с данными цифрового пространственного режима сканирования может иметь существенное диагностическое значение. А их динамика на фоне лечения позволит оценить эффективность проводимого лечения.
В ходе эмпирических исследований пациентов с различными заболеваниями глазного дна, а также здоровых добровольцев, нами был разработан свой алгоритм ультразвуковых исследований, позволяющий существенно повысить диагностическую значимость ультразвуковых методов анализа. Последний и является сутью настоящего изобретения.
Ближайшим аналогом предлагаемого изобретения является способ того же назначения, включающий традиционное проведение ультразвукового исследования в пространственном режиме сканирования серой шкалы при расположении плоскости сканирования вдоль передне-задней (или аксиальной) оси глаза (Диагностический ультразвук. Офтальмология. Под ред. А.В.Зубарева. - соавтор Е.А.Катькова. - Практическое руководство. - 2002 - ООО "СТРОМ" - С.120).
Задачей предлагаемого изобретения является разработка принципиально новых подходов с повышением качества, надежности и точности диагностики заболеваний центральных отделов заднего отрезка глаза.
Техническим результатом изобретения является уточнение характера и протяженности патологического процесса, уровня поражения (сетчатка, хориоидея, склера), степени вовлеченности в патологический процесс оболочек глаза.
Технический результат достигается благодаря использованию собственного алгоритма исследований, включающего совокупность следующих предложенных приемов:
- используют цифровое ультразвуковое пространственное сканирование;
- исследования проводят, ориентируя аксиальную плоскость сканирования одновременно через центр ДЗН и патологический очаг, что позволяет уточнить локализацию и протяженность патологического процесса;
- применяют комбинацию из нескольких ультразвуковых режимов сканирования (цифровое ультразвуковое пространственное сканирование, цветовое и энергетическое картирование, а также импульсную допплерографию), что дает возможность определить уровень поражения и степень вовлеченности в патологический процесс оболочек.
Способ осуществляется следующим способом.
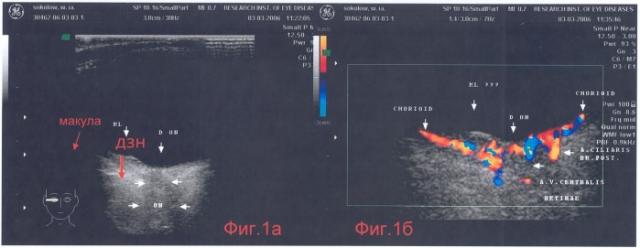
Проводят цифровое пространственное сканирование центральных отделов глаза и орбиты до получения четкого изображения одновременно диска зрительного нерва и макулярной зоны (фиг.1а).
Полученное изображение подвергают контрастированию с помощью цветового, энергетического картирования и импульсной допплерографии (фиг.1б).
На полученном при контрастировании изображении определяют толщину и плотность сетчатки, толщину и ангиоархитектонику сосудов хориоидеи, толщину и плотность склеры.
Анализируют состояние диска зрительного нерва: определяют его размеры, пространственную конфигурацию, плотность, характер васкуляризации, связь с оболочками глаза.
Определяют количественные показатели кровотока в сосудах зрительного нерва, в магистральных сосудах глазного яблока и орбиты.
На основе этого же изображения формируют объемное виртуальное изображение центрального отдела заднего отрезка глаза, вычисляют его объем.
Анализируют характер его пространственной сосудистой сети, определяют денситометрические индексы плотности и ваксулогенности.
При наличии патологического очага определяют его локализацию за счет маркировки в трех взаимоперпендикулярных плоскостях на виртуальной модели, размеры, пространственную конфигурацию, плотность, характер васкуляризации, связь с оболочками глаза.
Пример 1. Пациент Л. Поступил с диагнозом: ОД - почти зрелая возрастная катаракта. ОС: начальная возрастная катаракта, возрастная макулодистрофия.
Поступил на оперативное лечение катаракты в стационар. При подготовке к операции было обращено внимание на низкие показатели электрофизиологических исследований. Так, ретинальная острота зрения на ОД=0,1, на ОС=0,7.
Объективно: на правом глазу глазное дно не просматривалось. Рефлекс с глазного дна отсутствовал по причине непрозрачности оптических сред.
При УЗ-диагностике провели цифровое пространственное сканирование центральных отделов глаза по описанному алгоритму. Получено четкое изображение одновременно диска зрительного нерва и центральных отделов глазного дна (фиг.1а). При этом обнаружено куполообразное образование, расположенное в центральном отделе глазного дна.
Дифференциальная диагностика на этом этапе исследования включала: отслойку сетчатки, отслойку сосудистой оболочки, внутриглазную опухоль, субхориоидальное или субретинальное кровоизлияние, гигантскую кисту сетчатки, псевдотуморозную форму возрастной макулодистрофии.
Полученное изображение подвергли контрастированию с помощью цветового, энергетического картирования и импульсной допплерографии.
На полученном при контрастировании изображении было установлено, что патологический очаг находится на расстоянии 0,28 см от диска зрительного нерва, то есть практически в макуле. Определены толщина (0,15 см) и плотность сетчатки (см фиг.1б-1в), ее прилежание к хориоидее, толщина и ангиоархитектоника сосудов хориоидеи (см. фиг.1г), толщина и плотность склеры. Было установлено, что купол внутриглазного образования сформирован вторично отслоенной, утолщенной сетчаткой; что прилежащая к патологическому очагу хориоидея истончена (0,056 против 0,097 см в норме), при этом склера сохраняла свои нормальные анатомо-физиологические характеристики (толщину, плотность) и интимно прилежала к хориоидее. Таким образом, был выявлен уровень поражения: патологическое образование располагалось между внутренними отделами хориоидеи и сетчаткой.
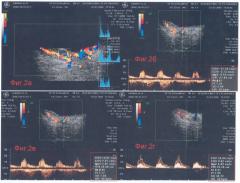
Это образование имело неоднородную акустическую плотность (фиг.2а), которая в различных отделах образования варьировала от низкой до высокой, в сочетании с низким индексом васкулогенности, это свидетельствовало в пользу формирования скорее фиброзно-соединительнотканного образования, например рубца, чем в пользу опухоли. Последняя, как известно, характеризуется акустической гомогенностью, умеренной акустической плотностью и средне-высокими индексами васкулогенности.
Анализ количественных показателей кровотока в магистральных сосудах зрительного нерва, сетчатки, в хориоидее выявил некоторые отклонения в гемодинамике магистральных сосудов сетчатки и в хориоидее (фиг.2б-2в-2г) в сторону их снижения.
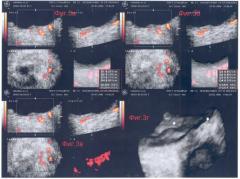
Было сформировано объемное виртуальное изображение, на котором вычислен объем патологического очага (фиг.3а), он оказался равным: V=0,203 см.
Далее был проведен анализ пространственной сосудистой сети. Оказалось, что в патологическом образовании отсутствуют собственные новообразованные сосуды. Однако ангиоархитектоника хориоидеи имела существенные отклонения. Они проявлялись в неравномерности калибра крупных хориоидальных сосудов, нарушении интимности их прилежания друг к другу, за счет чего формировались промежутки и пустоты (фиг.3б-в).
Проанализировали характер поверхности и структуры патологического образования (фиг.3г). Оно имело бугристую поверхность, неравномерную толщину и акустическую гетерогенность.
Все выше указанные УЗ-данные укладывались в картину псведотуморозной формы возрастной макулодистрофии и объясняли низкие элетрофизиологические показатели у пациента.
В дальнейшем пациенту по его настоянию была проведена экстракция катаракты без гарантий на высокие зрительные функции. После чего пациент вновь был подвергнут обследованию. При ангиографическом исследовании, проведенном в постоперационном периоде была диагностирована макулодистрофия по псевдотуморозному варианту. В клинико-ангиографической картине присутствовали как элементы экссудации (фиг.4а-г), субхориоидального кровоизлияния, так и рубцевания. Вновь установленные факты подтверждали УЗ-данные о гетерогенности образования, а также верифицировали УЗ-диагноз.
Таким образом, предлагаемый способ исследования центральных отделов заднего отрезка глаза является высоко точным и надежным способом диагностики.
1. Способ исследования центрального отдела заднего отрезка глаза, включающий проведение ультразвукового исследования, отличающийся тем, что проводят цифровое пространственное сканирование центральных отделов глаза и орбиты до получения четкого изображения одновременно диска зрительного нерва и макулярной зоны, затем полученное изображение подвергают контрастированию с помощью цветового, энергетического картирования и импульсной допплерографии, на этом изображении определяют толщину и плотность сетчатки, толщину и ангиоархитектонику сосудов хориоидеи, наличие новообразованных сосудов, толщину и плотность склеры, анализируют состояние диска зрительного нерва: его размеры, пространственную конфигурацию, плотность, характер васкуляризации, связь с оболочками глаза, определяют количественные показатели кровотока в зрительном нерве, в магистральных сосудах глазного яблока и орбиты, после чего на основе этого же изображения формируют объемное виртуальное изображение, вычисляют его объем, анализируют характер его поверхности, внутреннюю структуру, проводят анализ его пространственной сосудистой сети, определяют денситометрические индексы плотности и васкулогенности.
2. Способ по п.1, отличающийся тем, что при наличии патологического образования в центральных отделах заднего отрезка глаза определяют его локализацию, размеры, пространственную конфигурацию, плотность, характер васкуляризации, связь с оболочками глаза.