Способ изготовления многофункционального мультичипа, мультичип для последовательного или параллельного скрининга биополимеров, способ анализа биополимеров и набор для осуществления способа
Иллюстрации
Показать всеИзобретение относится к молекулярной биологии и может быть использовано в фармакологии, медицине и в охране окружающей среды. При изготовлении мультичипа используют многоуровневую систему идентификации. На поверхности индивидуальных чипов мультичипа размещают первый идентификатор, содержащий первый код, и второй идентификатор, содержащий второй код. На поверхности общей зоны мультичипа размещают третий идентификатор, содержащий третий или второй код. Мультичип, полученный указанным способом, используют для диагностики ДНК путем гибридизации продуктов амплификации исследуемой ДНК с зондами, содержащимися на поверхности указанного мультичипа или на поверхности чипов, полученных отделением от указанного мультичипа. Мультичип также используют в наборе для идентификации биополимеров совместно с реагентами для подготовки образца и проведения идентификации биополимеров. Применение изобретения позволяет повысить эффективность и снизить стоимость анализа биополимеров. 4 н. и 21 з.п. ф-лы, 10 ил.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к молекулярной биологии, фармакологии, медицине и охране окружающей среды. В частности, к способу изготовления и применения мультичипа, который позволяет проводить как последовательные, так и параллельные процедуры диагностики, например, на основе белковых или ДНК-овых зондов с применением разных типов меток и способов обработки полученных результатов.
Уровень техники
Известны два подхода к выбору типа биочипов, используемых в молекулярной биологии, фармакологии, медицине и охране окружающей среды. Первый основан на выпуске индивидуальных чипов с высокой плотностью точек - до 10000 на см2 [1]. Эти чипы дороги и в основном используются при проведении научных исследований для сканирования библиотек фрагментов ДНК, при разработке лекарственных средств или применяются в больших медицинских центрах. Другой тип чипов проблемно ориентирован на проведение анализов в небольших медицинских центрах или лабораторных условиях, где требуется диагностировать не более 100 фрагментов ДНК или белков на отдельном чипе. Основное требование к таким чипам связано с максимальной простотой получения результата и малой стоимостью анализа.
Известные чипы, изготовленные на основе предметных стекол, несмотря на свое широкое распространение [2, 3] имеют недостатки, связанные с тем, что при подготовке слайда к диагностике требуется выполнить большое число операций по установке и креплению отдельных слайдов в разных устройствах на разных этапах изготовления чипов, к которым можно отнести: модификацию поверхности, очистку поверхности и ее промывку, нанесение олигонуклеотидов, ДНК или белков, проведение гибридизации, установку в сканер для анализа результатов диагностики. Причем из-за неточной установки чипов и смещения чипов относительно друг друга и относительно основания, на которое они устанавливаются, возможны ошибки при нанесении олигонуклеотидов на выбранную зону чипа и ошибки в интерпретации результатов.
Для устранения данных ошибок разработаны способы более точной установки чипов [4], которые усложняют устройство крепления и не позволяют закрепить большое число чипов на рабочей поверхности роботов для нанесения точек. Известны технические решения, которые позволяют учитывать смещение чипов, например, за счет введения большого количества реперных точек на каждом чипе и на общей поверхности мультичипа [5], либо за счет применения сложных устройств, имеющих большие габаритные размеры [6], либо посредством контроля в реальном времени установки каждого отдельного чипа на общей платформе [7], что значительно усложняет структуру роботов.
Наиболее близким к настоящему изобретению относится способ изготовления чипов, в соответствии с которым рабочую поверхность, выполненную в форме прямоугольника [8] или круга [9], разбивают на сектора, в которых размещают рабочие зоны, относящиеся к отдельным чипам. В текстах патентов предусматривается возможность отделения от общего носителя отдельных чипов [10]. Однако в других патентах это техническое решение критикуется, поскольку отделение от несущего элемента мультичипа, выполненного, например, из стекла, связано с большим количеством брака из-за его хрупкости [11]. Кроме того, области, принадлежащие индивидуальным чипам и отделенные от мультичипа, могут не содержать идентификаторов и другой информации, идентифицирующей принадлежность чипа [12]. В этом случае каждую отделенную область мультичипа вклеивают в индивидуальный держатель, что требует дополнительных затрат, которые могут превышать затраты на изготовление отдельных чипов по стандартным процедурам.
Существует много примеров применения идентификаторов для идентификации биочипов. Например, известно изобретение [25], в котором чип имеет два штрих-кода для идентификации двух рабочих зон. Известно изобретение [10], в котором каждая индивидуальная зона с принадлежащей ей кодированной информацией в виде одного идентификатора может быть отделена от мультичипа и использована индивидуально. Известно изобретение [26], в котором рассматриваются вопросы применения идентификаторов совместно с компьютером для контроля качества изготовления чипов.
Известно изобретение [31], в котором рассмотрены варианты изготовления биочипов с большим количеством идентификаторов, выполненных в виде буквенных цифровых или цветовых графических изображений, которые идентифицируют отдельные кластеры или группы кластеров, размещенных на рабочей поверхности биочипа. С этой целью на поверхность биочипа наносится множество буквенно-цифровых кодов или кодов, комбинируемых с цветовыми точками, расположенных рядом с соответствующими кластерами. Такое техническое решение позволяет повысить надежность идентификации множества исследуемых ДНК друг относительно друга, но размещение большого числа идентификаторов на рабочем поле биочипа резко ограничивает полезную рабочую площадь биочипа, на которой могут быть размещены кластеры.
Применение мультичипов, выполненных на основе известных изобретений [10], с размещенными индивидуальными чипами на гладкой ровной поверхности несущего элемента мультичипа может привести к ошибочным результатам диагностики из-за перекрестного загрязнения образцами близлежащих зон отдельных чипов при перетекании гибридизационной смеси с чипа на чип.
Известно, что для устранения проблем кросс-контаминации в поверхности отдельных чипов формируют углубления, в которые наносят гибридизационную смесь, либо приклеивают или механически прикрепляют разделители, выполненные в виде полых цилиндров [13], либо разделяют общую плоскую поверхность основы чипа с помощью прямоугольных решеток [20], либо на твердую или гибкую основу приклеивают чипы, выполненные в виде плоских пластин [28], тем самым создавая пьедестал для сформированных индивидуальных кластеров.
Известен мультичип [30], который устраняет проблемы кросс-контаминации. Мультичип состоит из подставки и нескольких биочипов, представляющих собой последовательно соединенные микрокюветы, в которых иммобилизируются белки. Микрокюветы соединены между собой «мостиками», которые можно переламывать и разделять кюветы. Каждая микрокювета снабжена собственным отдельным пространством для осуществления реакций, то есть использование одной микрокюветы не мешает использованию другой. В подставке, выполненной в качестве независимого узла, выполнены крепежные отверстия, в которые устанавливают последовательно соединенные микрокюветы. На боковой поверхности подставки имеются цифровые и буквенные идентификаторы, с помощью которых определяют местоположение микрокювет с белковыми образцами.
Однако данное техническое решение не предполагает идентификации отдельных микрокювет, относящихся к отдельным чипам, и не предполагает связи между временным положением отдельных чипов и характеристикой данных чипов для задач идентификации. Вместо этого использована простая буквенная и цифровая идентификация положения отдельных микрокювет на время размещения чипов в подставке, что широко известно и используется в конструкции разных типов микроплашек.
Вопросы защиты от кросс-контаминации решаются за счет формирования углублений в микрокюветах. Конструкция мультичипа состоит из раздельных узлов. Такое решение дает возможность введения в процесс диагностики ошибок оператора из-за простоты смены положения микрокювет, не снабженных идентификаторами друг относительно друга на поверхности подставки.
Решение задач идентификации чипов, снижение кросс-контаминации или обеспечение возможности отделения отдельных чипов друг от друга не рассматриваются в совокупности друг с другом и решаются как разные технические задачи.
Задача настоящего изобретения состоит в повышении эффективности диагностики за счет создания новой конструкции мультичипа и создании недорогого способа последовательной или параллельной диагностики на основе мультичипа
Другой задачей настоящего изобретения является создание мультичипа для последовательного или параллельного диагностического скрининга биополимеров с усовершенствованной идентификацией как самого мультичипа, так и индивидуальных чипов, отделяемых от мультичипа, что позволяет идентифицировать индивидуальный чип относительно группы чипов, входящих в состав мультичипа.
Сущность изобретения
Одним из объектов изобретения является мультичип для последовательного или параллельного диагностического скрининга биополимеров, содержащий несущий элемент, на поверхности которого размещен массив, содержащий N индивидуальных чипов, на поверхности каждого из которых размещены кластеры с биологическими зондами и идентификаторы. Мультичип дополнительно содержит общую зону, которая размещена планарно по отношению к массиву из N чипов и расположена по границе массива или в центре массива чипов, причем общая зона выполнена в форме прямоугольника или креста и содержит, по меньшей мере, два технологических отверстия. Соединение между каждым из чипов мультичипа друг с другом и/или соединение чипов с общей зоной выполнено с возможностью разделения, при этом на поверхности индивидуальных чипов размещены первый идентификатор, содержащий первый код, второй идентификатор, содержащий второй код, а на поверхности общей зоны мультичипа размещен третий идентификатор, который имеет третий код или код, идентичный второму коду.
Другим объектом изобретения является способ изготовления мультичипа для последовательного или параллельного скрининга биополимеров, выполненного на основе плоского твердого несущего элемента, на котором размещают N индивидуальных чипов с множеством кластеров, содержащих выбранные типы зондов. Способ характеризуется тем, что на поверхность индивидуальных чипов наносят первый и необязательно второй идентификаторы, характеризующие параметры индивидуального чипа, входящего в мультичип, а на несущем элементе мультичипа дополнительно формируют общую зону, на которой выполняют крепежные отверстия и наносят третий идентификатор, причем первый идентификатор связан с первым кодом, второй идентификатор связан со вторым кодом, отличным от первого кода, третий идентификатор имеет третий код или код, идентичный второму коду, причем указанные коды образуют уникальные N пар кодов, характеризующих многофункциональный чип.
Другим объектом изобретения является способ диагностики биополимеров, включающий обеспечение исследуемых образцов исследуемой ДНК, прямых и обратных праймеров, проведение мультиплексной ПЦР, гибридизации амплифицированных продуктов на поверхности мультичипа, детекции результатов диагностики и идентификацию результатов. В указанном способе используют мультичип, содержащий первый, второй и третий идентификаторы, причем перед проведением этапа идентификации заносят данные диагностики и параметры первого, второго и третьего идентификаторов в базу данных для быстрого поиска и идентификации параметров индивидуальных чипов или групп индивидуальных чипов друг относительно друга.
Идентификацию и интерпретацию результатов диагностики осуществляют с применением программных средств и баз данных путем сравнения данных, полученных при сканировании чипа.
Другим объектом изобретения является набор для идентификации биополимеров на основе ДНК-овых или белковых зондов, включающий: а) биологический мультичип, б) реагенты для подготовки образца и проведения идентификации, причем набор может дополнительно содержать сканер, использующий в качестве возбуждающего источника флуоресценции свет диодных лазеров и укомплектованный ПЗС-камерой или сканер для измерения поглощения света, а также содержать устройство для интерпретации и хранения результатов идентификации на основе компьютера.
Перечень фигур
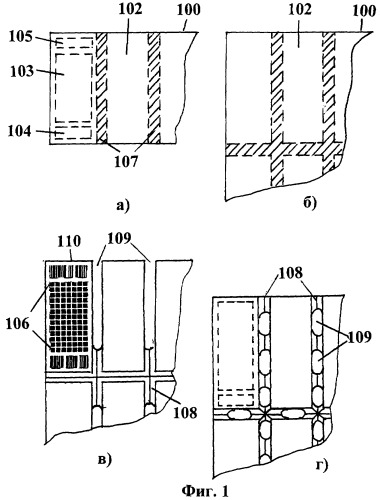
Фиг.1. Размещение основных элементов мультичипа на поверхности несущего элемента:
а) и б) - распределение зон на несущем элементе мультичипа;
в) вариант мультичипа с комбинацией выемок и сквозных отверстий между чипами с размещением двух идентификаторов;
г) вариант мультичипа с выемками между чипами с размещением одного идентификатора.
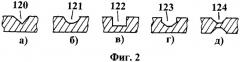
Фиг.2. Сечение несущего элемента мультичипа для разных вариантов выемок:
а) треугольная выемка, б) сферическая выемка, в) прямоугольная выемка, г) многоугольная выемка, д) вариант выемки с двух сторон несущего элемента.
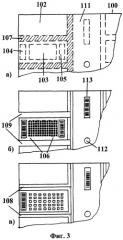
Фиг.3. Размещение основных элементов мультичипа на поверхности несущего элемента с формированием общей зоны на несущем элементе:
а) распределение зон на несущем элементе мультичипа;
б) вариант мультичипа с комбинацией выемок и сквозных отверстий между чипами с размещением трех идентификаторов;
в) вариант мультичипа с комбинацией выемок и сквозных отверстий между чипами с размещением двух идентификаторов.
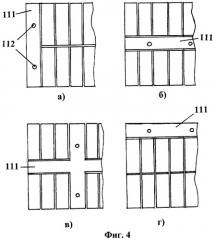
Фиг.4. Размещение основных элементов мультичипа на поверхности несущего элемента с разными вариантами расположения общей зоны мультичипа:
а) боковое, б) центральное, в) крестообразное, г) верхнее размещение общей зоны.
Фиг.5. Изометрическая проекция поперечного разреза ванны для модификации поверхностей нескольких несущих элементов, выполненных в прямоугольной форме, с размещением общей зоны крепления с верхней стороны мультичипа.
Фиг.6. Вид сборки двух вариантов индивидуальных биочипов и рамки для установки в сканер.
Фиг.7. Блок-схема системы для сбора, обработки и передачи информации о данных, считанных с мультичипов на индивидуальные компьютеры пользователей.
Фиг.8. Изображение точек при детекции флуоресцентно меченных зондов.
Фиг.9. Изображение точек при детекции хромогенных зондов.
Фиг.10. Изображение медицинского чипа.
Перечень сокращений.
1. ПММА - полиметилметакрилат.
2. ПВХ - поливинилхлорид.
3. EDC - гидрохлорид диметиламинопропилэтилкарбодиимида.
4. FAM - 6-карбоксифлуоресцеин.
5. APTES - 3-аминопропилтриэтоксисилан.
6. Позиции 100 - относятся к конструктивным элементам мультичипа.
7. Позиции 200 - относятся к системе для анализа результатов диагностики.
Описание изобретения
К одному из объектов настоящего изобретения относится мультичип для последовательной или параллельной диагностики биополимеров, к группе которых можно отнести ДНК, пептиды антитела и другие биологически активные вещества. Такие анализы проводятся в медицине, ветеринарии, при производстве продуктов питания, при контроле параметров окружающей среды и в криминалистике.
Основным аспектом данного изобретения является повышение достоверности полученных результатов анализа за счет разработки новой конструкции мультичипа,
Было обнаружено, что решение поставленных технических задач возможно с помощью новой конструкции мультичипа, в которой реализовано техническое решение, связанное с совершенствованием идентификации биочипов и снижением кросс-контаминации, влияющих на повышение достоверности полученных результатов анализа.
В отличие от известных решений, которые для повышения достоверности полученных результатов обеспечивали либо более совершенную идентификацию отдельных чипов [31], или обеспечивали снижение уровня кросс-контаминации между отдельными кластерами, размещенными на поверхности биочипа [30], предлагаемое техническое решение позволяет выполнить поставленные задачи на основе общего технического решения.
Было обнаружено, что введение в структуру мультичипа общей зоны, сопряженной с частью внешней границы, по меньшей мере, одного чипа, входящего в состав мультичипа, с возможностью легкого отсоединения общей зоны от индивидуальных биочипов позволяет реализовать поставленные технические задачи, обеспечивая синергетический вклад, обеспечиваемый возможностями общей зоны содержать третий идентификатор, общий для всех индивидуальных биочипов, и выемками и/или выемками в комбинации со сквозными отверстиями, с помощью которых крепятся индивидуальные чипы друг с другом и/или с общей зоной, и обеспечивается снижение кросс-контаминации за счет стекания излишков гибридизационной смеси в выемки или отверстия.
Под общей зоной понимается часть общей планарной поверхности мультичипа, на основной части которой размещены N индивидуальных чипов. Включение общей зоны в состав мультичипа позволяет разместить на ней дополнительные элементы конструкции, такие как идентификатор и отверстия для крепления мультичипа в процессе его изготовления, либо крепления в процессе диагностики. Кроме того, отделенный от чипов элемент, содержащий общую зону с расположенными на ее поверхности третьим идентификатором, и, по меньшей мере, одним отверстием, может выполнять дополнительную функцию идентификации объектов диагностики. К таким объектам можно отнести объекты хранения исследуемых образцов, например коробки, к которым крепится элемент с идентификатором. Элемент с третьим идентификатором может быть размещен рядом с диагностируемым больным и закреплен, например, на кровати рядом с информацией о больном или размещен в карте больного для быстрого поиска в базах данных информации о проведенных ранее диагностиках.
Другой проблемой, решаемой настоящим изобретением, связанной с повышением достоверности полученных результатов, является снижение или устранение перекрестного загрязнения при гибридизации. В предлагаемом изобретении проблема кросс-контаминации решается одновременно с формированием возможности отсоединения общей зоны от массива чипов и/или отсоединения чипов друг от друга.
Возможность отсоединения общей зоны от индивидуальных биочипов или отсоединения чипов друг от друга осуществляют за счет формирования на лицевой планарной поверхности мультичипа выемок или комбинации выемок и сквозных отверстий, выполненных в виде перфораций, прорезей, промежутков или интервалов между боковыми границами чипов. В этом случае излишки гибридизационной смеси будут стекать в выемки и/или сквозные отверстия.
Формирование планарной поверхности, на которой размещена общая зона и массив чипов, которые выполнены с возможностью отсоединения друг от друга за счет выемок или выемок и сквозных отверстий, осуществляют за счет стандартных и простых процедур, которые выбирают из группы, включающей, но не ограничивающей штамповку, термоформовку, отливку, механическую обработку, лазерную резку или комбинацию этих способов обработки.
Таким образом, введение общей зоны в мультичип позволяет повысить достоверность результатов диагностики за счет формирования двух- или трехуровневой идентификации данных.
При этом на каждом из индивидуальных чипов размещают, по крайней мере, один первый идентификатор, относящийся к идентификации данных об объекте исследования и, необязательно, второй идентификатор, на котором размещены данные производителя о дате изготовления, типе и параметрах зондов. В общей зоне крепления всех чипов мультичип дополнительно содержит третий идентификатор, который имеет третий код или код, идентичный второму коду.
Первый идентификатор связан с первым кодом, второй идентификатор связан со вторым кодом, отличным от первого кода. Указанные коды образуют уникальные N пар кодов, характеризующих многофункциональный чип. Идентификатор может быть выполнен в виде цифровых и/или буквенных обозначений, которые выполняют функцию кода, или в виде штрих-кодов или их комбинаций.
В качестве примера, включающего, но не ограничивающего объема данного изобретения, ниже приведены параметры, которые могут быть введены в параметры первого идентификатора при определении или диагностики заболеваний млекопитающих.
Первый идентификатор отдельного чипа может включать в себя следующие данные, входящие в группу, состоящую из: а) кода болезни, б) кода, характеризующего объект, из которого взята проба (кровь, лимфа, соскоб, слюна и т.д.), в) кода пациента или кода данных, идентифицирующий пациента (ФИО, возраст), г) кода медицинского учреждения и/или страховой компании, д) дату диагностики.
В свою очередь параметры второго и третьего идентификатора, идентифицирующие мультичип, могут содержать: а) код номера партии и/или даты изготовления, б) код фирмы изготовителя, в) код, идентифицирующий способ модификации поверхности, г) код типа скрининга (последовательный, параллельный), д) код количества индивидуальных чипов, е) код количества кластеров.
Такая информация может быть полезна для выяснения качественных характеристик не только мультичипа, но и его составных компонентов. Причем сочетание первого и второго кода или первого, второго и третьего кода должна обеспечить уникальный код, соответствующий только одному мультичипу. Обращение к такому уникальному коду обеспечит быстрый поиск информации в базах данных о всех образцах при параллельном скрининге либо к информации о последовательных измерениях.
При отливке или штамповке несущего элемента мультичипа возможно формировать дополнительные углубления глубиной от 0,1 до 4,5 мм (в зависимости от толщины чипа), что позволяет свободно отделять от мультичипа отдельные чипы или группу чипов для проведения сканирования в выбранном сканере либо сканировать мультичип целиком на планшетном сканере с одновременным считыванием данных всех идентификаторов.
На фиг.1 показаны варианты размещения основных элементов мультичипа на поверхности несущего элемента без участка со сформированной общей зоной. На фиг.1(а) и фиг.1(б) приведено распределение зон на несущем элементе мультичипа для разных вариантов. В общем случае мультичип содержит несущий элемент 100, на поверхности которого размещают N чипов в секторах 102, количество N индивидуальных чипов в мультичипе выбирают не менее 2. На поверхности каждого сектора 102, принадлежащего индивидуальному чипу, формируют группу зон: а) рабочую зону чипа для нанесения зондов 103, б) зону для нанесения первого идентификатора 104 и необязательно второго идентификатора 105. Причем рабочая зона индивидуального чипа состоит из группы кластеров 106, каждый из которых формируется своим зондом. В группу типов зондов, которые выбирают для размещения на рабочей поверхности чипа, кроме зондов, относящихся к диагностике проб, входит группа зондов, относящихся к положительным или отрицательным контролям, а также группа зондов, выполненных в форме меток, например меток, идентифицирующих положение чипа. Дополнительно каждый сектор контактирует с зоной 107, контактируемой с границами, по крайней мере, двух индивидуальных чипов прилегающих к внешнему контуру каждого сектора. В зоне 107 выполняют выемки 108 и/или сквозные отверстия между чипами 109. На фиг.1(в) приведен вариант мультичипа с комбинацией выемок и сквозных отверстий между чипами с размещением двух идентификаторов. На фиг.1(г) приведен вариант мультичипа с одним идентификатором. Выемки и/или сквозные отверстия между чипами упрощают отделение индивидуальных чипов 110 от несущего элемента 100 или друг относительно друга. Если используют комбинацию выемок и сквозных отверстий в зоне 107, то соотношение между длинами выемок и сквозных отверстий между чипами выбирают в пределах от 1:10 до 10:1. Отношение ширины выемки к ширине сквозного отверстия можно выбирать в пределах от 1:10 до 10:1. Ширину выемки выбирают в пределах от 0,1 мм до 5 мм.
Возможность простого отделения индивидуальных чипов от мультичипа позволяет проведение последовательных скринингов с использованием одного мультичипа, в котором все индивидуальные чипы выполнены при одинаковых условиях, что позволяет сравнивать отдельные чипы в процессе проведения последовательных диагностик, например, при лечении пациента. На фиг.1(а) приведен вариант мультичипа с формированием на поверхности мультичипа одних выемок без сквозных отверстий между чипами и с размещением двух идентификаторов. Такое решение предпочтительно при проведении массовых скринингов, когда все чипы мультичипа должны проходить параллельную обработку и после проведения диагностики могут быть одновременно отделены от мультичипа. На фиг.2 приведены примеры форм сечений несущего элемента мультичипа для разных вариантов выемок: а) треугольная выемка 120, б) сферическая выемка 121, в) прямоугольная выемка 122, г) многоугольная выемка 123, д) вариант выемки с двух сторон несущего элемента 124. Причем выемки, предпочтительно при штамповке или отливке, могут быть организованы как с одной, так и с двух сторон мультичипа. Толщину несущего элемента выбирают от 0,5 до 5 мм. При этом отношение толщины слоя несущего элемента к глубине выемки мультичипа выбирается исходя из механических и физических параметров выбранного материала (твердость, хрупкость) для мультичипа и может составлять отношение от 2:1 до 100:1.
На фиг.3 показаны варианты размещения основных элементов мультичипа на поверхности несущего элемента, на котором формируется общая зона 111. Общая зона 111 несущего элемента мультичипа 100 может быть расположена по границе или в центре массива чипов. Она может представлять форму прямоугольника или иметь, например, крестообразную форму. Общая зона выполняет две функции. Первая связана с ее использованием для формирования на ней установочных и крепежных отверстий 112, которые способствуют креплению заготовок мультичипов при модификации поверхности, многочисленных промывках и очистках поверхности перед нанесением зондов. Второй функцией общей зоны является размещение на ее поверхности третьего идентификатора 113, на котором может быть размещена информация, полезная для последующего анализа данных диагностики при проведении параллельного или последовательного скрининга биополимеров. На фиг.3(а) приведено распределение зон на несущем элементе мультичипа. В общем случае мультичип содержит несущий элемент 100, на поверхности которого размещают N чипов, размещенных в секторах 102, на поверхности каждого сектора формируют группу зон: а) рабочую зону чипа для нанесения зондов 103, б) зону для нанесения первого идентификатора 104 и необязательно второго идентификатора 105. Причем рабочая зона индивидуального чипа состоит из группы кластеров 106, каждый из которых формируется своим зондом. В группу зондов, размещаемых на поверхности рабочей зоны, кроме зондов относящихся к диагностике проб, входит группа зондов, относящихся к положительным или отрицательным контролям, а также группа зондов, выполненных в форме меток, например меток, идентифицирующих положение чипа. Каждый сектор 102 контактирует с зоной 107, контактируемой с границами по крайней мере двух индивидуальных чипов прилегающих к внешнему контуру каждого сектора и границей общей зоны мультичипа. В зоне 107 выполняют выемки 108 и/или сквозные отверстия между чипами 109. На фиг.3(б) приведен вариант мультичипа с комбинацией выемок и сквозных отверстий между чипами с размещением трех идентификаторов. Выемки и/или сквозные отверстия между чипами обеспечивают отделение чипов 110 от несущего элемента 100 или друг относительно друга. На фиг.3(б) приведен вариант мультичипа с выемками между чипами и с размещением двух идентификаторов.
На фиг.4 приведены варианты размещения общей зоны чипа 111 на поверхности мультичипа. На фиг.4(а) приведен вариант бокового размещения общей зоны. На фиг.4(б) приведен вариант центрального размещения зоны. На фиг.4(в) приведена крестообразная форма общей зоны. На фиг.4(г) приведено расположение общей зоны в верхней части мультичипа.
Приведенные примеры включают, но не ограничивают других вариантов размещения индивидуальных чипов и общей зоны друг относительно друга. В общей зоне размещают отверстия 112, с помощью которых несколько заготовок мультичипов могут быть закреплены перед установкой в устройства, в которых происходит один из этапов подготовки поверхности, например этап модификации поверхности или этап нанесения ДНК-овых или белковых зондов.
В качестве примера, который включает, но не ограничивает других вариантов, на фиг.5 приведена изометрическая проекция поперечного разреза ванны 114 для модификации или для проведения промывок поверхностей множества мультичипов, выполненных в прямоугольной форме, с размещением зоны крепления с верхней стороны мультичипа.
При использовании лазерной или механической обработки для формирования выемок и/или сквозных отверстий между чипами предпочтительно одновременно наносить выемки или сквозные отверстия между чипами на поверхности нескольких неразделенных несущих элементов. Для этого от листа пластика отрезают прямоугольную заготовку, на которой можно разместить несколько мультичипов. После формирования сквозных отверстий между чипами и/или выемок мультичипы отделяют друг от друга.
Наиболее предпочтительна штамповка, термоштамповка или отливка с помощью матриц, в процессе которых сквозные отверстия между чипами и/или выемки формируются одновременно с формированием поверхности несущего элемента с зонами для индивидуальных чипов.
Форма мультичипа
Известно выполнение мультичипа в форме прямоугольных платформ [13], прямоугольных листов [10] или в форме плоского диска [9]. Предпочтительной формой мультичипа является плоский лист разной толщины. В рамках настоящего изобретения форму мультичипа выбирают на основании предварительной информации о типе материала для мультичипа, о предполагаемом способе модификации поверхности, информации о предполагаемом способе обработки данных анализа и выборе оборудования для съема и обработки информации. Удовлетворяющая форма мультичипа может представлять собой прямоугольник, квадрат, диск, многоугольник. Толщина несущего элемента может составлять от 0,5 до 5 мм.
В варианте, когда форма мультичипа представляет собой форму прямоугольника, предпочтительно, чтобы соотношения между шириной и длиной мультичипа лежали в пределах от 1:1 до 1:50. В некоторых вариантах предпочтительно выбирать размеры мультичипа в пределах размеров стандартных листов бумаги, например, размер А4, на которые рассчитаны сканеры. Учитывая высокие характеристики разрешения современных сканеров и совершенство способов нанесения зондов на поверхность чипов, более предпочтительно использовать не только стандартные размеры индивидуальных чипов 25 мм×75 мм, но и другие размеры. Например, для сокращения расходов на подготовку индивидуальных чипов в составе мультичипа возможно использовать чипы, габариты которых составляют значение 12,5 мм×75 мм, либо мини-чипы размером 25 мм×37,5 м либо 12,5 мм×37,5 мм. На фиг.6 приведены варианты размещения индивидуальных чипов в стандартных рамках (15) для последующего сканирования. Фиг.6(а) показывает размещение чипа с шириной 25 мм, а фиг.6(б) показывает размещение чипа с шириной 12,5 мм.
Материал несущего элемента
Материал несущего элемента должен обеспечивать несколько функций, способствующих проведению достоверных анализов. Материал должен обеспечивать достаточную стабильность формы в период проведения подготовки поверхности, например ее модификации с целью более эффективной иммобилизации зондов к поверхности чипа. Материал должен выдерживать обработку его поверхности водными и другими растворами. Выбор материала зависит от способа детектирования и регистрации сигнала. При выборе способа детектирования сигнала по уровню флуоресценции необходимо учитывать свойства собственной флуоресценции некоторых материалов и необходимость компенсирования фонового сигнала и повышения отношения сигнала к шуму.
Известно [10], что в качестве основы для создания мультичипов можно использовать нитроцеллюлозу, стекло, силиконы, пластики, тефлоны, металлы и их комбинации. Однако, как уже указывалось, не все материалы, перечисленные в группе, обладают способностью ковалентно иммобилизовать зонды, представляющие собой модифицированные или немодифицированные олигонуклеотидов. В качестве материала несущего элемента для создания мультичипа предлагается использовать полимеры, стекло, керамику или их композиции.
Для такого материала, как стекло, разработано большое число способов модификации поверхности для последующей иммобилизации зондов. Однако массовое применение стеклянных мультичипов ограничивается хрупкостью этого материала, достаточно большим весом и необходимостью выполнения шагов по защите чипов при транспортировке. Выполнение двухсторонних выемок или выемок и сквозных отверстий между чипами дает возможность отделения стеклянных слайдов друг от друга без нарушения основы чипа.
Полимеры не обладают хрупкостью и могут быть изготовлены с помощью разных технологий, включающих, но не ограничивающих способы штамповки, отливки, механическую обработку. Группа используемых полимеров включает, но не ограничивает полиметилметакрилат, полибутилметакрилат, поливинилхлорид, поликарбонат, сополимеры метилметакрилата и/или сополимеров бутилметакрилата с другими мономерами, такими как стирол, акрилонитрил и др. Более предпочтительно использовать полиметилметакрилат, который имеет меньший уровень автофлуоресценции, прозрачен и может составлять основу композитных несущих поверхностей. Поливинилхлорид позволяет эффективно проводить модификацию поверхности и являться основой для изготовления индивидуальных чипов и мультичипов.
Способы модификации поверхности несущего элемента мультичипа
Известны патенты, в которых приведены способы модификации поверхности стекла, полимеров, металлов. Наиболее часто для модификации поверхности используют разнообразные кремнийорганические соединения, в том числе производные триалкоксисиланов.
В некоторых случаях покрытие стеклянной подложки осуществляют APTES в газовой фазе [14, 15]. Следует отметить, что в случае применения для покрытия стекла производных алкоксисиланов происходит их ковалентная пришивка за счет образования силоксановых мостиков. Известна модификация поверхности полимеров действием различных триалкоксисиланов или их производных [16], например способ модификации поверхности полимеров действием золь-геля, получаемого при гидролизе несущего нужную функциональную группу триалкоксисилана совместно с тетраалкоксисиланом [17]. Известен способ модификации сложноэфирных групп на поверхности полимеров, который заключается в их аминолизе под действием полиаминов [18, 19]. На полученной таким образом аминированной поверхности проводят иммобилизацию зонда в присутствии конденсирующего агента и/или гетеробифункционального кросс-линкера. В качестве примера, включающего, но не ограничивающего рамки данного изобретения, рассматривается применение методов модификации стеклянных подложек с применением функциональных кремнийорганичесих соединений. На стадии модификации на стеклянную подложку действуют раствором соединения формулы Y-X-Si(OR)3, где Х - алкильный, арильный или алкиларильный мостик, R - алкил или арил, Y - требуемая функциональная группа, в подходящем растворителе. В качестве модифицирующих агентов могут применяться триалкоксисиланы, содержащие функциональную группу, необходимую для дальнейшей иммобилизации биомолекул, например эпокси-, меркапто-, амино-, акрилоил- и др. Подходящими модифицирующими агентами могут быть:
3-(глицидилокси)пропилтриэтоксисилан, 3-(глицидилокси)пропилтриметоксисилан, 3-меркаптопропилтриэтоксисилан, 3-меркаптопропилтриметоксисилан, 3-аминопропилтриэтоксисилан, 3-аминопропилтриметоксисилан, 3-(акрилоилокси)пропилтриэтоксисилан, 3-(акрилоилокси)пропилтриметоксисилан. В качестве растворителя можно использовать этанол, метанол, пропанол, воду или их смеси.
В ходе процесса вода вызывает гидролиз алкоксигрупп, находящихся в растворе и на поверхности подложки, которые затем подвергаются самопроизвольной поликонденсации. В результате с поверхностью подложки силоксановыми мостиками оказываются связанными большое число молекул алкоксисилана, несущие требуемые функциональные группы. Концентрация модифицирующего агента может варьировать в пределах от 0,1 до 20% по объему. Температуру проведения модификации выбирают в пределах от 15 до 30°С. Предпочтительно использовать комнатную температуру. Длительность стадии модификации выбирают от 30 мин до 2 часов, предпочтительно 1 час.
Для ковалентной модификации полимерных подложек, включающих эл