Способ прогнозирования устойчивости организма к стрессорному воздействию
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к способам прогнозирования устойчивости организма человека к стрессорному воздействию. Для осуществления способа проводят забор периферической крови человека. Из нее получают лейкоцитарную суспензию, которую инкубируют с ингибитором цАМФ-фосфодиэстеразы и без ингибитора, затем производят запись кривых люминолзависимой хемилюминесцентной реакции (ХЛ) и рассчитывают индекс стимуляции (ИС) по формуле ИС=Sингибитор/Sконтроль, где Sингибитор - интенсивность ХЛ клеток в пробе с ингибитором цАМФ-фосфодиэстеразы, Sконтроль - интенсивность ХЛ в контрольной пробе без ингибитора. При этом, если ИС≥0,6, то организм устойчив к действию стрессорного фактора, если ИС<0,6, то организм не устойчив к действию стрессорного фактора. Использование изобретения позволяет прогнозировать устойчивость организма к стрессорному воздействию, в частности прогнозировать вероятность развития тяжелых осложнений в послеоперационном периоде. 2 з.п. ф-лы, 4 табл., 4 ил.
Реферат
Изобретение относится к медицине и относится к прогнозированию устойчивости организма к стрессорному воздействию.
Стресс как биологическая категория представляет собой типовую адаптационную реакцию организма на изменение гомеостаза. Эта реакция возникает при воздействии различных возмущающих факторов (стрессоров) и развивается за счет активации комплекса регуляторных систем, объединяемых в понятия - стресс-реализующие и стресс-лимитирующие системы. Стрессовая реакция, как известно, имеет стадии развития, возникновение которых не зависит от природы стрессора, но зависит от суммарной дозы его биологической активности (т.е. интенсивности и длительности воздействия), а также от устойчивости организма к действию возмущающих факторов.
Развитие стресс-реакции начинается со стадии «срочной» (аварийной) адаптации, которая переходит в стадию устойчивой «долговременной адаптации», если суммарная доза биологической активности стрессора оказывается умеренной силы (Ф.З.Меерсон 1981; М.Г.Пшенникова 2002). При чрезмерно высокой дозе активности стрессора и низкой устойчивости, т.е. предрасположенности к нему организма - адаптация не развивается, а возникают характерные стрессорные повреждения в органах, которые приводят к развитию болезни (болезни адаптации) или гибели организма.
По современным представлениям предрасположенность и устойчивость к стрессорным повреждениям обусловлены как генетическими (врожденными), так и фенотипическими (приобретенными) особенностями функционирования стресс-лимитирующих систем. Установлено (М.Г.Пшенникова 2002), что более высокая устойчивость организма к стрессорным повреждениям наблюдается при исходно более высокой базальной активности стресс-лимитирующих систем, а более низкая устойчивость имеет место при исходно более низкой базальной активности этих систем.
При повторных или длительных воздействиях стрессоров исходно высокая активность стресс-лимитирующих систем истощается, вследствие чего создаются условия для реализации повреждающего эффекта стресса; в то же время исходно более низкая активность стресс-лимитирующих систем повышается в процессе адаптации и нивелирует негативные эффекты стресс реакции (Ф.З.Меерсон 1981, 1993; Ф.З.Меерсон, М.Г.Пшенникова 1988, М.Г.Пшенникова и др. 1999, Meezson 1991).
Вышеизложенные системные представления о механизмах развития стрессорного повреждения дают основания полагать, что у больных с длительными хроническими заболеваниями (хронический стресс), у которых компенсация клинического состояния достигается за счет высокой активности стресс-лимитирующих систем, радикальные методы лечения (хирургическая операция, радиационное облучение, химиотерапия и др.), будучи дополнительными стрессорными факторами, могут резко снизить резервы устойчивости организма и усугубить тяжесть клинического состояния больных. Именно среди таких больных в послеоперационном периоде высока смертность, а также достоверно более высокая частота развития таких тяжелых осложнений как полиорганная недостаточность, сепсис и др.
Из-за опасности усугубления клинического состояния больных при назначении радикальных методов лечения актуальной проблемой становится объективная оценка исходных адаптационных резервов организма больных и контролируемое повышение их во избежание развития осложнений.
Еще из работ Г.Селье известно, что стрессорное повреждение всегда сопровождается инволюцией лимфоидных органов, снижением количества и функции Т- и В-лимфоцитов, а также ингибированием активности фагоцитирующих клеток крови - гранулоцитов, моноцитов и тканевых макрофагов (Гаркави и др., 2001). В костном мозге как центральном органе иммуногенеза при стрессорном повреждении, наряду с активацией апоптоза, происходит ингибирование пролиферации стволовых и прогениторных клеток.
На основании вышеизложенного ближайшим аналогом предложенного способа мы считаем открытие Гаркави Л.Х., Квакина Е.Б., Уколова М.А. "Закономерности развития качественно отличающихся общих неспецифических адаптационных реакций организма". Диплом на открытие N 158 Комитета Совета Министров СССР по делам изобретений и открытий. Открытия в СССР, М., 1975, с.56-61, где на основе фазового характера изменений состава крови авторы открыли периодичную зависимость неспецифических реакций активации, тренировки, стресса и состояния ареактивности ("коэффициент реакции"), поддерживающих гомеостаз, от интенсивности (силы, дозы) действующего фактора. Для указанных реакций описаны изменения, происходящие в различных системах организма ("системный ответ").
Однако дать количественную оценку прогноза устойчивости организма на действие повреждающего стрессорного фактора авторам открытия не удалось.
В то же время обзор литературы показывает, что иммунокомпетентные клетки крови и костного мозга, как и большинство других клеток организма, для поддержания своей жизнедеятельности активно потребляют кислород в процессе фагоцитоза, а также митохондриального и микросомального окисления. Именно поэтому при стрессе мононуклеарные клетки становятся активными участниками окислительного или метаболического взрыва, при котором наряду с интенсификацией окисления глюкозы в гексозомонофосфатном шунте происходит избыточное образование активных форм кислорода (АФК) (А.Н.Гребенюк и др., 1998), которые и запускают адаптационный процесс на клеточном уровне (В.Х.Хавинсон и др. 2003).
Таким образом, сведения о мононуклеарных клетках, изложенные выше, указывали, на пригодность использования их у людей для прогнозирования устойчивости их организма к стрессорному воздействию.
Пригодность мононуклеарных клеток крови в качестве тест-системы для контроля адаптационных резервов организма может обосновываться также тем фактом, что активация иммунокомпетентных клеток индуцирует сложный каскад ферментативных реакций, включающей активацию аденилатциклазы (Ю.А.Владимиров и др. 1992), с участием которой осуществляется синтез ц-АМФ, избыточное накопление которого ингибирует активность клеток: реакцию фагоцитоза в нейтрофилах и гуморальный ответы Т- и В-лимфоцитов на чужеродные антигены.
Эти наблюдения позволили нам предположить, что ц-АМФ, накапливающийся в мононуклеарных клетках пациентов с высоким резервом устойчивости к стрессорному повреждению, будет стимулировать развитие адаптивной реакции, сопровождающейся окислительным стрессом с избыточной продукцией АФК. Накопление ц-АМФ в мононуклеарных клетках больных с низким резервом устойчивости к стрессорному повреждению будет стимулировать стрессорное повреждение и ингибировать продукцию АФК.
Учитывая это, нами предложена простая и достаточно эффективная методика прогнозирования устойчивости организма на стрессорное воздействие путем определения продукции АФК иммунокомпетентными клетками при избыточном накоплении в них ц-АМФ за счет ингибирования фермента фосфодиэстеразы, осуществляющей гидролиз ц-АМФ, с помощью солей акридонуксусной кислоты: натриевая соль - препараты «НЕОВИР» и «КАМЕДОН», а также N-метилглюкаминовая соль - препарат «ЦИКЛОФЕРОН» (низкомолекулярный индуктор интерферона - N-метилглюкаминовая соль карбоксиметилакридона), ООО «НТФФ Полисан» (Санкт-Петербург).
Способ включает в себя следующие этапы.
1. Проводят забор периферической крови человека любым известным способом, после чего осуществляют получение лейкоцитарной суспензии. Для этого 2 мл гепаринизированной крови смешивали с 1 мл подогретого до 37°С 3% раствора желатина и инкубировали в термостате при 37°С в течение 30 мин. После оседания эритроцитов слой плазмы, обогащенный лейкоцитами, отбирали в пластиковые пробирки и отмывали 10-кратным объемом фосфатно-солевого буфера (рН 7,4). Затем лейкоциты центрифугированием в течение 10 мин при 1000 об/мин ресуспендировали в растворе Хенкса без Са2+ и Mg2+. После подсчета числа лейкоцитов концентрацию клеток доводили до 106 кл/мл.
2. Хемилюминесцентный анализ динамики накопления активных форм кислорода (АФК). Для определения индекса стимуляции в две кюветы - контрольную и опытную вносили по 40·103 клеток. В опытную кювету дополнительно вносили 5 мкл/мл ингибитора цАМФ-фосфодиэстеразы - соль акридонуксусной кислоты, например препарат «Циклоферон» (12,5% раствор), являющийся индуктором интерферона, содержащий ингибитор цАМФ-фосфодиэстеразы производную акридонуксусной кислоты (10-карбоксиметил-9-акриданон) и N-метилглюкамин. В контрольную кювету вносили 5 мкл раствора Хэнкса. Контрольную и опытную кюветы инкубировали в термостате в течение 60 мин при 37°С. После инкубации лейкоцитарной взвеси проводили запись кривых хемилюминесцентной реакции (ХЛР) в течение 15 минут с использованием хемилюминометра «Хелюм-2001 01/01» (Россия) в комплексе с компьютером IBM-PC при температуре счетной камеры 37°С. В качестве усилителя свечения использовали люминол (5-амино-2,3-дигидро-1,4-фталазиндион, «Sigma») в конечной концентрации 10-3М, а в качестве активатора образования активных форм кислорода (АФК) - РМА (форбол-12-миристат-13-ацетат, «Sigma») в концентрации 10-6М.
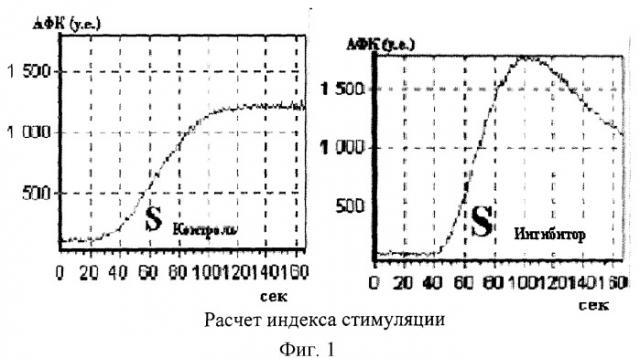
Суммарную продукцию активных форм кислорода (АФК) вычисляли как площадь под кривой ХЛ (фиг.1).
Рассчитывался индекс стимуляции (ИС), как отношение площади под кривой ХЛ с ингибитором цАМФ-фосфодиэстеразы, в качестве которого выступает соль акридонуксусной кислоты, (Sингибитор) к площади под кривой ХЛ клеток без добавления препарата (Sконтроль).
ИС=Sингибитор/Sконтроль,
где Sингибитор - интенсивность ХЛ клеток в пробе с ингибитором цАМФ-фосфодиэстеразы, Sконтроль - интенсивность ХЛ в контрольной пробе.
При этом, если ИС≥0,6, то организм устойчив к действию стрессорного фактора, если ИС<0,6, то организм не устойчив к действию стрессорного фактора.
Примеры реализации заявленного изобретения
В работе было проанализирована функциональная активность клеток иммунной системы у 300 человек, находящихся на лечении в НИИТиИО с 2001 по 2006 гг. Также в исследование было включено 25 человек с хроническими рецидивирующими вирусными инфекциями ЛОР-органов, 10 человек с онкологическими процессами. В качестве контроля были проанализированы данные от 70 клинически здоровых человек, взятых в качестве доноров.
Статистическая обработка материала проводилась с помощью пакета прикладных программ обработки данных «Statistica 6.0.» (Statsoft, США, 2002). Достоверность различий между экспериментальными группами по изучаемым параметрам оценивалась с помощью t-критерия Стьюдента для нормально распределенных количественных признаков с равными выборочными дисперсиями. Критическим уровнем статистической значимости при проверке статистических гипотез считали p≤0,05 [Реброва О.Ю, 2003].
Забор и исследования крови больных осуществляли при поступлении (перед хирургическим лечением), а также 1,5-2 месяца после проводимого лечения. У кардиохирургических больных, кроме того, исследования проводили на 1-7 сутки после операции; на 7-30 сутки после операционного периода выделяли также группу больных с инфекционными осложнениями и органными дисфункциями (n=14) и группу больных с развитием критического состояния, приведшего к летальному исходу (n=10).
Для подтверждения связи тяжести нарушения характеристик кривых ХЛР с уровнем адаптационных резервов организма нами проводилась количественная оценка иммунного статуса больных.
Состояние иммунной системы больных оценивали с использованием стандартных тестов, рекомендованных ВОЗ, в соответствии с разработанной схемой иммунологического обследования, адекватной для диагностики типа и степени вторичной иммунной недостаточности.
Клеточное звено иммунитета оценивали по количественному содержанию лейкоцитов, относительному (%) и абсолютному (в 1 мкл) содержанию лимфоцитов, Т-лимфоцитов (СD3+-клетки), их иммунорегуляторных субпопуляций Т-хелперов (CD4+-клетки) и цитотоксических Т-лимфоцитов (СD8+-клетки) и иммунорегуляторному индексу (ИРИ=CD4+/CD8+), а также относительному содержанию натуральных киллеров (СD16+/56+-клетки) с использованием комбинации моноклональных антител (МКАТ), меченных FITC и фикоэритрином (РЕ) (НПЦ «МедБиоСпектр» и «Сорбент»).
Функциональная активность клеточного звена иммунитета оценивалась по количеству Т-лимфоцитов, экспрессирующих на своей поверхности рецептор к интерлейкину-2 (СD25+-клетки) и антигены II класса гистосовместимости HLA-DR (HLA-DR+-клетки), а также числу пролиферирующих клеток (CD71+-клетки). Иммунофенотипирование проводили на проточном цитофлюориметре FACScan фирмы Becton Dickinson (США) [Пинегин Б.В., Ярилин В.А., 2001].
Гуморальное звено иммунитета включало комплексную оценку относительного и абсолютного содержания В-лимфоцитов (CD20+-клетки) иммунофлюоресцентным методом, концентрации иммуноглобулинов классов G, А, М в сыворотке крови методом радиальной иммунодиффузии в геле [Manchini et al., 1965], а также определение уровня низкомолекулярных (осаждение 6% ПЭГ) циркулирующих иммунных комплексов (ЦИК) [Новиков Д.К., 1996].
Фагоцитарную активность нейтрофилов крови определяли стандартным методом с использованием убитой взвеси Staph. Aureus [Фрейдлин И.С., 1986], подсчитывая число фагоцитирующих клеток на 100 нейтрофилов (фагоцитарный индекс, %), количество микробных тел, поглощенных в среднем одним нейтрофилом (фагоцитарное число).
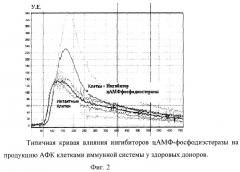
Проведенное исследование показало, что хемилюминесцентная реакция клеток крови на инкубацию с индуктором интерферона (ИИ) «Циклофероном», а также «Неовиром» и «Камедоном» у доноров и больных с тяжелыми хроническими заболеваниями сердца имеет диаметрально выраженные количественные и качественные различия
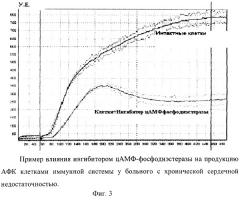
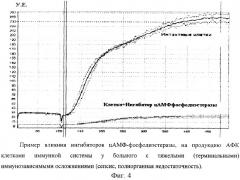
Добавление к клеткам ИИ у здоровых доноров повышало продукцию АФК (фиг.2), тогда как у больных с тяжелой хронической патологией наоборот снижало ее по сравнению с контролем (фиг.3, 4). Мы отметили также, что нарастание тяжести клинического состояния больных приводило к практически к полному ингибированию продукции АФК при добавлении ИИ (фиг.3).
Количественная оценка ИС и кинетические характеристики ХЛР у здоровых доноров и хронических кардиологических больных при поступлении и на различных этапах хирургического лечения представлены в табл.1.
Из таблицы видно, что у здоровых доноров значение ИС колеблются от 2,2 до 2,8 и в среднем составляет 2,5±0,31. У больных в предоперационном периоде ИС в среднем составлял 0,73. Сразу после операции (операционный стресс) эти показатели еще более резко отклонялись от значений нормы у здоровых доноров, однако в стадии реконвалесценции (через 1,5-2 месяца после операции) они вновь начинали восстанавливаться, свидетельствуя о повышении адаптационных резервов организма больных. Т.к. в стадии реконвалесценции нами наблюдалось не 250, а 226 больных: у 14 больных развились тяжелые иммунозависимые осложнения, а у 10 хирургическое лечение закончилось летальным исходом, то предстояло ответить на вопрос: возможно ли по показателям ХЛР в предоперационном периоде прогнозировать развитие опасных для жизни осложнений. Разбив всех оперированных больных по группам в зависимости от исходного значения ИС, мы отметили (табл.2), что при ИС≥0,6 процесс выздоровления больных шел быстрее и опасность развития осложнений (инфекционно-септические, органные дисфункции) была достоверно ниже, чем у больных с исходным значением ИС<0,6.
У больных с летальным исходом цифровые значения ИС имели тенденцию к еще более резкому снижению (все меньше 0,6). На фиг.4 представлена связь ИС с частотой развития осложнений в п/о периоде. Для восстановления адаптационных резервов организма больных в п/о периоде и повышения эффективности лечения инфекционных осложнений, а также органических дисфункций нами дополнительно проводилась иммунокоррегирующая терапия. Эффективность терапии контролировали по динамике изменения показателей ХЛР, иммунограммы, а также клинического состояния больных.
Из табл.3 видно, что иммунокоррекция способствовала повышению адаптационных резервов организма и резервов его устойчивости к стрессорным повреждениям, т.к. наступала коррекция клеточного и гуморального звена иммунитета (количество и функции Т- и В-лимфоцитов, фагоцитарная активность нейтрофилов), а также нормализация показателей ХЛР, в том числе ИС.
Мы установили также, что между значениями ИС и количеством лимфоцитов, а также значениями ИС и фагоцитарным индексом существует прочная и прямая корреляционная связь (R=0,9), которая наряду с позитивной динамикой клинического состояния больных подтверждает тот факт, что значение ИС отражают адаптационные резервы организма и могут служить мерой его устойчивости к стрессу.
Таким образом, представленные результаты показывают следующее.
1. Значение ИС больных отражают адаптационные резервы организма и могут служить мерой его устойчивости к стрессу.
2. У больных с тяжелыми хроническими заболеваниями ИС имеет значение меньше 0,6. При значениях ИС меньше 0,6 и необходимости выполнения хирургической операции возникает опасность развития тяжелых осложнений в п/о периоде - в виде инфекционных-септических осложнений и органных дисфункций, вплоть до полиорганной недостаточности.
| Таблица 1. | |||||
| Показатели хемилюминесцентной реакции лейкоцитарной суспензии у кардиохирургических больных в послеоперационном периоде. | |||||
| Показатель хемилюминесцентной реакции | Здоровые доноры(n=70) | Кардиохирургические больные | |||
| Больные при поступлении в стадии реконвалесценции(n=250) | Больные после операции (1-7 суток) (n=250) | Больные с осложнениями(n=14) | Больные с летальным исходом (n=10) | ||
| Индекс стимуляции | 2,50±0,31 | 0,73±0,23* | 0,22±0,10* | 0,10±0,05* | 0,01±0,03* |
| Интенсивность хемилюминесценции, S (103/у.e.) | 352,1±55,2 | 305,1±33,5 | 200,1±33,2 | 167,1±41,2* | 65,9±25,1* |
| Скорость образования АФК, V (у.e.) | 3,73±0,08 | 3,24±0,08* | 2,85±0,03* | 1,42±0,03* | 1,11±0,01* |
| Лаг-период, Т (с) | 12,5±1,8 | 14,2±1,7 | 15,2±3,0 | 25,2±4,2* | 38,5±3,6* |
| * - достоверное различие по сравнению с группой здоровых доноров крови (p<0,05) |
| Таблица 2. | ||||
| Показатели хемилюминесцентной реакции лейкоцитарной суспензии у кардиохирургических больных в послеоперационном периоде. | ||||
| Показатель хемилюминесцентной реакции | Здоровые доноры (n=70) | Кардиохирургические больные | ||
| Больные при поступлении в стадии реконвалесценции (n=250) | Больные с ИС≥0.6(n=70) | Больные с ИС<0.6 (n=180) | ||
| Индекс стимуляции после операции | 0,4±0,10* | 0,08±0,05* | ||
| Интенсивность хемилюминесценции, S (103/у.е.) | 352,1±55,2 | 305,1±33,5 | 240,1±31,1 | 150,1±31,2* |
| Скорость образования АФК, V (у.е.) | 3,73±0,08 | 3,24±0,08* | 3,00±0,02* | 1,22±0,03* |
| Лаг-период, Т (с) | 12,5±1,8 | 14,2±1,7 | 14,2±2,0 | 28,2±°1,2* |
| Инфекционные осложнения (%) | 2 | 13* | ||
| ПОН (%) | 0 | 5 | ||
| * - достоверное различие по сравнению с группой здоровых доноров крови (p<0,05) |
| Таблица 3.Динамика показателей иммунограммы кардиохирургических больных с осложненным послеоперационным периодом при проведении иммунокоррекции. | |||
| Показатель | Здоровые доноры крови (n=25) | Кардиохирургические больные | |
| До Иммунокоррекции (n=14) | После иммунокоррекции (n=14) | ||
| Интенсивность ХЛ, S, 103/у.е. | 352,1±55,2 | 167,1±41,2 | 308,8±22,2* |
| Скорость реакции, V (у.е.) | 3,73±0,08 | 1,42±0,03 | 2,77±0,05* |
| Лаг-период, Т (с) | 12,5±1,8 | 25,2±4,2 | 16,6±2,5* |
| Индекс стимуляции | 2,50±0,31 | 0,10±0,05 | 0,5±0,04* |
| Лимфоциты, % | 32,5±4,8 | 17,4±2,6 | 30,4±3,3* |
| Т-лимфоциты (CD3+), % | 67,5±4,6 | 46,5±8,8 | 59,2±4,3* |
| Т-хелперы (CD4+), % | 43,9±3,7 | 31,8±4,4 | 40,4±3,1* |
| Т-цитотоксические (CD8+), % | 28,1±3,6 | 15,0±2,2 | 20,7±2,5* |
| В-лимфоциты (CD20+), % | 10,1±1,5 | 5,2±2,0 | 6,9±1.9 |
| NK-клетки (СD16+), % | 13,9±1,6 | 5,6±1,1 | 9,0±1,5* |
| HLA-DR | 11,5±3,5 | 22,1±2,2 | 16,4±3,2* |
| IL2-R+-кл. (CD25+) | 3,2±1,6 | 8,8±2,4 | 4,4±2,0* |
| CD71+ | 3,0±0,5 | 17,2±3,1 | 14,4±2,2 |
| IgG, г/л | 13,0±0,9 | 11,1±1,4 | 13,3±1,1 |
| IgA, г/л | 2,5±0,4 | 1,3±0,2 | 1,9±0,2* |
| IgM, г/л | 1,5±0,2 | 1,0±0,3 | 13±0,4 |
| ЦИК, у.е. | 153,0±40,1 | 660,2±45,1 | 335,5±45,1* |
| Фагоцитарный индекс, % | 75,5±3,5 | 40,5±5,5 | 55,4±4,4* |
| Фагоцитарное число, у.е. | 5,5±1,7 | 2,4±0,6 | 4,1±1,1* |
| * - достоверное различие по сравнению с исходным уровнем (p<0,05); |
| Таблица 4.Динамика показателей фагоцитарной функции нейтрофилов у больных при проведении иммунокоррекции на основе индивидуального подбора иммуномодуляторов. | |||||
| Показатель | Контрольная группа(n=25) | До иммунокоррекции | После иммунокоррекции | ||
| Группа сравнения(n=23) | Основная группа(n=23) | Группа сравнения(n=23) | Основная группа(n=23) | ||
| Фагоцитарный индекс, % | 75,5±3,5 | 51,7±2,9x | 52,7±2,8x | 57,3±3,5 | 65,6±4,2↑* |
| Фагоцитарное число, у.е. | 5,5±1,7 | 3,5±0,3 | 3,1±0,2x | 4,0±0,1↑* | 5,0±0,8↑*+ |
| x - достоверное различие с группой контроля (p<0,05); | |||||
| * - достоверное различие по сравнению с исходным уровнем (p<0,05) | |||||
| + - достоверное различие с группой сравнения (p<0,05) | |||||
| ↑, ↓ - повышение/снижение показателя по сравнению с исходным уровнем |
Список литературы
1. Меерсон Ф.З. Адаптация, стресс и профилактика. М.: Наука, 1981, с.278.
2. Пшенникова М.Г. Стресс: регуляторные системы и устойчивость к стрессорным повреждениям. В книге «Дизрегуляционная патология» под ред. Академика РАМН Г.Н.Крыжановского М.: Медицина, 2002, стр.307-328.
3. Меерсон Ф.З. Адаптационная медицина: механизмы и защитные эффекты адаптации. М. Hypoxia Medical LTD, 1993, с.331.
4. Меерсон Ф.З., Пшенникова М.Г. Адаптация к стрессорным ситуациям и физическим нагрузкам. М.: Медицина, 1988, с.256.
5. Пшенникова М.Г., Бондаренко Н.А., Шимкович М.В. и др. Экспер. Биологии и медицины, 1999, т.128, №12, с.638-641.
6. Хавинсон В.Х., Баринов В.А., Арутюнян А.В., Малинин В.В. Свободнорадикальное окисление и старение. Санкт-Петербург, Наука, 2003, с.325.
7. Meerson F.Z. Adaptive protection of the heart: protecting against stress and ischemic damage. Boca Raton CRC Press, 1991, p.340.
1. Способ прогнозирования устойчивости организма человека к стрессорному воздействию, включающий забор его периферической крови, отличающийся тем, что из периферической крови человека получают лейкоцитарную суспензию, суспензию клеток инкубируют с ингибитором цАМФ-фосфодиэстеразы и без ингибитора, затем производят запись кривых люминолзависимой хемилюминесцентной реакции (ХЛ) и рассчитывают индекс стимуляции (ИС) по формуле:
ИС=Sингибитор/Sконтроль,
где Sингибитор - интенсивность ХЛ клеток в пробе с ингибитором цАМФ-фосфодиэстеразы,
Sконтроль - интенсивность ХЛ в контрольной пробе без ингибитора, при этом, если ИС≥0,6, то организм устойчив к действию стрессорного фактора, если ИС<0,6, то организм неустойчив к действию стрессорного фактора.
2. Способ по п.1, отличающийся тем, что в качестве ингибитора цАМФ-фосфодиэстеразы используют препараты, содержащие соль акридонуксусной кислоты.
3. Способ по п.2, отличающийся тем, что в качестве препарата, содержащего соль акридонуксусной кислоты используют «Циклоферон», и/или «Камедон», и/или «Неовир»