Иммуноферментная тест-система для определения поверхностного антигена вируса гепатита в и способ определения поверхностного антигена вирусного гепатита в
Иллюстрации
Показать всеИзобретение относится к области иммунологии, медицины и биотехнологии. Использование: выявление или подтверждение поверхностного антигена вируса гепатита В (HBsAg). Иммуноферментная тест-система для идентификации HBsAg в сыворотке (плазме) и препаратах крови (альбумине, фибринолизине, иммуноглобулинах и лейкоцитарном интерфероне) содержит: твердую фазу, содержащую иммуносорбент, представляющий собой сорбированные на стрипах планшета моноклональные антитела мыши к HBsAg; конъюгат-1 - биотин с моноклональными антителами к HBsAg и конъюгат-2 - стрептавидин, меченный пероксидазой хрена, представленные в виде жидких концентратов; положительный контрольный образец; отрицательный контрольный образец; промывочный раствор; раствор для разведения конъюгатов; субстратный буферный раствор; тетраметилбензидин в качестве хромогена; серную кислоту в качестве стоп-реагента; нейтрализующий реагент, жидкий или лиофилизированный, представляющий собой иммуноглобулины козы, содержащие антитела к HBsAg; контрольный реагент, жидкий или лиофилизированный, представляющий собой иммуноглобулины козы, не содержащие антител к HBsAg; слабоположительный контрольный образец, представляющий собой сыворотку крови в лиофилизированном виде, содержащую HBsAg в концентрации 0,02-0,06 МЕ/мл. Предложен также способ определения поверхностного антигена вирусного гепатита В (HBsAg) методом иммуноферментного анализа в биологическом образце с помощью данной тест-системы. Изобретение позволяет выявлять искомый антиген с чувствительностью 0,01 МЕ/мл при сохранении высокой специфичности. 2 н. и 2 з.п. ф-лы, 8 табл.
Реферат
Изобретение относится к области медицины, иммунологии и биотехнологии.
Использование: выявление поверхностного антигена вируса гепатита В (HBsAg) или подтверждение специфичности результатов выявления.
Сущность: получение иммуноферментной тест-системы для идентификации HBsAg в сыворотке (плазме) и препаратах крови (альбумине, фибринолизине, иммуноглобулинах и лейкоцитарном интерфероне), позволяющей выявлять искомый антиген с чувствительностью не менее 0,01 МЕ/мл.
Для диагностики гепатита В с помощью специфических тестов решающее значение имеет обнаружение в сыворотке крови поверхностного антигена вируса гепатита В - HBsAg, являющегося основным маркером заболевания, который регистрируется задолго до появления клинических признаков болезни. На ранних стадиях инфекционного процесса и перед исчезновением из циркуляции концентрация HBsAg может составлять несколько пг/мл.
Всеобщая вакцинация ускорила накопление мутантных форм вируса гепатита В. Наличие мутаций в вирусном геноме вызывает изменение структуры антигенных эпигонов HBsAg или биологических свойств вируса, например снижение секреции вируса из клеток. Вследствие этого снижается выявляемость HBsAg с помощью сертифицированных диагностических тестов [Weinberger K.M. et al., 2000].
Установлено, что при сочетанном инфицировании вирусами гепатитов В и С или вирусом гепатита В и ВИЧ происходит подавление репликации вируса гепатита В. Это приводит к тому, что количество HBsAg в сыворотке крови ниже предела чувствительности большинства используемых тест-систем, разрешенных к применению [Berger A. et al., 2000; Hofer M. et al., 1998; Schuttler C.G. et al., 2002].
Современные методы выявления HBsAg позволяют обнаруживать его в низких концентрациях. Существуют национальные критерии чувствительности и специфичности отечественных препаратов. Так, с 2003 года для тест-систем на HBsAg регламентируется чувствительность 0,1 МЕ/мл.
Однако выявление случаев возникновения гепатита В после переливания «серонегативной» по HBsAg крови свидетельствует о необходимости дальнейших работ по созданию и внедрению в практическое здравоохранение тест-систем, обладающих высокой чувствительностью с сохранением высокой специфичности. Поэтому создание иммуноферментной тест-системы для определения HBsAg в сыворотке крови в концентрации 0,01 МЕ/мл позволит уменьшить риск посттрансфузионного заражения вирусным гепатитом В, повысит качество скрининга донорской крови.
Одним из путей повышения чувствительности детекции HBsAg в иммуноферментном анализе может быть использование иммунохимического комплекса биотин-стрептавидин. При синтезе конъюгата антитело-биотин с одной молекулой антитела может быть связано до 90 молекул биотина. Молекула стрептавидина имеет 4 центра связывания биотина, поэтому каждый специфический иммунохимический комплекс на конечной стадии будет содержать не одну молекулу фермента, а несколько десятков. Использование для биотинилирования длинного спейсера значительно снижает стерические препятствия при взаимодействии меченных биотином антител со стрептавидином.
Наиболее близким техническим решением (прототипом) к заявленному изобретению по совокупности признаков является диагностический набор «Enzygnost HBsAg 5.0» (Dade Behring, Германия), основанный на двухстадийной постановке, в составе которого имеются биотиновый и стрептавидиновый конъюгаты (Medicines and Healthcare Products Regulatory Agency, 06/2003, Evaluation Report MHRA num-ber 03044). На первом этапе HBsAg, содержащийся в тестируемом образце, одновременно связывается с овечьими поликлональными антителами к HBsAg, сорбированными в лунки планшета, и с конъюгатом-1, являющимся мышиными моноклональными антителами к HBsAg, связанными с биотином. На втором этапе после отмывки не связавшихся реагентов конъюгат-2 (стрептавидин, меченный пероксидазой хрена) взаимодействует с конъюгатом-1. После отмывки не прореагировавших реагентов ферментативная активность связавшегося конъюгата-2 детектируется окрашенным продуктом взаимодействия фермента со смесью субстрата и хромогена. Интенсивность окрашивания пропорциональна концентрации HBsAg в исследуемом образце. Общее время реакции составляет 120 мин. Недостатком данного набора является то, что его чувствительность не превышает 0,1 МЕ/мл, что и является причиной, препятствующей достижению требуемого технического результата.
Задачей настоящего изобретения является получение тест-системы, с помощью которой достигается возможность выявления поверхностного антигена вируса гепатита В (HBsAg) в сыворотке (плазме) крови человека с чувствительностью 0,01 МЕ/мл при сохранении высокой специфичности.
Сущность предлагаемого технического решения состоит в том, что выявление HBsAg с чувствительностью 0,01 МЕ/мл проводят с помощью диагностической иммуноферментной тест-системы, построенной на основе использования пары конъюгатов, один из которых - моноклональные антитела к HBsAg, связанные с биотином, второй - стрептавидин, меченный пероксидазой хрена, причем в ходе постановки иммуноферментного анализа присутствует стадия совместного выдерживания в лунке исследуемого образца одновременно с двумя конъюгатами.
Тест-система для определения поверхностного антигена вирусного гепатита В (HBsAg) методом иммуноферментного анализа в биологическом образце содержит:
- в качестве твердой фазы иммуносорбент, представляющий собой сорбированные на стрипах полистиролового планшета моноклональные антитела мыши к HBsAg,
- первый конъюгат - (11-кратный концентрат), прозрачная или слегка опалесцирующая, фиолетового цвета жидкость, моноклональные антитела к HBsAg, связанные с биотином,
- второй конъюгат - прозрачная или слегка опалесцирующая, голубого цвета жидкость, стрептавидин, меченный пероксидазой хрена,
- положительный контрольный образец, инактивированный, прозрачная или слегка опалесцирующая, малиново-красного цвета жидкость, сыворотка крови человека, содержащая HBsAg, не содержащая антитела к ВИЧ-1,2 и вирусу гепатита С и антитела к HBsAg,
- отрицательный контрольный образец, инактивированный, прозрачная или слегка опалесцирующая, светло-зеленого цвета жидкость, сыворотка крови человека, не содержащая HBsAg, антитела к ВИЧ-1,2 и вирусу гепатита С,
- слабоположительный контрольный образец, лиофилизированный, сухая пористая аморфная масса, гигроскопичная, белого или светло-желтого цвета, представляет собой сыворотку крови человека, содержащую HBsAg в концентрации 0,02-0,06 МЕ/мл и не содержащую антитела к ВИЧ-1,2 и вирусу гепатита С и антитела к HBsAg,
- промывочный раствор - прозрачная или слегка опалесцирующая, бесцветная или светло-желтого цвета жидкость, 25-кратный концентрат фосфатно-солевого раствора, содержащий 2,5% твина-20,
- раствор для разведения конъюгата-1, непрозрачная зеленого цвета жидкость,
- раствор для разведения конъюгата-2, прозрачная желтого цвета жидкость,
растворы для разведения конъюгатов представляют собой белково-солевые растворы,
- субстратный буферный раствор, содержащий перекись водорода, прозрачная бесцветная жидкость,
- 3,3'5,5'-тетраметилбензидин в качестве хромогена, прозрачная бесцветная жидкость,
- стоп-реагент - раствор серной кислоты 0,75 моль/л, прозрачная бесцветная жидкость.
В набор включены нейтрализующий реагент, жидкий или лиофилизированный, представляющий собой иммуноглобулины козы, содержащие антитела к HBs-антигену; контрольный реагент, жидкий или лиофилизированный, представляющий собой иммуноглобулины козы, не содержащие антитела к HBs-антигену для подтверждения поверхностного антигена HBsAg.
В качестве биологического материала может быть исследована сыворотка или плазма крови, препарат крови, например, выбранный из группы: альбумин, фибролизин, иммуноглобулин, лейкоцитарный интерферон.
Технический результат, достигаемый настоящим изобретением, заключается в улучшении чувствительности детекции HBsAg до 0,01 МЕ/мл за счет выдерживания в лунке исследуемого образца непосредственно с биотинилированными антителами, а затем без стадии отмывки инкубационная смесь выдерживается с конъюгатом стрептавидин-пероксидаза хрена, что ведет к усилению специфического сигнала.
Данное техническое решение отличается от известных наличием фазы одновременного совместного выдерживания в лунке исследуемого образца с конъюгатами-1 и -2.
Иммуноферментная тест-система для определения (выявления или подтверждения) поверхностного антигена вируса гепатита В («ДС-ИФА-HBsAg-0,01») может быть выполнена в виде 2 наборов.
Изобретение иллюстрируется следующими примерами.
Пример 1
Для выявления поверхностного антигена гепатита В в сыворотке (плазме) и препаратах крови (альбумине, фибринолизине, иммуноглобулинах и лейкоцитарном интерфероне) предназначен набор 1 ("ДС-ИФА-HBsAg-0,01").
Реагенты, включенные в состав набора 1:
иммуносорбент - моноклональные антитела мыши к HBsAg, сорбированные на стрипах полистиролового планшета; конъюгат-1 - жидкий (концентрат x11) - антитела к HBsAg, конъюгированные с биотином; конъюгат-2 - (концентрат х11) жидкий - стрептавидин, меченный пероксидазой хрена; положительный контрольный образец (К+1), жидкий - сыворотка крови человека, содержащая HBsAg, не содержащая антитела к ВИЧ-1,2 и вирусу гепатита С, инактивированная; слабоположительный контрольный образец (К+2), лиофилизированный - HBsAg с концентрацией 0,04±0,02 МЕ/мл в сыворотке крови человека, не содержащий антитела к ВИЧ-1,2 и вирусу гепатита С, инактивированный; отрицательный контрольный образец (К-), жидкий - сыворотка крови человека, не содержащая HBsAg, не содержащая антитела к ВИЧ-1,2 и вирусу гепатита С, инактивированная; промывочный раствор (ПР, концентрат х25), жидкий; раствор для разведения концентрата конъюгата-1 (РРК-1), жидкий; раствор для разведения концентрата конъюгата-2 (РРК-2), жидкий; субстратный буферный раствор (СБ), жидкий; хромоген - тетраметилбензидин (ТМБ), жидкий; стоп-реагент - серная кислота, раствор, 0,75 моль/л.
Набор 1 рассчитан.
Комплект 1 с увеличенным объемом компонентов - на одновременное проведение 192 (96×2) определений, включая контрольные (комплект 1 может быть использован на автоматизированном ИФА-анализаторе).
Комплект 2 - на одновременное проведение 192 (96×2) определений, включая контрольные.
Комплект 3 с увеличенным объемом компонентов - на одновременное проведение 96 (8×12) определений, включая контрольные (комплект 3 может быть использован на автоматизированном ИФА-анализаторе).
Комплект 4 - на одновременное проведение 96 (8×12) определений, включая контрольные.
Приготовление растворов.
Слабоположительный контрольный образец. Готовят перед использованием. Содержимое флакона растворить физиологическим раствором в объеме, указанном на этикетке флакона, осторожно перемешать и выдержать до использования 5-10 мин.
Промывочный рабочий раствор - для промывания иммуносорбента. Содержимое флакона с концентратом ПР разводят в 25 раз дистиллированной водой. Полученный раствор тщательно перемешивают. Приготовленный промывочный раствор хранят не более 3-х суток при температуре от 2°С до 8°С.
Конъюгат-1, рабочий раствор. Готовят перед использованием. При использовании целого планшета к 5,0 мл раствора для разведения концентрата конъюгата-1 добавляют 0,5 мл концентрата конъюгата-1 и осторожно перемешивают.
Конъюгат-2, рабочий раствор. Готовят перед использованием. При использовании целого планшета к 5,0 мл раствора для разведения концентрата конъюгата-2 добавляют 0,5 мл концентрата конъюгата-2 и осторожно перемешивают.
Срок годности рабочих растворов конъюгатов - не более 30 мин в защищенном от света месте.
Субстратная смесь. Готовят перед использованием. 1,2 мл тетраметилбензидина перенести в 18,0 мл субстратного буферного раствора и содержимое флакона тщательно перемешать. Хранению не подлежит.
Оставшиеся неиспользованными реагенты хранить во флаконах, укупоренных пробками, на протяжении срока годности тест-системы при температуре от 2°С до 8°С.
Проведение ИФА.
Во избежание конденсации влаги внутри лунок необходимо выдержать иммуносорбент при комнатной температуре в закрытом пакете не менее 30 минут.
Перед использованием комплектов 3 и 4 необходимо вскрыть фольгированный пакет с иммуносорбентом. Вынуть из пакета рамку и необходимое количество стрипов. Пакет с неиспользованными стрипами тщательно герметизировать, не удаляя осушитель. После первого вскрытия пакета иммуносорбент стабилен в течение 1 месяца при температуре от 2°С до 8°С.
Перед использованием иммуносорбент любого комплекта промыть 3 раза рабочим раствором ПР, заливая его до краев лунок (от 380 до 400 мкл в лунку), не допуская при этом переливания промывочного раствора через края лунок, выдержать 40 с и удалить промывочный раствор в емкость для сбора инфицированного материала.
Затем в лунки планшета с сорбированными моноклональными антителами к HBsAg вносят по 100 мкл контрольных и исследуемых образцов. Покрытый крышкой планшет выдерживают 30 мин при температуре (42±0,5)°С в условиях влажной камеры. Затем, не удаляя содержимое лунок и не промывая планшет, во все лунки стрипов вносят по 50 мкл рабочего раствора конъюгата-1, окрашенного в зеленый цвет. При этом содержимое лунок изменяет свой цвет на серый. В случае тестирования плазмы или сыворотки, имеющих кислый рН, раствор в лунках становится ярко-желтым. При добавлении конъюгата-1 не следует допускать случайного заноса образца из одного стрипа в другой через наконечники. Содержимое лунок тщательно перемешивают осторожным постукиванием по краям планшета, после чего покрытый крышкой планшет выдерживают в течение 45 мин при температуре (42±0,5)°С в условиях влажной камеры. Затем, не удаляя содержимое лунок и не промывая планшет, во все лунки стрипов вносят по 50 мкл рабочего раствора конъюгата-2, окрашенного в желтый цвет. При добавлении конъюгата-2 не следует допускать случайного заноса образца из одного стрипа в другой через наконечники. Содержимое лунок тщательно перемешивают осторожным постукиванием по краям планшета, после чего покрытый крышкой планшет выдерживают в течение 45 мин при температуре (42±0,5)°С в условиях влажной камеры. Далее содержимое лунок удаляют в емкость для сбора инфицированного материала и планшет промывают 7 раз рабочим промывочным раствором. Во все лунки планшета вносят по 150 мкл субстратной смеси и выдерживают в течение 25 мин в защищенном от света месте при температуре от 20°С до 24°С. Реакцию останавливают добавлением во все лунки планшета по 50 мкл стоп-реагента и через 2-3 мин проводят учет результатов ИФА.
Учет результатов.
Учет результатов проводят спектрофотометрически при двух длинах волн: 450/620-680 нм с настройкой прибора "по воздуху". Допустим учет результатов при одной длине волны 450 нм. Реакцию следует учитывать, если средние значения оптической плотности (ОП) в лунках с К- не более 0,120, в лунках с К+1 - не менее 0,6. Значения ОП в лунках с К- не должны отличаться от среднего значения ОП К- более чем на 30%. Если одно из значений ОП К- выходит за этот предел, его следует исключить из расчета среднего значения. Если исключению подлежат более одного значения ОП К-, анализ следует повторить. Реакцию считают положительной, если значение ОП в лунке с образцом равно или превышает значение ОП критическое (ОП крит.). ОП крит. рассчитывают по формуле:
ОП крит. = ОП К- ср. + 0,060, где 0,060 - коэффициент, определяемый методом статистической обработки на предприятии-изготовителе.
Слабоположительный контрольный образец, содержащий HBsAg в концентрации 0,04±0,02 МЕ/мл, должен давать положительную реакцию. Общее время постановки ИФА составляет 145 мин.
При постановке иммуноферментного анализа на шейкере контрольные и исследуемые образцы вносят по 100 мкл вместе с рабочим раствором конъюгата-1 в количестве 50 мкл. Планшет выдерживают 40 мин на шейкере при скорости 500 об/мин и температуре (42±0,5)°С. Затем, не удаляя содержимое лунок и не промывая планшет, во все лунки стрипов вносят по 50 мкл рабочего раствора конъюгата-2. Планшет выдерживают 20 мин при 42°С на шейкере при скорости 500 об/мин и температуре (42±0,5)°С. Далее содержимое лунок удаляют в емкость для сбора инфицированного материала и планшет промывают 7 раз рабочим промывочным раствором. Во все лунки планшета вносят по 150 мкл субстратной смеси и выдерживают в течение 25 мин в защищенном от света месте при температуре от 20°С до 24°С. Реакцию останавливают добавлением во все лунки планшета по 50 мкл стоп-реагента и через 2-3 мин проводят учет результатов ИФА.
Общее время постановки ИФА при использовании шейкера составляет 85 мин.
В качестве еще одного варианта осуществления изобретения может быть подтверждение специфичности результатов выявления поверхностного антигена вируса гепатита В в сыворотке (плазме) и препаратах крови (альбумине, фибринолизине, иммуноглобулинах и лейкоцитарном интерфероне) с использованием набора 2 «ДС-ИФА-HBsAg-0,01-подтверждающая».
В дополнение к реагентам, включенным в состав набора 1, в состав набора 2 включены АНТИ-HBs-ПЛЮС (нейтрализующий реагент) - жидкий или лиофилизированный, иммуноглобулины козы, содержащие антитела к HBs-антигену; АНТИ-HBs-МИНУС (контрольный реагент) - жидкий или лиофилизированный, иммуноглобулины козы, не содержащие антитела к HBs-антигену. Лиофилизированное содержимое флаконов растворяют дистиллированной водой в объеме, указанном на этикетке.
Набор 2 рассчитан.
Комплект 5 с увеличенным объемом компонентов - на одновременное проведение 48 (4×12) подтверждающих определений, включая контрольные (комплект 1 может быть использован на автоматизированном ИФА-анализаторе).
Комплект 6 - на одновременное проведение 48 (4×12) подтверждающих определений, включая контрольные.
При постановке ИФА контрольные образцы и образцы, подлежащие подтверждению, внести каждый в две лунки по 100 мкл. В первые лунки с контрольными и подтверждаемыми образцами добавить по 25 мкл контрольного реагента - АНТИ-HBs-МИНУС, во вторые - по 25 мкл нейтрализующего реагента - АНТИ-HBs-ПЛЮС. Покрытый крышкой планшет выдержать в течение 30 мин при температуре (42,0±0,5)°С в условиях влажной камеры. Дальнейшее проведение ИФА, а также постановка на шейкере осуществляется аналогично, как описано выше при использовании набора 1.
Учет результатов проводить спектрофотометрически при двух длинах волн - 450 нм и 620-680 нм с настройкой прибора «по воздуху». Допустим учет результатов при одной длине волны - 450 нм. Реакцию следует учитывать, если среднее значение ОП в лунках с К- (без добавления контрольного или нейтрализующего реагентов) (ОП К- ср.) не более 0,12, а в лунке с К+1 (без добавления контрольного или нейтрализующего реагентов) (ОП К+) - не менее 0,6. Значение ОП в лунке с К+1 после добавления нейтрализующего реагента (ОПн К+1) должно быть равным или меньше половины суммы ОП в лунке с К+1 после добавления контрольного реагента (ОПк К+1) и ОП К- ср., т.е. ОПн К+1≤0,5×(ОПк К+1+ОП К- ср.). Значения ОП К- после добавления нейтрализующего и контрольного реагентов должны быть ниже значения ОП критического (ОП крит.), т.е. ОПн К- и ОПк К-<ОП крит. ОП крит. рассчитывают по формуле:
ОП крит. = ОП К- ср. + 0,06, где 0,06 - коэффициент, определяемый методом статистической обработки результатов постановки ИФА на предприятии-изготовителе.
Реакцию считают положительной, если значение ОП в лунке с образцом равно или превышает ОП крит.
Слабоположительный контрольный образец, содержащий HBsAg в концентрации 0,04±0,02 МЕ/мл, должен давать положительную реакцию.
Интерпретация результатов
Образец считают содержащим HBsAg, если
а) ОПк ≥ ОП крит.,
б) ОПн ≤ 0,5×(ОПк+ОП К- ср.),
где ОПк - ОП образца с контрольным реагентом, а ОПн - ОП образца с нейтрализующим реагентом. В этом случае присутствие в образце HBsAg следует считать доказанным и дальнейшая проверка не требуется.
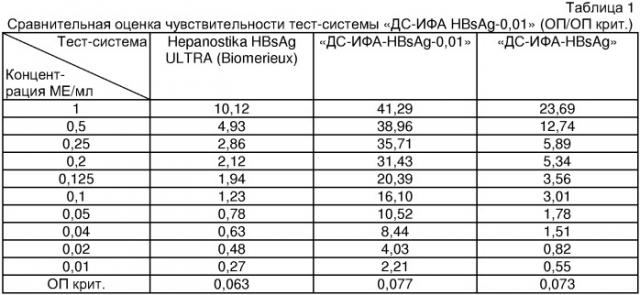
Определение аналитической чувствительности тест-системы «ДС-ИФА-HBsAg-0,01» проводилось с использованием Отраслевого Стандартного Образца HBsAg вируса гепатита В ОСО 42-28-311-03П (ООО НПО «Диагностические системы»), откалиброванного по Международному Стандарту - Second International Standard for HBsAg, subtype adw2, genotype A, NIBSC code number: 00/588, в сравнении с тест-системой «ДС-ИФА-HBsAg» и «Hepanostika HBsAg ULTRA» (Biomerieux). Были приготовлены 10 последовательных разведений ОСО от 1 МЕ/мл до 0,01 МЕ/мл, с нормальной донорской плазмой, не содержащей антител к HBsAg. Полученные данные представлены в таблице 1.
Аналитическая чувствительность тест-системы «ДС-ИФА-HBsAg-0,01» составила 0,01 МЕ/мл.
Оценка клинической чувствительности тест-системы «ДС-ИФА-HBsAg-0,01» проводилась с использованием стандартных панелей сывороток, содержащих и не содержащих HBsAg.
В таблице 2 представлены результаты сравнительного тестирования стандартной панели сывороток, содержащих и не содержащих HBsAg (ЗАО «Вектор-Бест»), серия 001.
Была проведена сравнительная характеристика чувствительности и специфичности четырех тест-систем с использованием референс-панели сывороток крови человека, содержащих и не содержащих поверхностный антиген вируса гепатита В (HBsAg) субтипы ау и ad OCO 42-28-364-04П (Медицинский центр «Авиценна», Бостон Биомедика), серия №1. Полученные данные приведены в таблице 3.
| Таблица 3 | ||||||
| Результаты тестирования референс-панели сывороток крови человека, содержащих и не содержащих поверхностный антиген вируса гепатита В (HBsAg) субтипы ay и ad (ОП/ОП крит.) | ||||||
| № | Субтип HBsAg | Концентрация HBsAg нг/мл | «ДС-ИФА-HBsAg-0,01» | Abbott Auszyme EIA | ИФА-HBsAg/м (ООО НПО «Диагностические системы», Россия) | BIO-RAD Genetic systems HBsAg EIA |
| 01 | - | - | 0,68 | 0,1 | 0,26 | Отр |
| 02 | - | - | 0,53 | 0,1 | 0,33 | Отр |
| 03 | - | - | 0,49 | 0,1 | 0,13 | Отр |
| 04 | - | - | 0,38 | 0,1 | 0,29 | Отр |
| 05 | ad | 1 | 40,11 | 3,4 | 21,50 | Поз |
| 06 | ad | 0,6 | 39,73 | 2,2 | 12,50 | Поз |
| 07 | ad | 0,2 | 17,22 | 1,0 | 3,22 | Поз |
| 08 | ay | 0,9 | 39,62 | 3,5 | 12,70 | Поз |
| 09 | ay | 0,8 | 39,94 | 3,1 | 13,10 | Поз |
| 10 | ay | 0,6 | 38,31 | 2,1 | 12,20 | Поз |
| 11 | ay | 0,4 | 30,35 | 1,4 | 4,37 | Поз |
| 12 | ay | 0,2 | 17,76 | 0,7 | 3,51 | Поз |
| 13 | ay | 0,1 | 7,31 | 0,4 | 1,21 | Поз |
| 14 | Неразв. образец | 2-3 | 42,26 | 8,2 | 23,98 | Поз |
| 15 | Неразв. образец | 2-3 | 40,85 | 10,1 | 22,17 | Поз |
| 16 | Неразв. образец | 1-1,5 | 42,51 | 4,0 | 28,23 | Поз |
| 17 | Неразв. образец | 0,5-0,7 | 40,87 | 2,0 | 19,52 | Поз |
| 18 | Неразв.образец | 0,5-0,7 | 40,03 | 2,5 | 15,10 | Поз |
| 19 | Неразв. образец | 0,1-0,25 | 25,27 | 1,2 | 5,33 | Поз |
| 20 | Неразв. образец | 0,1-0,25 | 19,54 | 0,6 | 3,62 | Поз |
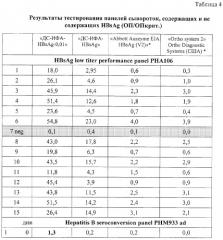
В таблице 4 представлены результаты сравнительного исследования клинической чувствительности тест-системы «ДС-ИФА-HBsAg-0,01» с использованием панелей производства BBI Diagnostics (Boston Biomedica Inc. (BBI), West Bridgewater, Mass., USA) и Zeptometrix Corporation.
Новый тест с идентичной чувствительностью выявляет HBsAg субтипов ad и ay со значительным преимуществом относительно теста сравнения - системы Abbott Auszyme EIA HBsAg (V2). Из данных таблиц видно, что тест-система «ДС-ИФА-HBsAg-0,01» с идентичной чувствительностью определяет HBsAg субтипов ay и ad во всех позитивных образцах, представленных в панелях. Коэффициенты позитивности многих HBsAg-положительных образцов в тест-системе «ДС-ИФА-HBsAg-0,01» существенно превышают коэффициенты позитивности этих же образцов, протестированных на альтернативных тестах. В образцах низкотитражной панели (от 0,05 до 0,6 IU/ml) новая тест-система позволяет также детектировать HBsAg с более высокими коэффициентами позитивности в сравнении с альтернативными тестами.
Анализ сероконверсионных панелей показал, что тест-система «ДС-ИФА-HBsAg-0,01» позволяет детектировать HBsAg в положительных образцах на более раннем сроке его появления, по сравнению с зарубежными тест-системами, данные по которым приведены в паспортах к панелям. По результатам анализа двух панелей образцов, полученных от одного донора в динамике в период сероконверсии (от момента появления до момента исчезновения HBsAg) (РНМ935А (М) и РНМ935 В), следует, что новая система в сравнении с альтернативными тестами импортного производства начинает выявлять HBsAg на более раннем сроке его появления и продолжает определять на более позднем сроке по мере его исчезновения, в результате чего позитивный по HBsAg период увеличивается на 28 дней в сравнении с системой Abbott Prism HBsAg*.
Было установлено, что использование тест-системы «ДС-ИФА-HBsAg-0,01» для анализа образцов сероконверсионных панелей позволяет выявлять HBsAg одновременно с вирусной ДНК (BBI-PHM933, BBI-PHM934, BBI-РНМ935А (М), ZeptoMetrix Corporation Cat. No. HBV6281), а в двух случаях (ZeptoMetrix Corporation Cat. No. HBV6277 и Cat. No. HBV6279) опережает время 1-ой детекции ДНК.
Известно, что существует проблема выявления HBsAg при коинфицировании. Было проанализировано 473 образца сыворотки крови анти-ВИЧ-позитивных лиц. Среди них в 66 был выявлен HBsAg в тесте «ДС-ИФА-HBsAg». Дополнительно выявлено 16 образцов, содержащих HBsAg в концентрации ниже 0,1 МЕ/мл. Причем 7 из них содержали антитела к HBcore-антигену, а 9 образцов не имели никаких других маркеров, кроме HBsAg, детектируемого только в системе с высокой чувствительностью (таблица 5). Следовательно, повышение чувствительности тестов для выявления HBsAg позволит снизить количество случаев скрытого гепатита В как с наличием дополнительного маркера анти-НВс, так и при отсутствии любых маркеров.
При тестировании 3348 образцов сыворотки крови доноров и 381 образца сыворотки крови беременных женщин в тест-системе «ДС-ИФА-HBsAg-0,01» было выявлено 6 и 1 образец, соответственно, содержащих HBsAg в концентрации ниже 0,1 МЕ/мл.
За счет повышенной чувствительности нового теста мутантные варианты HBsAg показывают более высокую реактивность в сравнении с другими системами (таблица 6).
| Таблица 6 | |||||
| Сравнительное определение мутантных форм рекомбинатного HBsAg (ОПm/ОП крит.) | |||||
| adw2 | ДС-ИФА-HBsAg | ДС-ИФА-HBsAg-0,01 | "Hepanostika" (Biomerieux) | «Рекоматгеп-В-стрип» (Эколаб) | «Вектогеп-HBsAg-стрип» компл. №4 |
| K141Е | 1,6 | 10,4 | 8,6 | 1,3 | 2,2 |
| Q129H | 1,2 | 13,0 | 16,6 | 1,4 | 2,3 |
| Q129L | 1,5 | 14,1 | 11,0 | 1,7 | 1,2 |
| M133L | 2,8 | 16,9 | 13,6 | 1,6 | 2,2 |
| T126N | 2,9 | 17,7 | 8,1 | 1,6 | 1,4 |
| G145RI | 1,4 | 9,1 | 5,8 | 1,2 | 1,7 |
| G145RII | 1,6 | 15,7 | 18,8 | 1,2 | 0,8 |
| K142S | 2,0 | 5,6 | 44,1 | 1,5 | 1,3 |
| P142S | 1,5 | 11,8 | 54,8 | 1,5 | 1,4 |
| Т143К | 1,5 | 11,7 | 2,9 | 1,2 | 0,6 |
| K141BI | 3,6 | 2,5 | 54,6 | 0,9 | 0,9 |
| ayw1 G145R | 2,5 | 27,4 | 45,1 | 2,1 | 3,3 |
Для оценки специфичности тест-системы «ДС-ИФА-HBsAg-0,01» были использованы образцы сыворотки крови доноров; образцы сыворотки крови больных с различными инфекционными заболеваниями, не связанными с HBV-пневмонией, ангиной, бронхитом, вирусным гепатитом С; образцы сыворотки крови больных с различными неинфекционными заболеваниями - с патологией сердечно-сосудистой системы, желудочно-кишечного тракта, онкозаболеваниями и др.; образцы сыворотки крови беременных женщин; образцы сыворотки крови ВИЧ-инфицированных лиц. Всего протестировано 4710 образцов. Данные по числу ложноположительных результатов в тест-системе «ДС-ИФА-HBsAg-0,01» в группе здоровых и различных группах больных представлены в таблице 7.
| Таблица 7 | |||
| Оценка специфичности тест-системы «ДС-ИФА-HBsAg-0,01» на разных категориях населения | |||
| Обследуемая группа | Количество исследуемых образцов | Количество ложноположительных результатов | % специфичности в данной группе |
| Здоровые доноры | 3348 | 7 | 99,8 |
| Больные с различными инфекционными заболеваниями, не связанными с вирусным гепатитом В | 392 | 5 | 98,7 |
| Больные с различными неинфекционными заболеваниями | 95 | 1 | 98,9 |
| Беременные женщины | 381 | 3 | 99,2 |
| ВИЧ-инфицированные | 494 | 4 | 99,2 |
| Всего | 4710 | 20 | 99,6 |
Таким образом, проведенные исследования показали, что специфичность тест-системы «ДС-ИФА-HBsAg-0,01» составляет 99,6% при исследовании образцов сыворотки крови нормальных доноров и больных с различными инфекционными и соматическими заболеваниями.
Была изучена возможность использования нового теста для детекции HBsAg в препаратах крови. В ходе исследований анализировался широкий спектр препаратов крови разных фирм-производителей: альбумин, фибринолизин, лейкоцитарный интерферон, иммуноглобулин нормальный для внутривенного введения и внутримышечного введения, иммуноглобулин противоаллергический и иммуноглобулин антистафилококковый. Жидкие препараты крови используют неразведенными; лиофильно высушенные препараты крови перед исследованием в тест-системе разводят в соответствии с инструкцией по применению данного препарата. Специфичность тест-системы по отношению к препаратам крови (были взяты пять разных серий препаратов) была исследована на трех экспериментально-производственных сериях тест-системы (таблица 8).
| Таблица 8 | |||
| Специфичность тест-системы «ДС-ИФА-HBsAg-0,01», установленная при исследовании препаратов крови | |||
| Наименование препарата | ОП препаратов (о.е.) средняя (n=5) для каждой серии тест-системы | ||
| С.1 | С.2 | С.3 | |
| Альбумин | 0,017 | 0,025 | 0,032 |
| Фибринолизин | 0,007 | 0,009 | 0,005 |
| Иммуноглобулин внутривенный | 0,009 | 0,011 | 0,015 |
| Иммуноглобулин внутримышечный | 0,014 | 0,008 | 0,010 |
| Интерферон | 0,005 | 0,007 | 0,008 |
| ОП крит.(о. е.) | 0,072 о.е. | 0,069 о.е. | 0,075 о.е. |
Из данных таблицы видно, что значения ОП всех препаратов были ниже ОП крит. (о.е.), т.е. тест-система «ДС-ИФА-HBsAg-0,01» показала 100% специфичность при тестировании препаратов крови.
Преимущество предлагаемой тест-системы для выявления HBsAg «ДС-ИФА-HBsAg-0,01» заключается в возможности детекции HBsAg в сыворотке (плазме) и препаратах крови с чувствительностью 0,01 МЕ/мл при сохранении высокой специфичности.
1. Тест-система для определения поверхностного антигена вирусного гепатита В (HBsAg) методом иммуноферментного анализа в биологическом образце, характеризующаяся тем, что содержит твердую фазу, содержащую иммуносорбент, представляющий собой сорбированные на стрипах планшета моноклональные антитела мыши к HBsAg; конъюгат-1 - биотин с моноклональными антителами к HBsAg и конъюгат-2 - стрептавидин, меченный пероксидазой хрена, представленные в виде жидких концентратов; положительный контрольный образец; отрицательный контрольный образец; промывочный раствор; растворы для разведения конъюгатов; субстратный буферный раствор; тетраметилбензидин в качестве хромогена; серную кислоту в качестве стоп-реагента; нейтрализующий реагент, жидкий или лиофилизированный, представляющий собой иммуноглобулины козы, содержащие антитела к HBsAg; контрольный реагент, жидкий или лиофилизированный, представляющий собой иммуноглобулины козы, не содержащие антител к HBsAg; слабоположительный контрольный образец, представляющий собой сыворотку крови в лиофилизированном виде, содержащую HBsAg в концентрации 0,02-0,06 МЕ/мл.
2. Тест-система по п.1, отличающаяся тем, что биологический материал представляет собой сыворотку или плазму крови.
3. Тест-система по п.1, отличающаяся тем, что биологический материал представляет собой препарат крови, выбранный из группы альбумин, фибролизин, иммуноглобулин, лейкоцитарный интерферон.
4. Способ определения поверхностного антигена вирусного гепатита В (HBsAg) методом иммуноферментного анализа в биологическом образце с помощью тест-системы по п.1, включающий выдерживание контрольных и исследуемых биологических образцов, внесенных в лунки планшета с сорбированными моноклональными антителами мыши к HBsAg при температуре (42±0,5)°С с последующим добавлением окрашенного раствора конъюгата, который представляет собой моноклональные антитела к HBsAg, связанные с биотином, а затем без стадии отмывки инкубационную смесь тщательно смешивают и выдерживают с окрашенным раствором конъюгата, представляющего собой стрептавидин, меченный пероксидазой хрена, при температуре (42±0,5)°С, реакцию останавливают добавлением стоп-реагента и проводят учет результатов спектрофотометрическим методом.